在离子液体体系中由微晶纤维素直接制得5-羟甲基糠醛
杨 伟 伟, 王 少 君
( 大连工业大学 轻工与化学工程学院, 辽宁 大连 116034 )
0 引 言
平台化合物目前主要是在石油资源中获得,随着石油、煤等不可再生资源的迅速消耗,石油化工的成本将不断提高。可再生生物质生产能源和有机化工原料,确定新的平台化合物,是目前以低碳经济实现可持续发展为目标的绿色化学的重要研究内容[1]。5-羟甲基糠醛是一种重要的化工原料,它的分子中含有一个羟甲基和一个醛基,可以通过加氢、氧化脱氢、水解等化学反应,合成许多化合物和高分子材料[2-6],有望成为基于生物质资源的新型平台化合物。
目前制备合成5-HMF的原料多为果糖和葡萄糖。MOREAU 等[7]采用蔗糖为反应物,在离子液体[Hmim][Cl]中制备5-HMF。实验结果表明蔗糖在离子液体中水解为果糖和葡萄糖,30 min 以后水解得到的果糖几乎全部被转化为5-HMF,但是水解得到的葡萄糖只有3%发生了进一步的转化。SERGIO等[8]使用离子液体[Bmim][Cl]和CrCl3,使用甲苯作为同步萃取剂,在100 ℃条件下催化葡萄糖制备5-HMF,4 h 后5-HMF产率提高到91%。ZHAO H 等[9]在离子液体体系中用金属氯化物催化果糖、葡萄糖制得5-HMF,其中以果糖为原料,得到5-HMF的收率最高。而用纤维素为原料直接制得5-HMF 的过程目前大部分需要通过使用无机酸或者有机溶剂等成本高、易污染环境、后处理困难的手段来实现[10-11]。最近几年通过绿色温和可控的条件,使用纤维素甚至用秸秆来生产5-HMF已经成为研究的重点和热点,但目前关于此类的公开报道还不多见。
本文通过合成绿色无污染的离子液体为反应溶剂和反应的催化剂,作用于微晶纤维素直接得到5-HMF。
1 实 验
1.1 仪器与药品
液相色谱仪,真空干燥箱,恒温磁力搅拌器,旋转蒸发仪。
微晶纤维素(DP=312),上海昌为医药辅料技术有限公司;N-甲基咪唑,化学纯;氯丁烷,化学纯;98%的硫酸,化学纯;CrCl3,化学纯。
1.2 离子液体的制备
1.2.1 离子液体[Bmim][Cl]的制备
根据文献[12]合成离子液体[Bmim][Cl]。
1.2.2 离子液体[Bmim][HSO4]的制备
在配有电动搅拌的250 mL三口圆底烧瓶内加入0.1 mol的[Bmim][Cl]离子液体,然后在搅拌下慢慢滴加等摩尔的98%浓硫酸,滴加过程中以冰水浴冷却,控制滴速使瓶内温度维持在30 ℃以下。加毕,在回流下继续搅拌并升温至60~70 ℃,反应6 h后停止搅拌,待反应物冷却至室温后,加入乙醚洗涤,洗涤后的产品60 ℃真空抽干1 h得[Bmim][HSO4]离子液体[13]。
1.3 在离子液体中催化微晶纤维素生成5-HMF
将微晶纤维素,离子液体[Bmim][Cl]和[Bmim][HSO4]置于55 ℃真空干燥箱过夜除水。
称取4 g [Bmim][Cl]置于反应器中,在一定温度的油浴中磁力搅拌。加入0.02 g 微晶纤维素,搅拌30 min后溶液澄清透明。加入一定质量的[Bmim][HSO4]和CrCl3,并开始计时,反应一定时间后,将反应器浸入到冰水中淬灭反应。向反应液中加入甲醇水溶液定容,搅拌至一相,过滤后进行HPLC的分析。
1.3.1 5-HMF的测定
实验中采用的是外标法对5-HMF进行定量分析,所谓外标法就是以被测组分的纯品作为标准品,以质量浓度为横坐标,峰面积为纵坐标作出被测化合物的标准曲线,再根据标准曲线求出样品中该组分的质量浓度。
HPLC分析检测条件:检测波长,284 nm;色谱柱,Kromasil C-18,250 mm×4.6 mm;检测器,紫外检测器;工作站,N2000色谱工作站;流动相,V(甲醇)∶V(水)=10∶90;柱温,室温;流动相体积流量,1 mL/min;进样量,20 μL。
1.3.2 5-HMF的标准曲线的绘制
分别对5-HMF配制不同浓度的标准样品,利用液相色谱测试做出标准曲线,外标法定量。标准曲线见图1。
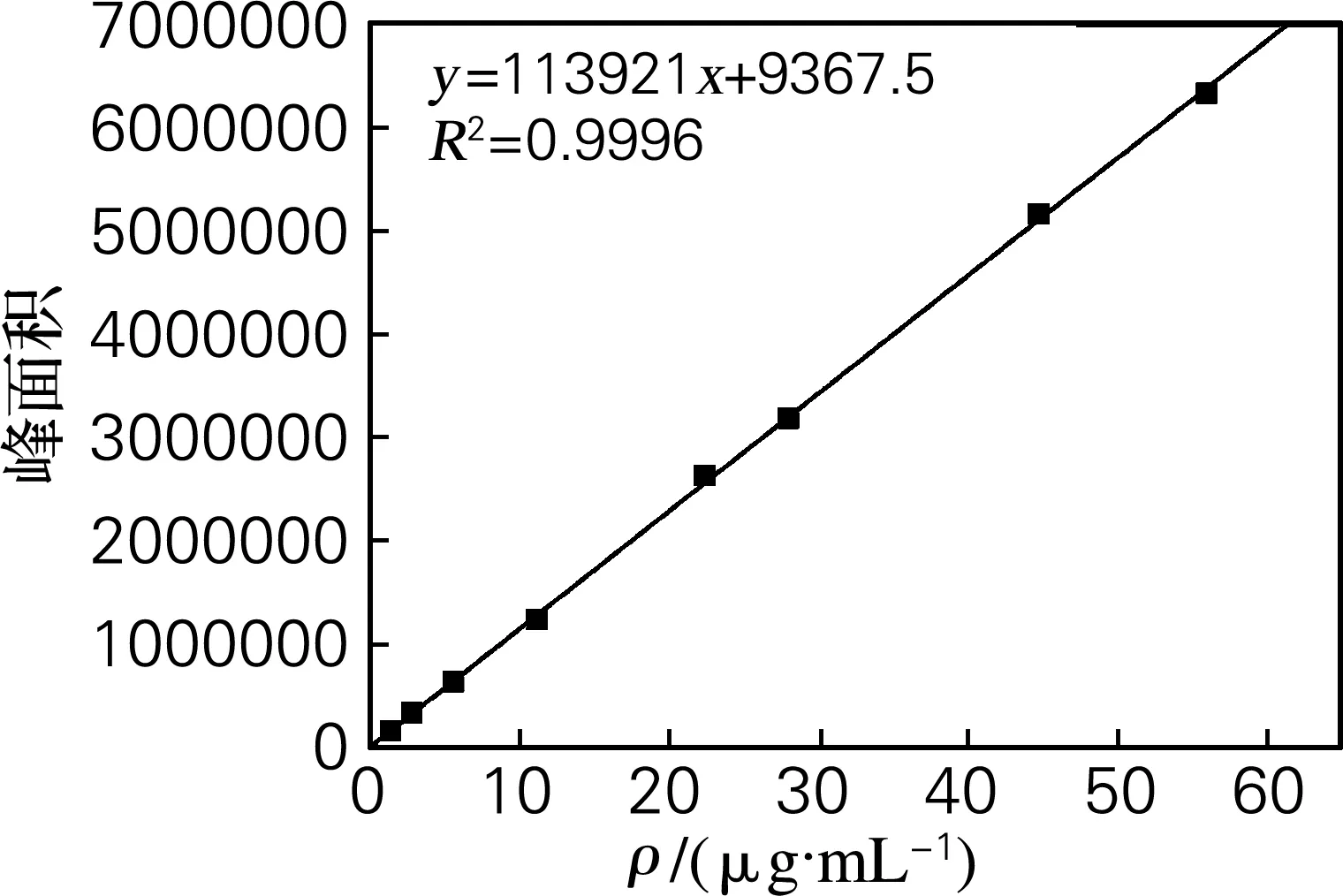
图1 5-HMF的标准曲线
1.3.3 5-HMF收率的计算
依据公式计算5-HMF的摩尔收率
式中,X为5-HMF的摩尔收率;X1为5-HMF质量浓度(根据标准曲线计算而得);V为定容后的体积;m为微晶纤维素的质量;198为微晶纤维素的一个葡萄糖单元相对分子质量;126为5-HMF的相对分子质量。
2 结果与讨论
将微晶纤维素加入[Bmim][Cl]离子液体中,不加[Bmim][HSO4]和CrCl3,反应温度为120 ℃下进行空白实验,反应180 min后产物中只检测到痕量的5-HMF。说明在此条件下,[Bmim][Cl]本身不能催化微晶纤维素得到5-HMF。[Bmim][Cl]在此体系中起到溶剂的作用。将微晶纤维素加入[Bmim][Cl]离子液体中,只添加[Bmim][HSO4]或者CrCl3,得到5-HMF的量非常少。这进一步说明,在离子液体-CrCl3体系中,微晶纤维素向5-HMF 的转化是经由离子液体[Bmim][HSO4]和CrCl3的协同作用完成的。
2.1 温度对催化微晶纤维素生成5-HMF的影响
在催化剂用量[Bmim][HSO4] 1 g和CrCl30.4 g 、反应时间4 h条件下考察反应温度对催化微晶纤维素生成5-HMF的影响,结果见图2。
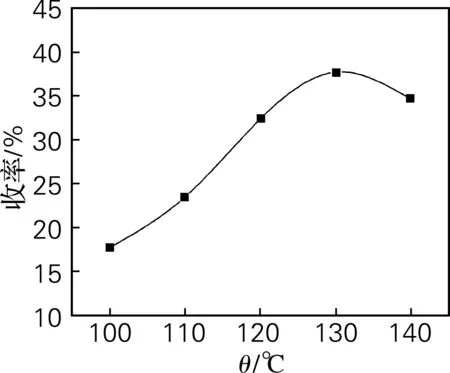
图2 反应温度对5-HMF收率的影响
Fig.2 Effect of the reaction temperature on the yield of 5-HMF
由图2可见,在温度低于130 ℃ 时,5-HMF的收率随着反应温度的增加而增加。根据化学反应速率方程可知,反应温度升高,反应速率常数增大,微晶纤维素降解反应的速率也会增大,5-HMF 的收率也会因此而升高。随着反应温度的继续升高,微晶纤维素转化为其他产物的速率也会增大,5-HMF也会进一步降解,转化为乙酰丙酸、甲酸等副产物[9]。降解产物变得更加复杂,5-HMF的收率会因此而下降。因此选择130 ℃ 为适宜的反应温度。
2.2 时间对催化微晶纤维素生成5-HMF的影响
在反应温度120 ℃、催化剂用量为[Bmim][HSO4] 1 g和CrCl30.4 g条件下,考察反应时间对催化微晶纤维素生成5-HMF的影响,结果见图3。

图3 反应时间对5-HMF收率的影响
从图3中可以看出,反应时间低于4 h时,5-HMF 的收率和反应时间成正比关系;超过4 h时,随着时间的增加5-HMF的收率减少。分析认为随着反应时间的增加,微晶纤维素的转化率随之增加,5-HMF的收率也会相应提高,随着反应时间的继续增加,5-HMF可能会与微晶纤维素降解的中间产物还原糖等物质进一步发生聚合反应,使得5-HMF的收率下降。因此,最佳反应时间为4 h。
2.3 催化剂用量对催化微晶纤维素生成5-HMF的影响
反应温度120 ℃、反应时间4 h,在此条件下考察[Bmim][HSO4]和CrCl3的用量对催化微晶纤维素生成5-HMF的影响,结果见表1。
表1 催化剂[Bmim][HSO4]和CrCl3的量对5-HMF收率的影响
Tab.1 Effect of the amounts of [Bmim][HSO4] and CrCl3on the yield of 5-HMF
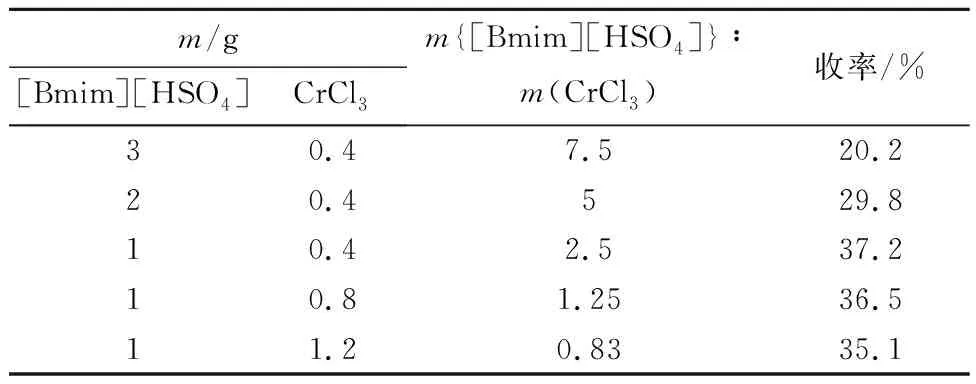
m/g[Bmim][HSO4]CrCl3m{[Bmim][HSO4]}∶m(CrCl3)收率/%30.47.520.220.4529.810.42.537.210.81.2536.511.20.8335.1
从表1可见,[Bmim][HSO4]和CrCl3的质量比在7.5和2.5之间时,随着[Bmim][HSO4]和CrCl3质量比的减少,5-HMF的收率逐步提高;而当CrCl3的量继续增加,[Bmim][HSO4]和CrCl3的质量比低于2.5时,5-HMF的收率会略有下降,下降的幅度较小。这是因为纤维素的降解反应需要在酸性体系下进行,随着催化剂[Bmim][HSO4]量的增加,溶液的酸性不断增强,使得整个反应的速率和反应程度都增加。但是[Bmim][HSO4]的量过大,整个体系的酸性过强,会使得微晶纤维素水解生成的还原糖等副产物的速率增加。同时,5-HMF也会被进一步降解,5-HMF的收率会因此降低。所以,酸性较强或较弱都不利于5-HMF的生成。
当[Bmim][HSO4]的量固定在1 g,增加CrCl3的量,[Bmim][HSO4]和CrCl3的质量比低于2.5时,5-HMF的收率也会有所下降。这主要是因为离子液体[Bmim][Cl]-CrCl3具有Lewis酸性,增加CrCl3的量,同样会增加整个体系的酸性,降低5-HMF的收率[14]。所以[Bmim][HSO4]与CrCl3的质量比选择1.25时为适宜的催化剂量。
2.4 水的质量分数对催化微晶纤维素生成5-HMF 的影响
从糖类在酸催化作用下降解生成5-HMF的机理[15-16]中可以得到,反应起始阶段纤维素水解反应中,需要水来参加反应,整个反应缺少水会影响反应的速率。纤维素水解生成的还原糖类物质如葡萄糖、果糖等在这种缺水的条件下又会脱水生成目标产物5-HMF,生成的水重新参与到反应的起始阶段——水解反应。每生成1分子葡萄糖需要消耗1分子水,而1分子葡萄糖紧接着脱除3分子水而得到5-HMF,即水解消耗的水又通过脱水反应得到补充。这样下来使得整个反应可以依次循环下来继续反应。假如在整个反应体系中增加水的含量,会使得在起始阶段的反应速率很快,但随着整个反应体系中水的量的增加,5-HMF 进一步水解成乙酰丙酸和甲酸的可能性也就随之增加,所以5-HMF收率会随水含量的增加而降低。综合考虑起来,决定在这个反应中,无需加入额外的水。
3 结 论
以离子液体[Bmim][Cl]为溶剂,微晶纤维素为反应的起始原料,以官能化的酸性离子液体[Bmim][HSO4]和CrCl3为复配催化剂,进行纤维素的降解反应制得5-HMF。实验结果表明,当[Bmim][Cl]用量为4 g,微晶纤维素为0.02 g,在130 ℃ 下搅拌后加入1 g [Bmim][HSO4]和0.4 g CrCl3,反应4 h,5-HMF的收率最大可以达到37%。
[1] 岑沛霖,穆江华,赵春晖,等. 从可再生资源获得新型绿色“平台化合物”乙酰丙酸的研究与开发[J]. 生物加工过程, 2003, 1(1):17-22.
[2] 王军,张春鹏,欧阳平凯. 5-经甲基糠醛制备及应用的研究进展[J]. 化工进展, 2008, 27(5):702-708.
[3] 严永清,朱丹妮,陈婷,等. 5-羟甲基-2-糠醛的医药用途:中国,1182589[P]. 1998-05-27.
[4] 李林,魏海峰,张兰,等. 5-羟甲基糠醛类用于制备神经系统用药的用途:中国,03146245.6[P]. 2005-01-19.
[5] 杜莹,潘柯,严孝强,等. 5-羟甲基-2-糠醛及其衍生物、类似物的医药用途:中国,1589784[P]. 2005-03-09.
[6] LESHKOV Y R, CHHEDA J N, DUMESIC J A. Phase modifiers promote efficient production of hydroxymethylfurfural from fructose[J]. Science, 2006, 312(5782):1933-1937.
[7] MOREAU C, FINIELS A, VANOYE L. Dehydration of fructose and sucrose into 5-hydroxymethylfurfural in the presence of 1-H-3-methyl inidazolium chloride acting both as solventand catalyst[J]. Journal of Molecular Catalysis A:Chemical, 2006, 253:165-169.
[8] LIMA S, NEVES P, ANTUNES M. Conversion of mono-dipolysaccharides into furan compounds using 1-alkyl-3-methylimidazolium ionic liquids[J]. Applied Catalysis A:General, 2009, 363(1/2):93-99.
[9] ZHAO H, HOLLADAY J E, BROWN H, et al. Metal chlorides in ionic liquid solvents convert sugars to 5-hydroxymethylfurfural[J]. Science, 2007, 316(5831):1597-1600.
[10] 何北海,林鹿,孙润仓,等. 木质纤维素化学水解产生可发酵糖研究[J]. 化学进展, 2007, 19(7/8):1141-1146.
[11] 庄新妹,王树荣,骆仲映,等. 纤维素低浓度酸水解试验及产物分析研究[J]. 太阳能学报, 2006, 27(5):519-524.
[12] SWATLOSKI R P, SPEAR S K, HOLBREY J D. Dissolution of cellose with ionic liquids[J]. Journal of the American Chemical Society, 2002, 124(18):4974-4975.
[13] 王雯娟. 新型功能化离子液体的合成及其酸催化有机反应性能的研究[D]. 上海:华东师范大学, 2008.
[14] 王要令,张罡. 离子液体[Emim]Br-FeCl3的合成与酸性研究[J]. 化工时刊, 2009, 23(7):48-49.
[15] DAM H E, KIEBOOM A P G, BEKKUM H. The conversion of fructose and glucose in acid media:formation of hydroxymethylfurfural[J]. Starch, 1986, 38(3):95-101.
[16] ANTAL M J, MOK W S, RICHARDS G N. Four-carbon model compounds for the reactions of sugars in water at high temperature[J]. Carbohydrate Research, 1990, 199(1):91-97.

