八钼酸季铵盐催化H2O2氧化醇制备醛酮
张 家 荣, 李 军, 王 普 光, 董 晓 丽, 高 爽
( 1.大连工业大学 轻工与化学工程学院, 辽宁 大连 116034; 2.中国科学院 大连化学物理研究所, 辽宁 大连 116023; 3.陕西延长石油(集团)有限公司, 陕西 西安 710075 )
0 引 言
醇类选择性氧化成羰基化合物是有机合成中的一个重要反应,并广泛应用于实验室和工业生产中,且在精细化学工业中起着关键的作用[1]。工业上多采用化学计量氧化法进行生产,采用含高价锰、铬等金属的盐类或氧化物作为氧化剂,如Jones试剂、吡啶重铬酸盐、吡啶氯铬酸盐等[2],其生产成本高、产生大量的无机废物污染环境并且产品分离提纯不易[3]。所以从环境保护和原子经济性的角度来看,这些方法必须要改进或淘汰[4-5]。近20年来,各国学者一直致力于研究如何用廉价、清洁的氧源替换过去的高毒昂贵的氧化剂用于醇的氧化。过氧化氢是一种理想的环境友好氧源,反应后生成对环境无害的水,且价格低廉、来源丰富。以过氧化氢为氧源的催化氧化早期由于缺乏有效的催化剂,加上过氧化氢在金属离子存在下容易发生分解反应,在20世纪80年代前研究的并不多。1979年Jacobson等[6]发现在过氧化氢的作用下,钼、钨与六甲基磷酰胺或吡考啉酸形成的过氧配合物可以氧化仲醇,过氧化氢浓度为90%。2007年Guo等[7]报道八钼酸吡啶盐催化过氧化氢在回流反应条件下氧化苯甲醇可得到85%的苯甲醛产率,但对脂肪仲醇的氧化结果不好。Zhang等[8]一直在对杂多酸催化H2O2液相选择氧化醇制醛酮进行研究,本文以廉价易得的脂肪族季铵盐替代烷基吡啶盐为原料合成了一系列的八钼酸烷基铵盐催化剂,考察该类催化剂在H2O2氧化醇制备醛酮的反应活性。
1 实 验
1.1 仪 器
傅里叶变换红外表征:采用Bruker Tensor 27型傅立叶变换红外光谱仪测定催化剂的化学结构,扫描范围400~4 000 cm-1,分辨率为2 cm-1,将催化剂样品与KBr按照质量比1∶200混合,研磨后,放入不锈钢模具内压成圆形锭片,进行测量。气相色谱仪采用Agilent 4890气相色谱仪。色谱柱:SE-30毛细管柱(0.53 mm×50 m),进样器温度250 ℃。检测器为FID(离子火焰检测器),温度250 ℃,高纯N2作载气,体积流量约为8.0 mL/min。苯甲醇氧化反应的分析条件为:100 ℃保持7.0 min,15 ℃/min升至250 ℃,保持6.0 min。
1.2 催化剂合成
催化剂[n-C16H33(CH3)3N]4Mo8O26按文献[7]方法制备,在10 mL的水中加入3 g (0.012 5 mol) 钼酸钠(Na2MoO4·2H2O),加入5 mL 12% HCl (0.019 mol),制成溶液A。在25 mL 的水中加入十六烷基三甲氯化铵(7.44 g, 0.023 mol)制成溶液B。在搅拌条件下,把溶液B升温至70 ℃,慢慢滴加溶液A,有大量白色固体生成,滴加完成后,搅拌20 min。过滤,水洗,室温干燥,得 3.10 g (收率92%)白色固体粉末。IR:3445, 2913, 2840, 1466, 952, 915, 857, 799, 716, 660 cm-1。与文献[9]对比确认合成催化剂为[n-C16H33(CH3)3N]4Mo8O26。
1.3 苯甲醇氧化制备苯甲醛的操作步骤
在70 mL单口圆底烧瓶中加入苯甲醇(1.08 g,10 mmol),15% H2O2(2.50 g, 12 mmol),催化剂(0.05 g),内标正壬烷(0.5 g),进行回流反应。反应完成后,在冰水中冷却20 min,然后离心分离,在得到的液体中加入30 mL二氯甲烷(分3次加入,各10 mL)进行萃取,合并有机相,再用无水硫酸钠进行干燥,最后通过GC分析、内标定量得到反应的转化率和选择性。
2 结果与讨论
2.1 不同季铵盐阳离子对苯甲醇氧化苯甲醛的影响
以苯甲醇氧化苯甲醛为模型反应对反应条件进行了考察。表1为催化剂八钼酸季铵盐中不同季铵盐阳离子对催化剂催化活性的影响。由表1可见,无催化剂存在下,苯甲醇氧化制苯甲醛的收率和选择性仅为3.2%和29.1%。在催化剂存在下,随着催化剂中C链的长度由1增加到18(Entry 2~6),苯甲醛的收率由50.5%提高到75.3%,说明季铵盐中C链的长度对反应是有影响的。有研究表明[10],如果季铵盐阳离子中烷基较小,C数较低,制备的催化剂在水中的溶解度较大,反应时催化剂一直可以溶于水相。相反,如果阳离子中烷基较大,C数较高,那么制备的催化剂在有机相中的溶解度必然较大,而苯甲醇与H2O2的反应是水油两相反应,所以催化剂中烷基的C数会对反应有影响。含有四丁基铵阳离子(Entry 8)的催化剂只得到18.1%的苯甲醛的收率,这可能是因为位阻的原因。综合考虑选用[n-C16H33(CH3)3N]4Mo8O26为催化剂对其他反应条件进行了考察。
表1 八钼酸季铵盐(Q4Mo8O26)中季铵盐阳离子对催化活性的影响
Tab.1 Effect of the ammonium ion of Q4Mo8O26on the reaction

序号阳离子收率/%选择性/%1-3.229.12[(CH3)4N]+50.578.23[PhCH2N(CH3)3]+67.579.74[n-C12H25(CH3)3N]+72.481.45[n-C16H33(CH3)3N]+75.784.56[n-C18H37(CH3)3N]+75.382.37[π-C5H5NC16H33]+59.370.08[(C4H9)4N]+18.181.9注:n(苯甲醇)∶n(H2O2)(15%)=1∶1.2,苯甲醇(1.08 g, 10 mmol),催化剂(0.05 g),90 ℃,2.0 h。收率和选择性基于苯甲醇。
2.2 苯甲醇和H2O2 摩尔比对苯甲醇氧化苯甲醛的影响
表2是苯甲醇与H2O2的摩尔比对氧化反应的影响。由表2可知,当苯甲醇与H2O2的摩尔比为1∶1.2时,苯甲醛的收率和选择性分别为75.7%和84.5%。当苯甲醇与H2O2的摩尔比为1∶1.5~1∶2.5时,苯甲醛的收率和选择性均降低,这是因为增加H2O2的用量使产物苯甲醛进一步氧化成苯甲酸。所以苯甲醇与H2O2的摩尔比为1∶1.2时,反应结果最好。
表2 苯甲醇和H2O2摩尔比对反应的影响
Tab.2 Effect of molar ratio of benzyl alcohol to H2O2on the reaction
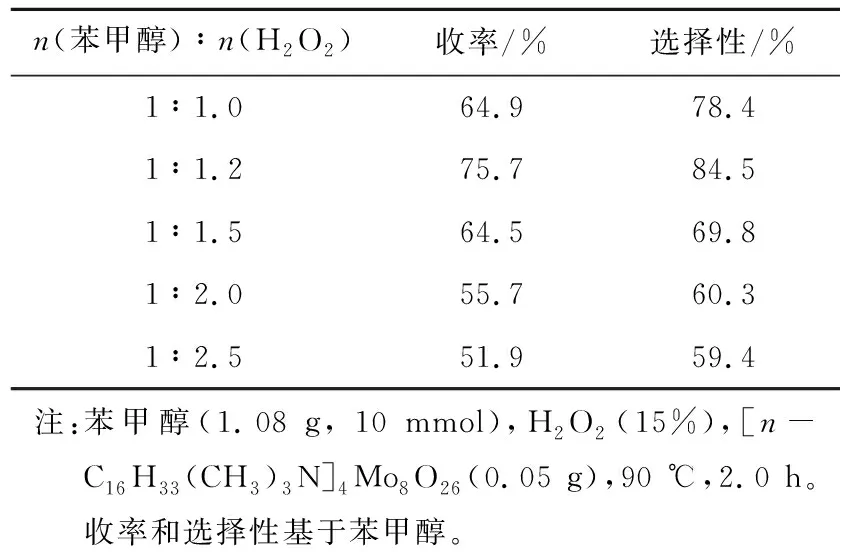
n(苯甲醇)∶n(H2O2)收率/%选择性/%1∶1.064.978.41∶1.275.784.51∶1.564.569.81∶2.055.760.31∶2.551.959.4注:苯甲醇(1.08 g, 10 mmol),H2O2(15%),[n-C16H33(CH3)3N]4Mo8O26 (0.05 g),90 ℃,2.0 h。收率和选择性基于苯甲醇。
2.3 H2O2质量分数对反应的影响
H2O2质量分数对反应有很大影响,由表3可见,随着H2O2质量分数由8%提高到15%,苯甲醛的收率和选择性分别由8.8%和26.7%增加到75.7%和84.5%,再提高H2O2的质量分数,则苯甲醛的收率和选择性均有所降低,分别由15% H2O2时的75.7%和84.5%降低到30% H2O2时的55.8%和73.3%,50% H2O2的35.1% 和63.4%。所以H2O2的质量分数为15%是适宜的。
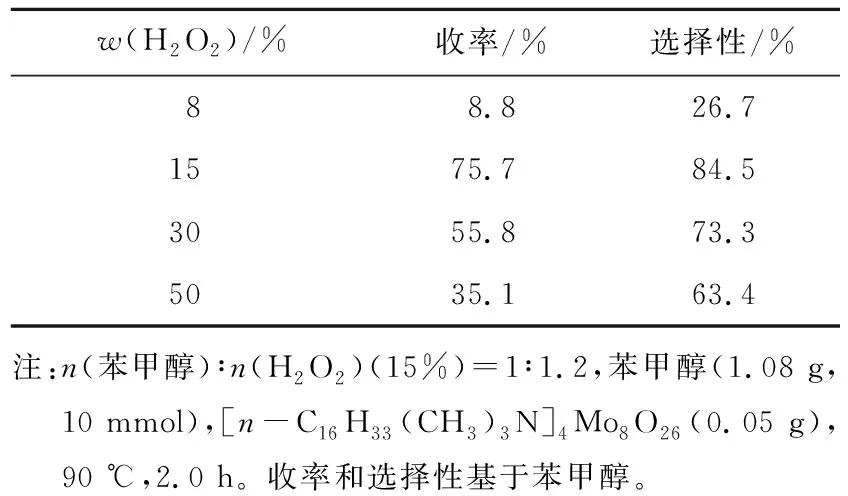
表3 H2O2质量分数对反应的影响
2.4 反应温度的影响
表4为反应温度的影响。由表4可见,反应温度由90 ℃升高到100 ℃,苯甲醛的收率和选择性分别由75.7%和90.0%提高到79.6%和91.6%,继续提高反应温度苯甲醛的收率变化不大,但选择性有所降低,由100 ℃的91.6%降低到120 ℃的86.6%。所以100 ℃是适宜的反应温度。

表4 反应温度的影响
2.5 反应时间的影响
表5为反应时间的影响。由表5可见,当反应时间由0.5 h延长到1.0 h,苯甲醛的收率和选择性分别由55.6%和83.9%提高到79.6%和91.6%,再延长反应时间苯甲醛的收率和选择性均有所下降,这是由于苯甲醛可以进一步被氧化成苯甲酸,随着反应时间的延长,苯甲醛的浓度越来越大,它被氧化成苯甲酸的量也会越多,所以1.0 h 是最佳反应时间。
通过条件考察,苯甲醇氧化制苯甲醛的适宜反应条件为:n(苯甲醇)∶n(H2O2)=1∶1.2,H2O2的质量分数为15%,催化剂[n-C16H33(CH3)3N]4Mo8O26用量为0.05 g,100 ℃,1.0 h。

表5 反应时间的影响
2.6 不同醇的氧化
从以上考察中得到了适宜的反应条件,进而对不同醇的氧化进行了考察,结果见表6。由表6可见,芳香族仲醇的反应活性高于脂肪族仲醇,例如在相同的反应条件下(底物与过氧化氢的摩尔比为1∶1.2,反应时间为1 h),1-苯乙醇可以得到98.5%的苯乙酮收率(Entry 5),而其他脂肪族的仲醇得到12.5%~74.3%的收率(Entry 1~4)。脂肪族仲醇氧化为酮的收率可以通过提高H2O2用量来提高,以2-戊醇氧化生成2-戊酮为例(Entry 2),当2-戊醇与H2O2的摩尔比由1∶1.2提高到1∶2时,2-戊酮的收率由74.3%提高到99.5%。至于2-丁醇只得到28.7%的丁酮收率(Entry 1),这可能是由于催化剂中季铵盐含有16个C原子的长链烷基结构,亲油性强,而丁醇只含有4个C,可以与水互溶,二者在反应介质中不能很好地接触,即催化剂的阳离子C数与底物的C数不匹配,从而影响反应结果。

表6 不同醇的氧化
3 结 论
合成了一种用于醇氧化反应的催化剂[n-C16H33(CH3)3N]4Mo8O26。该催化剂在H2O2氧化醇的反应中具有很好的活性和选择性,不仅可以使苯甲醇高选择性地生成苯甲醛,而且在仲醇的氧化反应中也表现出很高的活性和选择性。
[1] SHLDON R A, KOCHI J. Metal catalyzed oxidations of organic compounds[M]. New York:Academic Press, 1981.
[2] HOLUM J R. Study of the chromium(Ⅵ) oxide-pyridine complex[J]. Journal of Organ Chemistry, 1961, 26:4814-4816.
[3] ZHAO Wei, ZHANG Yingshuai, MA Baochun. Oxidation of alcohols with hydrogen peroxide in water catalyzed by recyclable keggin-type tungstoborate catalyst[J]. Catalysis Communications, 2010,11(6):853-857.
[4] MA Baochun, ZHANG Yingshuai, DING Yong. A water-soluble dilacunary silicotungstate as an effective catalyst for oxidation alcohols in water with hydrogen peroxide[J]. Catalysis Communications, 2010, 11(9):853-857.
[5] 许招会,廖维林,王甡. 磷钨酸镧催化合成缩醛(酮)的研究[J]. 分子催化, 2008, 22(1):39-43.
[6] JACOBSON S E, MUCCIGROSSO D A, MARES D. Oxidations with solid potassium permanganate[J]. Journal of Organ Chemistry, 1979, 44:921-924.
[7] GUO Minglin, LI Zuizhen. Selective oxidation of benzyl alcohol to benzaldehyde with hydrogen peroxide over tetra-alkylpyridinium octamolybdate catalysts[J]. Green Chemistry, 2007, 9:421-423.
[8] ZHANG Shengjun, ZHAO Gongda, GAO Shuang. Secondary alcohols oxidation with hydrogen peroxide catalyzed by [n-C16H33N(CH3)3]3PW12O40:Transform-and-retransform process between catalytic precursor and catalytic activity species[J]. Journal of Molecular Catalysis A: Chemical, 2008, 289:22-27.
[10] 李坤兰,周宁,奚祖威. 溶剂和杂多酸盐中季铵阳离子对环己烯环氧化反应控制相转移催化的影响[J]. 催化学报, 2002, 23(2):125-126.

