没食子酸清除DPPH自由基的微量电化学滴定
李晓芬,王炯,李桥丽,高云涛,张公信,周学进
(云南民族大学民族药资源化学国家民委-教育部重点实验室,云南昆明650500)
没食子酸清除DPPH自由基的微量电化学滴定
李晓芬,王炯,李桥丽,高云涛,张公信,周学进
(云南民族大学民族药资源化学国家民委-教育部重点实验室,云南昆明650500)
电化学研究表明,没食子酸在石墨电极上有一不可逆的氧化峰,峰电位为Epa=0.48 V,且在0.38 V(vs.SCE)处有一灵敏的差分脉冲伏安氧化峰,其峰电流与浓度具有良好的线性关系,ipa=2.408c+3.028,r=0.999 6.建立了没食子酸清除DPPH自由基的新型微量电化学滴定法,研究了没食子酸和DPPH自由基反应的化学计量关系,测得没食子酸和DPPH自由基反应的化学计量比为1∶3,该结果与光谱分析法相符,并对没食子酸清除DPPH自由基的电化学氧化机理进行了探讨.
没食子酸;DPPH自由基;电化学滴定;化学计量;电化学氧化机理
没食子酸(gallic acid,GA)又称五倍子酸,化学名称为3,4,5-三羟基苯甲酸,结构见图1.是一种典型的天然植物酚酸类化合物,也是许多中草药的有效成分[1-4].药理学研究表明,GA具有较强的清除自由基和抗氧化作用,还具有抗菌、抗病毒、抗肿瘤、抗诱变等功效[5-7].

1,1-二苯基-2-苦基肼(DPPH)自由基是一种人工合成的稳定的自由基,常用于评价物质的抗氧化活性[8-13].目前活性物质的抗氧化能力多以清除率达50%时的质量浓度IC50值为定量评价指标,但IC50因测定体系和自由基初始浓度不同而有很大差异,且易受测定条件影响,因此发展一种新的、更可靠的评估方法具有重要意义.本文在对GA电化学氧化机理研究的基础上提出一种新型微量电化学滴定分析方法,该法在一定量的GA中逐渐定量加入DPPH,记录加入DPPH后GA氧化峰电流的变化,根据滴定结果计算GA与DPPH反应的化学计量关系,以化学计量关系评价活性物质的抗氧化活性,在此基础上对GA与DPPH反应机理进行研究.
1 实验部分
1.1 主要实验仪器和试剂
MEC-12B多功能微机电化学分析仪(江苏江分电分析仪器有限公司),pH-213型酸度计.三电极系统:工作电极为石墨电极,参比电极为饱和甘汞电极(SCE),对电极为铂片电极.8453型UV-Vis分光光度计(美国安捷伦公司).
GA标准品(纯度﹥99%,购自国药集团浙江华东医药有限公司);DPPH(1,1-二苯基-2-苦基肼,纯度﹥99%,Sigma公司);芦丁标准品(纯度﹥99%,购于Sigma公司);柠檬酸-磷酸氢二钠缓冲溶液;配制GA (1 mg/mL)、芦丁(1 mg/mL)和DPPH(0.1 mg/mL,用无水乙醇配制)的标准储备液,4℃储存备用.经分光光度法测定,DPPH醇溶液的光吸收值可在1 h内基本不变.所有试剂均为分析纯,实验用水均为二次蒸馏水.
1.2 实验方法
1.2.1 循环伏安法(CV)
取一定量的1 mg/mL GA溶液于10 mL比色管中,用0.1 mol/L pH=4.40的柠檬酸-磷酸氢二钠缓冲溶液稀释定容,转移至电解池中,接通三电极系统,在0.1~0.8 V电位范围内,以70 mV/s的扫速进行循环伏安扫描,记录CV曲线.
1.2.2 差分脉冲伏安法(DPV)
取一定量的1 mg/mL GA溶液于10 mL比色管中,用0.1 mol/L pH=4.40的柠檬酸-磷酸氢二钠缓冲溶液稀释定容,转移至电解池中,接通三电极系统,在0.1~0.8 V电位范围内,以150 ms脉冲宽度、10 mV脉冲幅度、200 ms脉冲间隔进行扫描,记录DPV曲线.作峰电流与浓度的差分脉冲伏安标准曲线.线性方程为ipa=2.408 c+3.028,r=0.999 6,在浓度为1.0×10-7~7.0×10-5mol/L范围内ipa与c呈线性关系.
1.2.3 动力学参数的测定
从GA的循环伏安曲线可获得电子转移数n、质子数m、电子转移系数α和速率常数ks等动力学常数,为推测物质在电极上的电化学氧化反应机理提供了依据.
1.2.4 微量电化学滴定
在含有一定量的GA(5.0×10-5mol/L)溶液中,用微量进样器以每次10.0 μL逐渐定量加入1.0× 10-3mol/L DPPH,记录每次滴加DPPH后GA的DPV曲线及其氧化峰电流.根据GA的差分脉冲伏安标准曲线计算GA浓度,根据DPPH加入量与没食子酸的浓度变化关系绘制电化学滴定曲线,以达到最大清除时DPPH与GA物质的量之比,可以确定DPPH与GA反应的化学计量关系.
1.2.5 DPPH分光光度法标准曲线的绘制
分别取0,0.5,1,2,3,4,5 mL标准液在25 mL比色管中定容至刻度,其质量浓度依次为:0,1,2,4,6,8,10 μg/mL.在516 nm处测定上述标准溶液的吸光度,绘制标准曲线.得到其线性回归方程为:A=0.027 9 c+ 0.000 8,相关系数r=0.999 8,表明DPPH浓度与其吸光度呈良好的线性关系.
1.2.6 GA对DPPH自由基的清除作用
准确移取4.5 mL DPPH标准液于10 mL比色管中,分别加入不同浓度的GA标准溶液,空白管为4.5 mL DDPH标准液,并用无水乙醇定容至5.0 mL,置于暗处静置30 min,取出后以无水乙醇为参比于516 nm处分别测定其吸光度.计算其清除率,并与芦丁进行对照,清除率按下式计算:

式中:A0为空白管的吸光度;A样为样品管的吸光度.
2 结果与分析
2.1 循环伏安(CV)分析
图2中a是GA的循环伏安曲线,b、c是GA中加入DPPH溶液后的循环伏安曲线.从图2a可知,石墨电极在底液(柠檬酸-磷酸氢二钠)中不出峰,加入一定量的GA标准溶液后,GA在Epa=0.48 V处出现1个明显的氧化峰,说明GA在石墨电极上发生了不可逆的电化学氧化反应,氧化产物不易在电极表面上还原出来.当在GA溶液中加入不同浓度的DPPH时,GA的峰电流明显减少,DPPH浓度越高,GA峰电流越低,表明GA被DPPH所消耗,同时峰电位也发生了负移.
2.2 差分脉冲伏安(DPV)分析
GA的差分脉冲伏安图见图3中的a曲线所示,GA在0.38 V处有一灵敏的氧化峰,峰电流与GA浓度具有良好的线性关系,ipa=2.408c+3.028(r=0.999 6),说明通过氧化峰电流可以定量计算GA的浓度.图3中的b~e曲线是GA中加入不同浓度的DPPH后峰电流的变化,从图可知,在GA中加入不同浓度的DPPH后,GA的氧化峰电流呈线性减少,可计算出加入量与峰电流的关系.
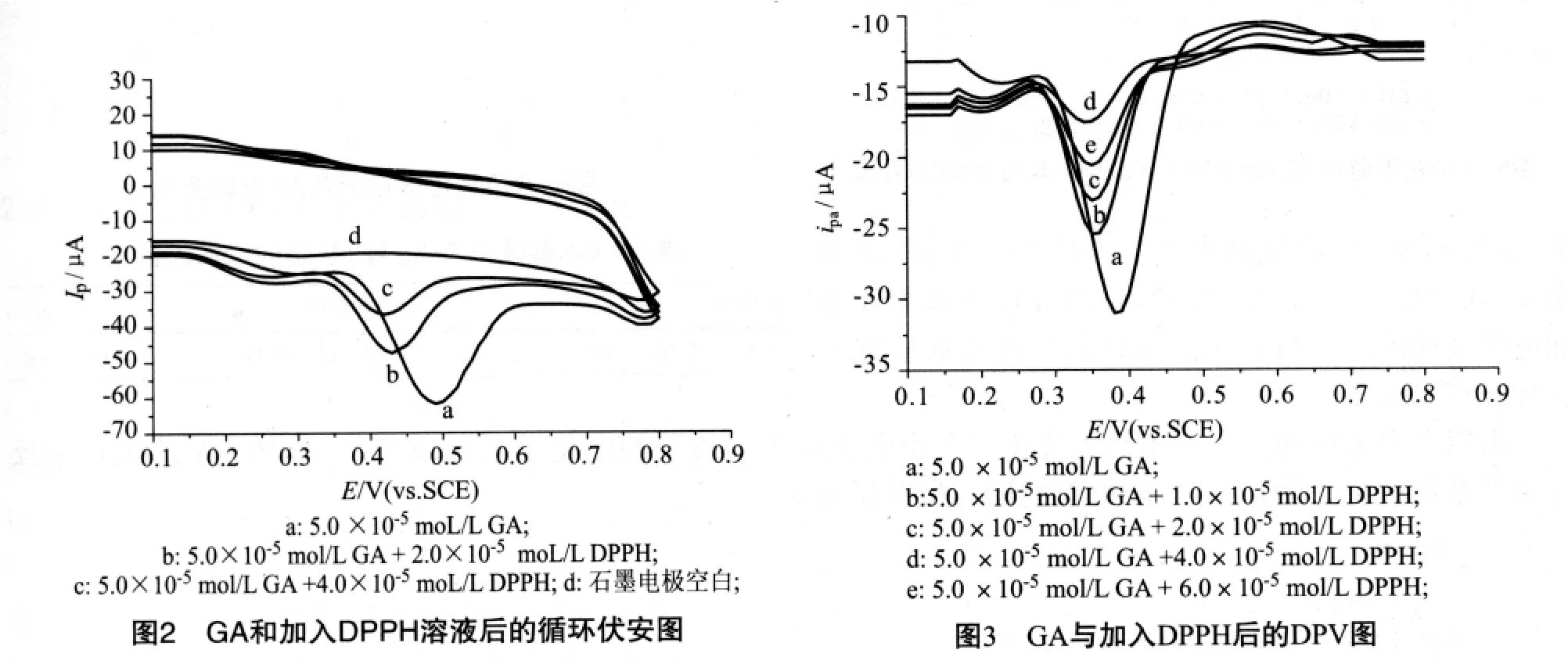
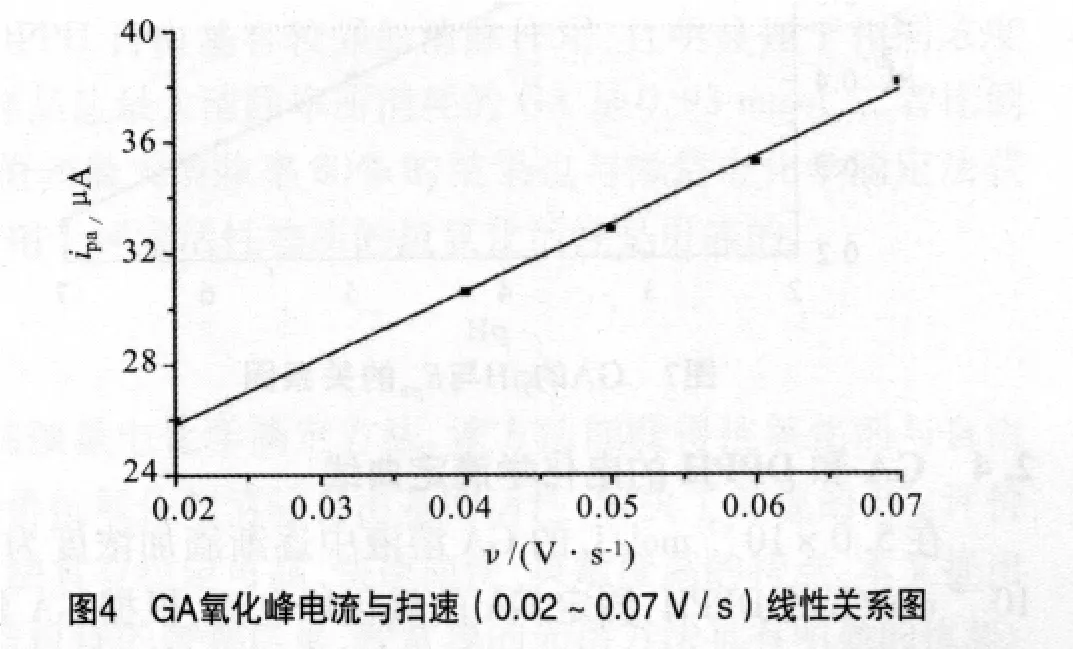

表1 GA氧化峰电流与扫速的线性关系
2.3 动力学参数的测定
2.3.1 电子转移数n的测定
电子转移数n是电极反应参数之一,由图4及表1可知GA的峰电流和扫速呈线性关系,反应过程又受吸附控制,此吸附体系满足Laviron理论中Langmuir吸附等温式:

式中Q为循环伏安单一过程的峰面积(以电量计);ipa为氧化峰电流;F=96 485 C/mol;R= 8.314 5 J/(K·mol);T=298.15 K;ΓT为吸附量(mol·cm-2);A为石墨电极的面积,约为0.282 6 cm2.由式(1)可知,只需测得某扫描速度下的峰面积和ipa值,即可求得n,从而通过式(2)再求出ΓT.经计算可知,扫速为0.07 V/s时,GA的电子转移数n为3.01,则吸附量ΓT分别为2.27×10-10mol/cm2.
2.3.2 参加电极反应的质子数m的测定
由图5和图6可知,底液的酸度是影响物质峰电位和峰电流的重要因素之一,底液pH值不同,同等浓度的GA在电极上的电化学响应不同,则参与电极反应的质子数m可由底液pH值对峰电位的影响来求得.根据能斯特方程:
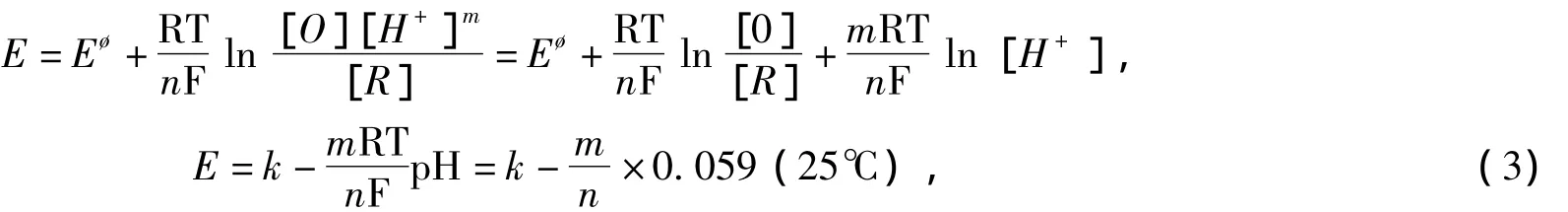

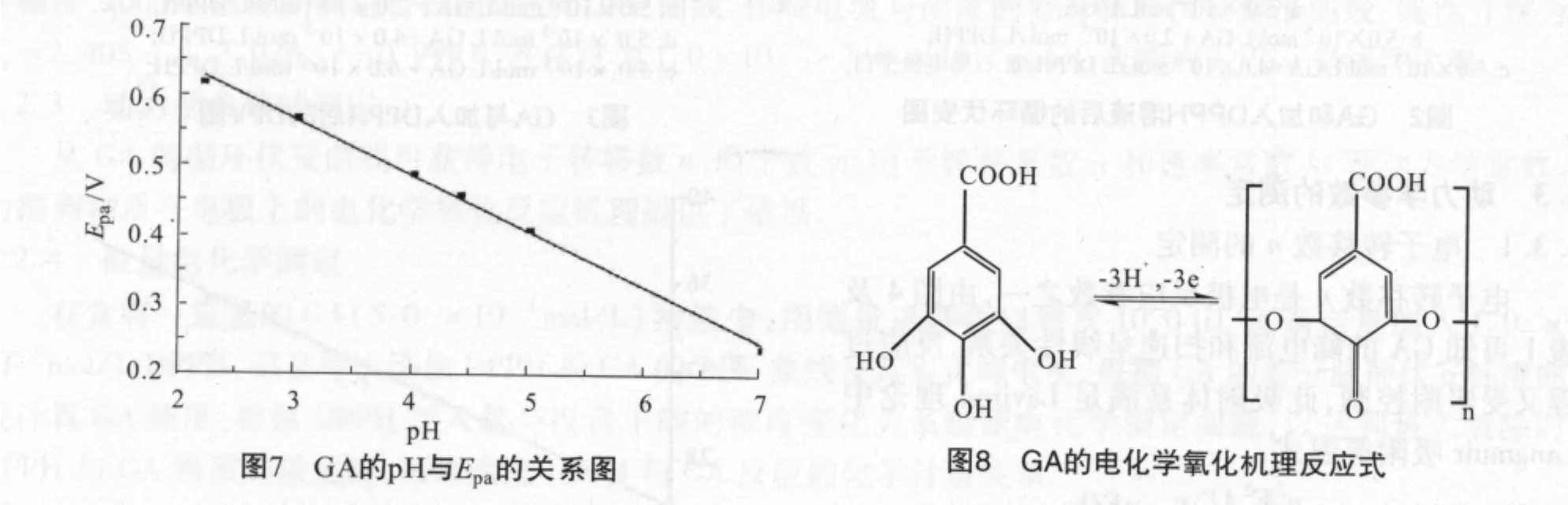
由式(3)可知,只需绘制出Epa-pH的关系图,其斜率k=0.059 m/n(温度为25℃),由n即可求解出参加电极反应的质子数m,Epa-pH的线性关系见图7,线性方程见表2.
由以上研究可知,GA在电极上发生了3个电子和3个质子的电化学氧化反应,可推知GA的电化学反应为羟基被氧化为酮基的过程,可能的反应机理见图8.

表2 GA的峰电位Epa与pH值的线性关系

2.4 GA和DPPH的电化学滴定曲线
在5.0×10-5mol/L的GA溶液中逐渐滴加浓度为4.0× 10-4mol/L的DPPH,测定GA的氧化峰电流,根据GA氧化峰电流与浓度关系计算出加入DPPH后GA的浓度变化,绘制DPPH加入量与余下GA的物质的量的关系,结果见图9所示.从图9可知,加入DPPH后,GA的氧化峰电流迅速下降,但DPPH加入量达到一定浓度时,GA的氧化峰电流趋于稳定,表明所加入的GA很大部分已经被DPPH消耗,其拐点对应达到最大清除时DPPH和GA反应完全时的化学计量点.通过计算化学计量点时DPPH加入量与已消耗GA物质的量的比值,可以确定DPPH与GA的化学计量关系.图9中2条切线相交的坐标值视为溶液中剩余的GA和加入DPPH的物质的量比.经计算,达到最大清除时,GA与DPPH的化学计量比约为1∶3,也就是说1 mol的GA可以清除约3 mol的DPPH,该计量关系表明了GA清除DPPH的能力,此结果与光谱学研究的结果相符.
通常GA等具有递电子和递质子能力的抗氧化剂对DPPH的清除作用是通过抗氧化剂把电子和质子传递给DPPH,从而生成稳定的分子态DPPH2[15],其反应式见图10.结合GA与DPPH的滴定曲线,在此基础上可以进一步推出GA和DPPH的电化学反应方程式为图11.该反应的计量关系与GA和DPPH得失电子数相符.


2.5 GA清除DDPH自由基的光谱学研究
将DPPH在516 nm处的吸光度值与质量浓度作线性回归分析,得到方程:A=0.027 9 c+0.000 8,其相关系数r=0.999 8,表明DPPH浓度与其吸光度呈正相关关系.GA与芦丁对DPPH自由基的清除作用见图12.清除率随质量浓度的增加逐渐增大,达到一定浓度时,清除率保持稳定.当清除率达50%时,GA的质量浓度为:IC50=0.000 92 mg/mL,GA的质量浓度≥0.002 mg/mL时,清除率达最大,为79.17%.当清除率达到50%时,芦丁的质量浓度为:IC50=0.003 992 mg/mL,芦丁的质量浓度≥0.008 mg/mL时,清除率达最大为74.46%.这说明GA对DPPH自由基有较强的清除作用,且明显强于相同浓度下的芦丁.在光谱学研究中,DPPH为2.739 mmol时样品达最大清除率所消耗的GA是0.93 mmol,二者比例为1∶3,此结果与电化学研究的结果相符.光谱法IC50值和最大清除率80%的结果也与微量电化学滴定法获得的化学计量结果相符,因此证明微量电化学计量法用于评定活性物质的抗氧化活性是可靠的.

3 结论
本文提出一个新的测定和评价物质抗氧化活性的微量电化学滴定方法.该方法能获得抗氧化剂与自由基的化学计量关系,利用该化学计量关系可更好的评价抗氧化剂清除自由基的活性,解决了常规的IC50评价方法受体系和自由基初始浓度影响较大的不足.该方法具有稳定可靠、快速简便、灵敏度高的特点.本文提出的微量电化学滴定法还能获得抗氧化剂和自由基反应机理的微观信息,较常规的光谱方法具有明显的优势.
[1]狄莹,石碧.植物多酚[M].北京:科学出版社,2000:11-12.
[2]KUMAR R A,JAYARAMAN A,LAKSHMANAN M,et al.Bioconversion of gallic acid into pyrogallol by immobilized Citrobacter freundii TB3[J].Journal of Fermentation and Bioengineering,1992,74(3):159-162.
[3]戴勇.3,4,5-三甲氧基苯甲醛的合成工艺改进[J].盐城工学院学报:自然科学版,2007,20(4):1-3
[4]吕丽丽.电子级没食子酸制备过程中若干基础问题研究[D].杭州:浙江大学,2008.
[5]朱艳媚.余甘子的研究进展[J].中华实用中西医杂志,2007,20(7):622-623.
[6]许红岩,王丽莉,王彦怀,等.没食子酸在Nafion/单壁碳纳米管/聚(3-甲基噻吩)复合膜修饰电极上电化学行为及测定[J].传感技术学报,2008,21(7):1113-1118.
[7]季宇彬.中药有效成分药理与应用[M].哈尔滨:黑龙江科学技术出版社,1995.
[8]王和才,胡秋辉.DPPH法测定紫红薯提取物清除自由基的能力[J].食品研究与开发,2010,31(1):132-134.
[9]莫绪生,邹碧群,刘贤贤,等.麻风树籽初提取物对DPPH自由基的清除能力研究[J].桂林师范高等专科学校学报,2010,24(2):174-175.
[10]陆艳丽,管毓相,方玉梅,等.千里光黄酮类化合物清除DPPH自由基的作用[J].食品科技,2010,35(3):197-199.
[11]郑善元,陈填烽,郑文杰,等.单丛茶水提物清除DPPH和ABTS自由基的光谱学研究[J].光谱学与光谱分析,2010,30(9):2418-2422.
[12]黄思梅,张镜.海南蒲桃原花青素DPPH自由基清除活性及稳定性的初步研究[J].食品科技,2010,35(3):204-206.
[13]张逸波,郑文杰,黄峙,等.硒杂环化合物SPO清除DPPH和ABTS自由基的光谱学研究[J].光谱学与光谱分析,2010,30(7):1866-1871.
[14]LAVIRON E.General expression of the linear potential sweep voltammogram in the case of diffusionless electrochemical systems[J].J Electroanal Chem,1979,101(l):19-28.
[15]杨盈,严宝珍,聂舟,等.α-生育酚与自由基DPPH的反应机理的研究[J].波谱学杂志,2008,25(3):331-336.
(责任编辑戴云)
Micro-Electrochemical Titration Analysis of the Scavenging Effect of Gallic Acid on DPPH Free Radicals
LI Xiao-fen,WANG Jiong,LI Qiao-li,GAO Yun-tao,ZHANG Gong-xin,ZHOU Xue-jin
(Key Laboratory of Chemistry in Ethnic Medicinal Resources,State Ethnic Affairs Commission and Ministry of Education,Yunnan University of Nationalities,Kunming 650500,China)
The electrochemical results indicated that gallic acid presented typical irreversible oxidation processes,and an irreversible oxidation peak was observed with the peak potentials of 0.48V(vs.SCE)on the graphite electrode.A sensitive differential pulse voltammetry anodic peak at Epa=0.38V(vs.SCE)was also detected with a good linear relationship between the peak current and the concentration:ipa=2.408 c+3.028,r=0.999 6.A novel micro-electrochemical titration method for evaluating the scavenging effect of gallic acid on DPPH free radicals was proposed,the stoichiometric relationship of gallic and DPPH was determined with a stoichiometric proportion of 1∶3(gallic to DPPH),which was coincident with the results of spectrophotometry.Electrochemical oxidation mechanism of the scavenging effect of gallic acid on DPPH free radicals was also investigated.
gallicacid;DPPHfreeradical;electrochemicaltitration;stoichiometry;electrochemical oxidation mechanism
O 657.7;R 284.1
A
1672-8513(2012)04-0243-06
10.3969/j.issn.1672-8513.2012.04.003
2011-08-29.
云南省创新团队项目(2011HC008);民族药资源化学国家民委-教育部重点实验室开放基金(MJY07010).
李晓芬(1986-),女,硕士研究生.主要研究方向:分析化学.
高云涛(1962-),男,教授,硕士生导师.主要研究方向:分析化学.

