维生素C的紫外分光光度法测定研究
何保山,左春艳,王 丹,王金水
(1.河南工业大学 粮油食品学院,河南 郑州 450001;2.河南工业大学 生物工程学院,河南 郑州 450001)
维生素C的紫外分光光度法测定研究
何保山1,左春艳1,王 丹1,王金水2
(1.河南工业大学 粮油食品学院,河南 郑州 450001;2.河南工业大学 生物工程学院,河南 郑州 450001)
应用紫外分光光度法分析技术建立了快速测定维生素C的检测方法.利用样品中维生素C在弱酸条件下将三价铁离子还原为亚铁离子,生成的亚铁离子与邻二氮菲形成橙红色络合物,在最大吸收波长510 nm处生成物吸光值与样品中维生素C质量浓度成比例,结果显示维生素C质量浓度在1~30 μg/mL的范围内具有良好的线性关系,相关系数为0.998,相对标准偏差为0.3%~1.0%,加标回收率为97.18%~102.67%.方法操作简便、可靠,可以用于样品中维生素C的快速测定.
紫外分光光度法;快速测定;维生素C;邻二氮菲
0 前言
维生素C是人体重要的维生素之一,广泛存在于植物组织中,如新鲜的水果、蔬菜,特别是枣、辣椒、猕猴桃、柑橘等食品中.作为人体正常生理代谢的一种重要化合物,维生素C广泛参与机体氧化还原等复杂代谢过程,维持体内多种支持组织及细胞间质的生成,促进生长和抗体的形成,增强免疫活性,人体缺乏维生素C时会患坏血病,故维生素C又称抗坏血酸[1].另外,维生素C被用作营养强化剂、抗氧化剂、增效剂添加在食品中,对食品既起到品质改良、稳定风味作用,又具有保鲜功能.因此,对维生素C测定方法的研究对人体医疗保健、健康饮食、食品保鲜等方面都具有重要的现实意义.
近年来文献报道维生素C的测定方法主要有滴定法[2-4]、化学发光分析法[5-6]、高效液相色谱法[7-8]和电化学[9-11]等.其中,滴定法是一种传统和经典的维生素C检测方法,具有结果直观、方便实用的特点,但操作步骤比较繁琐,测量结果容易受样品中其他有色物质的干扰.化学发光分析法和高效液相色谱法是20世纪60年代以后发展起来的检测技术,应用于维生素C的检测具有灵敏度高、结果可靠的特点,但通常检测所需的仪器比较昂贵,且需要专业人士操作,应用范围受到一定的限制.电化学法是将被测物质浓度转化为一种电信号加以测量的分析方法,与常规分析方法相比,具有仪器设备简单、便于携带、易自动化的特点,但这种分析方法易受其他物质干扰,目前尚处于研究阶段.
笔者利用维生素C在弱酸条件下与三价铁离子和邻二氮菲间的特异性显色反应,基于紫外分光光度装置建立了快速测定维生素C的分析方法,并对反应时间、反应条件进行了优化,取得了满意的结果.
1 材料与方法
1.1 试验材料
维生素C:天津市科密欧化学试剂有限公司;邻二氮菲:国药集团化学试剂有限公司;硫酸铁铵:天津市瑞金特化学品有限公司;冰乙酸:开封市芳晶化学试剂有限公司;三水合乙酸钠、氢氧化钠:汕头市西陇化工厂有限公司.所用试剂均为分析纯,所用水为二次蒸馏水.试验在室温下进行.
1.2 仪器与设备
TU-1901双光束紫外可见分光光度计:北京普析通用仪器有限责任公司.
1.3 试验方法
1.3.1 缓冲溶液(pH 4.75)的配制
准确称取13.6 g三水合乙酸钠、准确量取6 mL乙酸置于50 mL蒸馏水中,充分溶解,用1%的氢氧化钠溶液调节pH至4.75,备用.
1.3.2 邻二氮菲﹙4.0 mg/mL﹚的配制
准确称取4.0 mg邻二氮菲置于1 000 μL的缓冲溶液中,充分溶解,备用.
1.3.3 硫酸铁铵﹙2.4 mg/mL﹚的配制
准确称取2.4 mg邻二氮菲置于1 000 μL的缓冲溶液中,充分溶解,备用.
1.3.4 维生素C标准溶液(2.5 mg/mL)的配制
准确称取2.5 mg维生素C样品置于1 000 μL的缓冲溶液中,充分溶解.
1.3.5 样品中维生素的测定
测试时,首先分别移取150 μL邻二氮菲、150 μL硫酸铁铵、2 150 μL缓冲溶液至比色皿中,再移取50 μL检测试样至比色皿中,立即置于TU-1901双光束紫外分光光度计中测量其在波长510 nm的吸光值,通过吸光值与维生素C质量浓度间的响应关系得知样品中维生素C的含量.
2 结果与分析
2.1 维生素C与显色剂间生成物最大吸收波长的确定
试验中首先对维生素C与显色剂间结合反应的光谱特点进行考察.分别对游离的显色剂 (邻二氮菲、硫酸铁铵)溶液以及维生素C与显色剂间的反应溶液进行光谱扫描,结果如图1所示.由图1可以看出,在200~900 nm之间的整个扫描区间内,游离显色剂溶液并没有明显的吸收峰 (图1中曲线1).当溶液中引入维生素C后,游离显色剂与维生素C间发生快速显色反应,光谱曲线在波长510 nm处出现了明显的吸收峰(图1中曲线2),峰值为2.285,此应为游离的显色剂与维生素C反应后生成物的特征吸收峰.因此,试验中将显色反应的最大吸收波长定为510 nm.
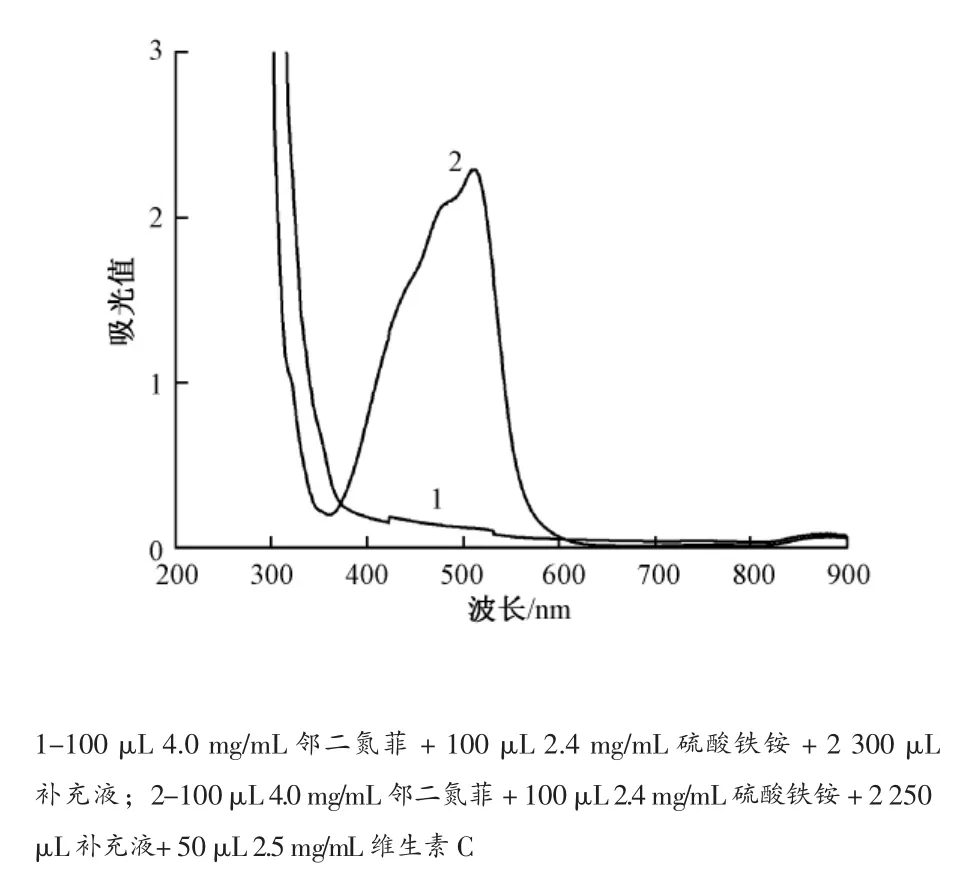
图1 显色剂与维生素C间的光谱扫描曲线
2.2 反应时间的确定
试验中将测量波长点定为510 nm,依次移取100 μL邻二氮菲、100 μL硫酸铁铵、2 250 μL补充液和50 μL的维生素C标准溶液置于比色皿中充分混合,在紫外可见光分光光度计上进行时间扫描,结果如图2所示.由图2可以看出,维生素C与显色剂间的结合反应非常迅速,1 min后生成物吸光值即可达到稳定,因此,选择反应时间为1 min.
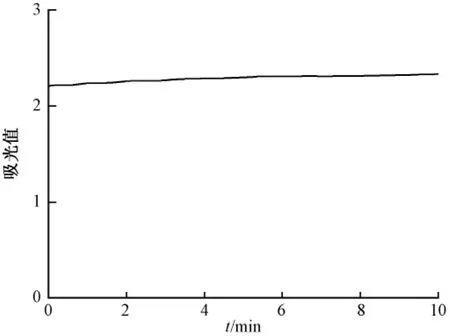
图2 维生素C与显色剂间反应的时间扫描曲线
2.3 邻二氮菲用量的优化
试验中比色皿内引入2.5 mg/mL维生素C溶液50 μL,2.4 mg/mL硫酸铁铵溶液150 μL,改变邻二氮菲用量,分别移取0 μL、50 μL、100 μL、150 μL、200 μL 4.0 mg/mL邻二氮菲溶液置于比色皿中,反应1 min,进行光谱扫描,结果如图3所示.由图3可以看出,反应体系中随着邻二氮菲引入量的增加,在最大吸收波长510 nm处生成物的吸光值也逐渐增大,当邻二氮菲引入量为150 μL时,峰值最大,当引入量超过150 μL时,峰值下降,因此,将邻二氮菲的引入量定为150 μL.
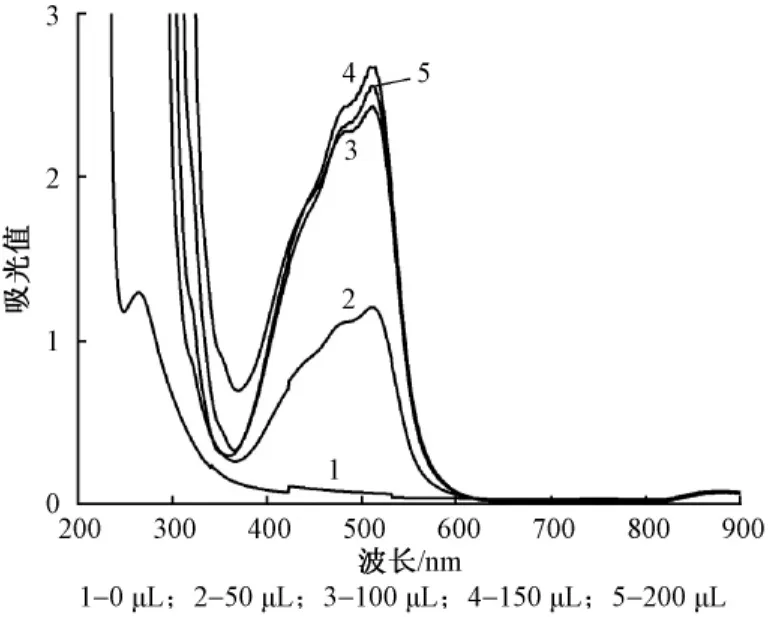
图3 不同用量的邻二氮菲与维生素C反应的光谱扫描曲线
2.4 硫酸铁铵用量的优化
试验中比色皿内引入2.5 mg/mL维生素C溶液50 μL,4.0 mg/mL邻二氮菲溶液150 μL,改变硫酸铁铵用量,分别移取0 μL、50 μL、100 μL、150 μL、200 μL、250 μL 4.0 mg/mL硫酸铁铵溶液置于比色皿中,反应1 min,进行光谱扫描,结果如图4所示.由图4可以看出,反应体系中随着硫酸铁铵引入量的增加,在最大吸收波长510 nm处生成物的吸光值也逐渐增大,当硫酸铁铵引入量大于150 μL时,峰值超过仪器检测上限,且峰形出现了较多尖锐的凸起,体系不再稳定,这说明此时结合反应需要更长的时间才能完成,因此,将硫酸铁铵的引入量定为150 μL.
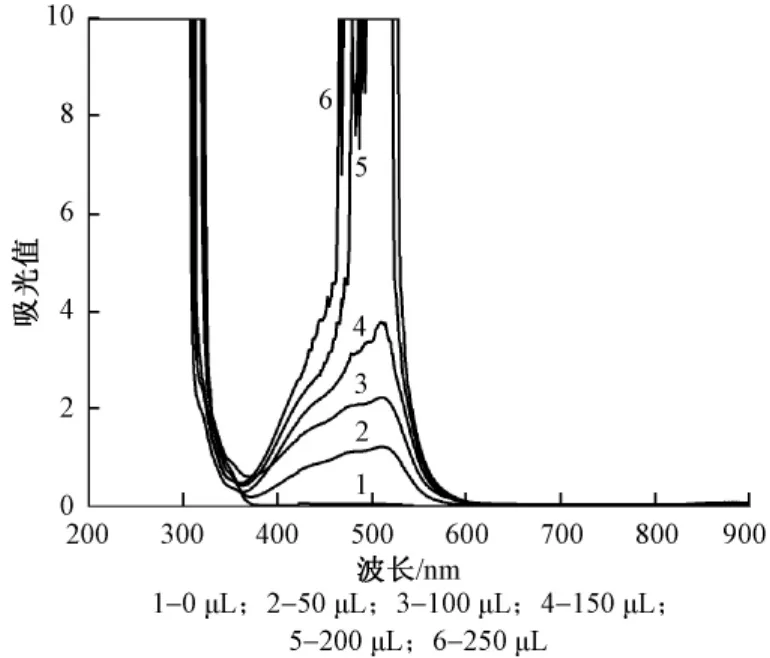
图4 不同用量的硫酸铁铵与维生素C反应的光谱扫描曲线
2.5 其他还原性物质对吸光值的影响
试验中将果糖、葡萄糖作为干扰物质引入维生素C和邻二氮菲、硫酸铁铵的反应体系中,结果显示,在相同试验条件下,上述两种物质不与邻二氮菲、硫酸铁铵发生反应,在最大吸收波长510 nm处不产生吸收(图5),对显色反应不产生影响.这说明本方法抗干扰能力强,对样品中维生素C的选择性高.
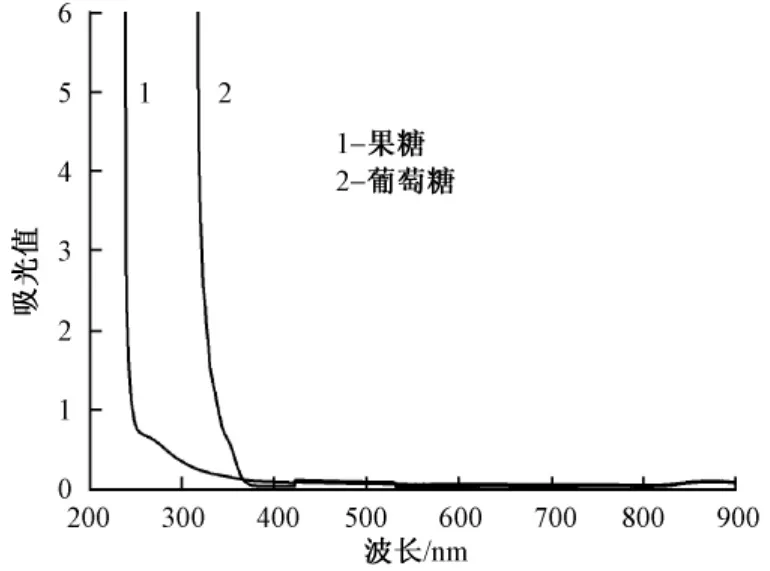
图5 果糖、葡萄糖对显色反应的影响
2.6 样品的测定
在最优化的检测条件下,应用上述建立的紫外分光光度法对质量浓度为1~30 μg/mL的维生素C样品进行检测,结果如图6所示.
由图6可以看出,维生素C在1~30 μg/mL的质量浓度范围内,吸光值与维生素C质量浓度呈线性相关,线性方程为y=0.046x+0.161,相关系数R=0.998.
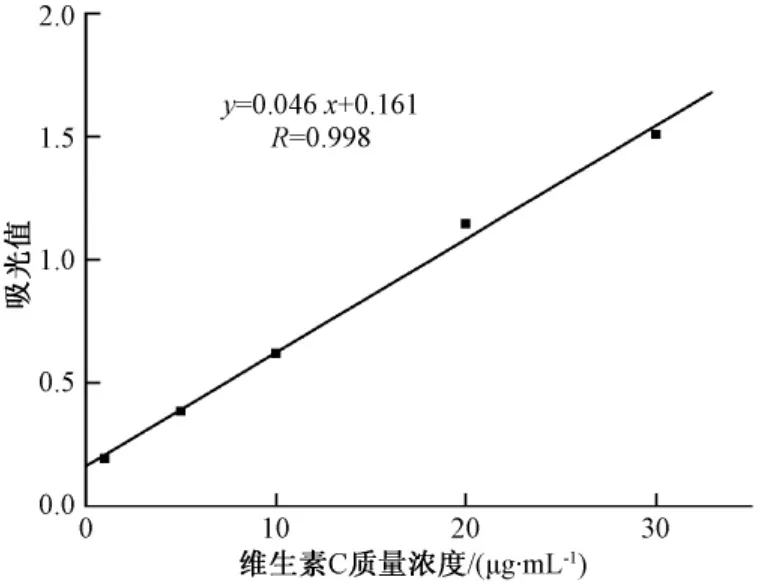
图6 维生素C质量浓度与吸光值的拟合直线图
2.7 样品分析
准确称取一定质量的市售草莓、青椒、柠檬,加入一定体积的缓冲液用纱布包裹放入干净的研钵中进行研磨,至浆状.取一定量样液置于离心管中,加入缓冲液,使总体积为1.5 mL,将离心管放入离心机内离心.准确移取50 μL上清液应用上述建立的紫外分光光度法在最大吸收波长处测定其吸光度值,根据已有的标准曲线,即可得出样液中维生素C的含量.每种样品平行测定3次,同时测定加标回收率,所得结果见表1.
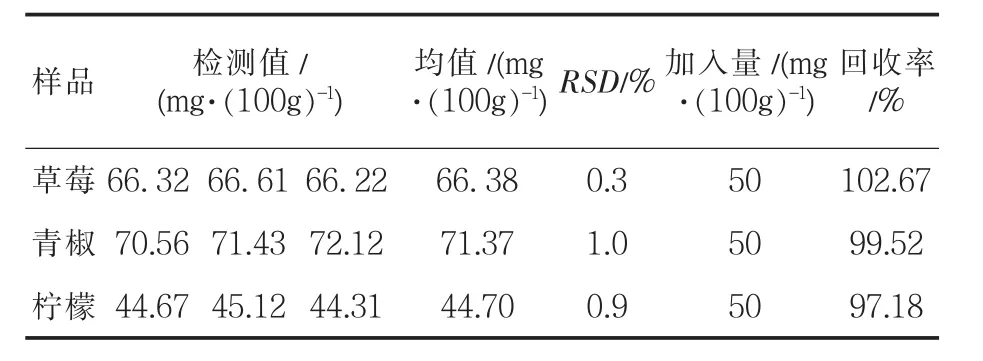
表1 蔬菜、水果中维生素C含量的测定
3 结论
本研究基于维生素C与邻二氮菲、硫酸铁铵间的快速显色反应,其生成物的吸光值与样品中维生素C质量浓度呈比例,建立了维生素C的光紫外分光光度法分析技术,反应时间1 min,在1~30 μg/mL的维生素C质量浓度范围内有较好的线性关系,相对标准偏差为0.3%~1.0%,回收率为97.18%~102.67%,实现了样品中维生素C含量的快速定量检测.
[1] Antonelli M L,D'Ascenzo G,Laganà A,et al. Food analyses:a new calorimetric method for ascorbic acid(vitamin C)determination[J].Talata,2002,58:961-967.
[2] 武文,詹秀环,宣亚文.碘量法测定蔬菜中维生素C的含量[J].安徽农业科学,2009,37(21):9845-9846.
[3] 叶青,江志波.酸碱滴定法与碘滴定法测定维生素C[J].理化检验-化学分册,2007,43(5):410, 412.
[4] Kovács-Hadady K,Fábián I.Determination of vi tamin C in effervescent tables containing other vitamins together with trace elements[J].Journal ofPharmaceuticaland BiomedicalAnalysis, 1996,14:1479-1486.
[5] 马泉莉,金永平,尤洪涛.化学发光抑制法测定抗坏血酸[J].光谱学与光谱分析,2002,22(6):888-890.
[6] 吴东梅,杨佳,汪敬武.固定化酶反应柱联用流动注射化学发光法测定抗坏血酸[J].南昌大学学报:理科版,2007,31(2):147-149,153.
[7] Koshiishi I,Mamura Y,Imanari T.Simult-a eous determination of vitamin C and its carbamylated derivatives by high-performance liquid chromatography with postcolumn derivatization[J]. Journal of Chromatography A,1998,806:340-344.
[8] Romeu-Nadal M,Morera-Pons S,Castellote A I, et al.Rapid high-performance liquid chromatographic method for Vitamin C determination in human milk versus an enzymatic method[J]. Journal of Chromatography B,2006,830:41-46.
[9] 王亚珍,郑武.L-半胱氨酸自组装金电极测定鲜橙多中抗坏血酸的含量[J].化学传感器,2008,28 (3):53-57.
[10] Thangamuthu R,Kumar S M S,Pillai K C. Direct amperometric determination of l-ascorbic acid (Vitamin C)at octacyanomolybdatedoped-poly(4-vinylpyridine)modified electrode in fruit juice and pharmaceuticals[J]. Sensors and Actuators B,2007,120:745-753.
[11] 万其进,喻玖宏,王刚.聚茜素红膜修饰电极控制电位扫描法分别测定多巴胺和抗坏血酸[J].高等学校化学学报,2000,21(11):1651-1654.
RESEARCH ON DETERMINATION OF VITAMIN C BY ULTRAVIOLET SPECTROPHOTOMETRY
HE Bao-shan1,ZUO Chun-yan1,WANG Dan1,WANG Jin-shui2
(1.School of Food Science and Technology,Henan University of Technology,Zhengzhou 450001,China; 2.School of Biotechnology Engineering,Henan University of Technology,Zhengzhou 450001,China)
In this paper,we established a new method for fast detecting vitamin C by using ultraviolet spectrophotometery.Under weak acidic conditions,ferric ion was reduced to ferrous ion by vitamin C,and ferrous ion could react with 1,10-phenanthroline to form an orange-red complex,and the absorbance of the complex at the maximal absorption wavelength of 510 nm was proportional to the mass concentration of vitamin C.The results showed that the absorbance of the complex was in good linear realationship with the mass concentration of vitamin C in the range of 1 to 30 μg/mL,with a correlation coefficient of 0.998,relative standard deviation from 0.3%to 1%, and a recovery from 97.18%to 102.67%.
ultraviolet spectrophotometery;rapid determination;vitamin C;1,10-phenanthroline
TS201.2
B
1673-2383(2012)04-0025-04
http://www.cnki.net/kcms/detail/41.1378.N.20120829.1722.201204.25_006.html
网络出版时间:2012-08-29 05:22:00 PM
2011-10-09
河南省重点科技攻关资助项目(102102310305);河南省教育厅自然科学研究资助项目(2011A550002);郑州市科技攻关资助项目(0910SGYS34370-3);郑州市科技攻关资助项目(2010GYXM482);河南工业大学博士基金资助项目(2009BS009);河南工业大学2010年研究生科技创新基金资助项目(10YJS007)
何保山(1978—),男,河南南阳人,博士,讲师,主要从事食品工程与品质安全控制、传感器技术和仪器仪表分析研究.

