新疆曼陀罗子对大鼠组织匀浆单胺氧化酶及乙酰胆碱酯酶的影响*
热比姑丽·伊斯拉木,阿布都吉力力·阿布都艾尼,尤力都孜·买买提,艾西木江·热甫卡提,闫 明
(1.新疆维吾尔自治区维吾尔医药研究所,新疆 乌鲁木齐 830000;2.新疆维吾尔自治区维吾尔医方剂学实验室,新疆 乌鲁木齐 830049)
用药安全性评价是药物临床前研究和临床评价的重要内容,维吾尔医药针对一些特色制剂及有毒性药材的使用和控制,以及临床前安全评价的研究较为滞后,这影响了维吾尔医药的发展。本研究特别要关注新疆曼陀罗子及其代表制剂镇痛艾比西帕丸在肝脏、肾脏和神经系统的毒性表现,为维吾尔医学常用毒性药材的合理应用提供信息。
1 材料与方法
1.1 材料与仪器
新疆曼陀罗子(亦称原药材,简称生品)由新疆维吾尔自治区维吾尔医医院药厂提供(批号为20090503);曼陀罗子提取物由新疆维吾尔自治区维阿堂药业有限公司提供(批号为20090719);曼陀罗子代表制剂镇痛艾比西帕丸(简称成品)由新疆喀什地区维吾尔医医院提供(新药准字Z04000972,批号为20091072);单胺氧化酶(MAO,批号为20101202),乙酰胆碱酯酶(TChE,批号为20101202),均购自南京建成生物工程研究所。JM31000型电子天平(余姚市纪铭称重校验设备有限公司);GL-16G型冷冻离心机(金坛市华峰仪器有限公司);721型可见分光光度计(上海第三分析仪器厂);CINTRA紫外可见分光光度计(澳大利亚GBC科学仪器设备有限公司)。
1.2 动物
SD大鼠,SPF级,220只,雌雄各半,体重80~120 g,由新疆实验动物研究中心提供,许可证号:SCXK(新)2003-0002。动物合格证号:2010-D3418。
1.3 对大鼠抗氧化指标的影响[3-5]
大鼠观察检疫1周后,按体重性别随机分为6组,分别为空白对照组、曼陀罗子提取物组(低、中、高剂量,分别为每kg含生药 1.55,3.10,6.20 g)、曼陀罗子生品组(每 kg 含生药 3.1 g)、曼陀罗子成品组(镇痛艾比西帕丸,每kg含生药2 g)。每组30只,雌雄各半。给药组(曼陀罗子提取物组、生品组、成品组)以每100 g体重1 mL体积灌胃给予相应的药物,对照组灌胃给予等体积的0.5%羧甲基纤维素钠(CMC-Na)混悬液,连续给药90 d。第91天,动物用乙醚麻醉,每组处死20只(雌雄各半);停药后15 d,每组处死10只(雌雄各半)。肝、肾、脑组织取相同部位,用生理盐水制备10%组织匀浆,用GL-16G型冷冻离心机分离组织,按试剂盒说明书检测大鼠肝、脑、肾组织MAO及TChE水平。
1.4 统计学分析
2 结果
与对照组比较,连续给药90 d内,提取物组(中、雌)肝组织匀浆TChE降低、肾组织匀浆MAO升高(P<0.05),其余组没有统计学差异;停药后15 d内,提取物组(高、雄)和生品组(雄)肝组织匀浆MAO降低(P<0.05),生品组(雌)脑组织匀浆MAO,TChE升高(P<0.05),其余组没有统计学差异。结果见表1和表2。
表1 连续给药90 d内对大鼠肝、脑、肾组织匀浆MAO及TChE指标的影响(±s,U/mgprot)
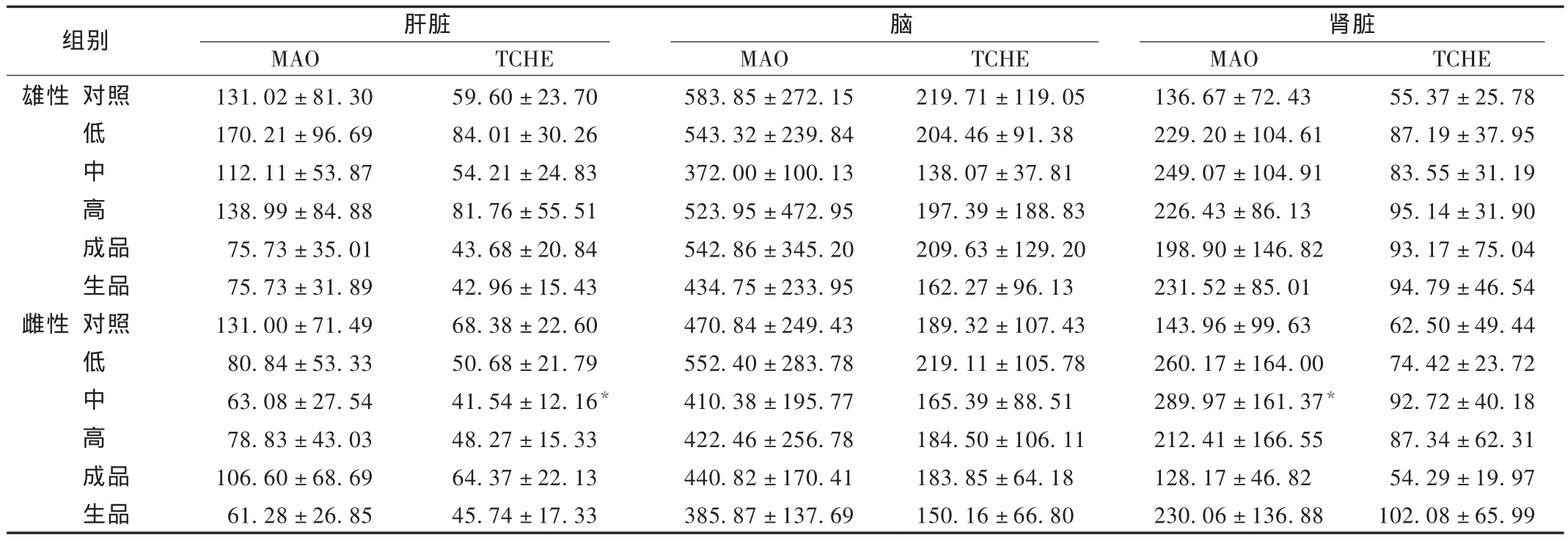
表1 连续给药90 d内对大鼠肝、脑、肾组织匀浆MAO及TChE指标的影响(±s,U/mgprot)
注:与对照组比较,*P <0.05。下表同。
组别 肝脏 脑 肾脏雄性 对照低中高成品生品雌性 对照低中高成品生品MAO 131.02±81.30 170.21±96.69 112.11±53.87 138.99±84.88 75.73±35.01 75.73±31.89 131.00±71.49 80.84±53.33 63.08±27.54 78.83±43.03 106.60±68.69 61.28±26.85 TCHE 59.60±23.70 84.01±30.26 54.21±24.83 81.76±55.51 43.68±20.84 42.96±15.43 68.38±22.60 50.68±21.79 41.54±12.16*48.27±15.33 64.37±22.13 45.74±17.33 MAO 583.85 ±272.15 543.32 ±239.84 372.00 ±100.13 523.95 ±472.95 542.86 ±345.20 434.75 ±233.95 470.84 ±249.43 552.40 ±283.78 410.38 ±195.77 422.46 ±256.78 440.82 ±170.41 385.87 ±137.69 TCHE 219.71±119.05 204.46±91.38 138.07±37.81 197.39±188.83 209.63±129.20 162.27±96.13 189.32±107.43 219.11±105.78 165.39±88.51 184.50±106.11 183.85±64.18 150.16±66.80 MAO 136.67±72.43 229.20±104.61 249.07±104.91 226.43±86.13 198.90±146.82 231.52±85.01 143.96±99.63 260.17±164.00 289.97±161.37*212.41±166.55 128.17±46.82 230.06±136.88 TCHE 55.37±25.78 87.19±37.95 83.55±31.19 95.14±31.90 93.17±75.04 94.79±46.54 62.50±49.44 74.42±23.72 92.72±40.18 87.34±62.31 54.29±19.97 102.08±65.99
表2 停药15 d内对大鼠肝、脑、肾组织匀浆MAO及TChE指标的影响(±s,U/mgprot)
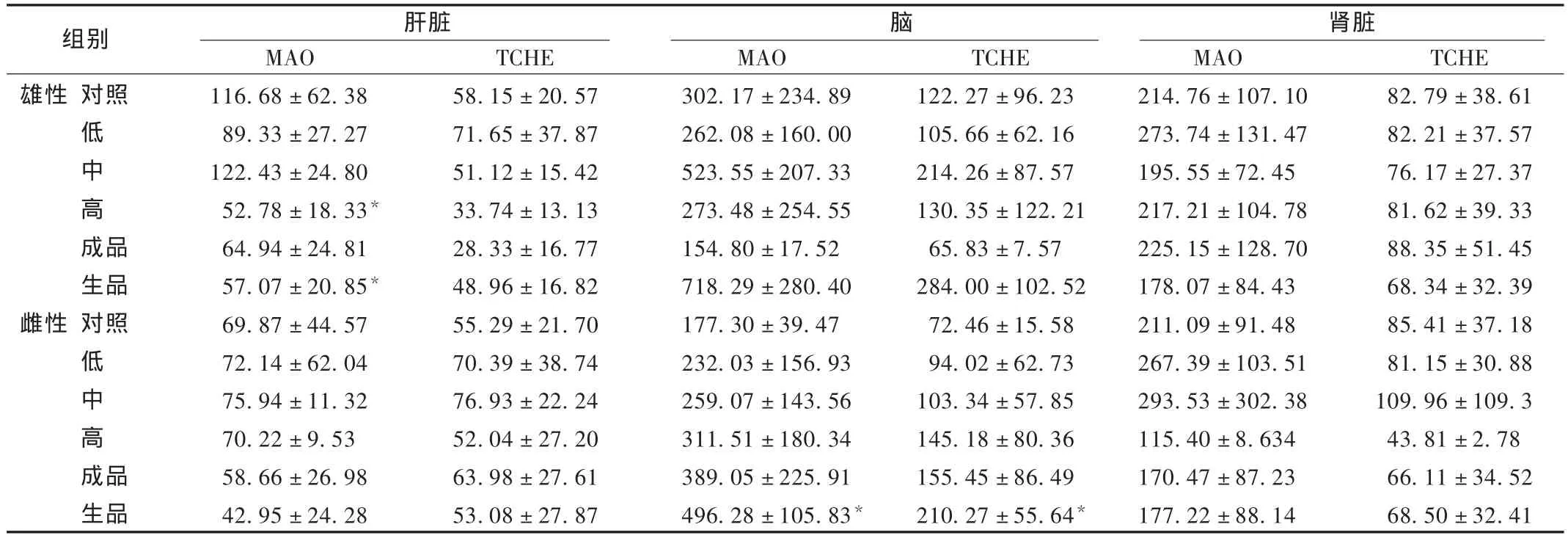
表2 停药15 d内对大鼠肝、脑、肾组织匀浆MAO及TChE指标的影响(±s,U/mgprot)
组别 肝脏 脑 肾脏雄性 对照低中高成品生品雌性 对照低中高成品生品MAO 116.68±62.38 89.33±27.27 122.43±24.80 52.78±18.33*64.94±24.81 57.07±20.85*69.87±44.57 72.14±62.04 75.94±11.32 70.22±9.53 58.66±26.98 42.95±24.28 TCHE 58.15±20.57 71.65±37.87 51.12±15.42 33.74±13.13 28.33±16.77 48.96±16.82 55.29±21.70 70.39±38.74 76.93±22.24 52.04±27.20 63.98±27.61 53.08±27.87 MAO 302.17±234.89 262.08±160.00 523.55±207.33 273.48±254.55 154.80±17.52 718.29±280.40 177.30±39.47 232.03±156.93 259.07±143.56 311.51±180.34 389.05±225.91 496.28±105.83*TCHE 122.27±96.23 105.66±62.16 214.26±87.57 130.35±122.21 65.83±7.57 284.00±102.52 72.46±15.58 94.02±62.73 103.34±57.85 145.18±80.36 155.45±86.49 210.27±55.64*MAO 214.76±107.10 273.74±131.47 195.55±72.45 217.21±104.78 225.15±128.70 178.07±84.43 211.09±91.48 267.39±103.51 293.53±302.38 115.40±8.634 170.47±87.23 177.22±88.14 TCHE 82.79±38.61 82.21±37.57 76.17±27.37 81.62±39.33 88.35±51.45 68.34±32.39 85.41±37.18 81.15±30.88 109.96±109.3 43.81±2.78 66.11±34.52 68.50±32.41
3 讨论
曼陀罗子[6-7],维吾尔药物名衣提·洋克·欧如合,别名节维孜·马斯力,是茄科植物曼陀罗 Datura stramonium L.的干燥成熟种子,药性四级干寒,味辛苦,有毒。最近,笔者分别对新疆曼陀罗子提取物、生品及炮制品进行了急性及亚急性毒性试验研究[8-11]。本试验初步阐明新疆曼陀罗子生品、提取物及其代表制剂镇痛艾比西帕丸对大鼠肝、肾、脑组织匀浆MAO及TChE指标研究。
乙酰胆碱是中枢胆碱能神经系统重要的神经递质,TChE是胆碱能神经递质乙酰胆碱的水解酶,直接参与植物神经功能调节、肌肉运动、大脑思维、记忆等重要功能。TChE活力改变时,以上各组织功能也会改变。MAO在体内分布很广,以肝、肾、脑组织中含量最多。组织中的MAO主要存在于线粒体上,和膜紧密结合。MAO活力改变时,以上各组织功能也会改变。本试验结果显示,与对照组比较,给药组对大鼠肝、脑、肾组织匀浆MAO及TChE影响虽有统计学差异,但其差异没有剂量和时间规律性。因此认为,在本实验条件下,新疆曼陀罗子及其代表制剂镇痛艾比西帕丸对大鼠肝、肾、脑组织匀浆MAO及TChE无明显影响。
[1]朱月琴.洋金花总生物碱提取工艺研究[J].时珍国医国药,2000,11(11):965-966.
[2]肖崇厚.中药化学(生物碱的提取与分离)[M].上海:上海科学技术出版社,2007:93.
[3]袁伯俊,缪明阳,李 波.药物毒理学实验方法与技术[M].北京:化学工业出版社,2007:200-210.
[4]徐叔云,卞如濂,陈 修.药理实验方法学[M].第3版.北京:人民卫生出版社,2003:226-229.
[5]谢秀琼.中药新制剂开发与应用[M].北京:人民卫生出版社,2002:527-535.
[6]易沙克江·马合穆德.中国医学百科全书-维吾尔医学[M].上海:上海科学技术出版社,2005:302-303.
[7]伊德力斯·巴克.中华人民共和国卫生部药品标准-维吾尔药分册[M].乌鲁木齐:新疆科技卫生出版社,1999:95.
[8]李治建,阿布都吉力力,闫 明,等.曼陀罗子提取物小鼠急性毒性实验研究[J].中国民族医药杂志,2010,16(5):41-42.
[9]热比姑丽·伊斯拉木,尤力都孜·买买提,希尔艾力·吐尔逊,等.新疆曼陀罗子炮制前后急性毒性及生物碱含量间的关系[J].中国医药导刊,2010,12(9):1 567 -1 568.
[10]热比姑丽·伊斯拉木,尤力都孜·买买提,艾西木江·热甫开提,等.新疆曼陀罗子炮制品一般毒性研究[J].中国基层医药,2010,17(19):2 595-2 597.
[11]热比姑丽·伊斯拉木,尤力都孜·买买提,买合苏提·卡德尔,等.新疆曼陀罗子急性及亚急性毒性试验研究[J].医药导刊,2010,29(12):1 546-1 548.

