超高效液相色谱质谱法快速检测动物源性食品中的四种兽药残留
沙美兰,曹 鹏,2,*,李金强,王倩倩,关丽丽,牟 妍
(1.烟台出入境检验检疫局,山东烟台 264000;2.山东农业大学食品科学与工程学院,山东泰安271018)
超高效液相色谱质谱法快速检测动物源性食品中的四种兽药残留
沙美兰1,曹 鹏1,2,*,李金强1,王倩倩1,关丽丽1,牟 妍1
(1.烟台出入境检验检疫局,山东烟台 264000;2.山东农业大学食品科学与工程学院,山东泰安271018)
建立了采用超高效液相色谱串联质谱仪快速检测动物组织中甲氧苄胺嘧啶、克林霉素、泰妙菌素和吡喹酮四种药物残留的分析方法。动物组织样品经乙腈提取后,用正己烷去除脂肪等杂质,Waters Acquily UPLC BEH C18色谱柱分离,以乙腈和0.1%甲酸水溶液为流动相进行梯度洗脱,电喷雾正离子(ESI+)模式电离,液相色谱-质谱法(UPLCMS/MS)测定。结果表明:4种药物在2.5~200μg/L范围内呈现良好的线性关系,相关系数R2均大于0.996,在此范围内添加回收率为65.8%~95.9%,相对标准偏差为3.2%~13.1%,定量下限为0.5μg/kg。
超高效液相色谱串联质谱,甲氧苄胺嘧啶,克林霉素,泰妙菌素,吡喹酮,动物源性食品
Abstract:An ultra performance liquid chromatography coulped to tandem mass spectrometry(UPLC-MS/MS)method was established for the determination of trimethoprim,clindymycin,tiamulin and praziquantel residues in animal origin food.The sample was extracted with acetonitrile,purified by hexane,and detected on Waters Acquity UPLC BEH C18column by a gradient elution using acetonitrile(A)—0.1%formic acid(B) as mobile phase with a flow rate of 0.3mL/min.The calibration curves were good linear between the peak areas and concentrations of 4 veterinaries in the range of 2.5~200μg/L,with correlation coefficients more than 0.996.The average recoveries at this concentration levels ranged from 65.8%to 95.9%,the RSD was in the range of 3.2%~13.1%.The limits of quantification of 4 drugs in animal origin food were 0.5μg/kg.
Key words:UPLC-MS/MS;trimethoprim;clindymycin;tiamulin;praziquantel;animal original foods
最近,随着食品安全事件的频繁出现,人们对食品安全也愈发的重视,虽然国家对相关药物做了规范,但是在利益的驱使下,还是有不少滥用抗生素的现象。甲氧苄胺嘧啶、泰妙菌素、吡喹酮和克林霉素这四种药物作为抗生素和抗菌素因其特有的效果,目前已经被广泛应用于畜禽类和水产品的养殖中,主要用于防治呼吸系统疾病和寄生虫疾病中等。但是,人们长期食用含有这些药物残留的食物,会对身体健康带来很大的安全隐患。2010年6月,韩国增加针对水产品的检测项目,新增抗生素类中就包括甲氧苄胺嘧啶(trimethoprim)、克林霉素(clindymycin)、泰妙菌素(tiamulin)、吡喹酮(praziquantel),在鱼类或甲壳类中的限量分别为0.05、0.1、0.1、0.02mg/kg。目前,除了泰妙菌素,其他3种药物分别有相应的国家标准和行业标准[1-3],但是每个项目均为独立的前处理方法和仪器检测方法,并且很多文献报道也仅是局限于一种药物在各种基质中的检测,主要是液相色谱法[4-9]和液相色谱—质谱法[10-14],不能同时、快速的进行分析检测。本实验针对这4种常见药物建立了一种快速、简便、灵敏度高、专属性强的超高效液相色谱-串联质谱(UPLC-MS/MS)方法,对人们的身体健康和控制产品质量具有十分重要的意义。
1 材料与方法
1.1 材料与仪器
甲氧苄胺嘧啶(CAS:738-70-5,99.5%)、泰妙菌素(CAS:55297-95-5,98.5%)、克林霉素(CAS:18323-44-9,99.0%)、吡喹酮(CAS:55268-74-1,99.0%) 均购自德国Dr.Ehrenstorfer;乙腈、甲醇、正己烷 德国默克公司,色谱纯;水 为超纯水;硫酸钠(分析纯)、甲酸(色谱纯)、乙酸铵(色谱纯) 天津科密欧化学试剂有限公司。
Waters Acquity UPLC-Quattro Premier XE,配有电喷雾离子源(ESI)及MassLynx V4.1数据处理系统美国Waters公司;旋转蒸发仪 瑞士BUCHI;超纯水仪 美国Millipore公司;DL-5C离心机 上海安亭科学仪器厂;FJ200-9均质器 上海标本模型厂。
1.2 实验方法
1.2.1 样品制备 鸡肉、猪肉、石鲽鱼、雪蟹取可食用部分用食品搅拌机制成均匀样品,冷冻保存,备用。
1.2.2 标准储备溶液喹酮的配制 分别称取0.0100g标准物质,用乙腈配制成100mg/L的标准储备液,4℃避光保存。
1.2.3 混合标准溶液的配制 准确移取一定量的标准储备液置于容量瓶中,用乙腈与水混合溶液(4∶6,V/V)稀释成适当浓度的标准工作液并定容至刻度线,4℃避光保存。
1.2.4 样品处理 准确称取5.0g(精确至0.01)均质样品、5g无水硫酸钠,置于50mL离心管中,加入20mL乙腈,振荡提取,5000r/min离心5min,上清液转移至125mL分液漏斗中,残渣中加入15mL乙腈,再次提取1次,合并上清液至分液漏斗中。向分液漏斗中加入20mL乙腈饱和的正己烷,振荡摇匀,静置分层,取下层乙腈至鸡心瓶中。40℃水浴条件下旋转蒸发至干,准确加入1mL乙腈/水(4∶6,V/V)含0.1%的甲酸混合溶液,超声使其完全溶解,将溶液转移至2.0mL小离心管中,向其中再加入1mL乙腈饱和正己烷,12000r/min高速离心10min。吸下层过0.22μm的滤膜。
1.2.5 色谱、质谱条件
1.2.5.1 液相色谱条件色谱柱 Waters ACQUITY UPLC BEH C18(2.1mm×50mm,1.7μm);流动相:乙腈(A),0.1%甲酸水溶液(B),梯度洗脱:0~3min,10%A线性变化至90%A,3~4min,维持90%A,4~5min,维持10%A;流速:0.3mL/min;柱温40℃;进样量:2μL。
1.2.5.2 质谱条件 电喷雾离子源(ESI+);毛细管电压为3.0kV;源温120℃;脱溶剂温度为350℃;脱溶剂气流速为600L/h;锥孔反吹气流速为50L/h。多反应监测各离子对及各优化参数见表1。
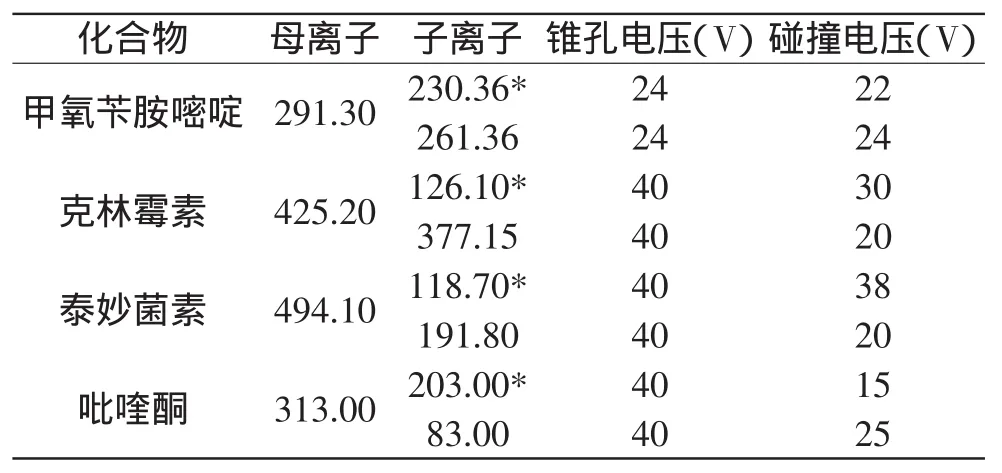
表1 4种药物的多反应监测质谱参数Table 1 MS parameters of MRM mode for 4 drugs
2 结果与讨论
2.1 提取与净化条件的优化
4种药物均为极性物质,对提取液的选择主要集中在乙酸乙酯、二氯甲烷、甲醇、乙腈,经过一系列的实验比较(图1),发现用乙腈提取能满足所有组分回收率在理想范围内,且杂质干扰少,故本方法最终采用常用的试剂乙腈提取,同时达到沉淀蛋白的目的。
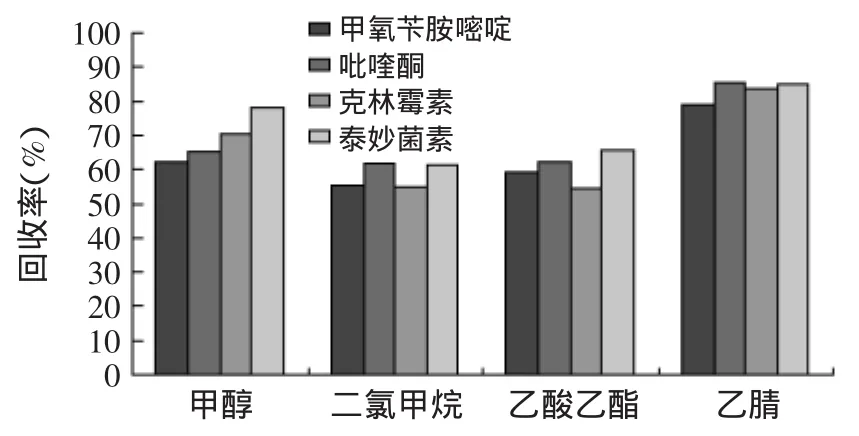
图1 不同提取溶剂下回收率的比较Fig.1 The comparison of recovery with different extraction solvents
净化方法的确定比较了固相萃取小柱和液液分配萃取两种净化方法。采用固相萃取柱对鸡肉、猪肉等动物组织有明显的提取净化效果,但对粘稠性胶体状复杂性样品如鱼、虾等则存在易堵塞、不宜洗脱、操作繁琐、成本较高等问题。本文旨在快速检测,故舍弃固相萃取净化的步骤,而采用正己烷与乙腈液液分配去除脂肪等杂质,定容后再用乙腈饱和正己烷去除油脂等大分子杂质,能有效地消除基质干扰,同时灵敏度也能满足检测需要,提高了工作效率,达到了快速检测的目的。另外,在样品提取过程中,加入无水硫酸钠可以有效防止样品中的水分及干扰成分进入提取液,同时硫酸钠的存在可促使蛋白质变性分散,防止样品形成块状影响提取效率。
2.2 定容液的优化
除了试剂要保证充分提取外,定容液也是一个重要的控制点。4种药物中,除了甲氧苄胺嘧啶的极性较大外,其他3种均为弱极性药物,要同时分析这4种药物,并均获得良好的回收率,首先采用了甲醇+水体系,分别为2+8,4+6,6+4,但这4种药物均洗脱不充分,回收率比较低;之后改用乙腈+水体系,分别为2+8,4+6,6+4。结果表明,乙腈比例低,回收率低;乙腈比例高,甲氧苄胺嘧啶的峰形变差。最终选用乙腈+水(4+6)效果最好,每个组分的峰形和回收率都能达到满意的结果。另外,由于甲氧苄氨嘧啶是强极性物质,含有电负性强的原子,在定容液中加入0.1%的甲酸(体积比),甲氧苄胺嘧啶的回收率有所提高,见图2。
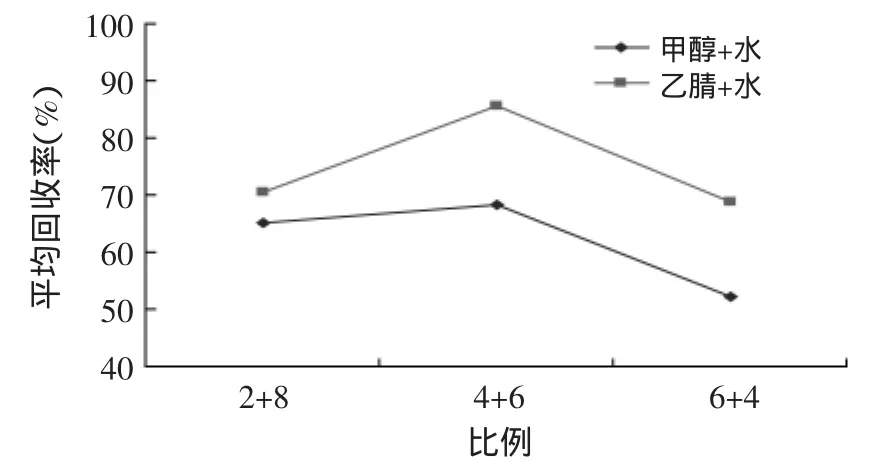
图2 不同定容体系的回收率Fig.2 The recovery of different constant systems
2.3 色谱条件的优化
本实验比较了Waters ACQUITY UPLC HSS T3Column(2.1mm×50mm,1.8μm)、Waters ACQUITY SHIELD RP18Column(2.1mm×50mm,1.7μm)、Waters ACQUITY UPLC BEH C18Column(2.1mm×50mm,1.7μm)三种柱子,发现BEH C18对这4种药物的保留性、灵敏度和峰形都表现出明显的优势。最终选择以BEH C18色谱柱为分离柱。
采用乙腈和0.1%甲酸水溶液为流动相进行梯度洗脱,4种药物均分离良好,峰形尖锐对称,5min内就能完成一个样品的检测,且目标峰没有基质干扰。
乙腈和水是实验室常备试剂,省去了配制流动相的步骤,同时对柱子的损耗也比用盐做流动相要小的多,同时也节省了冲洗柱子的时间,大大提高了工作效率。另外,已有研究表明,在流动相中加入甲酸有利于准分子离子的生成[15],促进化合物的电离,提高灵敏度。
2.4 质谱条件的优化
实验首先采用1mg/L各种药物标准溶液,以蠕动泵进样方式在电喷雾正离子模式下进行母离子全扫描,找出准确的分子离子作为母离子,然后以分子离子为母离子对其子离子进行全扫描,最后选取丰度较强的2个子离子,优化其锥孔电压、碰撞能量等质谱参数。选择丰度较大并且响应稳定的来做定量离子。
2.5 线性范围、标准曲线及定量下限
准确配制2.5、10、20、50、100、200μg/L的系列标准工液,从低浓度到高浓度依次进样。以各药物定量离子的质量色谱峰面积为纵坐标,质量浓度(μg/L)为横坐标,绘制标准曲线,可以看出4种药物在2.5~200μg/L范围内呈现良好的线性关系,相关系数R2均大于0.996,见表2。

表2 4种兽药的线性范围、线性方程及相关系数Table 2 Linear ranges,regression equation and related coefficient for 4 drugs
采用空白组织中添加目标化合物的方法,根据特征离子质量色谱峰信噪比S/N≥10为方法定量下限,得出4种药物在样品(猪肉、鸡肉、石鲽鱼、雪蟹)中的定量下限均为0.5μg/kg。空白鸡肉中添加4种2.5μg/kg标准溶液的特征离子质量色谱图见图3。
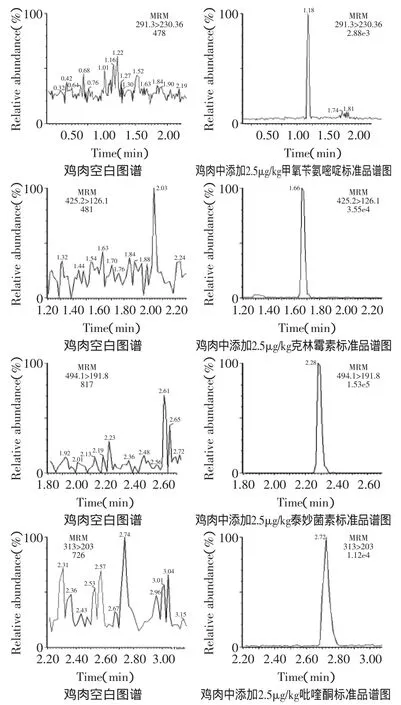
图3 鸡肉样品空白与添加标准品回收的质量色谱图Fig.3 MRM spectra of blank sample of chicken and blank chicken sample with addition of the 4 drugs
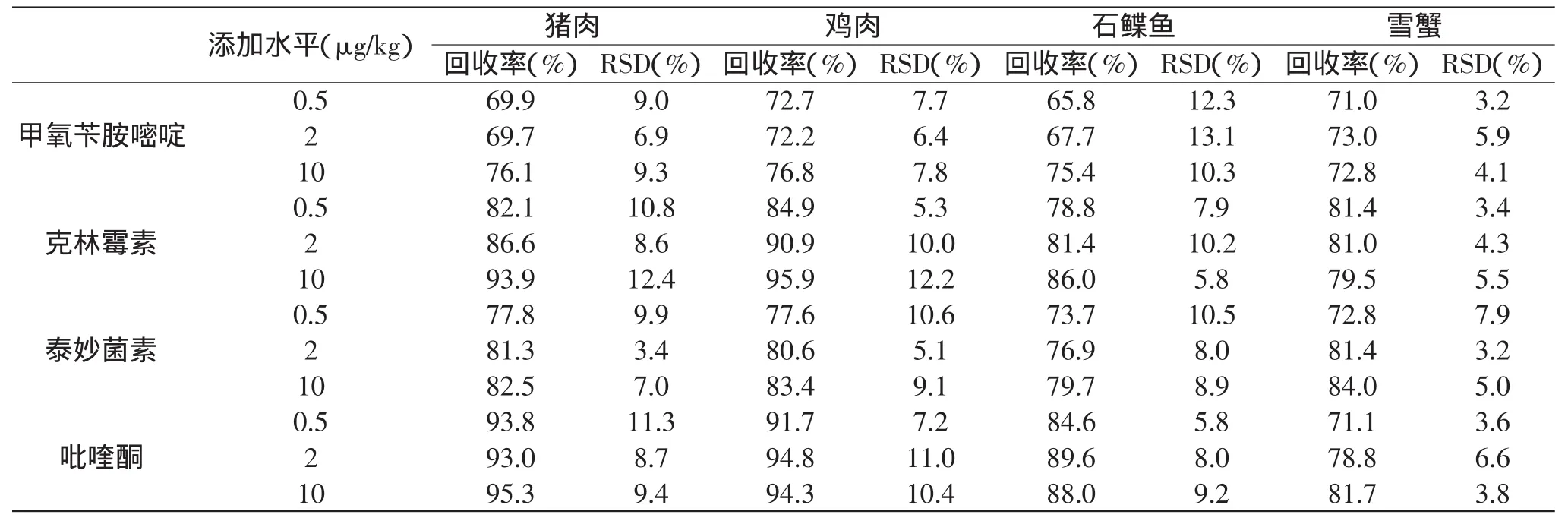
表3 添加回收率的结果(n=5)Table 3 Results of recovery(n=5)
2.6 回收率与重复性
分别对四种基质(猪肉、鸡肉、石鲽鱼、雪蟹)的样品进行了3个水平(0.5、2、10μg/kg)的添加回收实验,每一添加水平重复5次。结果表明,4种药物在空白样品中的平均加标回收率在65.8%~95.9%,相对标准偏差为3.2%~13.1%。符合残留检测方法对回收率与精密度的要求。回收率和相对标准偏差见表3。
3 结论
通过对样品前处理条件的优化和改进,建立了以鸡肉、猪肉、石鲽鱼和雪蟹为代表的动物源性食品中4种常见药物残留检测的UPLC-MS/MS方法。该法前处理简单易操作,分析时间短,5min就能完成一个样品的检测,并且线性范围宽,灵敏度高,检测结果准确,定量限(LOQ)可达到0.5μg/kg,能满足兽药残留高通量分析的要求。
[1]庞国芳,王飞,曹彦忠,等.GB/T 20762-2006畜禽肉中林可霉素、竹桃霉素、红霉素、替米考星、泰乐菌素、克林霉素、螺旋霉素、吉它霉素、交沙霉素残留量的测定液相色谱—串联质谱法[S].中国标准出版社:中国国家标准化管理委员会,2007.
[2]杨长志,康庆贺,马东升,等.SN/T 1769-2006进出口肉及肉制品中甲氧苄胺嘧啶残留量测定方法液相色谱法[S].中国标准出版社:中华人民共和国国家质量监督检验检疫总局,2006.
[3]林峰,林海丹,吴映璇,等.SN/T 1979-2007进出口动物源性食品中吡喹酮残留量检测方法液相色谱—质谱/质谱法[S].中国标准出版社:中华人民共和国国家质量监督检验检疫总局,2007.
[4]王玲,吴晓苹,施点望,等.固相萃取一高效液相色谱法测定鱼组织中吡喹酮和克螨特残留[J].分析实验室,2003,22(11):153-154.
[5]沈晓盛,于慧娟,蔡永琼,等.高效液相色谱法测定水产品中残留的吡喹酮[J].色谱,2007,25(6):861-863.
[6]朱晓华,翁棋兰,王静,等.高效液相色谱同时检测鱼肉组织中4种磺胺与甲氧苄啶的残留量[J].南京农业大学学报,2009,32(4):138-142.
[7]程林丽,张素霞,沈建忠,等.高效液相色谱法快速检测猪组织中泰秒菌素残留[J].分析化学研究简报,2009,37(5):718-720.
[8]刘振伟,姜兆兴,曹旭,等.固相萃取一高效液相色谱法测定动物组织中甲氧苄氨嘧啶及磺胺类药物残留[J].中国动物检疫,2010,27(5):36-38.
[9]童敬,饶钦雄.生物样品中克林霉素检测方法的研究进展[J].中国兽药杂志,2010,44(3):48-51.
[10]余建新,胡小钟,林雁飞,等.尿样及动物组织中甲氧苄氨嘧啶残留量的高效液相色谱-串联质谱测定法[J].分析测试学报,2005,24(3):107-109.
[11]林峰,林海丹,吴映璇,等.动物源性食品中吡喹酮残留量的LC-MS/MS测定[J].分析测试学报,2007,26(5):621-624.
[12]孙雷,张骊,王树槐,等.超高效液相色谱-串联质谱法对动物源食品中13种林可胺类及大环内酯类药物残留的检测[J].分析测试学报,2009,28(9):1058-1061.
[13]唐才明,黄秋鑫,余以义,等.高效液相色谱-串联质谱法对水环境中微量磺胺大环内酯类抗生素、甲氧苄胺嘧啶与氯霉素的检测[J].分析测试学报,2009,28(8):909-913.
[14]王志杰,冷凯良,孙伟红,等.高效液相色谱-串联质谱内标法同时测定水产品中15种喹酮类药物残留量[J].分析科学学报,2010,26(4):409-414.
[15]ARDERY R E.Liquid chromatography—mass spectrometry:An introduction[M].New York:John Wiley&Sons,2003:147-148.
Rapid determination of four veterinary drugs residue in animal products by UPLC-MS/MS
SHA Mei-lan1,CAO Peng1,2,*,LI Jin-qiang1,WANG Qian-qian1,GUAN Li-li1,MU Yan1
(1.Yantai Entry-exit Inspection and Quarantine Bureau,Yantai 264000,China;2.College of Food Science and Engineering,Shandong Agricultural University,Tai’an 271018,China)
TS207.5+3
A
1002-0306(2012)16-0082-04
2011-12-26 *通讯联系人
沙美兰(1981-),女,助理工程师,研究方向:兽残检测。

