不同方法制备阿托伐他汀钙微丸的比较研究
王明浩1,陈 超1,黄春玉2,谢 俊2,汤卫国2,周建平1*
1中国药科大学药剂学教研室,南京 210009;2南京金陵药业股份有限公司技术中心,南京 210009
微丸(Pellet)是一种直径在0.5~1.5 mm范围内的球形或类球形制剂[1],作为一种多单元体系,其具有外形美观、流动性好、胃肠道刺激性小、生物利用度高、装量准确、易制成复方制剂等特点。微丸的制备方法一般有:挤出滚圆法(Extrusion and Spheronization)、 热熔融挤出法(Hot melt extrusion)、层积制丸法(Layering pelletization)(包括溶液载药、混悬液载药以及粉末层积载药)[2]、球形结晶法(Spherical crystallization)等。主要的制丸设备有包衣锅、挤出-滚圆机、离心造粒机、流化床等。
阿托伐他汀(Atorvastatin)作为第二代他汀类药物,是HMG-CoA还原酶抑制剂,其主要以钙盐形式制成制剂[3]。阿托伐他汀钙为白色到类白色晶状粉末,不溶于pH小于等于4的水溶液,微溶于纯化水、pH 7.4的磷酸盐缓冲溶液、乙腈、乙醇,易溶于甲醇[4]。阿托伐他汀钙制剂最早由美国辉瑞公司于1997年上市,目前市场上主要的剂型有普通片、胶囊剂和分散片,尚未见阿托伐他汀钙微丸品种。本文即以水难溶性药物阿托伐他汀钙为模型药物,选用了目前应用比较广泛的3种制丸方法,即:挤出滚圆法、粉末层积法以及混悬液载药法,分别使用挤出-滚圆机、离心造粒机、流化床3台设备制备了阿托伐他汀钙微丸,对比了3种方法的可行性,并对制得微丸的质量做出评价。
1 仪器与试剂
1.1 仪器
E-35A型挤出机、R-250型滚圆机(重庆英格制药机械有限公司);WL-300型离心式制丸机(重庆市科旭制药机械设备制造有限公司);流化床(重庆精工制药机械责任有限公司);电热鼓风干燥箱(上海一恒科学仪器有限公司);紫外可见分光光度计(北京莱伯泰科仪器有限公司);显微镜(Novel公司);CJY-300B片剂脆碎度测试仪(上海黄海药检仪器有限公司);BT-1000粉体综合特性测试仪(丹东百特仪器有限公司);标准检验筛(浙江省上虞市道墟张兴纱筛厂)。
1.2 药品与试剂
阿托伐他汀钙(湖南迪诺制药有限公司);微晶纤维素WJ-102(MCC,安徽山河药用辅料股份有限公司);药用淀粉(江苏昕宇药业有限公司);羟丙甲纤维素E5(HPMC-E5,卡乐康公司);聚山梨酯80(上海申宇医药化工有限公司);蔗糖(嘉兴市白浪淀粉制品有限公司);其余试剂为分析纯。
2 方法与结果
2.1 阿托伐他汀钙体外分析方法的建立
2.1.1 标准曲线的建立 精密称取阿托伐他汀钙对照品适量,置50 mL量瓶中,用适量甲醇溶解,以纯化水稀释备用。精密量取上述溶液适量,用水稀释定容,分别制成阿托伐他汀钙含量为4、6、8、10、12、14 μg·mL-1的对照品溶液,于 244 nm 处测定吸光度,以吸光度A对浓度C做准曲线,回归方程为:A=0.0432C-0.005(r=0.9999)。
2.1.2 含量测定 取阿托伐他汀钙微丸适量,于研钵中研磨至粉状,精密称取细粉适量,置200 mL量瓶中,加适量纯化水,超声后定容,经0.45 μm微孔滤膜过滤,于244 nm处测定吸光度,按标准曲线计算药物含量。
2.2 阿托伐他汀钙微丸的制备
2.2.1 挤出滚圆法制备阿托伐他汀钙微丸 取处方量的阿托伐他汀钙药粉与微晶纤维素及淀粉共200 g,过 100 目筛混合(比例为 1∶3∶6);向混粉中缓慢加入含1%聚山梨酯80的水溶液适量,制得软材;将所得软材经挤出机挤压成形,挤出频率为20 Hz,筛板孔径为0.8 mm;置条形物于滚圆机中抛圆,其中转盘频率为25 Hz,控制风机频率5~15 Hz;将制得微丸置60℃电热鼓风干燥箱中干燥。
微晶纤维素(MCC)用量的考察 MCC被认为是良好的成球促进剂,有“分子海绵”之称。在控制载药量不变的情况下,分别选取了含MCC15%、30%、45%的3个处方制成微丸。结果表明,在MCC含量较低的情况下,软材难于成型,挤出困难或挤出条粘连;当MCC含量较高时,微丸更易制得,且丸芯质量较高,但在烘干后其收缩严重,导致目标粒径下微丸收率下降,综合考虑,选定MCC的量为30%。
润湿剂种类的选择 润湿剂对软材的性质影响较大,进而会影响微丸的质量。分别选择4%的HPMC-E5水溶液、纯化水以及20%乙醇为润湿剂,初步结果显示,HPMC-E5水溶液制得的微丸在滚圆过程中易粘连,烘干后相对较硬,且部分呈椭圆形,圆整度差;而采用20%乙醇溶液制备微丸时,滚圆过程中会形成大量细粉,进而形成小微丸,影响收率。相对来说,以纯化水为润湿剂制得的微丸圆整度更好,且粒径分布均一,微丸收率较高,为此,确定润湿剂种类为纯化水。
2.2.2 离心造粒粉末层积法制备阿托伐他汀钙微丸 取空白丸芯180 g置离心造粒机内,以浓度3%的HPMC-E5水溶液为粘合剂,其中聚山梨酯80含量为3%。调整主机转速为200 r·min-1,风机频率为7 Hz,喷液转速为 18 r·min-1,待丸芯充分润湿后,降低喷液速度至10 r·min-1,同时开始供药粉,转速为5 r·min-1,至 20 g 药粉完全加入,500 r·min-1抛圆1 min,取出制得的微丸,在60℃烘箱中干燥。
供药粉速度的选择 离心造粒过程中关键步骤之一的就是保持喷液与供粉之间的平衡。在固定喷液转速的前提下,分别选择供粉速度为3 r·min-1、5 r·min-1、8 r·min-1,考察了其对微丸制备的影响。结果显示供粉速度过慢微丸间极易粘连聚集,而较高的供粉速率使得操作空间粉尘变大,且部分药粉累积于机器的底盘与外壁上,致使载药效率下降。故实验中选择适中的供粉速度5 r·min-1。
粘合剂种类的选择 对于粉末层积载药来说,粘合剂对最终微丸的质量影响很大。本研究中选择了40%的蔗糖水溶液与3%的HPMC-E5水溶液作比较,发现两者都会使少量药物粘结。在对微丸表面的观察中发现,3%的HPMC-E5水溶液(含3%聚山梨脂80)制得的微丸表面更圆整,光滑。
2.2.3 流化床混悬液载药法制备阿托伐他汀钙微丸 载药工艺采用底喷。取淀粉空白丸芯270 g置流化床中。制备含药量为10%的混悬液300 g,其中聚山梨酯80浓度为1%、HPMC-E5的浓度为3%。在持续搅拌下进行载药,控制物料温度为40~45℃,喷液速度为4 r·min-1,风机频率为19 Hz,雾化压力为1.4 MPa。制得的微丸放置于60℃的烘箱中干燥。
混悬液中药物固态含量的考察 对于混悬液载药,理论上其固体含量可为10%~30%,混悬液中固态含量的浓度可能会影响到载药的效率。考虑到实际情况,分别制备了固态含量为7.5%、10%、12.5%的混悬液,载药后考察其载药效率,结果依次为79.64%、84.75%、81.16%,这表明提高混悬液固态含量并不能提高载药率,而由于混悬液中固态含量的提高,操作过程中喷枪更容易堵塞;对于较低的固态含量,由于喷液量加大,致使操作时间增长,效率降低,故最终选择固态含量为10%的混悬液载药。
混悬液中粘合剂浓度的选择 实验中发现载药过程中会有大量细粉出现,其多为未粘到丸芯上的药粉,故须提高粘合剂浓度。分别考察了粘合剂(HPMC-E5)浓度为3%、4%、5%时制得的微丸的载药率,以期能有所提高。结果显示,3个浓度下载药效率分别为:80.56%、81.02%、79.25%,并未见明显提升,反而由于HPMC-E5浓度的提高,微丸出现较多粘连,致使整体收率下降。故确定粘合剂浓度为3%。
2.3 阿托伐他汀钙微丸的质量评价
依据“2.2”中方法,每种方法重复制备3批微丸,对所得微丸的质量进行评价(见表1)。
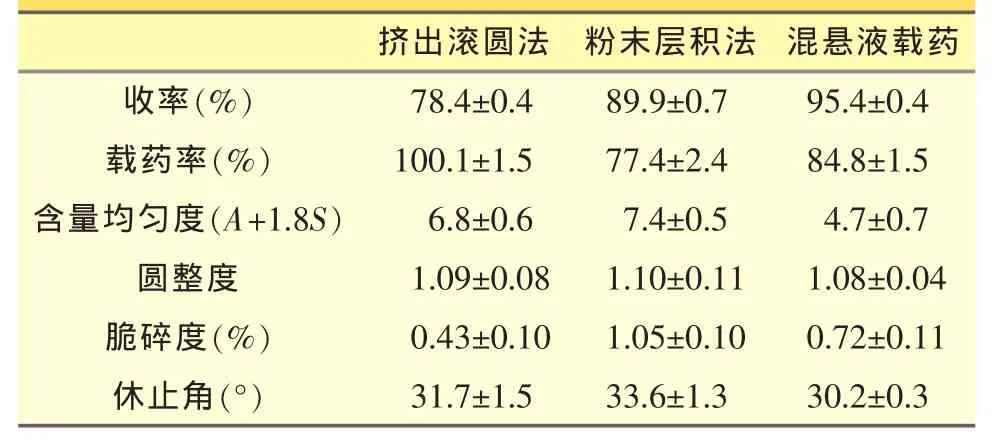
表1 3种方法制备阿托伐他汀钙微丸的质量评价(n=3)
2.3.1 粒径分布与收率 以分样筛筛分所得微丸,选取 18~24 目、24~30 目、30~40 目微丸称重,统计粒径分布百分数并计算目标粒径为24~30目下的微丸收率。可见3种方法中流化床混悬液载药法制得的微丸粒径分布最为集中(见图1),其收率最高;粉末层积法次之,而挤出滚圆法的粒径分布较为分散,且目标粒径下收率明显低于上述两法。
2.3.2 载药率 即微丸的实际含药量与理论含药量的百分比[5]。结果显示,粉末层积法与流化床混悬液载药的载药率均明显小于100%,表明载药过程中会有一部分药物损耗,而粉末层积的载药效率最低,药物损耗最大。
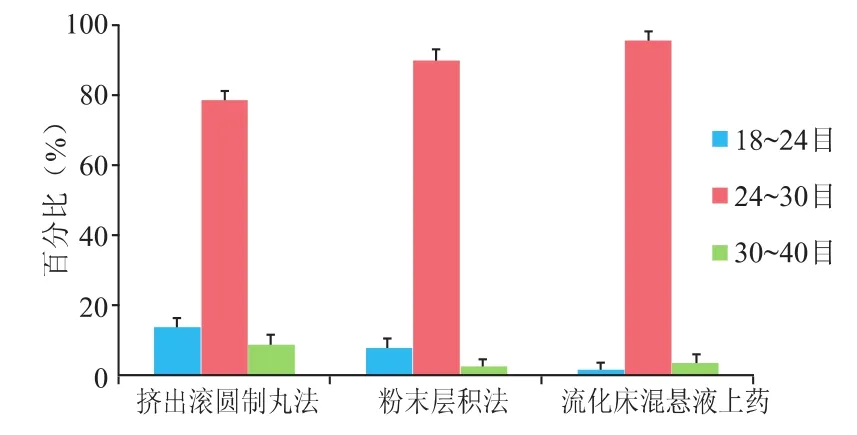
图1 3种方法制备阿托伐他汀钙微丸的粒径分布图
2.3.3 含量均匀度 取微丸适量,分别测定以标示量为100的相对含量X,求其均值和标准差,以及标示量与均值之差的绝对值A,计算A+1.8S值。结果显示,3种方法制得微丸的A+1.8S值均小于15,含量均匀度符合规定要求。
2.3.4 圆整度与表面光洁度 采用Image-Pro Plus 6.0软件,以伸长度为主要指标处理并分析微丸的圆整度[6],在显微镜下观察微丸的表面光洁度。分析结果显示,3种方法下所得的微丸圆整度均较好。表面光洁度的观察结果显示(见图2),粉末层积法制得的微丸表面相对粗糙,凹凸不平;而流化床混悬液载药所得微丸表面也凹凸不平,但好于前者;挤出滚圆所得丸芯的表面最光滑,更适合进一步的包衣操作。

图2 3种方法制备阿托伐他汀钙微丸的显微照片
2.3.5 脆碎度 脆碎度是衡量丸核剥落趋势的指标[7]。取一定量的微丸加入25颗直径7mm的玻璃珠,置于脆碎度仪中旋转10min,用80目筛筛除细粉,计算微丸失重百分率。结果显示3种方法制得的微丸脆碎度均较低,而挤出滚圆法制得的微丸脆碎度最低,质量较好。
2.3.6 休止角 休止角常用来表示粉体的流动性。使用BT-1000型粉体综合特性测试仪测定微丸的休止角。结果显示,流化床混悬液载药制得的微丸的休止角最小,表现出较好的流动性。
3 讨 论
3.1 挤出滚圆制丸法
挤出滚圆制丸法是近年来研究和应用最广泛的制丸方法之一。挤出滚圆法制得的微丸表面光滑,圆整度好,脆碎度低,更重要的是,3种方法中挤出滚圆的操作时间最短,效率更高。但是,在比较中可以发现,挤出滚圆制丸最大的缺陷在于所得微丸粒径分布相对较宽,致使目标粒径下收率较低。这主要是由于挤出滚圆是由软材经挤出再滚圆,制备过程中对丸芯的直径难于有效控制。在生产中通过将“废料”回收后二次挤出滚圆等方法可一定程度上改善收率,使得挤出滚圆法成为更经济可靠的制丸方法。
3.2 离心造粒粉末层积载药
离心造粒粉末层积载药被认为是一种较为先进的制丸技术,目前有多个上市品种应用此法。但此法对粉末的润湿性要求较高。阿托伐他汀钙做为一种水难溶性药物,润湿性相对较差,这就造成在层积过程中粉末未能充分被粘合剂所润湿,药粉难于在丸芯表面铺展,进而造成部分药粉粘于底盘和侧壁,最终影响载药效率。同时粉末的粒径不够细也影响了微丸表面的光洁度。笔者在对一些润湿性较好的药物研究中发现,制得的微丸质量均较为理想,并未出现上述问题。总体说来,该方法操作时间较短,且操作简便,但对于润湿性较差的药物,相对其他制丸方法使用离心造粒粉末层积载药难于制得高质量的微丸,而改善药物的润湿性以及挑选合适的粘合剂将会是研究的重点。
3.3 流化床混悬液载药
流化床混悬液载药与离心造粒粉末层积法同属于层积载药法,可以发现由于丸芯处于流化床中相对比较密闭的空间且其干燥效率更高,因而流化床的收率和载药效率也较高。而由于两者均是依靠粘合剂将药物粉末粘于丸芯表面,则影响了微丸表面的光洁度,同时也升高了脆碎度。对于流化床混悬液载药法,最大的问题在于其操作时间较长,并且为保证操作过程中不堵液,混悬液的配制方法也较为繁琐。但是,该法仍有较大的改进空间,流化床混悬液载药是一种很有潜力的微丸载药方法。
阿托伐他汀钙微丸采用上述3种制备方法,均能制得质量良好,适合工业化生产的微丸。以挤出滚圆制丸法和流化床混悬液载药法的优势更明显。在具体的生产过程中,可根据实际情况选择合适的制丸方式。
[1]平其能,胡一桥,周建平,等.现代药剂学[M].北京:中国医药科技出版社,1998:551-3.
[2]Vikash K,Kumar MS,Amit L,et al.Multiple unit dosage form-pelletand pelletization techniques∶An overview[J].IJRAP,2011,2(1)∶121-5.
[3]Lennernas H.Clinical pharmacokinetics of atorvastain[J].Clin Pharmacokinet,2003,42(13)∶1141-60.
[4]Kim MS,Jin SJ,Kim JS,et al.Preparation,characterization and in vivo evaluation of amorphous atorvastatin calcium nanoparticles using supercritical antisolvent(SAS)process[J].Eur J Pharm Sci,2008,69(2)∶454-65.
[5]陈 挺,陈庆华.盐酸苯丙醇胺微丸的制备工艺研究[J].中国医药工业杂志,1999,30(8):345-8.
[6]方 昀,张钧寿,周建平.应用图像分析优化微丸挤出滚圆工艺参数[J]. 药学与临床研究,2009,17(5):382-5.
[7]王晓丽,李晓明,刘吉成.离心造粒法制备盐酸二甲双胍微丸[J]. 医药导报,2008,27(9):1092-4.

