过渡金属氧化物掺杂 Ce0.8Nd0.2O1.9固体电解质的结构和电性能
周德凤, 刘建伟, 杨国程, 李朝辉, 罗 飞
(长春工业大学 化学与生命科学学院,吉林 长春 130012)
0 引 言
CeO2基电解质在中低温(500~800℃)条件下比YSZ(氧化钇稳定氧化锆)有更高的离子电导率,被认为是最有希望的中温固体电解质材料。在CeO2中掺入三价稀土金属氧化物或二价碱土金属氧化物,通过电荷补偿可以产生氧空位而使其浓度增加,进而提高其离子电导率,并且增加CeO2基电解质的稳定性[1-2]。但是 CeO2基电解质存在的问题之一是在1500℃以下很难致密化[3]。高的烧结温度可引起电解质和电极之间的原子扩散,不但会影响电极与电解质的接触面,甚至会影响整个电解质层,导致电池性能下降[4]。在CeO2基电解质中加入少量的过渡金属氧化物(Transitional Metal Oxides ,TMOs)如MnO2[5-6],Fe2O3[7-8]或 CoO[9-10]可降低体系的烧结温度。如Zheng[8]等 在 Ce0.8Sm0.2O1.9掺杂1.5% (x)FeO1.5,可使烧结温度降低约100~150℃,有效地提高材料总电导率;在Gd0.1Ce0.9O2-δ中 加 入1%(x)CoO,可使烧结温度从1400~1550℃降到950~1200℃,600℃的电导率约为0.01s·cm-1[10];在纯CeO2中掺杂1% (x)MnO2,使烧结温度降低约 200 ℃[6]。然而,TMOs对Nd2O3掺杂CeO2(NDC)体系影响的研究还很缺乏。文中将1%(x)MnO2,Fe2O3和CoO分别掺杂到NDC体系中,比较不同过渡金属掺杂对NDC体系致密度、微观结构和导电性能的影响。
1 实验部分
1.1 材料的制备
以分析纯 Ce(NO3)3·6H2O(99.9%(ω,下同))和高纯 Nd2O3(99.99%,上海国药集团)作为起始原料,按化学计量比 Ce0.8Nd0.2O1.9(NDC)精确称量以上原料,Nd2O3用硝酸溶解,加入柠檬酸和无水乙醇,分别称取相应质量的C4H6MnO4·4H2O(≥99.0%),Fe(NO3)3·9H2O(≥98.5%)和Co(CH3COO)2·6H2O(≥99.5%)加入到上述溶液中,30~40℃加热搅拌使溶液混合均匀,然后水浴加热(70~80℃)蒸发约12h形成凝胶,在电磁炉上翻炒直至自然生成蓬松的粉末。将粉末在550℃预烧10h,除去残留的有机物。然后将上述粉末在玛瑙研钵中研磨成很细的粉末,在压力约为10MPa下压成直径约13mm、厚度约1.2mm的圆片,在1300℃烧结6h得到陶瓷样片。样品分别标记为NDC(Ce0.8Nd0.2O1.9),NDC+1MnO2(NDC+1%(x)MnO2),NDC+1FeO1.5(NDC+1%(x)FeO1.5)和NDC+1CoO(NDC+1%(x)CoO)。样片经抛光清洗后,两面涂上银浆,700℃加热30min,进行导电性能测试。阿基米德方法测试样品的实际密度。
1.2 材料的表征
通过日本理学D/MAX2000/PC型X射线衍射仪测定样品的XRD图谱,Cu Ka1为发射光源,扫描范围在20°~100°,速度为5°·min-1;Philips XL-30场发射扫描电子显微镜(FE-SEM)(日本)观测样品的微观结构;使用美国PARSTAT公司的2733电化学工作站测定样品在300~800℃的阻抗谱图(升温,间隔为50℃),频率范围0.1Hz~1.0MHz,交流微扰电压为10mV,温度由UGB2805型自控温度仪控制。用ZSimpWin软件计算电阻,模拟阻抗谱图。
2 结果与讨论
2.1 XRD分析
1300℃烧结6h的XRD谱图如图1所示。
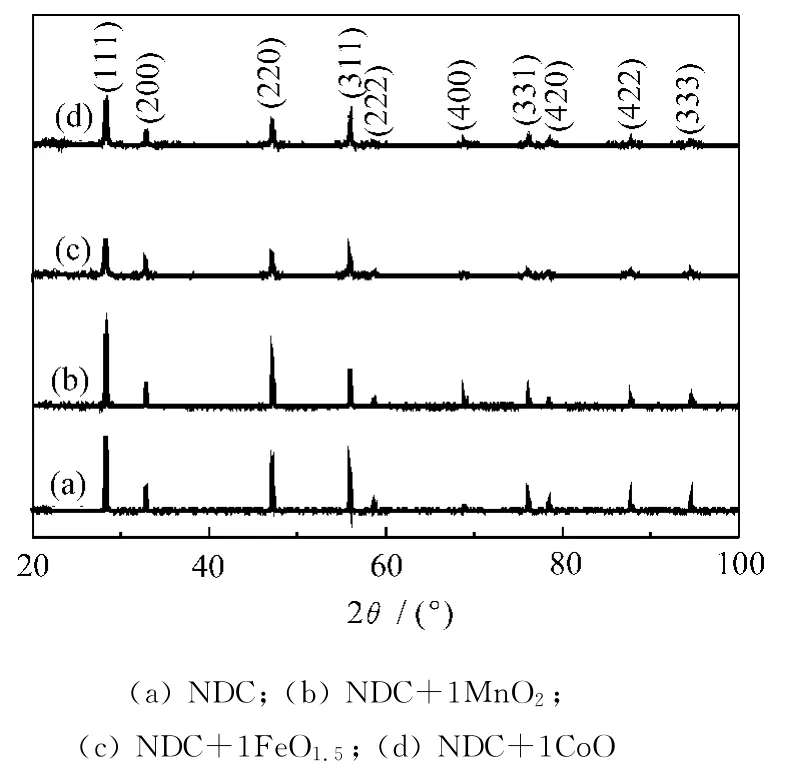
图1 样品于1300℃烧结6h的XRD谱图
图1是样品在1300℃烧结6h的XRD谱图,从图中可以看出,所有样品均呈现单一的立方萤石结构,没有观察到第二相,说明1%(x)TMOs的加入没有改变NDC的立方萤石结构。
2.2 致密度分析
掺杂TMOs与无掺杂样品的密度见表1。
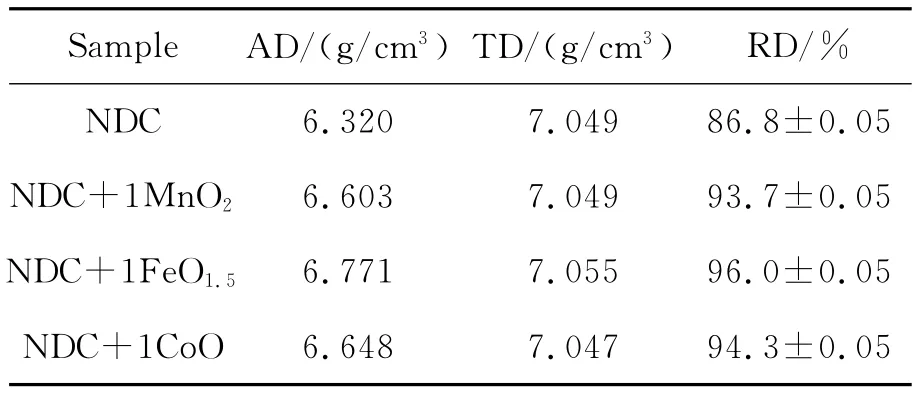
表1 样品在1300℃烧结6h的相对密度
采用阿基米德排水法测试样品的实际密度(AD),Jade软件分析XRD数据获得样品的理论密度(TD),实际密度与理论密度的比值为样品的相对密度(RD)。从表中可以看出,掺杂TMOs样品的相对密度(>93%)均大于无掺杂NDC样品(86.8%)。由此说明,在NDC中掺杂1%(x)的TMOs有助于样品致密化,降低烧结温度。主要原因是TMOs改变了CeO2的早期烧结机制。即在低温(<1350℃)烧结时,TMOs很容易在晶粒表面扩散,在晶粒之间形成一层很薄的非晶质膜[11]。晶粒的重排程度取决于晶粒之间的摩擦力,而TMOs形成的这层薄膜会减小粒子间的摩擦力,有利于晶粒发生重排,加速了烧结过程。另外,也增加了晶粒表面之间的接触,促进晶粒间的质量扩散,使样品进一步致密化。
2.3 FE-SEM 分析
由烧结样品的场发射扫描电子显微镜图如图2所示。
纯体系NDC样品的晶粒(图2(a))排列不整齐,而且有很多张开的气孔。在同样条件下,NDC+1%(x)TMOs体系晶粒比纯体系NDC的晶粒大(图2(b)、图2(c)和图2(d)),并且排列整齐致密,气孔消失。说明少量TMOs加入NDC体系可促进材料致密化,降低烧结温度,具有烧结助剂的作用。这主要是因为TMOs会改变晶粒表面的张力和摩擦力,促进晶粒重排,即发生粘性流动机制[12],加速了晶粒之间的质量扩散,使晶粒加快生长,致密度增加(见表1)。

图2 样品于1300℃烧结6h的场发射扫描电镜图
2.4 交流阻抗谱图分析
理想的阻抗谱图由3个半圆弧组成[13],由左向右第一个半圆弧(高频)对应晶粒电阻(Rgi),中间的半圆弧对应晶界电阻(Rgb),第三个半圆弧(低频)对应极化电阻(Rel)。由于仪器有限的频率范围以及晶粒、晶界电阻随温度的变化不同,实际测量中会出现不同的谱图。
350℃空气中测试1300℃烧结6h样品的阻抗谱图如图3所示。
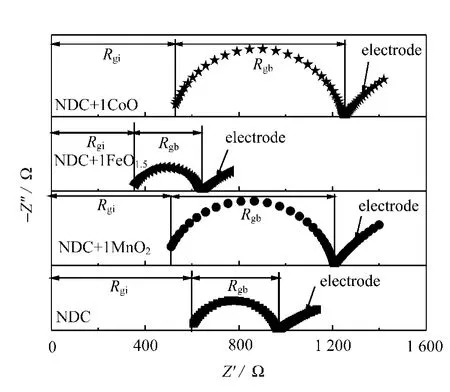
图3 在350℃空气中测试1300℃烧结6h样品的阻抗谱图
所有阻抗谱图均由1个圆弧和1小段弧组成。交流阻抗谱图中圆弧的起点与实轴的交点即代表样品的晶粒电阻Rgi,圆弧低频端与实轴的交点坐标即为样品的总电阻Rtol(Rtol=Rgi+Rgb,Rgb为晶界电阻)。采用ZSimpWin阻抗分析软件对样品的阻抗谱图进行拟合分析,得到350℃测试样品的电阻值见表2。
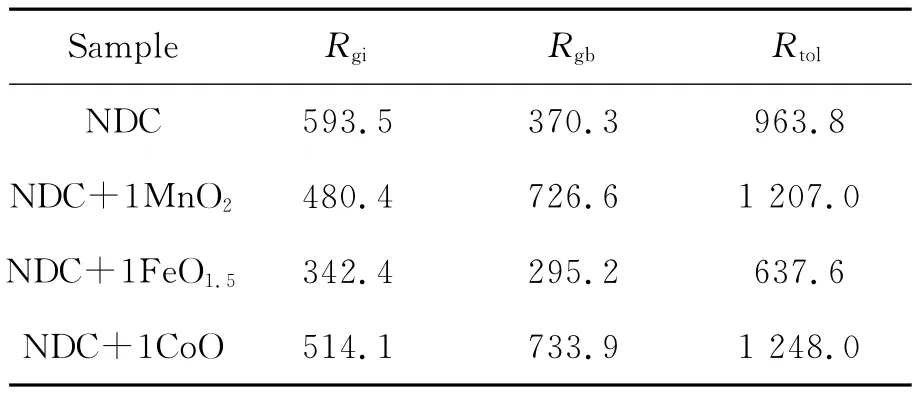
表2 1300℃烧结6h的样品在350℃测试的电阻值Ω
结合图3和表2可以看出,与无掺杂的NDC晶粒电阻(593.5Ω)相比,掺杂1%(x)MnO2(480.4Ω),1%(x)FeO1.5(342.4Ω)或 1%(x)CoO(514.1Ω)的样品均不同程度地减小晶粒电阻(见表2),这主要与样品的致密度有关。因为NDC样品有很多的气孔(图2a),这些气孔会阻碍氧离子的穿过,增大晶粒电阻。而TMOs的掺杂改变了晶粒表面的摩擦力,促进晶粒长大,排除大部分气孔(见图2),同时致密度增加,因而晶粒电阻减小。样品 NDC+1MnO2(726.6Ω)或NDC+1CoO(733.9Ω)的晶界电阻有所增加,分别是NDC(370.3Ω)的1.96和2倍,而 NDC+1FeO1.5(295.2Ω)的晶界电阻却小于 NDC(见表2),说明MnO2或CoO与Fe2O3的掺杂对材料晶界的影响不同。具体原因在电性能分析中详细讨论。
2.5 电性能分析
样品的晶粒电导率和总电导率与温度的阿仑尼乌斯关系如图4所示。

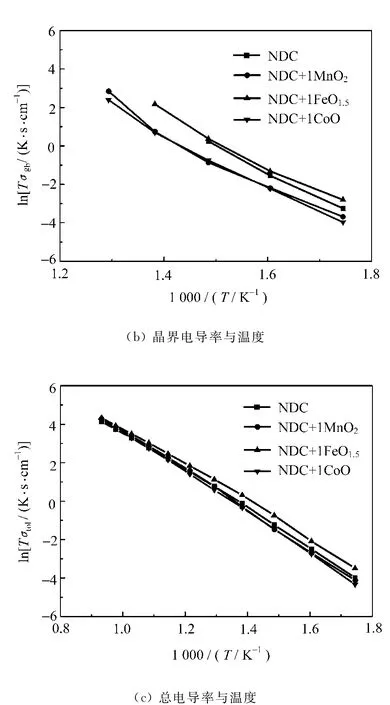
图4 样品的阿仑尼乌斯曲线
样品电导率和电导激活能值见表3。
由图4(a)和表3可知,掺杂 MnO2,Fe2O3或CoO样品NDC+1%(x)TMOs的晶粒电导率高于NDC样品。晶粒电导率的提高主要是因为TMOs的掺杂提高了样品的致密度。TMOs在烧结时易在晶粒表面扩散,改变晶粒之间的表面张力和摩擦力,从而使晶粒发生重排,同时,加速晶粒之间质量扩散,促使晶粒长大(图2(b),(c)和(d)),排除部分气孔,提高致密度,因此晶粒电阻减小,晶粒电导率提高。另外,在NDC样品中掺杂MnO2,Fe2O3或CoO后样品在300~800℃的晶粒电导激活能略有降低也是晶粒电导率提高的一个原因(见表3)。其中 NDC+1(x)%FeO1.5有最大的相对密度和最低的晶粒电导激活能(0.75eV),因而有最大晶粒电导率。300℃时,NDC+1%(x)FeO1.5(0.106×10-3s·cm-1),NDC+1%(x)MnO2(0.813×10-4s·cm-1)和NDC+1%(x)CoO(0.724×10-4s·cm-1)的晶粒电导率分别是NDC(0.628×10-4s·cm-1)晶粒电导率的1.69,1.29和1.15倍。

表3 样品的电导率a和电导激活能b值
MnO2,Fe2O3或CoO掺杂于NDC体系对晶界的影响有明显的不同(见图4(b)和表3)。掺杂MnO2或CoO样品的晶界电导率小于纯体系NDC,而掺杂Fe2O3样品的晶界电导率却略高于纯体系NDC。这是因为MnO2或CoO掺杂会促进杂质 SiO2在晶界传播[14-15],而 Fe2O3会抑制SiO2在晶界的传播。CeO2固溶体中的晶界杂质SiO2主要是来源于前驱体材料和材料制备过程中引入。SiO2在烧结过程中晶粒表面形成非晶质薄膜,阻碍了氧离子穿过晶界,致使晶界电阻增大,晶界电导率降低。由于MnO2或CoO在低温(<1350℃)时会与SiO2形成粘性物质,促进SiO2的扩散,影响氧离子在晶界的传导,对晶界电导率产生消极的影响[16-17],这种消极影响会因SiO2含量的增大而更加明显[16]。掺杂Fe2O3样品的晶界电导率略高于NDC,是因为加入的Fe2O3会改变SiO2玻璃相的湿润性质,抑制晶界SiO2扩散形成SiO2薄膜[18],对杂质SiO2有一定的清除作用,晶界电导率略有提高(图4b)。在300℃时,NDC+1%(x)FeO1.5的晶界电导率(0.106×10-3s·cm-1)是 NDC 晶界电导率(0.672×10-4s·cm-1)的1.58倍;而 NDC+1%(x)MnO2(0.440×10-4s·cm-1)和 NDC+1%(x)CoO(0.329×10-4s·cm-1)的晶界电导率与NDC的晶界电导率相比分别减小了34.5%和51%。
所有样品在300~800℃温度区间的总电导率出现线性分段关系(见图4(c))。由表3可知,在300~450℃的总电导激活能都大于在450~800℃温度区域的总电导激活能。这是因为材料中的氧空位达到一定浓度时,固溶过程中产生的 Nd′Ce和氧空位会由于静电吸引力形成缔合缺陷 Nd′Ce·。在低温(300~450 ℃)范围内,缔合状态下的氧空位迁移需打开缔合缺陷,电导激活能包括氧空位的解缔能和迁移能,因此电导激活能较高;而在高温(450~800℃)范围内,缔合缺陷体被解缔释放出氧空位,进而电导激活能主要是氧空位的迁移能,因此,电导激活化能比低温时低。在整个温度范围内,NDC+1(x)%FeO1.5有最高的总电导率和最低的总电导激活能。是因为Fe2O3掺杂于NDC样品不仅提高晶粒电导率,而且清除了晶界杂质SiO2的有害影响,在一定程度上增加了晶界电导率。在300℃时,NDC+1%(x)FeO1.5的总电导率(0.531×10-4s·cm-1)是无掺杂 NDC总电导率(0.324×10-4s·cm-1)的1.64倍。而MnO2或CoO的掺杂虽然在一定程度上提高了NDC的晶粒电导率,却很大程度地减小了晶界电导率,晶粒电导率和晶界电导率的共同影响导致NDC+1%(x)MnO2(0.285×10-4s·cm-1)和NDC+1%(x)CoO(0.226×10-4s·cm-1)的总电导率略低于NDC的总电导率。
3 结 语
用溶胶凝胶法成功地合成了掺杂与无掺杂1%(x)TMOs的NDC电解质材料。发现MnO2,Fe2O3和CoO均具有烧结助剂的作用,促进了电解质材料的致密化,在1300℃烧结6h的相对密度可达93%以上。在NDC体系中加入1%(x)MnO2或 1%(x)CoO 促进了晶界杂质SiO2的传播,对氧离子在晶界的传导产生一定的消极影响,导致NDC+1%(x)MnO2和NDC+1%(x)CoO在300~450℃温度区间的总电导率略低于NDC。而1%(x)FeO1.5加入NDC体系可抑制晶界杂质SiO2的传播,体系的晶界电导率略有提高。NDC+1%(x)FeO1.5具有最高的总电导率和最低的总电导激活能。在300℃时,NDC+1%(x)FeO1.5总电导率是 NDC 的 1.64 倍。Fe2O3具有烧结助剂和晶界清除剂的双重作用。
[1]Yan D T,Liu X M,Bai X Y,et al.Electrical properties of grain boundaries and size effects in samarium-doped ceria[J].Power Sources,2010,195:6486-6490.
[2]Molenda J,Swierczek K,Zajac W.Functional materials for the IT-SOFC[J].Power Sources,2007,173:657-670.
[3]Yahiro H,Eguchi K,Arai H,et al.High temperature fuel cell with ceria-yttria solid electrolyte[J].Electrochem.Soc.,1988,135:2077-2080.
[4]Yoshida H,Inagaki T.Effects of additives on the sintering properties of samaria-doped ceria[J].Alloy.Compd.,2006,632:408-412.
[5]Park S H,Yoo H I.Defect-chemical role of Mn in Gd-doped CeO2[J].Solid State Ionics,2005,176:1485-1490.
[6]Zhang T S,Hing P,Huang H,et al.Sintering study on commercial CeO2powder with small amount of MnO2doping[J].Mater.Lett.,2002,57:507-512.
[7]Zajac W,Suescun L,Sweierczek K,et al.Structural and electrical properties of grain boundaries in Ce0.85Gd0.15O1.925solid electrolyte modified by addition of transition metal ions[J].Power Soures,2009,194:2-9.
[8]Zheng Y F,Zhou M,Ge L,et al.Effect of Dy on the properties of Sm-doped ceria electrolyte for ITSOFCs[J].Alloy.Compd.,2011,509:1244-1248.
[9]Ayawanna J,Wattanasiriwech D,Wattanasiriwech S,et al.Effects of cobalt metal addition on sintering and ionic conductivity of Sm(Y)-doped ceria solid electrolyte for SOFC[J].Solid State Ionics,2009,180:1388-1394.
[10]Han M F,Zhou S,Liu Z,et al.Fabrication,sintering and electrical properties of cobalt oxide doped Gd0.1Ce0.9O2-δ[J].Solid State Ionics,2011,192:181-184.
[11]Bonnet J P,Dolet N,Heiz J M.Low-temperature sintering of0·99SnO2-0·01CuO:Influence of copper surface diffusion[J].Eur.Ceram.Soc.,1996,16:1163-1169.
[12]Zhang T S,Hing P,Huang H T,et al.Earlystage sintering mechanisms of Fe-doped CeO2[J].Mater.Sci.,2002,21:75-77.
[13]Zhang T S,Ma J,Chen Y Z,et al.Different conduction behaviors of grain boundaries in SiO2-containing 8YSZ and CGO20electrolytes[J].Solid State Ionics,2006,177:1227-1235.
[14]Zhang T S,Kong L B,Zeng Z Q,et al.Sintering behavior and ionic conductivity of Ce0.8Gd0.2O1.9with a small amount of MnO2doping[J].Solid State Electrochem.,2003,7:348-354.
[15]Zhang T S,Du Z H,Li S,et al.Transitional metal-doped 8mol%yttria-stabilized zirconia electrolytes[J].Solid State Ionics,2009,180:1311-1317.
[16]Zhang T S,Ma J,Leng Y J,et al.Effect of transition metal oxides on densification and electrical properties of Si-containing Ce0.8Gd0.2O1.9ceramics[J].Solid State Ionics,2004,168:187-195.
[17]Appel C C,Bonanos N.Structural and electrical characterisation of silica-containing yttria-stabilised zirconia[J].Eur.Ceram.Soc.,1999,19:847-851.
[18]Zhang T S,Ma J,Luo L H,et al.Preparation and properties of dense Ce0.9Gd0.1O2-δceramics for use as electrolytes in IT-SOFCs[J].Alloy.Compd.,2006,422:46-52.
- 长春工业大学学报的其它文章
- 畸变图像拼接算法研究
- 氩氧精炼低碳铬铁过程喷溅预报及控制

