肝移植患者乙肝免疫球蛋白血药浓度回顾性分析
郭媛媛,张建军,朱志军,郑虹,沈中阳,张弋#(1.天津医科大学第一中心临床医院,天津300070;.天津市第一中心医院,天津 30019)
近年来临床应用乙肝免疫球蛋白(HBIG)联合拉米夫定(LAM)预防肝移植后乙肝复发效果显著[1]。目前,全世界已广泛联用这2种药预防肝移植后乙肝再复发。但HBIG使用剂量并没有规定的标准,且在不同地区应用情况各不相同[2]。又因该药个体差异较大,不同医院通过定期进行血药浓度监测,控制HBIG滴度在有效范围内以调整用量。本研究对HBIG治疗的30例肝移植患者进行常规HBIG滴度监测,并按术前乙肝病毒核酸定量(HBV-DNA)及乙肝病毒e抗原(HBeAg)情况进行分组,分别考察HBIG用量、滴度及乙肝表面抗原(HBsAg)阴转率的关系。
1 资料与方法
1.1 入选标准和排除标准
入选标准:在天津市第一中心医院首次行肝移植手术的中国籍患者,没有合并其他移植。年龄18~70岁,性别不限。术前诊断均为乙肝相关性终末期肝病且术前血清HBsAg阳性。采用他克莫司+吗替麦考酚酯+强的松三联免疫抑制方案。常规检查供体的血清病毒学及肝脏活检,结果均为阴性。
排除标准:血清乙肝表面抗体(HBsAb)阳性,对人免疫球蛋白过敏。考虑到影响正常服用药物的一些因素,故将有明显精神障碍(肝性脑病除外)、癫痫患者或患有神经性厌食症、吸收不良综合征或胃肠切除术等患者排除在外。
1.2 研究对象
严格依据入选及排除标准,从2005年11月-2007年1月行肝移植手术的患者中筛选出30例。其中男性22例,女性8例,年龄(53.40±8.30)岁(32~68岁),体重(68.82±12.02)kg。肝移植患者术前基本资料统计见表1。

表1 肝移植患者术前基本资料统计Tab 1 General information of liver transp lantation patient before operation
1.3 方法
30例肝移植患者均在术中无肝期静脉注射(iv)HBIG 5 000 IU,术后第1周每天1 000 IU,以后每周iv HBIG 1次,每次1 000 IU,3周;以后改为每个月iv HBIG 1次,每次1 000 IU,并给予LAM每日100mg,配合他克莫司+吗替麦考酚酯+强的松三联免疫抑制方案。有文献表明,HBeAg(+)或HBV-DNA(+)是乙肝病毒处于高复制状态的标志[3],而HBV-DNA>103拷贝·m L-1是阳性界值。因此,根据术前HBV-DNA及HBeAg水平将患者分为2组:术前HBV-DNA(+)和(或)HBeAg(+)为高复制组,术前HBV-DNA(-)且HBeAg(-)为低复制组,并在术后定期监测患者HBIG滴度及HBsAg阴转率等。
1.4 统计方法
用SPSS 16.0软件包进行统计学处理。计量数据均用±s表示,单样本资料的分布特征用K-S检验,组间计量资料均数比较用单因素方差分析(One-Way Anova);计数资料率的比较用行列表卡方检验。P<0.05为差异有统计学意义。
2 结果
2.1 术后不同时间点HBIG滴度定量分析
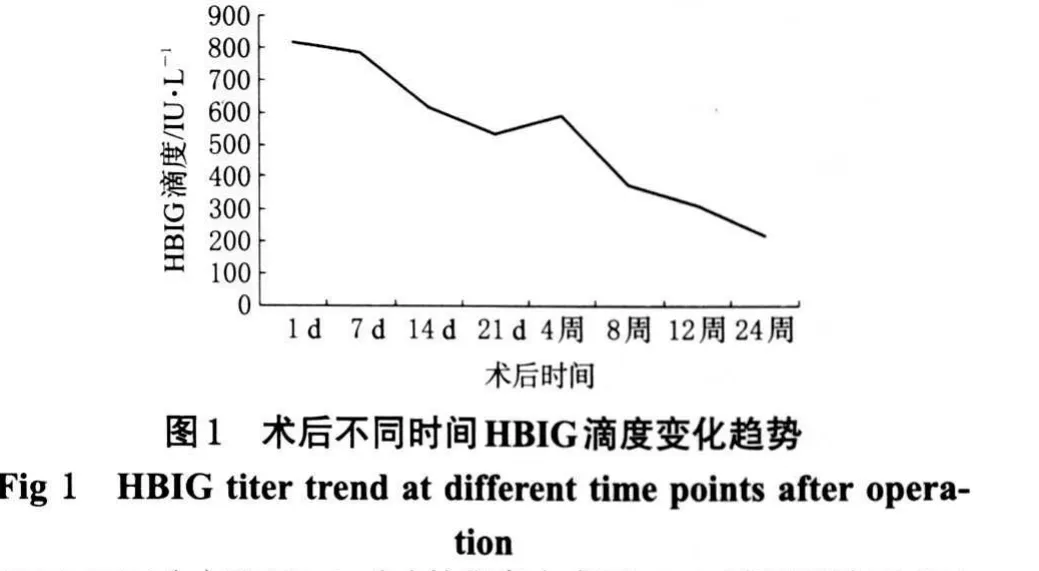
为减少乙肝复发,血清中需保持一定的抗体滴度,移植术后2周>500 IU·L-1,术后1个月>200 IU·L-1,以后维持在100 IU·L-1以上[4]。30例肝移植患者术后1 d HBIG累积用量为6 000 IU,HBIG的平均滴度水平已达到500 IU·L-1。术后3个月HBIG滴度水平维持在100 IU·L-1以上的患者占83.3%,术后半年占76.7%。术后14 d,达到HBIG标准滴度的患者比例较少,为53.3%。术后不同时间点HBIG定量及人数分布见表2。HBIG滴度随术后时间延长趋于稳定,在术后8周后,HBIG滴度维持在目标浓度100 IU·L-1以上并维持相对稳定,此时HBIG累积用量为16 000 IU,用法为每月1 000 IU。术后不同时间HBIG滴度变化趋势见图1。
2.2 不同时期HBsAg阴转率
术后1 d时,HBIG滴度>500 IU·L-1的患者中仅有1例HBsAg未转阴。但在术后7 d,HBIG累积用量为12 000 IU,HBIG达到有效保护滴度的患者,HBsAg阴转率均达到100%。
2.3 术后不同时间点组间HBIG滴度定量分析
高复制组与低复制组HBIG滴度水平差异无统计学意义(P>0.05),但高复制组HBIG滴度降低速度较低复制组快,术后至4周降低速度的差异有统计学意义(P<0.05)。术前HBV-DNA(+)且HBeAg(+)的患者在术后14 d,累积用量13 000 IU时,HBIG滴度为(441.08±338.74)IU·L-1,平均值<500 IU·L-1。术后不同时间点各组HBIG滴度定量见表3。
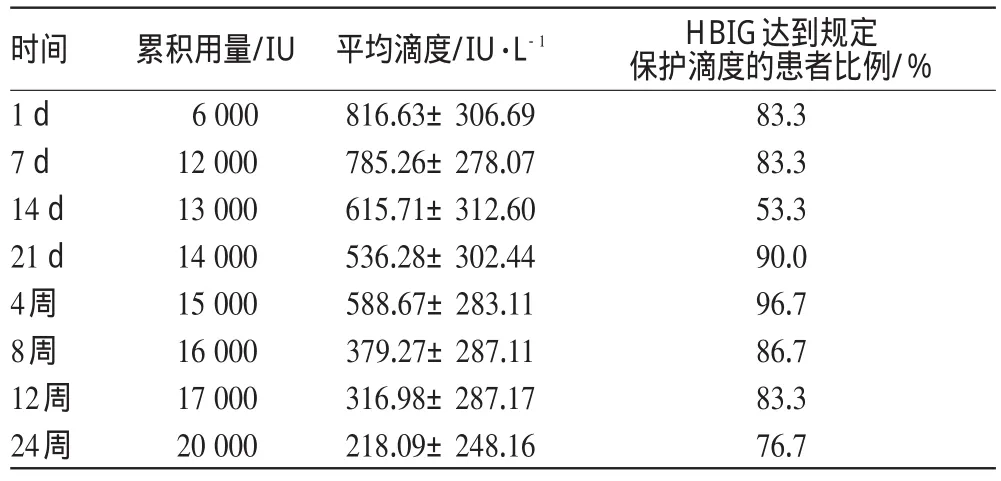
表2 术后不同时间HBIG定量及人数分布Tab 2 HBIG titer and percentage of patients at different time pointsafter operation
2.4 不同组术后不同时间HBsAg阴转率比较
高复制组患者术后21 d,HBIG累积用量为14 000 IU时,HBsAg全部转阴;而对于低复制状态的患者术后7 d HBsAg全部转阴,此时HBIG累积用量为12 000 IU。组间HBsAg阴转率差异有统计学意义(P<0.05)。
3 讨论
目前文献报道的预防HBV复发的方案包括单独使用HBIG或抗病毒药及联合应用抗病毒药和HBIG,现被广泛接受及承认的用药方案是长期LAM联合小剂量HBIG[5]。因LAM易出现耐药性,停药后易出现反跳且易出现YMDD变异(HBV-DNA聚合酶P区发生变异的简称)等,单独用药时治疗效果不满意;而与HBIG联用能取得较好的治疗效果[6]。但在实际应用时,HBIG注射剂量及时间间隔等并没有明确规定[7]。国内、外大部分研究侧重于肝移植术后HBV复发的研究[8],本研究则考察了HBIG累积用量,并将累积用量与HBIG滴度相结合进行考察,证明术后HBIG用量、滴度及HBsAg阴转率与术前HBV-DNA和HBeAg状态有关。
从肝移植后乙型肝炎复发机制和HBIG作用原理可知,如果能在新肝血流开放前或开放后的早期内将血液中的HBIG提高到并维持在有效浓度(>500 IU·L-1),那么就能充分“中和”血液循环中原有的或新从肝外组织中释放入血的病毒颗粒,并封闭肝细胞表面的HBsAg受体,从而避免病毒侵袭肝细胞[9]。因为自病毒颗粒与肝细胞接触到病毒进入肝细胞所需时间并不明确,所以在新肝血流开放后,HBIG越早达到保护滴度,术后治疗效果越好[9,10]。一般认为无肝期和术后早期(术后7 d内)经静脉给予大量HBIG对预防乙肝复发有重要意义[11]。Marzano等[12]通过对比术后6个月iv HBIG与肌肉注射(im)HBIG药动学方面的差异,得出结论:iv与im HBIG半衰期(t1/2)差异并无统计学意义,t1/2=21.4 d。因此,本研究中术后早期短时间高密度iv HBIG就是为了让HBIG集中封闭肝外组织释放入血的病毒。术后21 d后,可根据HBIGt1/2=21.4 d,采用1个月iv HBIG 1次的方案,便可保证在HBIG半衰期前达到保护滴度,这样既减少了长期大剂量使用HBIG可能引起的副作用,又降低了患者的费用。因此,实时监测HBIG滴度、在不同时期将血药浓度维持在相应范围内,对有效预防乙肝复发是非常有必要的。从本研究的结果可以看出,30例患者术后1 d HBIG累积用量为6 000 IU时,HBIG滴度水平虽已>500 IU·L-1,但尚有1例HBsAg未转阴。术后7 d使用HBIG累积用量12 000 IU时,HBIG滴度仍保持在500 IU·L-1以上,HBsAg阴转率均已达到100%。因此,不必盲目加大HBIG用量。而且,HBIG的大剂量使用可引起头痛、背痛、胸痛及肌肉注射用药局部的硬结、肿胀和疼痛[13]。
术前HBsAg(+)同时伴有HBeAg(+)或HBV-DNA(+)的患者称之为高复制;把术前HBsAg(+)但HBeAg和HBV-DNA均为(-)的患者称之为低复制[14]。HBV-DNA阳性界值为103拷贝·m L-1,>103拷贝·m L-1判定为阳性[15]。目前认为,患者术前HBeAg或HBV-DNA状态与肝移植术后HBV复发明显相关,HBeAg或HBV-DNA(+)者术后复发率增加[16]。在所有纳入本研究的肝移植患者中,高复制组共有22例患者,其中HBV-DNA(+)且HBeAg(+)患者有4例,这些患者是最应该关注的;低复制组即HBeAg(-)且HBV-DNA(-)的患者共有8例。高复制组与低复制组HBIG滴度水平差异并无统计学意义(P>0.05),可能是由于当HBIG滴度>1 000 IU·L-1时按1 000 IU统计,这就可能造成低复制组较高滴度HBIG未能充分检测,从而造成整体数据上差异无统计学意义。但从数据可以看出,在术后7~14 d,术前HBV-DNA(+)且HBeAg(+)的患者HBIG滴度降低速度(-39.54 IU·L-1·d-1)高于低复制组(-13.74 IU·L-1·d-1),二者差异有统计学意义(P<0.05);同样的,术后14~21 d,HBV-DNA(+)且HBeAg(+)患者HBIG滴度降低迅速,且在术后14 d时小于保护滴度500 IU·L-1。这说明术前病毒复制很高的患者HBIG剂量可能较少。术前HBV-DNA(+)且HBeAg(+)的患者,术后14 d,HBIG累积用量为13 000 IU时,HBIG滴度低于有效保护浓度且在术后21 d HBsAg才全部转阴,而且其中有1例患者,HBV-DNA(+)直至术后14 d,此时HBIG累积用量为13 000 IU。而低复制组在术后7 d,HBIG累积用量为12 000 IU时HBsAg即全部转阴。这也提示我们,对于HBV处于高复制状态的患者,HBIG的剂量可能偏小,应当将HBV高复制患者区别开来,适当提高围手术期HBIG的使用剂量。Dickson等[17]研究显示,术前HBV-DNA(+)的患者HBIG体内半衰期(t1/2=8.52 d)较术前HBV-DNA(-)患者半衰期(t1/2=20.6 d)短,二者差异有统计学意义(P<0.05)。这说明对于术前病毒复制较高的患者应给予高剂量的HBIG,以维持术后早期滴度水平高于500 IU·L-1。Wang等[18]通过将患者按术前HBV-DNA阴、阳性分为2组,得出的结论为:术前高复制组HBIG滴度较低,需要高剂量的HBIG。Roche和Samuel的研究表明,对于术前HBV-DNA(+)的患者术后HBIG滴度应维持在500 IU·L-1,并联合服用LAM[19]。
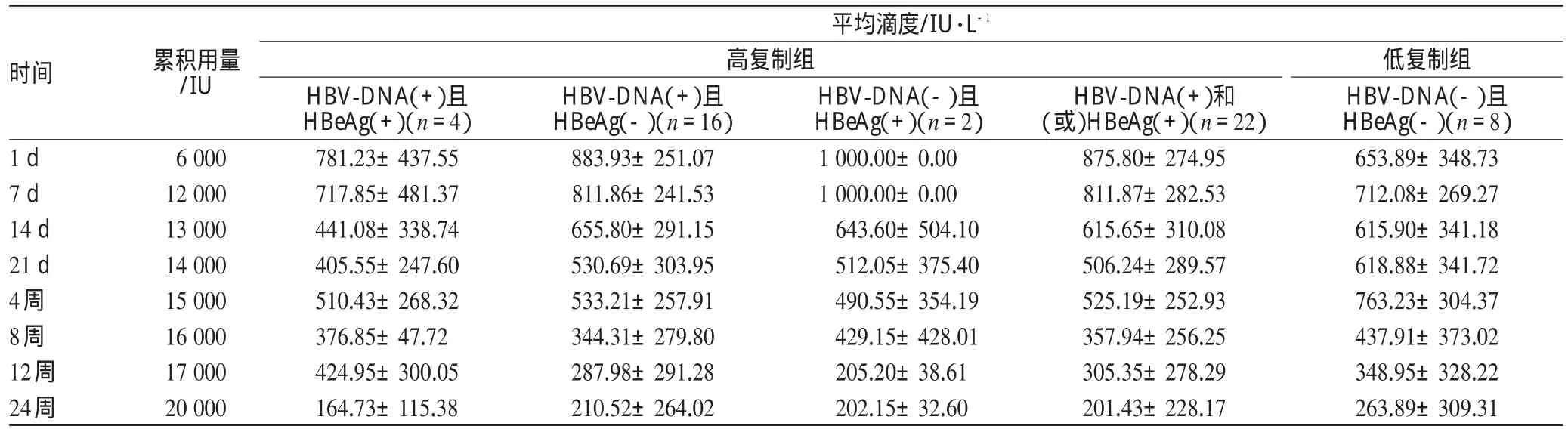
表3 术后不同时间点各组HBIG滴度定量Tab 3 HBIG titer of differentgroupsat different time pointsafter operation
HBIG预防HBV复发的有效性取决于患者肝病种类、HBIG用量及时间间隔,而术前病毒复制状态是最关键的[20]。术前HBV-DNA及HBeAg水平可以指导临床更加合理地应用HBIG。虽然对于HBIG的给药方式、使用剂量及时间间隔没有明确规定,但被大家普遍认同的方案是最终保持HBIG滴度在100 IU·L-1以上[21]。欧美国家的常规用法为经静脉给药,无肝期10 000 IU,术后1周每天10 000 IU,此后每1~3个月用2 000~10 000 IU。维持血清HBIG滴度第1周在500 IU·L-1以上,1周~3个月内不得低于250 IU·L-1,3个月后不得低于100 IU·L-1[22]。我国大陆用法尚不一致,有的医院使用先iv再im的方式,有的医院始终经iv。在本研究中,始终采取iv,使用方法为无肝期5 000 IU,术后1周每天1 000 IU,2~4周每天1 000 IU,以后每个月1 000 IU。我们并不主张术中和术后均im给药,这样不仅使血清HBIG滴度上升慢、HBsAg阴转速度慢,术后乙型肝炎复发的潜在风险大,而且注射局部硬结、肿胀和疼痛等不良反应发生率高[8]。因此,为了早期达到较高的HBIG滴度,本研究采用静脉给药,但费用问题随之而来,持续静脉给药费用高,有文献统计大约为序贯给药(先iv后im)的20倍[23]。因此,对于给药方式也需要改进,可选择既能有效控制乙肝复发又能减少开销的序贯给药,这样既能在术后早期快速使HBIG达到保护滴度[9],又能在长期的用药过程中减少费用。全世界对于术后预防方案大体分为以下3步:(1)术中无肝期im 4 000~10 000 IU;(2)术后3~7 d iv 2 000~10 000 IU;(3)以后每2周iv 400~2 000 IU[24]。乙肝复发主要取决于术前病毒复制状态[25],对于术后预防方案只要保证HBIG在术后不同时期达到保护滴度即可有效预防乙肝复发,而且因为现在被普遍接受的预防方案是LAM联合小剂量的HBIG,LAM抑制了HBV复制[26],从而大大减少了HBIG的用量。因此,由于长期大剂量使用HBIG带来不良反应也大大降低了。本研究结果显示,术前高复制患者较低复制患者需要更大剂量的HBIG才能更早达到有效的滴度。因此,要考虑到术前患者体内的病毒负荷、复制状态等不同危险因素,注意合理调整术后HBIG使用方案以达到个体化。本研究还有很多不足的地方,如:高复制组术前HBV-DNA(-)且HBeAg(+)患者仅有2例,这可能是由于患者在等待肝移植期间一直服用抗病毒药使体内乙肝病毒处于低拷贝复制,也可能是由于标本在运送中核酸比蛋白更容易降解[27],因此入组病例人数较少;本研究时间有限,收集患者人数较少,未充分考察出可能影响HBIG滴度变化的因素,还有待增大样本量进一步探究。
[1]Saab S,Ham MY,Stone MA,etal.Decision analysismodel for hepatitis B prophylaxis one year after liver transplantation[J].Liver Transpl,2009,15(4):413.
[2]ButiM,Mas A,Prieto M,etal.Adherence to lamivudine after an early withdrawal of hepatitis B immune globulin playsan important role in the long-term prevention of hepatitis B virus recurrence[J].Transplantation,2007,84(5):650.
[3]Lo CM,Cheung CK,Lau GK,etal.Significanceof hepatitis B virus genotype in liver transplantation for chronic hepatitis B[J].Am JTransplant,2005,5(8):1 893.
[4]成 军.第二届北京国际肝炎及肝病学研讨会巡礼[J].国外医学-流行病学传染病学分册,2000,27(3):134.
[5]Yasunaka T,TakakiA,YagiT,etal.Serum hepatitis B virus DNA before liver transplantation correlates with HBV reinfection rate even under successful low-dose hepatitis B immunoglobulin prophylaxis[J].Hepatol Int,2011,5(4):918.
[6]魏 欣,张旭东,王 莉.拉米夫定联合用药治疗慢性乙型肝炎的应用进展[J].中国药房,2008,19(17):1 351.
[7]Han SH,Martin P,Edelstein M,et al.Conversion fromintravenous to intramuscular hepatitis B immune globulin in combination with lamivudine is safe and cost-effective in patients receiving long-term prophylaxis to preventhepatitis B recurrence after liver transplantation[J].Liver Transpl,2003,9(2):182.
[8]Marzano A,Gaia S,Ghisetti V,et al.Viral load at the time of liver transplantation and risk of hepatitis B virus recurrence[J].Liver Transpl,2005,11(4):402.
[9]牛玉坚.乙型肝炎免疫球蛋白在预防肝移植后乙型肝炎复发中的作用[J].中华器官移植杂志,2006,27(12):763.
[10]Shouval D,Samuel D.Hepatitis B immune globulin to prevent hepatitis B virus graft reinfection follow ing liver transplantation:a concise review[J].Hepatology,2000,32(6):1 189.
[11]王正昕,傅志仁,丁国善,等.原位肝移植术后乙型肝炎病毒再感染的预防(附68例报告)[J].外科理论与实践,2004,9(2):125.
[12]Marzano A,Marengo A,Andreone P,et al.Pharmacokineticsand efficacy of intravenousor intramuscular hepatitis B immunoglobulins in prophylaxis of hepatitis B after liver transplantation[J].Minerva Med,2010,101(6):373.
[13]Filipponi F,Franchello A,CarraiP,etal.Efficacy,safety,and pharmacokineticsof intramuscular hepatitis B immune globulin,Igantibe,for the prophylaxis of viral B hepatitis after liver transplantation[J].Dig Liver Dis,2010,42(7):509.
[14]朱志军.肝移植术后乙型肝炎复发的防治[J].外科理论与实践,2008,13(4):313.
[15]李欣华,郑 颖,裴立红,等.慢性乙型肝炎患者感染血清中HBeAg,HBeAb滴度与HBV-DNA拷贝数的相关性[J].浙江医学,2006,28(6):510.
[16]卢景宁,彭民浩,杨定华,等.肝移植术后预防乙型肝炎复发的临床研究[J].广西医科大学学报,2008,25(3):73.
[17]Dickson RC,Terrault NA,Ishitani M,et al.Protective antibody levels and dose requirements forⅣ5%Nabi Hepatitis B immune globulin combined with lamivudine in liver transplantation for hepatitis B-induced end stage liver disease[J].Liver Transpl,2006,12(1):124.
[18]Wang K,Zhu ZJ,Zheng H,et al.Protective hepatitis B surface antibodies in blood and ascites fluid in the early stage after liver transplantation for hepatitis B diseases[J].HepatolRes,2012,42(3):280.
[19]Roche B,Samuel D.Evolving strategies to prevent HBV recurrence[J].Liver Transpl,2004,10(10Suppl2):74.
[20]MehrabiA,Esmaeilzadeh M,FonouniH,etal.The role of HBIG as hepatitis B reinfection prophylaxis follow ing liver transplantation[J].Langenbecks Arch Surg,2012,397(5):697.
[21]Bihl F,Russmann S,Gurtner V,et al.Hyperimmune anti-HBs plasma asalternative to commercial immunoglobulins for prevention of HBV recurrence after liver transplantation[J].BMCGastroenterol,2010,10(4):71.
[22]Mohanty SR,Cotler SJ.Managementof hepatitis B in liver transplant patients[J].J Clin Gastroenterol,2005,39(1):58.
[23]FerrettiG,MerliM,Ginanni Corradini S,etal.Low-dose intramuscular hepatitis B immune globulin and lamivudine for long-term prophylaxis of hepatitis B recurrence after liver transplantation[J].Transplant Proc,2004,36(3):535.
[24]Dindoost P,Jazayeri SM,A lavian SM,etal.Hepatitis B immune globulin in liver transplantation prophylaxis:an update[J].HepatMon,2012,12(3):168.
[25]Zheng S,Chen Y,Liang T,etal.Prevention of hepatitis B recurrence after liver transplantation using lamivudine or lamivudine combined with hepatitis B Immunoglobulin prophylaxis[J].Liver Transpl,2006,12(2):253.
[26]黄燕萍,王宇明.联合用药治疗慢性乙型肝炎研究现状和进展[J].中国药房,2003,14(12):760.

