HPLC法测定注射用头孢呋辛钠含量
袁 琦,郭新社,杨 浩
(河南大学药学院 药物分析教研室,河南 开封 475001)
头孢呋辛钠(Cefuroxime Sodium),又名头孢呋肟,为半合成的第二代头孢菌素类抗生素[1]。因其对革兰氏阴性菌的β内酰胺酶相当稳定,有穿透血脑屏障等特点。临床上广泛应用于敏感菌引起的呼吸道、泌尿系统、皮肤、软组织、骨关节及女性生殖器等组织器官的感染,对败血症、脑膜炎也有效[2-3]。
头孢呋辛钠的测定方法主要有微生物法、旋光法、紫外分光光度法、近红外光谱法和高效液相色谱法等[4-5]。其中大多数测定方法无分离能力,无法排除一些杂质的干扰,不利于监控注射用药物的使用安全性。我们建立了高效液相色谱法测定注射用头孢呋辛钠的含量。该方法操作简便、快速、重现性好,可作为样品的检测方法。
1 仪器与试药
1.1 仪器
Waters-2695高效液相色谱仪(Waters公司);Waters-2489可变波长紫外检测器(Waters公司);UV-1600型紫外可见分光光度计(北京瑞利);BP-211D电子天平(德国Sartorius);色谱柱(大连伊利特科学有限公司)。
1.2 试药
头孢呋辛钠对照品(中国药品生物制品检定所30493-200704);注射用头孢呋辛钠(规格:0.75g,批号:091009,091010,091011,河南帅克制药有限公司);乙腈为色谱纯;醋酸、磷酸氢二钠、磷酸二氢钠均为分析纯;水为重蒸水。
2 方法与结果
2.1 色谱条件
色谱柱C18(5μm,4.6mm×250mm);流动相为pH3.4的缓冲液(取0.1mol/L醋酸钠溶液50mL,加0.1mol/L的醋酸溶液至1000mL)-乙腈(86∶14);流速1.0mL/min;检测波长254nm;进样量20μL;柱温:25℃。
2.2 溶液的制备
2.2.1 对照品溶液的制备 取对照品约50mg,精密称定,置100mL量瓶中,加流动相溶解并稀释至刻度,摇匀即得。
2.2.2 供试品溶液的制备 取本品约50mg,精密称定,置100mL量瓶中,加流动相溶解并稀释至刻度,摇匀即得 。
2.3 破坏试验
取头孢呋辛钠对照品适量,加流动相溶解并稀释成每1mL中含100μg的溶液。取上述溶液适量,在60℃水浴中加热10min,冷却,使部分头孢呋辛转变为去氨基甲酰头孢呋辛,取20μL注入液相色谱仪,头孢呋辛钠峰与杂质峰的分离度为4.371。
2.4 方法学考察
2.4.1 专属性 取“2.2”项下各溶液按上述色谱条件进样测定,结果见图1。由图1可知,空白溶剂对主成分测定无干扰,头孢呋辛钠的出峰时间为8.315min。


图1 头孢呋辛钠溶液色谱图
2.4.2 精密度 精密称取本品适量,用流动相溶解并稀释制成0.5g/L的溶液,取20μL注入色谱仪,记录色谱图。重复测定6次,RSD值为0.24%。
2.4.3 检测限与定量限 取本品,用流动相溶解制成0.0001g/L的溶液,进样20μL分析,记录色谱图,本品的最小检测量为2ng。10∶1信噪比作为本品的定量限,即定量限为10ng。
2.4.4 线性与范围 精密称取头孢呋辛钠对照品适量,加流动相定量溶解,配制成浓度为0.75、0.60、0.50、0.40、0.25g/L的溶液,取20μL注入色谱仪,记录色谱图。以色谱峰面积为纵坐标,以溶液中头孢呋辛钠的浓度为横坐标,绘制标准曲线,见图2。回归方程为:Y=19730707 X+874894,r=0.9991。结果表明,头孢呋辛钠在0.25~0.75g/L范围内,浓度与峰面积呈良好线性关系。
2.4.5 稳定性试验 按“2.2”项下方法配制供试品溶液(批号:091009),测定18h内供试品溶液稳定情况,重复测定6次。平均峰面积为20882496,RSD=0.73%。以上结果表明,头孢呋辛钠在选定色谱条件下,于18h内稳定。

图2 头孢呋辛钠线性图
2.4.6 加样回收率实验 取9个10mL容量瓶,分别精密加入已知浓度供试品(批号:091009)溶液4.0mL,再分别加入3.0、4.0、5.0mL对照品溶液,用甲醇稀释至刻度,摇匀,制备低、中、高3种质量浓度的供试品溶液,每种浓度制备3份样品。按样品测定项下方法测定含量,计算平均回收率为99.32%,RSD 值为0.28%。
2.5 含量测定
取“2.2”项下供试品约50mg,精密称定,置100mL量瓶中,加水溶解并稀释至刻度,摇匀,精密量取20μL注入液相色谱仪,记录色谱图。测得的峰面积代入回归方程计算出供试品中C16H16N4O8S的含量,结果各批样品含量均符合规定,结果见表1。
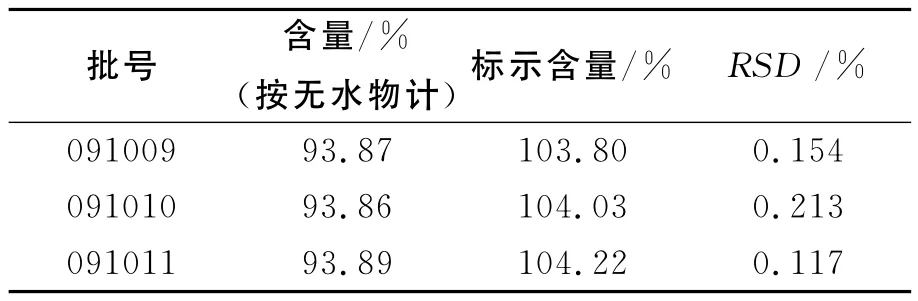
表1 注射用头孢呋辛钠的含量测定结果(n=3)
3 讨论
3.1 流动相的选择
按照《中国药典》(2010版)二部规定的流动相,头孢呋辛钠出峰时间约为35min,样品保留时间过长,色谱峰拖尾严重[6]。我们在实验中,以pH 3.4的醋酸盐缓冲溶液-乙腈(10∶1.6)为流动相,缩短了保留时间。破坏实验证实,在实验选定的色谱条件下,头孢呋辛钠与杂质峰能够完全分离[7],大大降低了时间成本和溶剂的消耗。
3.2 柱温的选择
通过实验发现,柱温的变化,对头孢呋辛钠的出峰时间影响较大,故在测定头孢呋辛钠的含量时,虽然是在室温下测定,最好还是把色谱柱放入柱温箱中,以保证柱温的恒定和测定结果的准确性。
高效液相色谱法测量头孢呋辛钠的含量,方法简便,测量准确,能很好地控制药品质量,保证了临床用药的安全。
[1]高硕,杨错,王红.头孢呋辛钠药动学的研究进展[J].中国药房,2012,23(1):85-86.
[2]邓宝军,林诗贵,李蜀巍,等.头孢呋辛的临床抗感染研究进展[J].中国临床药理学杂志,2000,16(5):390-393.
[3]白林,王晓蕾,王璐,等.头孢呋辛钠与5种常用输液的配伍稳定性研究[J].中国药师,2008,11(3):335-336.
[4]谢守霞,董淳.旋光法测定注射用头孢呋辛钠的含量[J].华西药学杂志,2003,18(3):219-222.
[5]杜美菊,陈玲.荷移分光光度法测定头孢呋辛钠的含量[J].商丘师范学院学报,2011,27(9):71-73.
[6]国家药典委员会编.中国药典:二部[S].北京:中国医药科技出版社,2010:1188-1190.
[7]陈兆坤,胡昌勤,沈永嘉.头孢呋辛钠的氨解研究[J].中国热带医学,2007,7(10):1770-1771.

