Ag/BaTiO3的制备及光催化性能
沈昱,程国伟,宋满堂
(1.大连交通大学 环境与化学工程学院,辽宁 大连 116028;2.大连大化工程设计有限公司,辽宁 大连116031)*
0 引言
BaTiO3是一种新型的功能材料,广泛应用于电容器、PTC元件、压电换能器等电子元器件的制造[1].因此,多年来BaTiO3的研究主要集中于铁、电陶瓷材料.王翔等人[2]进行了纳米BaTiO3/环氧树脂复合材料的制备及性能研究,杨芙丽等人[3]研究了锶掺杂对BaTiO3薄膜粒径与结晶温度的影响.利用钙钛矿型复合氧化物(ABO3)的较好构型应用于光催化的研究很多[4-5],它与TiO2等氧化物同样具有光催化性能,有时甚至更优于后者[6].而以BaTiO3作为光催化材料的报道不多,潘霞等人[7]曾做过以NiO作为载体,用溶胶-凝胶法在NiO载体上负载钛酸钡纳米涂层作为光催化剂的研究.
相对于Au、Pt和Pd,Ag因其价廉易得而广泛用于光催化材料的改性研究[8-10].任学昌等人[11]用光化学沉积法对纳米TiO2薄膜进行了Ag改性,以苯酚为模拟污染物,在不同波长光源及有氧和无氧条件下考察了Ag/TiO2薄膜的光催化活性.张靖峰等人[12]采用氨浸法制备了不同Ag负载量的纳米Ag/ZnO光催化剂,并研究了其催化降解壬基酚聚氧乙烯醚的性能.本文采用水热反应法合成了BaTiO3粉体,并采用光催化还原法、浸渍法和水热法分别对BaTiO3粉体进行Ag的掺杂改性,通过X-射线衍射 (XRD)、扫描电子显微镜(SEM)、紫外可见吸收光谱 (UV-vis)等手段对改性后的催化剂进行了表征,并以亚甲基蓝为模型污染物,在高压汞灯光照下,考察了不同改性方法、不同载Ag量对催化剂光催化活性的影响.
1 实验部分
1.1 催化剂的制备
1.1.1 BaTiO3催化剂的制备
取等物质的量的乙酸钡、钛酸丁酯分别溶于一定量的蒸馏水和无水乙醇中,得溶液A和溶液B.室温下搅拌,将A、B溶液混合均匀后用NaOH溶液调节溶液OH-浓度,搅拌得淡黄色溶胶,再将溶胶转移至水热反应釜中,于160℃烘箱内水热反应6 h,洗涤、过滤、烘干,研磨制成BaTiO3粉体.
1.1.2 光催化还原法制备Ag/BaTiO3
将5.0 g BaTiO3粉体置于超声波清洗器中充分分散,然后与一定量的0.1 mol/L AgNO3溶液一同加入光反应器中,用去离子水配制成500 mL悬浮液.通入空气,在机械搅拌条件下,在100 W高压钠灯光源下进行一定时间的光催化还原反应.将悬浮液进行过滤,滤饼在100℃烘干,即得光催化还原法制备的Ag/BaTiO3催化剂.为了加快载Ag速度,可在该体系中加入少量EDTA以缩短光催化还原反应的时间.
1.1.3 浸渍法制备Ag/BaTiO3
将1.0 g BaTiO3粉体溶于100 mL蒸馏水中,再加入5 mL 0.1 mol/L AgNO3溶液,超声分散后,于50℃下磁力搅拌一段时间,浸渍反应24 h,过滤,将滤饼于100℃烘干,研磨,即得浸渍法制备的Ag/BaTiO3催化剂.
1.1.4 水热法制备Ag/BaTiO3
将 1.0 g BaTiO3粉体溶于 5 mL 0.1 mol/L AgNO3溶液中,超声分散后,放入容积为40 mL的水热反应釜内,加蒸馏水至填充度为80%.于160℃反应6 h,过滤,洗涤,于 100℃干燥2 h,研磨,即得水热法制备的Ag/BaTiO3催化剂.
1.2 催化剂的表征
1.2.1 SEM 分析
采用JSM-6360LV型扫描电子显微镜对不同方法制备的Ag/BaTiO3催化剂进行微观结构、形态及颗粒大小的分析.
1.2.2 XRD 分析
采用日本岛津公司生产的XD-3A型X-射线衍射仪对不同方法制备的Ag/BaTiO3催化剂进行X射线衍射分析,扫描范围2θ=20°~80°.
1.2.3 紫外-可见吸收光谱分析
采用日本JASCO公司UV-550型紫外-可见分光光度计对不同方法制备的Ag/BaTiO3催化剂进行紫外-可见光谱吸收性质的测定.
1.3 光催化性能测试
本实验采用亚甲基蓝染料作为降解底物考察催化剂的光催化活性.称取不同条件制备的催化剂粉体0.1 g,分别置于表面皿中,然后取50 mL 10 mg/L亚甲基蓝染料溶液,搅拌一段时间使催化剂颗粒均匀地悬浮于溶液中.然后将催化体系转移至光催化反应器中,在40 W高压汞灯照射下进行光催化反应.每隔一段时间进行取样,在最大吸收波长665 nm处,通过分光光度计(721型)测定亚甲基蓝溶液的吸光度值A,利用R%=(A0-A)×100%/A0计算亚甲基蓝溶液的降解率.
2 结果与讨论
2.1 SEM 分析
图1为不同制备方法所制得的Ag/BaTiO3光催化剂的SEM照片.由图1(a)(光催化还原法)和图1(b)(浸渍法)可以看出,光催化还原法和浸渍法制得的Ag/BaTiO3粒径分布较为均匀,颗粒大小约为1 μm.而水热法所制得的Ag/BaTiO3(如图1(c))粉体粒度较大,有可能是因为团聚造成的,这可能会在很大程度上影响其光催化活性.

图1 不同方法制备Ag/BaTiO3的SEM照片
2.2 XRD 分析
三种不同制备方法所制得Ag/BaTiO3光催化剂的XRD图谱如图2所示.由图可以看出,三种方法制得的Ag/BaTiO3光催化剂的衍射峰都表现出锐钛矿相的特征峰.谱图上未见Ag的特征衍射峰,可能是因为Ag的量较少且高度分散于BaTiO3的载体上.采用水热法制备的Ag/BaTiO3光催化剂的结晶度较好,以锐钛矿相为主并混有少量金红石相的混晶,可能会提高光催化的降解效率.而从前述SEM照片上看,样品发生团聚现象,颗粒粒径较大,其光催化活性可能反而会有所降低.
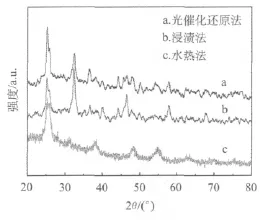
图2 不同方法制备Ag/BaTiO3的XRD图谱
2.3 紫外-可见吸收光谱分析
BaTiO3和Ag/BaTiO3(光催化还原法制备)光催化剂的紫外-可见吸收光谱如图3所示.由图可知,与纯的BaTiO3相比,Ag的掺入使催化剂粉体的光谱响应范围扩大,吸收带边向长波方向移动,并且催化剂在紫外和可见光区的光吸收强度都有一定程度的增强,这将有利于增大对光的利用率.
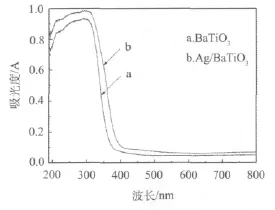
图3 掺Ag前后催化剂的紫外-可见吸收光谱
通过外推法估算样品对光吸收带边(λg)的禁带宽度Eg,在图中拐点处做切线,切线与X轴的交点即为λg的值.根据公式[13]:λg=1 240/Eg,推算所制备的BaTiO3和Ag/BaTiO3样品的禁带宽度分别为3.0 eV和2.61 eV.由计算的数值可知,光催化还原法制得的Ag/BaTiO3光催化剂的禁带宽度与未掺杂的BaTiO3相比明显变窄.Ag+半径(约126 pm)远大于 Ti4+的半径 (约68 pm),所以Ag+不能进入Ti-O的晶格,只能沉积在催化剂表面,沉积过程中Ag+会逐渐扩散到催化剂晶粒的表面.经光照和热处理后的Ag+可能先形成岛状 Ag+扩散层 (厚度约0.1 ~1.0 nm),然后形成片状金属粒子分散在BaTiO3表面,尤其是BaTiO3晶粒的边界上.
2.4 光催化性能分析
图4是亚甲基蓝溶液在不同催化剂作用下的降解率,由图可以看出,对亚甲基蓝溶液进行4 h的光催化降解后,不同制备方法所得Ag/BaTiO3的光催化性能较改性前都有不同程度的提高,其中光催化还原法制备的Ag/BaTiO3光催化剂的活性最佳.结合XRD和SEM分析,水热法制备的催化剂虽然结晶度比较好,但有严重的团聚现象发生,这在很大程度上影响了催化剂粉体的光催化活性;而光催化还原法制备的样品中,Ag可以直接生成在BaTiO3颗粒表面,而且金属能够均匀分布在光催化剂的表面,这就大大提高了它的光催化活性;而浸渍法得到的催化剂粉体在干燥过程中,可能会因Ag向表面的移动而使Ag的浓度降低,甚至未覆盖于催化剂的表面,导致催化剂表面的Ag分布不均匀,从而影响亚甲基蓝溶液的光催化降解效率.

图4 掺Ag前后的催化剂对亚甲基蓝溶液降解率的影响
利用光催化还原法对BaTiO3掺银,不同Ag掺杂量对亚甲基蓝溶液降解率的影响如图5所示.由图可知,改性后的催化剂对染料的降解率均比未改性的BaTiO3有明显提高.随着Ag掺杂量的增加,催化剂的光催化活性先增加后降低,载Ag量为1.0% 的Ag/BaTiO3的催化活性最佳,经过4 h的光催化降解,亚甲基蓝溶液的降解率为95%.Ag负载在BaTiO3表面,部分光生电子富集在Ag表面,这样在一定程度上降低了电子-空穴的复合几率,提高了光催化活性;而当过多的Ag负载在BaTiO3表面时,Ag又成为光生电子-空穴的复合中心,从而使得光催化剂产生的电子和空穴减少,导致了催化剂光催化活性的降低.
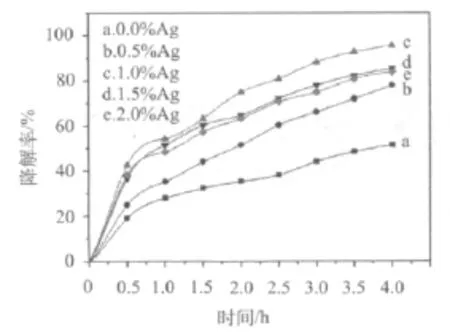
图5 不同银掺杂量对亚甲基蓝溶液降解率的影响
3 结论
分别采用光催化还原法、浸渍法和水热法三种不同的方法进行了BaTiO3的Ag掺杂改性.改性后的BaTiO3光催化剂都表现出锐钛矿相的特征峰,以水热法制得的晶型最为完整,但有颗粒团聚现象发生;光催化还原法和浸渍法制得的Ag/BaTiO3粒径分布较为均匀,颗粒大小约为1 μm.光催化还原法制得的Ag/BaTiO3光催化剂的禁带宽度与纯的BaTiO3相比明显变窄,且改性后的催化剂在紫外-可见光区对光的吸收强度均有一定程度的增加.利用光催化还原法制备的Ag/BaTiO3光催化剂的活性最佳,当掺Ag量为1.0%时,Ag/BaTiO3的光催化活性最高,经过4 h的光催化降解,亚甲基蓝溶液的降解率为95%.
[1]刘岗,严岩,王峰,等.电子陶瓷用钛酸钡粉体制备方法研究进展[J].绝缘材料,2006(1):56-63.
[2]王翔,卢同红,刘韩星,等.纳米钛酸钡/环氧树脂复合材料的制备及性能研究[J].沈阳建筑大学学报,2010,26(6):1155-1160.
[3]杨芙丽,申玉双,郭建晋,等.锶掺杂对BaTiO3薄膜粒径与结晶温度的影响[J].河北师范大学学报,2010,34(3):325-328.
[4]蒋勤,吴艳波,张守臣,等.溶胶-凝胶法制备钛酸锶粉体及其光催化性能的研究[J].工业催化,2006,14(12):60-63.
[5]CHEN Liang,ZHANG Shouchen,WANG Liqiu,et al.Photocatalytic activity of Zr:SrTiO3under UV illumination[J].Journal of Crystal Growth,2009,311:735-737.
[6]蒋勤,张守臣,王立秋,等.钙钛矿型光催化剂的制备及应用研究进展[J].化工进展,2006,25(2):136-139.
[7]潘霞,吴也凡,罗凌虹,等.卷心菜型的NiO为载体的钛酸钡光催化剂的性能研究[J].陶瓷学报,2010,31(1):25-28.
[8]MAN SIG LEE,SEONG-SOO HONG,MADJID MOHSENI.Synthesis of photocatalytic nanosized TiO2-Ag particles with sol-gel method using reduction agent[J].Journal of Molecular Catalysis A:Chemical,2005,242:135-140.
[9]GUO Guangmei,YU Binbin,YU Ping,et al.Synthesis and photocatalytic applications of Ag/TiO2-nanotubes[J].Talanta,2009,79:570--575.
[10]SAHOO C,GUPTA A K,PAL ANJALI.Photocatalytic degradation of Methyl Red dye in aqueous solutions under UV irradiation using Ag+doped TiO2[J].Desalination,2005,181:91-100.
[11]任学昌,史载锋,孔令仁.TiO2薄膜的Ag改性及光催化活性[J].催化学报,2006,27(9):815-822.
[12]张靖峰,杜志平,赵永红,等.纳米Ag/ZnO光催化剂及其催化降解壬基酚聚氧乙烯醚性能[J].催化学报,2007,28(5):457-462.
[13]李立清,刘宗耀,唐新村,等.B/Fe2O3共掺杂纳米TiO2可见光下的催化性能[J].中国有色金属学报,2006,16(12):2098-2103.

