[Ni(DTPB)Cl](NO3)3·5H2O 的合成、晶体结构和SOD模拟活性*
张 勇 王继猛 舒威虎 陈 琪 黄朝志 廖展如
(1湖北理工学院化学与材料工程学院,湖北黄石435003;2华中师范大学化学学院,湖北武汉430079)
镍是生物体(微生物、植物、动物和人)中必需的痕量元素,在生命过程中起着重要的作用。Ni-SOD(镍超氧化物歧化酶)是近年来发现的只存在于某些极少数原核细菌中的一种超氧化物歧化酶,它是单核镍酶,与CuZn-SOD(铜锌超氧化物歧化酶)一样,其活性中心都有组氨酸残基的咪唑基团参与中心金属离子的配位,且具有与CuZn-SOD相似的生物活性[1-2]。苯并咪唑基(Bzim)的碱性最接近组氨(His)[pKb(His)=9.96,pKb(Bzim)=8.47],可成为组氨酸残基较为理想的模拟物[3]。目前,用含有苯并咪唑的配体与过渡金属形成配合物模拟SOD的工作相当活跃[4-8]。
在本文中,我们选择了含有多个配位点的八齿配体 1,1,4,7,7- 五(2'- 苯并咪唑甲基)-二乙基三胺(C44H43N13,DTPB)来模拟SOD活性中心的组氨酸残基,合成了没有报道过的单核镍DTPB配合物,并用邻苯三酚自氧化法测试了其模拟SOD活性。
1 实验部分
1.1 仪器与试剂
除邻苯二胺为化学纯以外,实验所用试剂均为市售分析纯。所用仪器为Perkin-Elmer 2400元素分析仪,HP 8453 UV-Vis紫外光谱仪,AV-500型核磁共振仪,Perkin-Elmer 1700红外光谱仪(KBr压片法)。晶体结构测定使用Brucker Smart-2000 CCD单晶衍射仪。
1.2 配体DTPB的合成
配体DTPB的合成参照文献[9-10]稍作改进,其化学结构式见图1。将二乙三胺五乙酸(DTPA)和邻苯二胺(OPD)按物质的量之比1∶5投料,乙二醇做溶剂,控温在180~200°C,在 N2的气氛下回流6~8 h,直到无水蒸气放出。反应后将反应液趁热倒入适量的冰水中,得到大量的灰白色固体。以95%的乙醇作溶剂重结晶3次,得白色粉末,产率75%,元素分析和1HNMR数据与文献[9]的报道一致。

图 1 配体 DTPB(1,1,4,7,7- 五
(2'-苯并咪唑甲基)-二乙基三胺)的结构
1.3 标题配合物的合成
称取1 mmol DTPB(0.76 g)溶于40 mL乙醇中,缓慢加入 2.2 mmol NiCl2·6H2O(0.53 g)的20 mL的乙醇溶液,再加入4 mmol NaNO3(0.34 g),反应混合液在60℃的水浴中加热6 h,得浅蓝色透明溶液,过滤,将滤液于室温静置1周后,析出浅蓝色的块状晶体,即标题配合物[Ni(DTPB)Cl](NO3)3·5H2O,产率:75%。元素分析:实验值(计算值,%):C 47.24(47.10),H 4.86(4.69),N 17.24(17.13)。IR(KBr,cm-1):3 424(m,H-OH),2 942(m,C-H),1 626,1 532,1 428(m,苯环 C=C),327(w,Ni-Cl),288(m,Ni-N).UV-Vis[λmax,nm(ε,L mol-1cm-1)]:275(26 800)(溶剂为甲醇)。
1.4 晶体的测定
选取大小为 0.20 mm ×0.10 mm ×0.10 mm的浅蓝色块状标题化合物单晶置于Brucker Smart-2000 CCD单晶衍射仪上,采用石墨单色化的 Mo Kα 射线(λ=0.071 073 nm),于292(2)K,以 ω/2θ方式扫描,在 1.83°<θ<25.00°范围内共收集到衍射点22 029个,其中独立衍射点9 493个(Rint=0.073 9),I>2σ(I)的可观测的衍射点5 502个。全部衍射数据经Lp因子和经验吸收校正。晶体结构由直接法解出,非氢原子坐标是在以后的数轮差值Fourier合成中陆续确定的。对全部氢原子的坐标及各向异性参数用SHELXS-97程序,以最小二乘法对结构进行精修。标题化合物的剑桥晶体数据库编号:CCDC 606551。
2 结果与讨论
2.1 合成
改进的配体合成方法在合成时采用N2保护,这不仅可以阻止在高温条件下邻苯二胺的氧化,更便于用简单的重结晶方法来提纯配体,测定配体 DTPB的熔点为:157~158℃ (与文献[9]的报道一致),配体的产率也大大提高(文献[9]报道的产率为32%)。合成配合物采用的镍盐是过量的,但得到的却是单核镍配合物。
2.2 晶体结构
标题配合物的晶体属于三斜晶系,Pī空间群,晶胞参数为a=0.871 62(6)nm,b=1.515 6(11)nm,c=2.151 9(15)nm,α =99.538 0(10)°,β =90.226 0(10)°,γ =102.584 0(10)°,V=2.733 8(3)nm3,Dc=1.351 g/cm3,Z=2,F(000)=1 148,最终残差因子R1=0.071 0,wR2=0.167 9(对I>2σ(I)的衍射点)和R1=0.115 6,wR2=0.188 4(对所有的衍射点)。化合物的重要键长和键角列于表 1,化合物的阳离子结构见图2,晶胞堆积图见图3。
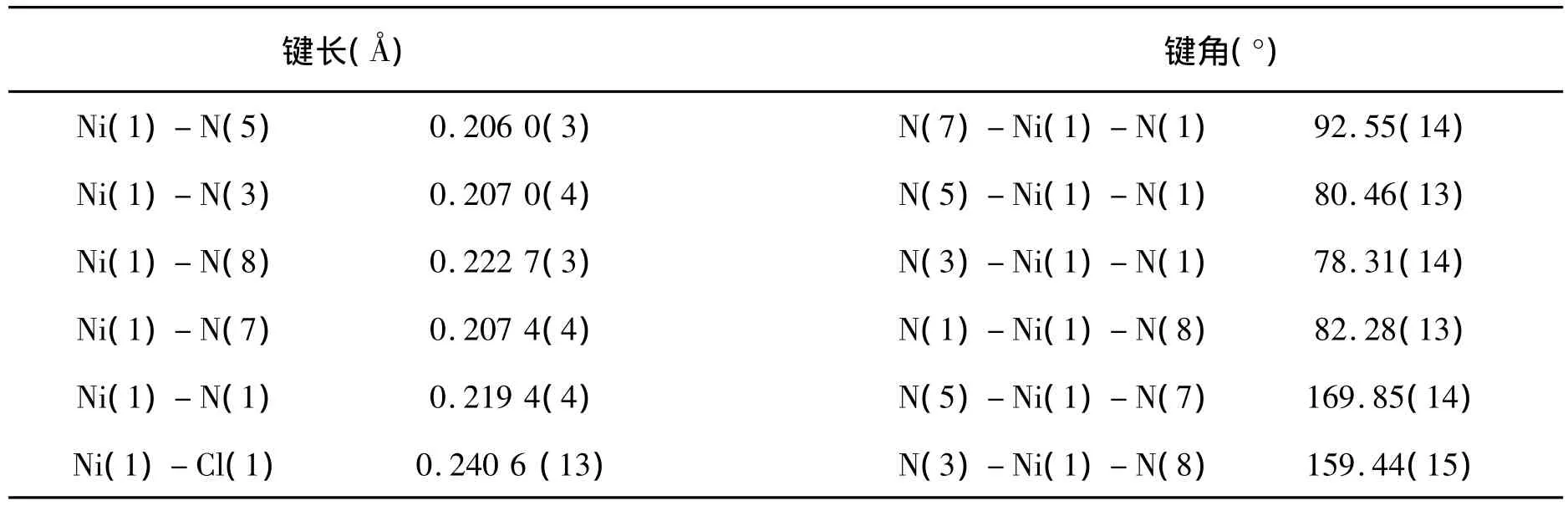
表1 配合物的部分键长和键角
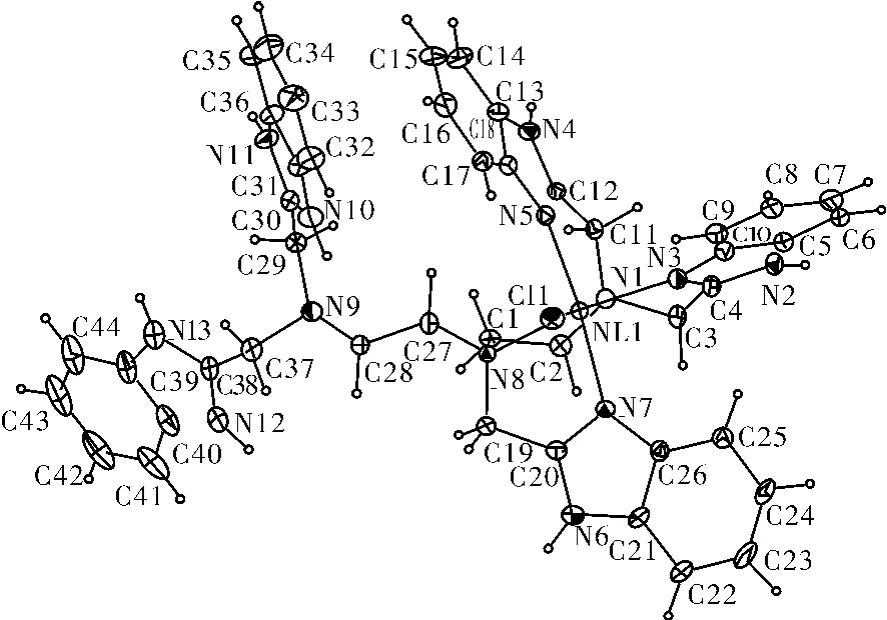
图2 配合物阳离子[Ni(DTPB)Cl]3+的结构(椭球概率30%)
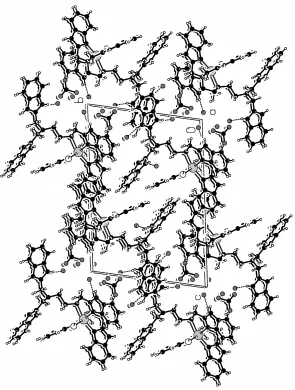
图3 标题化合物的晶胞堆积图
晶体结构分析表明,镍(II)离子与一个氯离子Cl(1),配体DTPB的3个苯并咪唑氮原子[N(3),N(5),N(7)]以及 DTPB的2个烷胺氮原子[N(1),N(8)]配位,形成一个六配位的扭曲八面体构型,其中配体的3个苯并咪唑氮N(3),N(5),N(7)和1个烷胺氮N(8)形成赤道平面,而烷胺氮N(1)和Cl(1)处于轴向位置,其轴向键角为177.85(10)°,稍微偏离了理想的180°。由表1可知,配体烷胺氮原子与Ni2+之间的距离[Ni(1)—N(1),0.219 4(4)nm;Ni(1)—N(8),0.222 7(3)nm]要明显长于苯并咪唑氮原子与镍(II)离子之间的距离[Ni(1)—N(3),0.207 4(4)nm;Ni(1)—N(5),0.206 0(3)nm;Ni(1)—N(7),0.207 4(4)nm],这与苯并咪唑失去H+后带负电荷的氮离子给电子的能力比烷胺氮原子给电子能力强的事实相符合[5]。处于轴向位置的N(1)与处于赤道位置的N(3),N(5),N(7),N(8)的键角大小分别为:N(7)—Ni(1)—N(1),92.55(14)°;N(5)—Ni(1)—N(1),80.46(13);N(3)—Ni(1)—N(1),78.31(14);N(1)—Ni(1)—N(8),82.28(13)°。后3个角偏离90°,而第1个角接近90°。处于轴向位置的Cl(1)与处于赤道位置的N(3),N(5),N(7),N(8)的键角大小与上述情况类似。此外,处于赤道平面二对对角位置的氮原子键角大小为:N(7)—Ni(1)—N(5),169.85(14)°;N(3)—Ni(1)—N(8),159.44(15)。它们都显著的偏离理想的180°键角,这说明由 N(3),N(5),N(7),N(8)构成的赤道平面并不规则。已报道有晶体结构的铜、锌和锰的DTPB-过渡金属配合物都是双核的[10-12],有趣的是标题化合物是单核的,且在其阳离子[Ni(DTPB)Cl]3+的结构中,没有配位的2个苯并咪唑环上都存在氮原子的质子化现象(N(10)或(N(11);N(12)或(N(13))。我们在合成配合物时所用金属盐是过量的(见1.3配合物的合成),配合物中氮原子的质子化来源可能是镍盐NiCl2·6H2O(强酸弱碱盐)在60℃的反应条件下水解造成的。苯并咪唑环上氮原子的质子化使得苯并咪唑环产生离域的正电荷,导致苯并咪唑环上氮原子与镍(II)离子的配位能力大大减弱,以致得到了本文所报道的单核化合物。
图3是标题化合物的单胞堆积图。晶胞中的阴离子NO-3虽未参与配位,但参与了氢键的形成,同时起电荷平衡的作用。从氢键的键长和键角(表 2)可以看出,溶剂H2O中的O原子,Cl原子,苯并咪唑的N原子,以及没有参与配位的NO-3相互作用产生了N—H…O,N—H…Cl,C—H…O等多种氢键,从而使标题化合物分子形成了一个三维的网状结构。
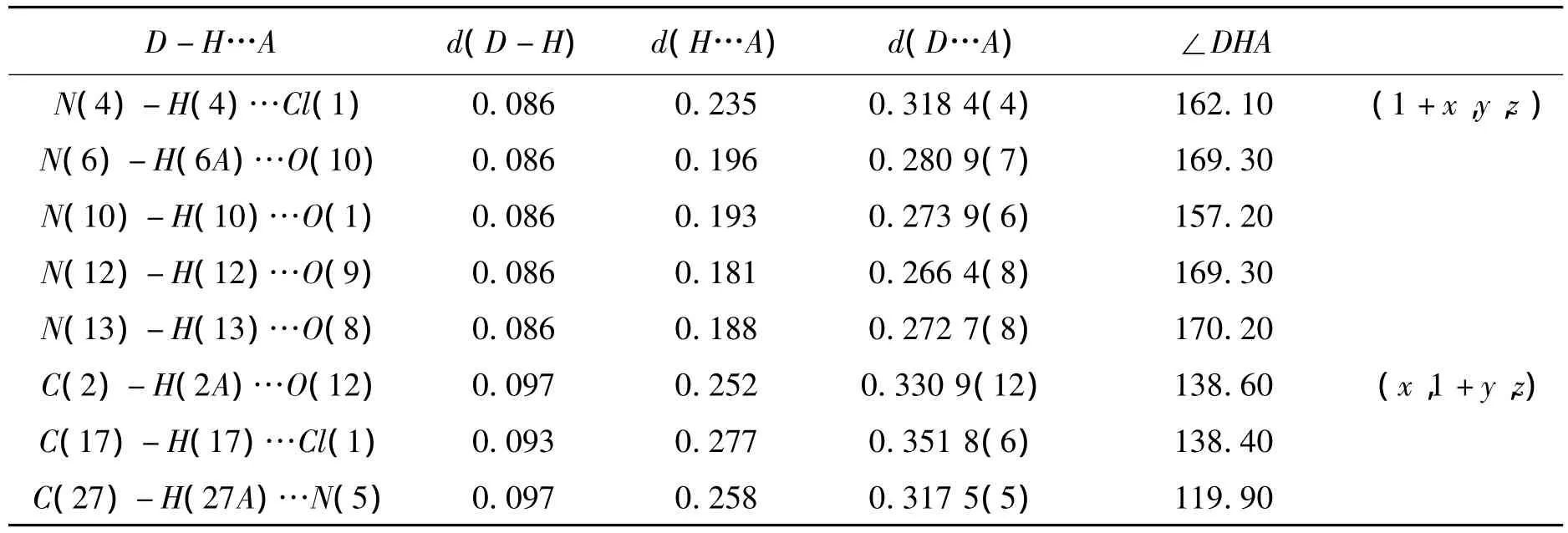
表2 氢键的键长和键角
2.3 SOD模拟活性
参照文献[5],利用邻苯三酚自氧化法,在固定波长320 nm处对标题化合物的SOD模拟活性进行了检测。IC50值的大小决定着模拟物清除O-2功效的高低,把抑制邻苯三酚自氧化速度50%时所需的配合物(或酶)的浓度定义为 IC50值,按下列公式计算[13]:IC50=M×V×ΔAP(Vtotal×(ΔA- ΔA'))×50%,式中M为配合物加入测定反应体系前的浓度;V为配合物加入测定反应体系前的体积;Vtotal为配合物的总体积;ΔA为邻苯三酚自氧化速度;ΔA'为加入配合物后邻苯三酚自氧化速度。抑制速率在35%~60%可用此公式计算。预实验结果表明,标题化合物在pH=8.2时可观测到抑制邻苯三酚自氧化的明显效果。通过测定并计算得到:在pH=8.2,温度为25℃时,标题化合物的 IC50为50.6 mg/L,而 SOD标准物质的 IC50为 0.32 mg/L。IC50值越小,配合物(或酶)的活性越高,由此可见标题化合物确实具有一定的SOD模拟活性。但和其他一些报道的SOD模拟酶相比,它的活性要低些,可能是由于中心金属离子已经达到了六配位的饱和结构,难以和反应底物进一步结合[14-15]。
3 结论
合成和表征了单核镍配合物[Ni(DTPB)Cl](NO3)3·5H2O(DTPB=1,1,4,7,7- 五(2'-苯并咪唑甲基)-二乙基三胺),并用邻苯三酚自氧化法测试了其模拟SOD活性。配合物属于三斜晶系,空间群为Pī,Ni(II)原子与一个氯离子,配体DTPB的3个苯并咪唑氮原子和2个烷胺氮原子配位,形成六配位的变形八面体构型。配合物具有一定的SOD模拟活性,其 IC50为 50.6 mg/L。
致 谢
感谢华中师范大学分析测试中心孟祥高博士对解析晶体结构所提供的帮助,感谢研究生导师廖展如教授对本文测试所提供的资金支持!
[1]Barondeau D P,Kassmann C J,Bruns C K,et al.Nickel Superoxide Dismutase Structure and Mechanism[J].Biochemistry,2004,43:8038-8047
[2]Fiedler A T,Bryngelson P A,Maroney M J,et al.Spectroscopic and Computational Studies of Ni Superoxide Dismutase:Electronic Structure Contributions to Enzymatic Function[J].Journal of the American Chemical Society,2005,127:5449-5462
[3]Main F.Model Systems Containing Pyrazole Chelates and Related Groups:Recent Developments and Perspectives[J].Coordination Chemistry Reviews,1992,120:325-359
[4]Zhu L,Liao Z R,Wang Z M,et al.Synthesis and Crystal Structure of Bicobalt(Ⅱ)Complex and Study of Activity[J].Chinese Journal of Inorganic Chemistry,2002,18:731-734
[5]Qin S D,Feng S S,Zhang H M,et al.Synthesis and Crystal Structure of Complex Ni(EDTB)·2Cl·CH3OH·C2H5OH and Its Superoxide Dismutase Mimic Activity[J].Acta Chimica Sinica,2005,63:1155-1160
[6]Liao Z R,Zheng X F,Luo B S,et al.Synthesis,Characterization and SOD-like Activities of Manganese-containing Complexes with N,N,N',N'-tetrakis(2 '-benzimidazolyl methyl)-1,2-ethanediam[J].Polyhedron,2001,20:2813-2822
[7]田春美,钟秋平.超氧化物歧化酶的现状研究进展[J].中国热带医学,2006,8(5):1730-1732
[8]丁书茂,杨旭.超氧化物歧化酶及其模拟化合物研究进展[J].高等函授学报(自然科学版),2004,17(1):1-5
[9]Sun Y,Yin Y X,Liu X L.Quantum Chemistry Calculation of 1,1,4,7,7-Penta(2'-benzimidazol-2-ylmethyl)-triazaheptane[J].Journal of Tianjin Normal University(Natural Science Edition),2004,24:5-7
[10]Birker P J M W L,Abraham J S,Verschoor G C,et al.A New Imidazole-containing Octadentate Ligand,Capable of Binding Two Metal Ions;the X-ray Structure of the Dinuclear ZnCl2Adduct of 1,1,4,7,7-penta(benzimidazol-2-ylmethyl)-1,4,7-triazaheptane[J].Journal of the Chemical Society,Chemistry Communication,1981:1124-1125
[11]Yan X X,Lu L P,Zhu M L.A Novel Bridged Asymmetric Binuclear Manganese(II)Complex with DTPB [DTPB is 1,1,4,7,7-pentakis(1H-benzimidazol-2-ylmethyl)-1,4,7-triazaheptane][J].Acta Crystallographica Section C,2004,60:m221-m223
[12]Meng X G,Liu L,Zhou C S,et al.Dinuclear Copper(II)Complexes of a Polybenzimidazole Ligand:Their Structures and Inductive Roles in DNA Condensation[J].Inorganic Chemistry,2008,47:6572-6574
[13]Wu H L,Gao Y C.Synthesis,Characterization and Mimic SOD Activity of Superoxide Dismutase Model Complexes[J].HuaXueTongBao,2003,11:770-774
[14]Luo Q H.Studies on Simulation Chemistry of Cu-Zn Superoxide Dismutase[J].Chemical Journal of Chinese Universities,1997,18(7):1012-1018
[15]Muller J,Felix K,Maichle C,et al.Phenyl-substituted copper di-Schiff base,a potent Cu2Zn2superoxide dismutase mimic surviving competitive biochelation[J].Inorganica Chimica Acta,1995,233(9):11-19

