2型糖尿病住院患者2 454例视网膜病变的危险因素分析
王 婕,吴 强 , 于浩泳, 李连喜, 包玉倩, 贾伟平
(上海交通大学附属第六人民医院:内分泌代谢科 上海市糖尿病重点实验室 上海市糖尿病临床医学中心1,眼科2, 上海200233)
近年来随着经济的快速发展和生活方式的改变,我国的糖尿病患者人数亦明显增加。中华医学会糖尿病学分会 2008年完成的全国糖尿病和代谢疾病研究(The China National Diabetes and Metabolic Disorders Study)表明,我国20岁以上人群中糖尿病和糖尿病前期的患病率已分别达 9.7%和15.5%,糖尿病患者数估计为9240万,糖尿病前期患者数约为1.5亿[1]。随着糖尿病人数的激增,糖尿病微血管并发症的危害也日益严重,其中糖尿病视网膜病变是导致成人失明的最主要原因[2],不仅严重影响了患者的生活质量,由此产生的医疗费用也给社会造成了极大的经济负担,有研究显示,中国2型糖尿病伴眼病的患者人均年治疗费用为无并发症患者的6.51倍[3]。最近的一项上海糖尿病并发症研究显示,社区糖尿病患者中,糖尿病视网膜病变(diabetic retinopathy, DR)的患病率为9.4%,其中糖尿病病程、血糖水平、糖化血红蛋白水平等是其独立危险因素[4]。而住院患者中 DR所占比例尚不可知,另外,住院患者受血压、血脂、血糖、病程、其他大血管和微血管并发症以及药物等多重因素影响,其 DR情况势必更加复杂。因此,本文就住院患者中糖尿病视网膜病变患病率展开调查并分析其分布特征,同时就影响 DR发生发展的因素进行深入探讨,以期为DR的防治提供科学依据。
1 对象与方法
1.1 研究对象
本研究入选上海交通大学附属第六人民医院内分泌代谢科住院2型糖尿病患者2454例,其中男性1276例,女性1178例,平均年龄(60.8±12.5)岁。本研究所有入选样本均按照世界卫生组织 1999年糖尿病的诊断标准确诊为2型糖尿病患者。同时,详细记录其家族史、高血压、血脂异常、心血管疾病史,女性患者询问其是否有巨大儿生产史。1型糖尿病、妊娠糖尿病及特殊类型糖尿病患者予以排除。本研究经上海交通大学附属第六人民医院医学伦理委员会批准,所有受试者均签署了知情同意书。
1.2 人体学参数及实验室检查
所有入选研究对象均测量血压、身高、体质量等基本人体学参数,同时计算体质量指数(body mass index, BMI)=体质量/身高2。血压测量采用标准水银血压计,测量3次后取平均值。
所有研究对象均抽取静脉血检测糖脂代谢指标,包括空腹血糖(fasting blood glucose, FBG)、餐后2小时血糖(2hPG,葡萄糖氧化酶-过氧化物酶法,上海生物制品研究所)、糖化血红蛋白(HbA1c;高压液相色谱法。Bio-Rad variant Ⅱ,NGSP,美国)以及甘油三酯(triglycerides, TG)、总胆固醇(total cholesterol, TC)、低密度脂蛋白胆固醇(low density lipoprotein cholesterol, LDL-C)和高密度脂蛋白胆固醇(high density lipoprotein cholesterol, HDL-C;全自动生化分析仪7600-20,HITACHI,日本)。
1.3 免散瞳眼底摄片进行视网膜病变分级
所有研究对象均进行眼底检查,使用免散瞳眼底数码成像系统(Canon CR6-45NM, Lake Success,New York, USA)进行眼底摄片。两个专业的眼科医师进行独立阅片,并根据糖尿病视网膜病变严重程度量表(Diabetic Retinopathy Disease Severity Scale)对DR进行分级[5]。0级:无明显异常;1级:轻度非增殖性视网膜病变(仅有微动脉瘤);2级:中度非增殖性视网膜病变;3级:重度非增殖性视网膜病变;1~3级均为非增殖性糖尿病视网膜病变(non-proliferative diabetic retinopathy, NPDR);4级:增殖性糖尿病视网膜病变(proliferative diabetic retinopathy, PDR)。
1.4 统计学处理
符合正态分布的连续变量均采用均数±标准差表示,非正态分布的变量采用中位数表示,两组间均数比较采用t检验或Wilcoxon秩和检验,不同组间率的比较采用趋势检验,DR风险因素分析采用logistic逐步回归分析,双侧P<0.05为差异具有统计学意义。所有数据处理及统计分析用 SAS 6.12(SAS Institute Inc.,Cary NC)进行。
2 结 果
2.1 住院2型糖尿病患者DR的患病率及其分布特征
本研究显示,其中803例患者存在DR,总体患病率为 32.7%(803/2454)。将研究对象按照是否存在DR分组后发现,两组患者在年龄、性别、病程、初次诊断年龄、BMI、收缩压及舒张压等指标差异具有统计学意义(P<0.05),DR组的年龄、病程大于非 DR组,收缩压及舒张压水平均高于非DR组,而诊断年龄小于DR组。研究对象基本临床特征见表1。
如表2~4 所示,将研究对象按年龄、病程、血糖水平等因素分层分析后发现,随着年龄的增加,病程的延长及 HbA1c的增高,DR患者的比例逐渐增高(P<0.05),NPDR的比例也逐渐升高(P<0.05),而PDR比例在不同年龄及HbA1c水平层次差异无统计学意义(P>0.05)。但是,随着病程的延长,PDR的发生率仍逐渐升高,差异具有统计学意义(P<0.0001)。
2.2 住院2型糖尿病患者DR的危险因素分析
将患者的诊断年龄、性别、病程,HbA1c,收缩压、舒张压等指标纳入logistic逐步回归分析后发现,病程(OR=1.107,95% CI 1.089~1.125,P<0.0001),HbA1c水平(OR=1.071,95% CI 1.024~1.119,P=0.0026),收缩压水平(OR=1.016,95%CI 1.010~1.022,P<0.0001)是2型糖尿病患者发生DR的独立危险因素,诊断年龄也与DR发生风险也具有关联趋势(OR=0.991,95% CI 0.981~1.000,P=0.0556)。而性别及舒张压水平与DR的关联无统计学差异(表5)。
3 讨 论
目前,关于 DR的患病率及分布特点在不同研究中存在较大差异。本研究结果显示,在2型糖尿病住院患者中,DR的患病率为32.7%,该结果与包括 BMES(35.5%),United Kingdom Prospective Diabetes Study(UKPDS, 37%),Pima Indians Study(31.8%)在内的多个欧洲国家研究结果相似[6-8],同时也与Beijing Eye Study(37.1%)及Sinapore EyeStudy(35.0%)这两个亚洲组织的结果类似[9,10]。但是,本研究调查所得患病率明显高于 AustralianDiabetes Obesity and Lifestyle Study(AusDiab,15.3%)及Chennai Urban Rural Epidemiology Study(CURES, 25.7%)[11,12],原因可能是这两项研究都是在普通人群中进行的调查,而我们的研究主要聚焦于已经确诊的2型糖尿病住院患者,后者与普通人群相比在年龄、病程及血糖等情况上都存在显著差异。
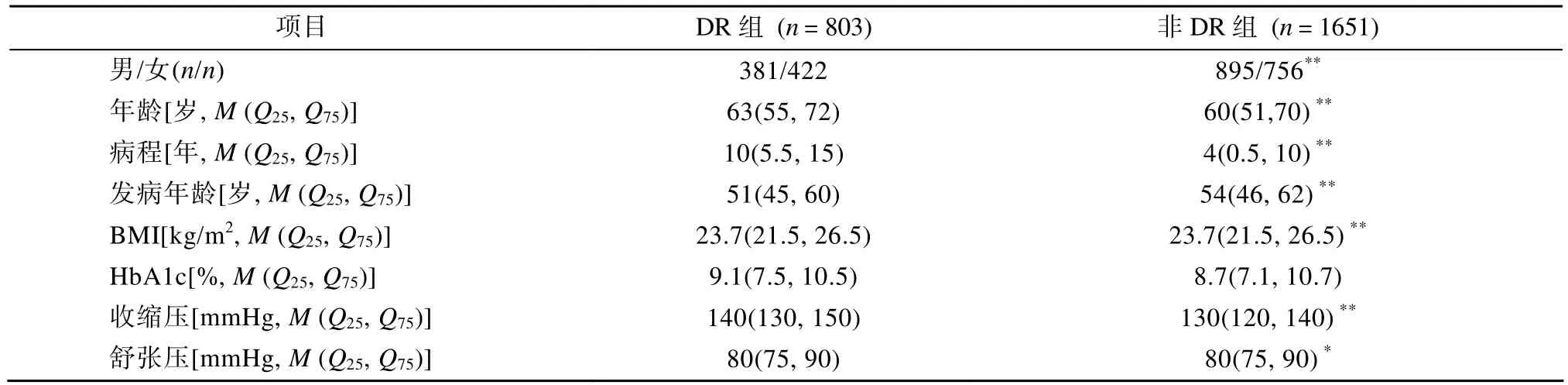
表1 入选2型糖尿病患者一般临床特征Table 1 Clinical characteristics of study population

表2 不同年龄段2型糖尿病患者视网膜病变及增殖性视网膜病变的患病率Table 2 Prevalence of diabetic retinopathy and proliferative diabetic retinopathy in type 2 diabetes in different age groups
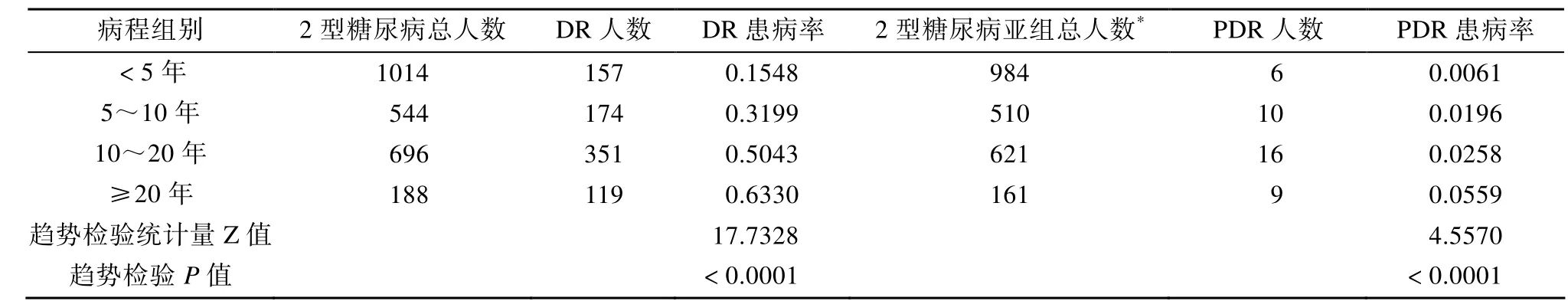
表3 不同病程2型糖尿病患者视网膜病变及增殖性视网膜病变的患病率Table 3 Prevalence of diabetic retinopathy and proliferative diabetic retinopathy in type 2 diabetes in different diabetes duration groups

表4 不同糖化血红蛋白水平2型糖尿病患者视网膜病变及增殖性视网膜病变的患病率Table 4 Prevalence of diabetic retinopathy and proliferative diabetic retinopathy in type 2 diabetes with different glycosylated hemoglobin levels groups

表5 2型糖尿病患者视网膜病变相关危险因素的逐步logistic回归分析Table 5 Identification of independent risk factors for diabetic retinopathy in patients with type 2 diabetes by stepwise logistic regression analysis
最近有一项包含了全球35个研究,共计22 896例2型糖尿病患者的调查表明,长病程,高血糖及高血压与 DR及其严重程度高度相关[13]。同时,DCCT及UKPDS的研究也表明,严格控制血糖可延缓DR的发生发展[7,14]。而本研究结果与以上研究结果高度一致,随着患者病程延长及HbA1c水平增高,DR患者的人数逐渐增高,同时 NPDR的比例也随之升高,而 logistic逐步回归结果也同样证实长病程、高HbA1c及收缩压水平是DR的独立危险因素。另外,我们按照患者年龄分层后,发现随着年龄的增长,DR及 NPDR人数逐渐上升,但是将年龄纳入logistic逐步回归后,却并未发现年龄与DR发病风险的相关性,而诊断年龄却与 DR的发生有一定相关趋势(OR=0.991,95% CI 0.981~1.000,P=0.0556),即诊断年龄越小,DR可能发生风险越高。我们认为病程在其中起到了不可忽视的作用,即DR和NPDR人数随年龄的增长而增加是通过病程起作用的,因此在logistic逐步回归分析,校正病程后,年龄与DR的风险相关性也随之消失。
与既往多项研究相一致的是,糖尿病患者中高血压与 DR的发生高度相关,也就是说,高血压是糖尿病患者发生 DR的独立危险因素,其内在机制可能在于高血压导致了血流动力的改变(如自身调节受损等)以及视网膜血管内皮细胞中血管生长因子表达上调,从而导致了DR的发生发展[15]。
尽管本研究针对2型糖尿病住院患者视网膜并发症的患病率及其危险因素进行了调查分析,但是本研究仅基于上海地区一所三级甲等医院的调查结果,其在上海地区以至南方地区的代表性仍需要多中心合作及更大样本的进一步证实。
综上所述,本研究系统分析了已经确诊的2型糖尿病住院患者糖尿病视网膜病变的患病情况及分布特点,并对影响 DR发生发展的风险因素做了综合的分析。针对相关因素进行早防早治,不仅可以有效避免部分高危人群发生 DR,还可以有效延缓DR的发展恶化,这对提高糖尿病患者的生活质量,减轻社会经济负担大有裨益。
[1]Yang W, Lu J, Weng J,et al. Prevalence of diabetes among men and women in China[J]. N Engl J Med, 2010, 362(12):1090-1101.
[2]Thylefors B, Negrel AD, Pararajasegaram R,et al. Global data on blindness[J]. Bull World Health Organ, 1995, 73(1):115-121.
[3]陈兴宝, 唐 玲, 陈慧云, 等. 2 型糖尿病并发症对患者治疗费用的影响评估[J]. 中国糖尿病杂志, 2003, 11(4):238-241.
[4]Pang C, Jia L, Jiang S,et al. Determination of diabetic retinopathy prevalence and associated risk factors in Chinese diabetic and pre-diabetic subjects: Shanghai diabetic complications study[J]. Diabetes Metab Res Rev, 2012, 28(3):276-283.
[5]Wilkinson CP, Ferris FL 3rd, Klein RE,et al. Proposed international clinical diabetic retinopathy and diabetic macular edema disease severity scales[J]. Ophthalmology,2003, 110(9): 1677-1682.
[6]Mitchell P, Smith W, Wang JJ,et al. Prevalence of diabetic retinopathy in an older community. The Blue Mountains Eye Study[J]. Ophthalmology, 1998, 105(3): 406-411.
[7]Stratton IM, Kohner EM, Aldington SJ,et al. UKPDS 50:risk factors for incidence and progression of retinopathy in Type II diabetes over 6 years from diagnosis[J]. Diabetologia,2001, 44(2): 156-163.
[8]Looker HC, Krakoff J, Knowler WC,et al. Longitudinal studies of incidence and progression of diabetic retinopathy assessed by retinal photography in pima indians[J]. Diabetes Care, 2003, 26(2): 320-326.
[9]Xie XW, Xu L, Jonas JB,et al. Prevalence of diabetic retinopathy among subjects with known diabetes in China:the Beijing Eye Study[J]. Eur J Ophthalmol, 2009, 19(1):91-99.
[10]Wong TY, Cheung N, Tay WT,et al. Prevalence and risk factors for diabetic retinopathy: the Singapore Malay Eye Study[J]. Ophthalmology, 2008, 115(11): 1869-1875.
[11]Tapp RJ, Shaw JE, Harper CA,et al. The prevalence of and factors associated with diabetic retinopathy in the Australian population[J]. Diabetes Care, 2003, 26(6): 1731-1737.
[12]Rema M, Premkumar S, Anitha B,et al. Prevalence of diabetic retinopathy in urban India: the Chennai Urban Rural Epidemiology Study (CURES) eye study, I[J]. Invest Ophthalmol Vis Sci, 2005, 46(7): 2328-2333.
[13]Yau JW, Rogers SL, Kawasaki R,et al. Global prevalence and major risk factors of diabetic retinopathy[J]. Diabetes Care, 2012, 35(3): 556-564.
[14]The relationship of glycemic exposure (HbA1c) to the risk of development and progression of retinopathy in the diabetes control and complications trial[J]. Diabetes, 1995, 44(8):968-983.
[15]Srivastava BK Rema M. Does hypertension play a role in diabetic retinopathy[J]? J Assoc Physicians India, 2005, 53:803-808.

