多奈哌齐联合维拉帕米对阿尔茨海默病模型大鼠学习记忆功能的保护作用
廖珏 董雯
(1.泸州医学院基础医学院病原生物中心,四川 泸州 646000;2.北京中医药大学东方学院临床医学系,河北 廊坊 065001)
阿尔茨海默病(Alzheimer′s disease,AD)是老年性痴呆的一种,多发生于中年或老年的早期,其发病率随年龄增长不断增高。目前,全球人口渐趋老龄化,AD的发病率将逐渐增高。AD涉及老年人的健康问题,带来严峻的社会问题和经济问题。因此,提高对AD的认识、重视,减少其发病,已迫在眉睫。关于AD其发病机制尚未明确,有文献报道[1-2]:AD患者胆碱能神经受到损伤和细胞内钙稳态失调。
多奈哌齐是近年来应用于临床的一种新型可逆性胆碱酯酶抑制剂,而维拉帕米是一种作用于慢通道的钙离子拮抗剂。本实验通过Aβ1-40右侧海马区立体定向微量注射法制备大鼠AD模型,用多奈哌齐与维拉帕米进行干预,观察药物对AD模型大鼠记忆障碍、大鼠海马系数比以及海马的AChE活性,并行尼氏染色光镜观察海马组织形态结构的变化。
1 材料与方法
1.1 材料
1.1.1 仪器与试剂
脑立体定位仪及定位图谱(美国 Myneurolab公司);颅骨钻;微量进样器;722分光光度计;Aβ1-40(美国Sigma公司),无菌生理盐水配置成2g·L-1溶液,置于37℃温箱中孵育1w,使其变为具有神经毒性的凝聚状态;多奈哌齐和维拉帕米由中国药品生物制品检定所提供;AChE测定试剂盒由南京建成生物工程研究所提供。
1.1.2 实验动物与分组
清洁级健康成年雄性SD大鼠(重庆滕鑫生物科技有限公司)40只,体重250±30g。随机分成4组,每组l0只,即假手术组、模型组、多奈哌齐组和联合用药组。
1.2 方法
1.2.1 AD大鼠模型的建立
参照《大鼠脑立体定位图谱》[3],选择右侧海马区(前囟向后3.5mm,中线右旁2.8mm,硬脑膜下2.5mm)为注射靶区。用骨钻钻开颅骨,暴露硬脑膜,用10μ1微量进样器自脑表面垂直进针2.5mm,以0.5μ1·min-1的速度均匀注入 Aβ1-40溶液5μ1,10min注射毕后,留针10min以保证溶液充分弥散,然后缓慢撤针,缝合切口,于缝合处予滴0.1ml庆大霉素注射液,并用4万U青霉素肌肉注射以抗感染,保暖至清醒,放回笼中常规饲养。假手术组以等量无菌生理盐水代替Aβ1-40溶液,其余操作同上。所有操作均在相对无菌条件下进行。
1.2.2 给药方法
假手术组、模型组:将蒸馏水按照大鼠体重8ml·kg-1灌胃,1 次 ·d-1;多 奈 哌 齐 组:大 鼠 多 奈 哌 齐 剂 量0.525mg·kg-1。将 制 备 的 多 奈 哌 齐 溶 液 给 予 一 次8ml·kg-1灌胃,1次·d-1;联合用药组:大鼠多奈哌齐剂量0.525mg·kg-1,维拉帕米剂量3mg·kg-1。将制备的多奈哌齐溶液和维拉帕米溶液混合给予一次8ml·kg-1灌胃,1次·d-1;每天上午10时灌胃给药,持续4w。
1.2.3 Morris水迷宫实验
灌胃4w后,采用Morris水迷宫对所有大鼠进行行为认知测试。在整个实验中保持操作者位置及周围环境的相对稳定。固定时问为每日9:00~16:00进行。Morris水迷宫[4]主要由圆形水池和自动录像及分析系统组成。定位航行试验:历时5 d,每日分上、下午两个时段,每个时段分别从4个不同的入水点,将大鼠面向池壁放人水中,记录2min内寻找平台所需总游泳路程(即逃避潜伏游程)。若大鼠人水后2min内未能找到平台,则将其置于平台上并停留l0s。每次训练问隔60s。
1.2.4 海马系数测定
行为学测试结束后,每只动物称重并处死,于冰浴中迅速取出脑组织,剥离出大脑皮层和海马组织,并精确称量海马湿重。同时按照下列公式计算海马系数:海马系数(%)=海马湿重(g)/体重(g)×100%。
1.2.5 海马组织中AChE活性的测定
乙酰胆碱酯酶(AChE)水解乙酰胆碱(ACh)生成胆碱及乙酸,胆碱可以与巯基显色剂反应生成TNB(对称三硝基苯,Sym-Trinitrobenzene)黄色化合物,根据颜色的深浅进行比色定量,水解产物胆碱的数量可反映胆碱酯酶的活力。取10%组织匀浆40μl,按试剂盒要求配试剂,混匀,静置15min,于412nm处测各管OD值。组织匀浆中AChE活力(U·mg-1prot)=(测定管OD值-对照管OD值)÷(标准管OD值-空白管OD值)×标准管浓度(1μmol·ml-1)÷蛋白含量(mg prot·ml-)。
1.2.6 尼氏染色
切片脱蜡,梯度酒精脱水后入蒸馏水。于预热至60℃的1%甲苯胺蓝30min后,以蒸馏水速洗,用95%酒精分色,镜检至神经元尼氏体清晰。无水酒精脱水,二甲苯透明,中性树胶封片。
1.3 统计学方法
2 结果
2.1 定位航行能力变化
定位航行试验,用于检测动物在水迷宫的学习能力[4]。经过5d寻找隐藏平台的定位航行训练,从表1可知,同模型组比较,假手术组、多奈哌齐组和联合用药组逃避潜伏游程均缩短,具有统计学显著性差异(P<0.01);同假手术组比较,多奈哌齐组和联合用药组逃避潜伏游程有所延长,但无统计学差异;多奈哌齐组与联合用药组之间逃避潜伏游程无统计学差异。
表1 逃避潜伏游程变化(m)(,n=10)
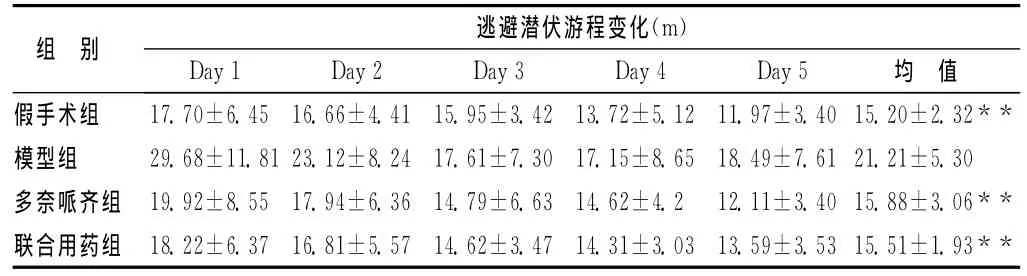
表1 逃避潜伏游程变化(m)(,n=10)
注:同模型组比较,**P<0.01。
组 别 逃避潜伏游程变化(m)Day 1 Day 2 Day 3 Day 4 Day 5 均 值假手术组 17.70±6.4516.66±4.4115.95±3.4213.72±5.1211.97±3.4015.20±2.32**模型组 29.68±11.8123.12±8.2417.61±7.3017.15±8.6518.49±7.6121.21±5.30多奈哌齐组 19.92±8.5517.94±6.3614.79±6.6314.62±4.212.11±3.4015.88±3.06**联合用药组 18.22±6.3716.81±5.5714.62±3.4714.31±3.0313.59±3.5315.51±1.93**
2.2 海马系数变化
从表2可见,同模型组比较,假手术组、多奈哌齐组和联合用药组具有统计学差异,其中假手术组和联合用药组具有统计学显著性差异;模型组海马系数显著降低,多奈哌齐组、联合用药组海马系数增加,提示药物具有抗海马萎缩的作用,其中联合用药效果更佳。
表2 海马系数以及海马组织AChE活性变化(,n=10)

表2 海马系数以及海马组织AChE活性变化(,n=10)
注:同模型组比较,*P<0.05,**P<0.01。
组 别 海马系数(10-4) AChE活性(U·mg-1 prot)假手术组 7.63±1.38** 0.83±0.46**模型组 5.40±0.66 3.08±1.50多奈哌齐组 7.17±1.21* 1.33±0.58*联合用药组 7.30±2.00** 1.04±0.54**
2.3 海马组织AChE活性变化
从表2可见,同模型组比较,假手术组、多奈哌齐组和联合用药组海马组织AChE活性减弱,具有统计学差异,其中假手术组和联合用药组具有统计学显著性差异;同假手术组比较,多奈哌齐组和联合用药组海马组织AChE活性有所增强,但无统计学差异;多奈哌齐组与联合用药组之间海马组织AChE活性差异较小,无统计学差异。
2.4 海马CA3神经元尼氏染色
假手术组海马CA3区组织结构正常,无病理变化,偶见神经细胞损伤和尼氏体丢失。海马锥体细胞排列整齐且紧密,胞浆染色清晰,尼氏体丰富。模型组海马CA3区出现神经细胞变性坏死。海马锥体细胞数目减少,结构模糊,胞体肿胀,排列散乱,并且胞浆内大面积的尼氏体丢失,尼氏体呈少而小,散在分布。多奈哌齐组与联合用药组海马CA3区基本病变减轻,同模型组比较,锥体细胞排列较整齐,较紧密,胞浆内尼氏体较丰富,较清晰,见图1。
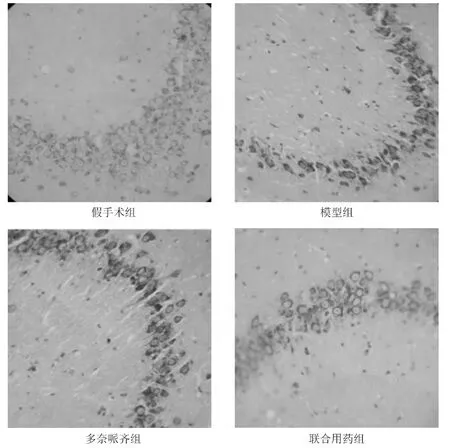
图1 海马CA3神经元尼氏染色(×400)
3 讨论
近年来,Aβ学说的推出为AD模型研究提供新的思路[4]。Aβ是AD大脑中老年斑的主要成分,是AD起始和进展的关键因子,是AD发病机制中的一个最重要环节[5]。
Morris水迷宫是英国心理学家Morris在1981年设计并应用于研究大脑学习和记忆的装置,能比较客观的衡量动物的空间记忆,工作记忆以及空间辨别能力的改变[6]。定位航行实验结果表明:模型组逃避潜伏游程较假手术组明显延长,多奈哌齐组和联合用药组明显短于模型组,说明模型组在实验期间学习能力有所下降,多奈哌齐组和联合用药组学习能力明显改善。逃避潜伏游程变化趋势看,假手术组越来越短,符合学习越来越快特点,模型组逃避潜伏游程上下波动,多奈哌齐组和联合用药组变化趋势不如假手术组,但是优于模型组,推测可能是注射Aβ1-40造成海马损伤,导致学习过程不稳定,而多奈哌齐组和联合用药组相对于模型组有所改善。
本文结果表明,模型组海马组织AChE活性升高,必然导致体内ACh水平下降。多奈哌齐组海马组织AChE活性有下降趋势,说明多奈哌齐作为可逆性中枢AChE抑制剂,具有较强的AChE抑制作用。本实验中,造模药物Aβ1-40可使AChE活性升高,加速Ach分解,破坏胆碱能神经传导相关的信号通路,进而使胆碱能系统受损,导致认知功能障碍[7,8]。通过抑制AChE活性、增高Ach生物学作用,减轻Aβ1-40的沉积作用,加快Aβ1-40的代谢,有效阻止胆碱能神经元的继续丢失,缓解AD患者记忆力下降和认知功能障碍的临床症状。联合用药组的大鼠大脑海马组织AChE活性有明显下降趋势,说明除多奈哌齐发挥AChE抑制作用外,维拉帕米也可减轻Aβ1-40对AChE活性的影响。体外实验表明Aβ可形成一种跨膜的离子通道,能有效转运Ca2+,维拉帕米作为钙离子抑制剂,可能抑制Aβ所致的Ca2+内流,从而减轻Aβ所引起的胆碱能神经的损害。
尼氏染色主要用于观察海马CA3区锥体细胞的形态特点。尼氏体是神经细胞体内的嗜碱性的小体或细粒,正常状态下神经元尼氏体都有比较固定的形态,是神经细胞存在的重要标志。当神经元受到损伤时,尼氏体会减少或脱失,因而尼氏体是反映神经元功能状态的可靠探针[6]。本实验采用甲苯胺蓝尼氏染色法,可准确地显示尼氏体,清晰显示神经元及其尼氏体的形态。模型组海马CA3区锥体细胞数量明显减少,排列稀疏,细胞间隙明显增大,细胞大面积丢失,残存的细胞有大部分尼氏体变得模糊不清或消失。假手术组海马CA3区锥体细胞胞浆内尼氏体丰富,细胞无丢失且排列整齐。多奈哌齐组和联合用药组海马CA3区锥体细胞胞浆内尼氏体较丰富,细胞无明显丢失,且排列较整齐。这些结果从组织学方面证实模型组具备的AD病理学特征。多奈哌齐和维拉帕米在一定程度上抑制Aβ1-40沉积,减少海马锥体细胞丢失,细胞组织结构正常,学习记忆功能得以较好的维持。
1 曾望远,董克礼.AD的病因机制研究概况[J].湖南中医杂志,2006,22(1):77-80.
2 宋博毅,李兴军.钙代谢障碍与老年痴呆[J].华北煤炭医学院学报,2006,9(5):625-626.
3 包新民,舒斯云.大鼠脑立体定位图谱[M].北京:人民卫生出版社,1991,44-44.
4 Morris R.Development of a water-maze procedure for studying spatial learning in the rat[J].J Neurosci Methods,1984,11(1):47-60.
5 陈罗西,郭玲玲,李亮.Moms圆形水迷宫的应用及其相关检测指标分析[J].辽宁中医药大学学报,2008,l0(8):55-57.
6 Morris RG,Garrud P,Rawlins JN,et al.Place navigation impaired in rats with hippocampal lesion[J].Nature,1982,297(5868):681-683.
7 Melo JB,Agostinho P,Oliv eira CR.Involvement of oxidative stress in the enhancement of acetylcholinesterase activity induced by amyloid beta-peptide[J].Neurosci Res,2003,45(1):117-127.
8 Lane,Roger M,Kivipelto,et a1.Acetylcholinesterase and Its Inhibition in Alzheimer′s disease[J].Clin Neuropharmacol,2004,27(3):141-149.
9 Sommer B.Alzheimer′s disease and the amyloid cascade hypothesis:ten years on[J].Curr Opin Pharmacol,2002,2(1):87-92.
10 黄欣,柳川.以Aβ为靶标治疗阿尔茨海默病的研究进展[J].生物技术通讯,2005,16(1):87-89.
11Yasuhara T,Shingo K,Muraoka K,et al.Neurirescue effects of VEGF on a rat model of Parkinson′s disease[J].J Brain Res,2005,1053(1-2):10-18.

