潜流人工湿地对污水厂尾水中有机物去除效果
杨长明,马 锐,汪盟盟,李建华
(同济大学长江水环境教育部重点实验室,上海200092)
与发达国家相比,我国城镇污水厂处理水平整体较为落后,经过城市污水处理厂处理过的二级出水水质仍然较差[1],满足不了日益增长的地表水水质改善需求,即使出水能稳定达到一级A排放标准,但相对于受纳水体来说,仍是重要的污染源.此外,尾水中还含有一些难以被生物吸收降解的有毒有害物质,直接排放不仅可能导致水体富营养化,而且造成生态毒性,危害人体健康[2].因此,对城镇污水处理厂出水进行深度处理显得尤为必要[3].随着国家对污染物排放总量控制日趋严格,为了保证出水能够达到受纳水体的水质标准且满足回用水水质的要求,污水厂二级出水即尾水深度处理技术,已经提上了日程,并逐渐成为污水处理技术体系中的重要组成部分[4].
城市污水尾水中含有大量难降解有机物,当排入天然水体中时,这些有机污染物会被生物氧化进而大量消耗水中的溶解氧(DO),导致DO浓度下降,使水中大量鱼虾贝类死亡[5].同时,这些有机物含有大量有毒有害成分,如农药、环境激素以及个人护理用品(PPCPs)等.因此,有机物削减是城镇污水处理厂尾水深度处理的重要考核指标之一[6].
人工湿地作为典型的生态处理技术,具有效率高、投资少、能耗低和维护简单的特点,可以适应低浓度污染物去除的要求,将人工湿地处理系统作为常规生物处理工艺的补充,能够最大限度地削减受纳水体的污染物负荷[7].目前,利用人工湿地对尾水深度处理的相关研究已有一些报道,但主要还是基于脱氮除磷效果评价[8],而关于人工湿地对尾水中有机物的去除过程表征研究还鲜有报道.越来越多的研究表明,有机污染物综合指标如化学需氧量(COD)和生化需氧量(BOD),已不足以表征所采用的处理工艺对尾水中有机物的去除过程及净化效率[9].
本文通过构建两种不同基质水平潜流人工湿地小试装置,采用凝胶过滤色谱(GFC)、紫外-可见光光谱(UV-VIS)以及三维荧光光谱(EEM)等技术,较系统地研究了城镇污水处理厂尾水中有机物在两种不同基质水平潜流人工湿地中的降解特性,以评价和探讨潜流人工湿地系统对尾水中有机物的去除效果和机理,也为今后完善和构建城镇污水处理厂尾水人工湿地深度处理工艺提供理论依据和技术支撑.
1 材料与方法
1.1 潜流人工湿地处理系统构建
综合各类人工湿地系统的优缺点及实际应用情况,选择水平潜流湿地系统作为试验平台.水平潜流湿地的水力负荷高,对BOD,COD,总悬浮物(SS),重金属等污染物的去除效果较好,虽然其脱氮除磷效果不及垂直潜流人工湿地,但是其相对造价较低,应用更为广泛[10].装置材料采用厚度为10mm的PVC硬质塑料板,尺寸均为1.55m×0.4m×0.8m(长×宽×深).填料填充高度为0.7m,有效水深为0.6m,湿地有效容积为0.42m3.植物栽种密度为16株·m-2.进水采用穿孔管布水,经过粒径为30~50mm砾石布水区进入湿地填料床.出水经粒径30~50mm砾石收水区进入底部穿孔管,流出湿地系统,试验装置如图1所示.试验装置共两套,分别为陶粒基质和沸石基质湿地系统,植物皆为黄菖蒲.小试装置构建于2009年11月,启动初期采用上海市崇明县城桥镇污水处理厂生活污水接种,启动期间间歇运行,日均换水45L.2010年3月初开始按不同工况连续运行.

图1 水平潜流人工湿地装置及取样点分布(1~9为取样点)Fig.1 Horizontal subsurface flow constructed wetland systems and sampling spot locations
1.2 研究方法
试验用水取自上海市崇明县城桥镇污水处理厂的二沉池出水,试验期间(2010年4月—2010年12月)进水主要污染物质量浓度分别为:COD 46.4~82.7mg·L-1,总氮(TN)4.51~11.30mg·L-1,总磷(TP)0.502~0.711mg·L-1,氨氮(NH3-N)0.716~3.000mg·L-1,其平均C/N比为8.36.由此可以看出,该污水厂尾水各项指标除了COD有超标外,其他各项指标均达到城镇污水厂污水排放一级A标准.
湿地系统运行2个月稳定期后,沿程和不同深度各取样点开始采集水样,每月取样1次,并立即带回试验室分析.所有水样经过0.45μm微孔滤膜过滤后进行水质指标分析:COD采用重铬酸钾法测定,TN采用碱性过硫酸钾消解、紫外-可见光光谱仪测定,NH3-N采用纳氏试剂分光光度法测定,TP采用过硫酸钾消解法、钼锑抗分光光度法测定.溶解性有机碳(DOC)质量分数采用总有机碳分析仪(TOCVCPN Analyzer,日本岛津)测定,具体方法参照《水和废水监测分析方法》[11].
进出水及沿程水中有机物分子质量分布采用GFC测定:样品需要经0.45μm微孔滤膜过滤后再进行测定,进样量为50μL.仪器型号为LC-10ADVP(日本Shimadzu公司).测定条件如下:色谱柱型号为TSK4000,流动相采用超纯水,进样形式为流体动力注入,视差检测器型号为RID-10A,控制器型号为SCL-10AVP,柱温箱型号为CTO-10ASVP.
各取样点水样的吸光度采用紫外-可见光光谱仪进行测定(SHIMADZU,UV2450UV-VIS),波长扫描范围为700~200nm,以1nm为步长中速扫描.使用超纯水作基线,空白为去离子水.三维荧光光谱(EEM)用荧光分光光度计测定,参数设置为光电倍增管(PMT)电压700V,带通Ex=5nm,Em=10nm,响应时间0.5s,扫描速度12 000nm· min-1,扫描光谱波长范围为Ex=220~400nm,Em=250~550nm,以超纯水作为空白.本文中出现的相对荧光强度(记为I)是指荧光光度计仪器检测出的荧光峰峰值.荧光强度用硫酸奎宁单位(QSU)来进行标准化,以消除不同仪器之间的差别,便于对不同文献的数据进行比较.1QSU等于溶解于0.1M硫酸溶液中的1μg·L-1硫酸奎宁溶液在350/450 nm(激发/发射)波长下的荧光强度.在测定前,水样用0.45μm膜过滤(Whatman GF/F)进行预处理.水样用去离子水稀释10倍.
2 结果与讨论
2.1 水平潜流人工湿地对尾水污染物总体去除效果
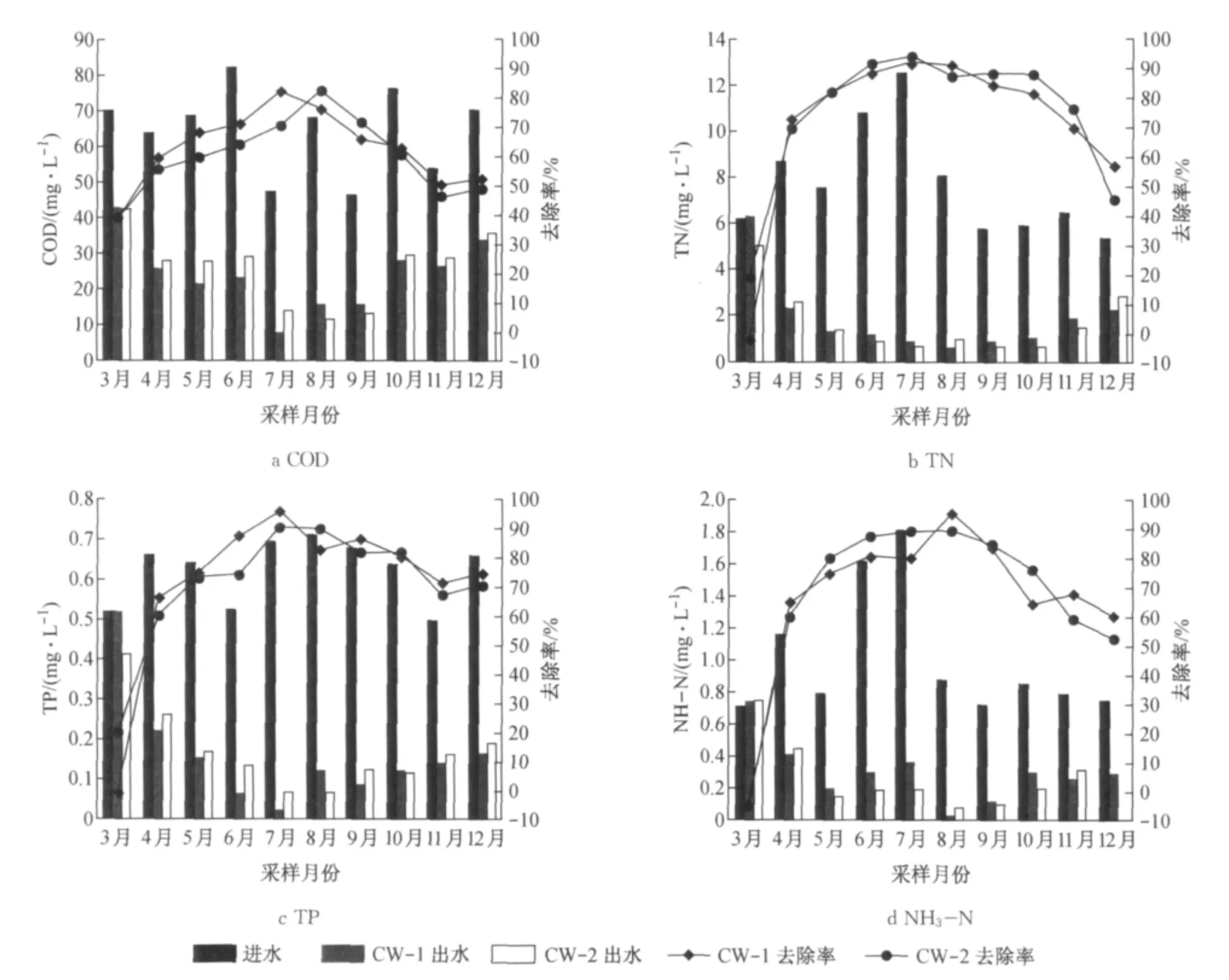
图2 湿地污染物进出水浓度与平均去除率Fig.2 Pollutant concentrations in influent and effluent of constructed wetland and average removal rates
两种不同类型基质潜流人工湿地系统进出水主要污染物浓度以及平均去除率如图2.图2表明,除去稳定阶段的3月份外,所构建的水平潜流人工湿地对污水厂尾水均具有较好的深度净化能力.两种潜流湿地对TP的去除率平均为75.6%,且随季节变化不大;对TN去除率在46.1%~94.5%之间,去除率随着温度的升高而提高,季节性变化较强;出水NH3-N能够稳定达到地表水Ⅱ类标准,TN基本能够稳定达到地表水Ⅳ类标准;出水中COD质量浓度较为稳定,分别为24.28±9.32mg·L-1,26.12± 10.12mg·L-1,平均去除率为63.0%,60.2%.出水除了小试装置调试运行的3月份以及冬季的12月份,出水均可稳定达到地表水Ⅳ类标准.通过对两种基质湿地比较后发现,陶粒基质湿地(CW-1)的去除效果略优于沸石基质湿地(CW-2).若以COD等为去除目标,推荐采用陶粒填料系统;若以TN为去除目标,推荐采用沸石填料系统.
2.2 水平潜流人工湿地中有机物分子质量分布特征
近年来发展起来的GFC是一种简单方便的分子量分布测定方法.它和滤膜过滤法相比,具有快速、灵敏和准确的特点[12].表1为2010年8月25日测定的两种水平潜流人工湿地处理系统中各样点溶解性有机物(DOM)重均分子质量(Mw).由表1可知,进水的Mw为343.2kDa,CW-1湿地出水的Mw为275.9kDa,CW-2湿地出水的Mw为264.9kDa.在经过人工湿地系统处理前后,污水中有机物的分子质量发生了较大的变化,Mw分别降低了19.6%和22.8%,说明两个湿地处理系统对有机污染物都有较好的降解作用,污染物都在向低碳小分子转化.
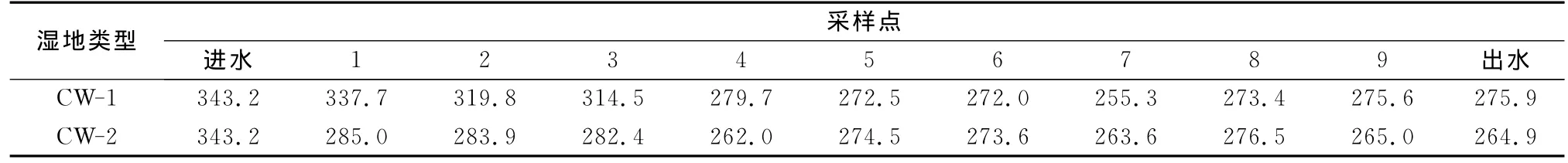
表1 水平潜流人工湿地各采样点水样中有机物的重均分子质量Tab.1 Molecular weight values in influent and effluent of constructed wetland kDa
由表1还可看出,两种基质类型人工湿地系统对于有机物的去除还是有些不同的,对于CW-2湿地,有机物基本上是在前1/4段就完成了大分子向低碳小分子的转化,Mw从进水的343.2kDa下降为283.9kDa,在1/2段后变化不大;而CW-1湿地是在前1/2段才基本完成.在CW-1湿地的前1/4段,有机物的重均分子质量随着深度的增加而减小,对于水平潜流人工湿地,湿地床的深度越深其DO越低,在厌氧状态下大分子有机物能较快地被水解酸化,然后分解转化为小分子有机物.
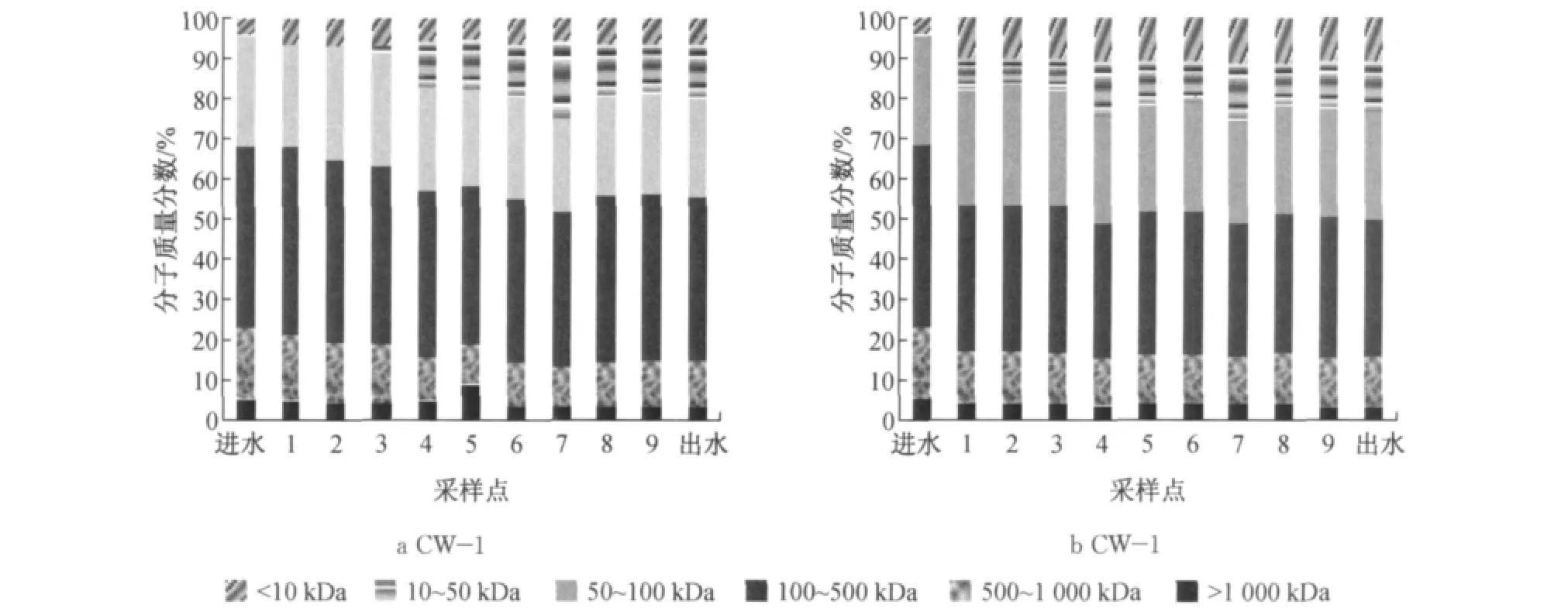
图3 水平潜流湿地各点水样中有机物各分子质量区间百分比Fig.3 Molecular weight distributions and percentage in influent and effluent of constructed wetland
人工湿地进出水样品中的分子质量分布如图3所示.由图3可以看出,进水中有机污染物的分子质量主要集中在50~1 000kDa范围内,占有机物总量的85.4%,10~50kDa的有机物几乎没有,只占到有机物总量的0.05%;人工湿地处理前后水样中有机物各分子质量区间都发生了不同程度的变化,两种湿地出水分子质量>1 000kDa的有机物质量分数从5.28%分别下降为3.6%和3.8%,500~1 000 kDa的有机物质量分数从17.9%分别下降为11.2%和11.9%,100~500kDa的有机物质量分数从44.9%分别下降为40.9%和33.9%,50~100kDa的有机物质量分数从27.49%分别变为24.2%和26.59%,10~50kDa的有机物质量分数则分别增加到13.6%和12.5%,<10kDa的有机物质量分数从4.3%分别变为6.3%和1.1%.表明大分子有机污染物质量分数在人工湿地处理前后都有不同程度的降低,而低于50kDa的有机污染物质量分数有明显增加.人工湿地污水中有机物分子质量的变化基本上在湿地沿程前1/2段就已经达到稳定.在人工湿地处理尾水的过程中,大分子的有机污染物在不断地向低分子有机物转化,湿地下层厌氧环境有利于大分子有机物分解转化的进行[13].
2.3 水平潜流人工湿地对溶解性有机物去除特性的光谱研究
两种基质水平潜流人工湿地各取样点溶解性有机碳(DOC)质量浓度特征吸光系数和比值见表2(2010年8月25日测定结果).从a355来看,基本上人工湿地中各点的吸光度值都呈现出沿程降低的趋势,但是在人工湿地的前1/2段,两个人工湿地a355值的变化趋势却略有不同,CW-1湿地随着湿地的长度逐渐下降,吸光度值降低了43.3%,而CW-2湿地的a355值却呈现出先上升后下降的趋势,从湿地进水口到湿地1/2处吸光度值下降了10.0%.在湿地的后1/2段,两种基质湿地的a355值基本没有发生变化.尾水经过人工湿地处理后,CW-1湿地出水的a355值明显低于CW-2湿地,分别为0.015和0.025.
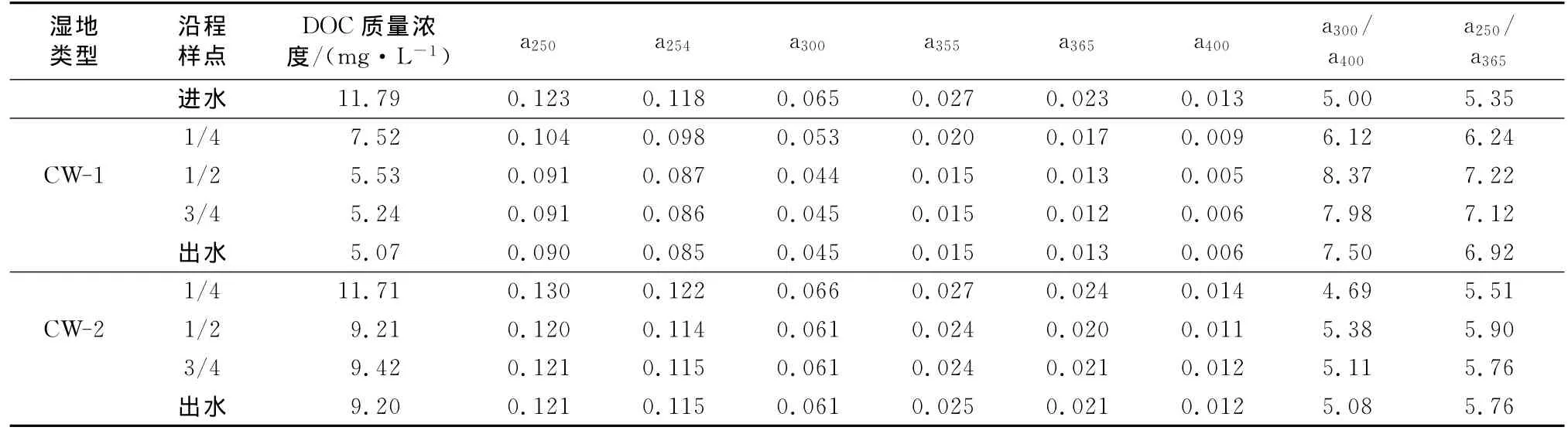
表2 两种不同基质水平潜流湿地各取样点DOC质量浓度、特征吸光系数及比值Tab.2 Molecular weight values in influent and effluent of constructed wetland 104 Da
a300/a400的比值越大,腐殖质的腐殖化程度、芳香性越低,总的来看各样点a300/a400比值均远大于3.5,这表示各点水样的腐殖化程度均不高,芳构化程度较低.两种基质湿地进水中的a300/a400比值均小于湿地出水,这说明经过人工湿地的处理,污水中的腐殖化程度和芳香性均有了不同程度的下降.在湿地中a300/a400的比值呈现出先升高后下降的趋势,腐殖化程度的变化趋势与之相反,先降低后略微升高.在湿地中腐殖化程度高的物质往往很难被植物和微生物利用分解,这个趋势可能反映了水平潜流人工湿地中有机物的利用状况,在人工湿地前半段,污水的腐殖化程度沿着其在湿地床中流动距离的增加而降低;在湿地后半段,随着植物、微生物生长活动所产生的复杂稳定的有机物——腐殖质的增多,出水的腐殖化程度也随之略微升高[14].
a250/a365的比值可表征水中DOM的分子质量,研究表明a250/a365与DOM的平均分子质量呈反比[15].从表中可以看出a250/a365值基本上是沿程逐渐升高,反映分子质量逐渐降低的趋势,与GFC所得的结论相一致.这可能是由于人工湿地系统对有机物良好的降解作用使得水中的大分子有机污染物不断地向低碳小分子转化,虽然植物、微生物的生长活动会产生一些复杂、稳定的大分子有机物,但是其产生量并不会影响水中的有机物向低碳小分子转化的趋势.与CW-2湿地系统相比,CW-1湿地水平潜流人工湿地系统对有机污染物向低碳小分子转化更为彻底,对有机污染物的去除效果更好.
2.4 三维荧光光谱扫描对溶解性有机物在湿地空间变化的特征
图4为2010年8月25日测定的水平潜流人工湿地各采样点水样中溶解性有机物的EEM图谱.由图4可明显看出,人工湿地进水中可以分辨出有4个荧光峰出现,分别是可见类富里酸(M)、紫外类富里酸(A)、色氨酸类芳香族蛋白质(S)和溶解性微生物代谢产物(T).经过人工湿地处理以后,城市污水处理厂尾水DOM 4个荧光峰均出现不同程度下降.相对于CW-2湿地,CW-1湿地对尾水中4个荧光峰削减更为明显.
对EEM图谱中4个特征峰的峰值强度变化进一步分析,从表3可以明显看出,两种基质潜流湿地出水中 M峰的相对荧光强度(I)分别降低了19.2%,13.6%;S峰降低了3.5%,2.2%;T峰降低了10.7%,12.6%,A峰几乎没有发生变化.M峰和T峰的I值在沿程上逐渐减小,M峰和T峰基本上全都是在人工湿地的前1/2段被削减,S峰呈现出先增大后减小的趋势.S峰和T峰属于类蛋白物质,其中S峰为色氨酸类芳香族蛋白质,T峰为溶解性微生物代谢产物;M峰和A峰属于类腐殖质物质.

图4 水平潜流湿地进出水溶解性有机物的EEM图谱Fig.4 EEM spectrum of DOM in influent and effluent of the subsurface constructed wetland

表3 水平潜流湿地各采样点EEM特征荧光峰比较Tab.3 EEM fluorescence peak in influent and effluent of the constructed wetland
有研究表明类蛋白峰能很好地表征水环境的污染状况[16],一般生活污水或微生物活动强烈的水体都可以表现出极强的类蛋白荧光,因此可以把S,T峰的削减视为有机污染物在湿地系统中的分解去除作用.本文研究发现,虽然T峰是溶解性微生物代谢产物,但是其还是能够被湿地中的植物、微生物所分解利用,S峰的荧光强度并没有明显的减小,这可能是因为色氨酸类芳香族蛋白质不能够被湿地中的植物与微生物所降解利用[17].M峰为可见类富里酸,A峰为紫外类富里酸,都属于类腐殖质物质,M峰强度的降低说明了本人工湿地系统只对类腐殖质中的可见类富里酸具有削减作用.一般来说,类腐殖质物质化学性质较为稳定、难于分解,较难被生物利用[18],而人工湿地系统对其却有较好的去除作用.
3 结论
(1)人工湿地进水重均分子质量(Mw)为343.2 kDa,经过CW-1和CW-2湿地系统处理后,污水中有机物的Mw分别降低了19.6%,22.8%,为275.9 kDa,264.9kDa.在潜流人工湿地沿程前1/4段,有机物的重均分子质量随着深度的增加而减小.CW-2湿地是前1/4段就基本上完成了对尾水中有机物大分子向低碳小分子的转化,Mw从进水的343.2kDa下降为283.9kDa,在1/2段后变化不大;CW-1湿地是在前1/2段才基本完成.
(2)人工湿地中各取样点的a355值都呈现出沿程降低的趋势.a355与a254和DOC的变化趋势一致.两种基质人工湿地中所取的样品在254nm和355nm处的吸光度值与DOC具有一定的线性关系,说明污水厂尾水中DOM在总有机质中占有很大比重.湿地各点a250/a365值基本上是沿程逐渐升高,分子质量逐渐降低的趋势.与CW-1湿地系统相比,CW-2水平潜流人工湿地系统对有机污染物向低碳小分子转化更为彻底,对有机污染物的去除效果更好.
(3)湿地进水中表征出四类溶解性有机物,色氨酸类芳香族蛋白质(S)、溶解性微生物代谢产物(T)、可见类富里酸(M)、紫外类富里酸(A).经过人工湿地净化处理后,出水中M峰、S峰、T峰的相对荧光强度都有不同程度的降低,A峰几乎没有发生变化;人工湿地进出水腐殖化程度都较低,湿地中的有机物有可能来自于微生物的生命活动和死亡分解.与CW-2湿地相比较,CW-1湿地水平潜流人工湿地系统对出水M峰、S峰、T峰削减更为明显.
[1] 潘洁,鲍建国,靳孟贵,等.改性膨润土处理污水处理厂二级出水的实验研究[J].环境科学与技术,2011,34(5):140.
PAN Jie,BAO Jianguo,JIN Menggui,et al.Modified bentonite for secondary effluent water from wastewater treatment plant[J].Environmental Science &Technology,2011,34(5):140.
[2] Angéline B,Pedro A I,Renato A Q.A theoretical estimation of the concentration of steroid estrogens in effluents released from municipal sewage treatment plants into aquatic ecosystems of central-southern Chile[J].Science of the Total Environment,2009,407(17):4965.
[3] 安红梅,吴立波,岳尚超.斜发沸石对城市污水处理厂二级出水中氨氮的处理效果研究[J].环境工程学报,2010,4(5):1111.
AN Hongmei,WU Libo,YUE Shangchao,et al.Experimental study on removal of ammonia nitrogen in secondary effluent by clinoptilolite[J].Chinese Journal of Environmental Engineering,2010,4(5):1111.
[4] 王文相,胡淳良,徐峥,等.芦村污水厂升级改造及四期工程深度处理工艺设计[J].中国给排水,2010,26(22):30.
WANG Wenxiang,HU Chunliang,XU Zheng,et al.Design of advanced treatment process in upgrading reconstruction project and fourth-phase project of Wuxi Lucun WWTP[J].China Water &Wastewater,2010,26(22):30.
[5] Reungoat J,Escher B I,Macova M,et al.Biofiltration of wastewater treatment plant effluent:effective removal of pharmaceuticals and personal care products and reduction of toxicity[J].Water Research,2011,45(9):2751.
[6] 邵永怡.固相萃取工作站-气相色谱法测定污水处理厂进出水中有机污染物[J].现代科学仪器,2009(5):94.
SHAO Yongyi.Detection of semi-volatile organic contaminant in influent and effluent from municipal sewage-treatment plant with auto-trace extraction workstation[J].Modern Scientific Instruments,2009(5):94.
[7] Jos T V,Arthur F M.Wetlands for wastewater treatment:opportunities and limitations[J].Ecological Engineering,1999,12(1-2):5.
[8] Ghosh D,Gopal B.Effect of hydraulic retention time on the treatment of secondary effluent in a subsurface flow constructed wetland[J].Ecological Engineering,2011,36(8):1044.
[9] 杨长明,马锐,山城幸,等.组合人工湿地对城镇污水处理厂尾水中有机物的去除特征研究[J].环境科学学报,2010,30(9):1804.
YANG Changming,MA Rui,Miyuki Yamashiro,et al.A pilot-scale study on removal characteristics of organic substances in municipal sewage plant effluent by a hybrid constructed wetland[J].Acta Scientiae Circumstantiae,2010,30(9):1804.
[10] Avila C,Pedescoll A,Matamoros V,et al.Capacity of a horizontal subsurface flow constructed wetland system for the removal of emerging pollutants:an injection experiment[J].Chemsphere,2010,81(9):1137.
[11] 国家环保总局.水和废水监测分析方法[M].第四版.北京:中国环境科学出版社,2002.
Department of Environment Protection of China.Analysis methods for water and wastewater[M].4th ed.Beijing:Chinese Environment Science Press,2002.
[12] Garcia-Lopez E,Anderstam B,Heimburger O,et al.Determination of high and low molecular weight molecules of icodextrin in plasma and dialysate,using gel filtration chromatography,in peritoneal dialysis patients[J].Peritoneal Dialysis International,2005,25(2):181.
[13] Farnet A M,Prudent P,Ziarelli F,et al.Solid-state C-13NMR to assess organic matter transformation in a subsurface wetland under cheese-dairy farm effluents[J].Bioresource Technology,2010,100(20):4899.
[14] Keller J K,Weisenhorn P B,Megonigal J P.Humic acids as electron acceptors in wetland decomposition[J].Soil Biology &Biochemistry,2009,41(7):1518.
[15] 钟润生,张锡辉,管运涛,等.三维荧光指纹光谱用于污染河流溶解性有机物来源示踪研究[J].光谱学与光谱分析,2008,28(2):347.
ZHONG Runsheng,ZHANG Xihui,GUAN Yuntao,et al.Three-dimensional fluorescence fingerprint for source determination of dissolved organic matters in polluted river[J].Spectroscopy and Spectral Analysis,2008,28(2):347.
[16] 傅平青,刘丛强,吴丰昌,等.溶解有机质的三维荧光光谱特征研究[J].光谱学与光谱分析,2005,25(12):20.
FU Pingqing,LIU Congqiang,WU Fengchang,et al.Threedimensional excitation emission matrix fluorescence spectroscopic characterization of dissolved organic matter[J].Spectroscopy and Spectral Analysis,2005,25(12):20.
[17] Tedetti M,Cuet P,Guigue C,et al.Characterization of dissolved organic matter in a coral reef ecosystem subjected to anthropogenic pressures(La Reunion Island,Indian Ocean)using multi-dimensional fluorescence spectroscopy[J].Science of the Total Environment,2010,409(11):2198.
[18] Yamashita Y,Scinto L J,Maie N,et al.Dissom matter characteristics across a subtropical wetland’s landscape:application of optical poperties in the assessment of environmental dynamics[J].Ecosystems,2010,13(7):1006.

