利奈唑胺治疗ICU脓毒症的临床评价
陈 畅,张 彧
(大连医科大学附属第一医院急诊ICU,辽宁大连 116011)
利奈唑胺治疗ICU脓毒症的临床评价
陈 畅,张 彧
(大连医科大学附属第一医院急诊ICU,辽宁大连 116011)
[目的]评价利奈唑胺治疗ICU脓毒症的疗效与安全性。[方法]收集接受利奈唑胺治疗60例脓毒症患者的临床资料。观察临床疗效、不良反应及病原学监测情况。[结果]60例脓毒症患者治疗总有效率为76.67%(46/60),耐甲氧西林金黄色葡萄球菌感染患者有效率75%(24/32),表皮葡萄球菌感染患者有效率83.33%(10/12),屎肠球菌感染患者有效率71.43%(10/14),粪肠球菌感染患者有效率83.33%(5/6),人葡萄球菌感染患者有效率100%(4/4),耳葡萄球菌感染患者有效率100%(2/2),微球菌属感染患者有效率100%(2/2),治疗过程中不良反应发生率为18.33%。[结论]利奈唑胺是治疗ICU重症感染有效、安全的药物。
利奈唑胺;脓毒症;有效性
革兰阳性菌是20世纪80年代以来美国脓毒症最主要的致病菌,临床能用于治疗的药物有限,细菌耐药情况日益严重,治疗难度大,死亡率居高不下。糖肽类抗生素是治疗耐药革兰阳性球菌感染的一线用药,但近年来有耐药菌株的报道,利奈唑胺于2004年4月由美国食品和药品管理局(FDA)批准上市,是全球第一个上市的人工合成的唑烷酮类抗菌药物,BassettiM等[1]表明利奈唑胺治疗革兰阳性球菌脓毒症疗效较好。利奈唑胺国内上市时间短,关于利奈唑胺临床应用方面国内报道较少。本文回顾性分析了2010年6月—2011年11月期间大连医科大学附属第一医院急诊ICU应用利奈唑胺治疗耐药革兰阳性球菌引起的脓毒症60例患者的临床资料,以评价其疗效及安全性。
1 资料与方法
1.1 临床资料
选取2010年6月—2011年l1月在大连医科大学附属第一医院急诊ICU住院接受利奈唑胺治疗的耐药革兰阳性球菌脓毒症患者60例(排除没有明确病原学依据或使用利奈唑胺<3 d者)。其中男34例,女26例,平均年龄58.90岁(17~90岁)。脓毒症、严重脓毒症诊断标准见文献[2]。患者有全身炎症反应综合征(SIRS)表现且有明确的感染灶诊断为脓毒症。脓毒症伴有器官功能障碍和低灌注诊断为严重脓毒症。本研究60例患者中有34例符合严重脓毒症的诊断标准。患者分别接受头孢三代、氟喹诺酮、碳青霉烯类等抗生素治疗3~8 d,因感染无法控制、培养结果为耐药革兰阳性球菌且合并脏器功能不全而使用利奈唑胺。患者的基础疾病及感染的高危因素见表1。
1.2 标本的采集
收集气道分泌物、尿液、血液、胸腹腔引流液、脓液及导管尖端进行培养。
1.3 观察项目
(1)临床疗效:体温、痰量、引流液量及颜色,其他临床症状、体征改善情况以及影像学表现;(2)不良反应:评价治疗前后患者肝、肾功能、电解质、血细胞及血气分析等指标,观察治疗中出现的异常情况;(3)病原学监测:革兰阳性球菌清除情况。
1.4 利奈唑胺使用方法与疗程
利奈唑胺注射液(600 mg/支),由辉瑞制药有限公司生产,用药方法:600 mg q12 h静注。疗程为9~20 d。同时用药期间根据细菌病原学结果继续或停止抗菌治疗。
1.5 临床疗效判断标准
根据卫生部2004年颁发的抗菌药物临床研究指导原则:(1)痊愈为临床症状、体征、实验室检查及病原学检查4项指标完全恢复正常;(2)显效为病情明显好转,但上述4项中有1项未完全恢复正常;(3)进步为用药后病情有所好转,但不明显;(4)无效为用药72 h病情未改善或加重。痊愈加显效合计为有效,据此计算有效率。

表1 应用利奈唑胺治疗患者的基础疾病及感染的高危因素Tab 1 Underlying diseases and risk factors associated with infections of the patients treated with linezolid
1.6 细菌学清除标准
按清除、未清除、替换3级评定。清除:治疗后连续2次培养病原菌消失;未清除:治疗后初始病原菌仍生长;替换:治疗后感染灶原致病菌消失,培养出新的病原菌。
1.7 安全性评价
按与药物有关、可能有关、可能无关、无关和无法评价5级评定临床反应及实验室检查异常与药物之间的关系。前二者划为不良反应,统计不良反应发生率。
1.8 肾功变化
根据患者的肾功肌酐正常与否分为两组,观察用药后患者肾功肌酐的变化与之前情况的关系。
1.9 统计学方法
采用SPSS14.0软件分析数据,计数资料用χ2检验,P<0.05为差异有统计学意义。
2 结果
2.1 临床疗效
60例患者共治愈38例(63.33%),显效8例(13.33%),进步8 例(13.33%),无效6 例(10%),总有效率为76.67%(46/60)。无效病例中有4例为MRSA感染的肺炎合并多脏器功能衰竭病例,1例为同时合并粪肠球菌血流感染及屎肠球菌泌尿系感染的慢性肾脏病5期病例,1例为合并MRSA肺部感染及屎肠球菌泌尿系感染的重症胰腺炎病例,患者因肝肾功能不全而选择利奈唑胺,治疗过程中因病情恶化而死亡。
2.2 细菌学检查结果
60例患者的感染部位共计72个;各感染部位比率见表2,其中肺部感染比率最高(52.78%);60例患者共检出致病菌株72株,各菌株比率及治疗有效率见表3,其中2例同时合并MRSA与人葡萄球菌,4例同时合并屎肠球菌与粪肠球菌,2例同时合并表皮葡萄球菌与耳葡萄球菌,2例同时合并屎肠球菌与人葡萄球菌,药敏结果对利奈唑胺均敏感。60例患者病原学监测情况:4例患者因死亡而终止,46例患者病原学监测结果显示耐药球菌已清除,清除率为76.67%。

表2 脓毒症患者的感染部位Tab 2 The site of infection of the patientswith sepsis
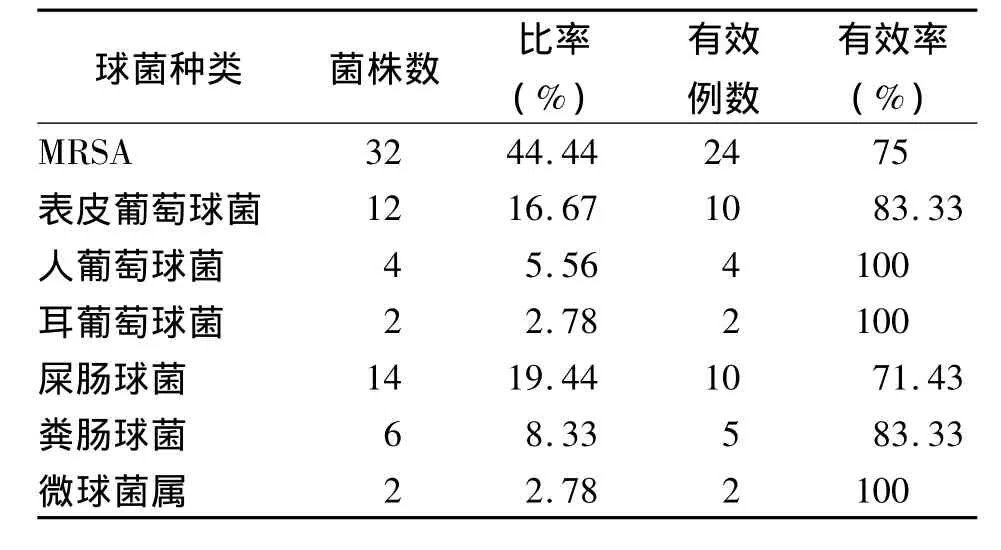
表3 球菌种类监测结果Tab 3 Moritoring results of staphylococcus species
2.3 不良反应
治疗过程中不良反应发生率为18.33%,有9例(15%)患者用药后肌酐水平较用药前升高;1例(1.67%)患者血小板治疗前为152×109/L,用药期间降至52×109/L,未予特殊治疗,继续用药血小板未继续下降,治疗结束停药后,血小板恢复正常;皮疹患者1例(1.67%),未发生其他不良反应。
2.4 肾功变化
用药后患者肾功能肌酐的变化,见表4。
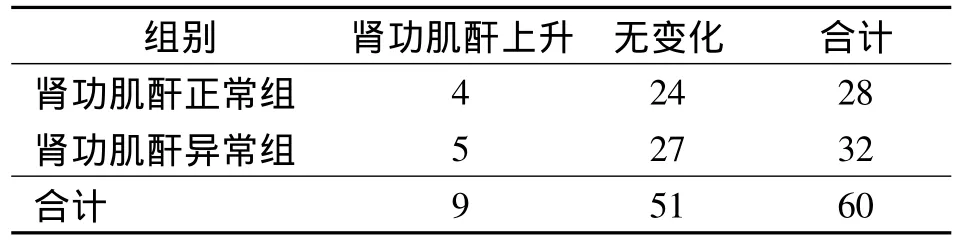
表4 两组肾功肌酐变化情况比较Tab 3 Comparison of the changes in the serum creatinine between two groups (n)
3 讨论
利奈唑胺能阻止细菌70S起始复合物形成,抑制细菌蛋白合成,不经过P450代谢,作用靶部位及作用方式独特,几乎全面覆盖G+菌,且用药后广泛分布于各组织中。国内外资料均有报道利奈唑胺对革兰阳性球菌有较好的抗菌活性[3]。本研究亦显示利奈唑胺对MRSA、表皮葡萄球菌、人葡萄球菌、耳葡萄球菌、微球菌、屎肠球菌及粪肠球菌均有良好的抗菌活性,治疗总有效率为76.67%,其中对人葡萄球菌、耳葡萄球菌及微球菌有效率均为100%,考虑两个菌种例数少,样本数量小存在偏倚。72株致病菌株中,MRSA(32株)所占比例最大,为44.44%,其治疗有效率为75%。
糖肽类抗生素是治疗MRSA肺炎的传统一线药物,国外报道 MRSA对万古霉素的 MIC=1μg/mL的临床分离率由2001年的20%已上升至2007年的70.4%[4]。虽然国内未发现万古霉素耐药菌株,但国外已反复报道耐万古霉素的MRSA菌株出现,目前国内外已有多个临床试验表明利奈唑胺对MRSA有较好的疗效。Falagas等[5]研究显示利奈唑胺对革兰阳性球菌疗效较好。Wunderink等[6]在研究呼吸机相关性肺炎患者时发现利奈唑胺对上皮黏液层有良好的渗透性,表明对呼吸机相关性肺炎的治疗利奈唑胺可能更具优势。本研究中38例肺部感染,治愈28例,提示利奈唑胺在肺部感染中疗效较好,与Sirvent[7]等报道利奈唑胺对清除器官组织中的感染有效相一致,分析主要是由于利奈唑胺在肺组织内浓度高,有良好的渗透性所致。
利奈唑胺已被美国FDA批准治疗皮肤软组织感染。有研究表明,利奈唑胺在治疗MRSA导致的复杂皮肤软组织感染上有优越性。本研究中皮肤软组织感染6例,其中4例为外伤后下肢皮肤脱套伤,2例车祸致复合伤存在烧伤,应用利奈唑胺均临床治愈,表明应用利奈唑胺可成功治疗皮肤软组织感染,有效率明显高于Hau的研究结果(89%),考虑可能与样本例数偏少有关。
革兰阳性球菌在血流感染中占重要地位。本研究血流感染12例,治愈10例,静脉导管相关性血流感染2例,MRSA阳性,且痊愈,表明利奈唑胺也可以用于治疗血流感染。但美国FDA目前为止并没有批准其治疗此类感染,故尚有待临床进一步证实。
ICU患者病情重,多合并器官功能障碍,肝肾功能不全,故应用安全有效的抗感染药物尤为重要,利奈唑胺具有肝肾双通道排泄的特点,对于肾功能不全患者,利奈唑胺60%可由肝脏代谢,30%由肾脏代谢,肾功能不全患者及轻中度肝功能损害的患者无需调整剂量。本研究接受利奈唑胺治疗的60例患者均被纳入安全评价,有5例合并肾功能不全患者在用药过程中出现肌酐较前轻度升高,经治疗感染控制后肾功恢复至治疗前水平;有3例在用药前存在肾功损害,用药后均降至正常,考虑与感染控制后炎症介质对肾脏的继发性损害消失有关。由表3可知,应用利奈唑胺后,两组肾功肌酐升高差异无显著性意义(P>0.05),表明利奈唑胺对肾功能不全的严重脓毒症患者较为安全。本研究有1例患者在利奈唑胺治疗过程中出现血小板下降,未停药,患者在感染控制停药后血小板逐步恢复正常,故临床出现血小板下降时要综合考虑患者临床情况决定是否停药,以免延误最佳治疗时机,但需严密监测血常规。本研究在治疗过程中亦未发生骨髓抑制、乳酸酸中毒。本研究表明利奈唑胺治疗ICU耐药革兰阳性球菌脓毒症安全有效,尚需大规模的前瞻性临床研究进一步证实。临床上要严格掌握利奈唑胺的适应证,尤其适合重症感染、脓毒症、多器官功能不全伴肝肾功能不全的患者,可及时的应用利奈唑胺以挽救患者的生命,有指征的应用利奈唑胺将有利于减少耐药的发生。
[1]Bassetti M,Ginocchio F,Giacobbe DR.New approaches for empiric therapy in Gram-positive sepsis Minerva Anestesiol[J].2011,77(8):821 -827.
[2]Levy MM,Fink MP,Marshall JC,et al.2001 SCCM/ESICM/ACCP/ATS/SIS International Sepsis Definitions Conference[J].Intensive Care Med,2003,29:530-538.
[3]Ross JE,Fritsche TR,Sader HS,etal.Oxazolidinone susceptibility patterns for 2005:International Report from the Zyvox Annual Appraisal of Potency and Spectrum Study[J].Int JAntimicrob Agents,2007,29(3):295 -301.
[4]Wang G,Hindler J,Ward K,etal.Increased vancomycin MICs for Staphylococcus aureus clinical isolates from a university hospital during a 5 -year period[J].JClin Microbiol,2006,44(11):3883 -3886.
[5]Falagas ME,Siempos II,Vardakas KZ.Linezolid versus glycopeptide or beta-lactam for treatment of Gram-positive bacterial infections:meta-analysis of randomized controlled trials[J].Lancet Infect Dis,2008,8(1):53 -56.
[6]Wunderink RG,Mendelson MH,Somero MS,et al.Microbiological response to Linezolid vs Vancomycin in ventilator-associated pneumonia due to Methicillin-resistant Staphylococcus aureus[J].Chest,2008,134:1200 -1207.
[7]Sirvent JM,Pneiro L,de la Torre M,etal.Linezolidmore efficacious than vancomycin to eradicate infecting organism in critically ill patientswith Gram - positive infections[J].Rev Esp Quimioter,2010,23(1):27 -35.
Clinical evaluation of linezolid in the treatment of sepsis in ICU
CHEN Chang,ZHANG Yu
(Department of Emergency ICU,the First Affiliated Hospital of Dalian Medical University,Dalian116011,China)
[Objective]To evaluate the efficacy and safety of linezolid in the treatment of sepsis in ICU.[Methods]A retrospective analysis of the clinical data was conducted for 60 patients with sepsis and treated with linezolid in emergency intensive care unit(EICU).[Results]The results showed the total efficacy rate was 76.67%(46/60),75%(24/32)among the patientswith the infection of Meticillin - resistant Staphylococcus aureus(MRSA),83.33%(10/12)among the patientswith the infection of Staphylococcus epidermidis,71.43%(10/14)among the patients with the infection of Enterococcus faecium,83.33%(5/6)among the patientswith the infection of Enterococcus faecalis,100%(4/4)among the patientswith the infection of Staphylococcus hominis,100%(2/2)among the patients with the infection of Staphylococcus auricularis,100%(2/2)among the patientswith the infection of Micrococcus,the drug- related side effect rate was 18.33%.[Conclusion]Linezolid is likely to be an effective and safe treatment for severe infections in ICU.
linezotid;sepsis;efficacy
R978.1
A
1671-7295(2012)03-0270-04
2012-03-01;
2012-04-02
陈 畅(1978-),女,辽宁大石桥人,主治医师,硕士。E-mail:xyxchang@hotmail.com
张 彧,教授。E-mail:St2389@sohu.com

