脂肪酸甲酯碳同位素测定值的校正方法对比研究
姚 远,赵江涛,曹蕴宁,王 政,刘卫国
(1.西安交通大学,人居环境与建筑工程学院,陕西 西安 710049;2.中国科学院地球环境研究所,黄土与第四纪地质国家重点实验室,陕西 西安 710075)
脂肪酸甲酯碳同位素测定值的校正方法对比研究
姚 远1,2,赵江涛2,曹蕴宁2,王 政2,刘卫国1,2
(1.西安交通大学,人居环境与建筑工程学院,陕西 西安 710049;2.中国科学院地球环境研究所,黄土与第四纪地质国家重点实验室,陕西 西安 710075)
气相色谱-燃烧-同位素比值质谱(GC-C-IRMS)分析脂肪酸单体化合物碳同位素时,首先对脂肪酸甲酯化,但是测得的δ13C值为脂肪酸甲酯的δ13C值,因此需要对其进行数学校正,才能得到脂肪酸δ13C值。为了得到准确的甲酯化使用的甲醇δ13C值,提高校正后的脂肪酸δ13C值的精准度,本研究利用3种不同方法测定甲醇δ13C值:1)甲醇与钠反应制备甲醇钠固体,离线测定甲醇钠固体δ13C值;2)液氮冷却石英管注样法制备甲醇结晶体,离线测定甲醇结晶体δ13C值;3)GC-C-IRMS顶空进样测定甲醇δ13C值。并通过离线测定得到脂肪酸单体化合物及其甲酯化后的脂肪酸甲酯δ13C值。然后用此3种不同方法测定的甲醇δ13C值分别对脂肪酸甲酯δ13C值进行数学校正,将计算得到的脂肪酸δ13C值与脂肪酸单体化合物δ13C值进行误差分析。研究结果表明:离线测定的甲醇结晶体δ13C值为-50.17‰,标准偏差为0.086‰(n=5),重现性优于其他两种方法,用其校正后的脂肪酸δ13C值与离线测定的脂肪酸δ13C值误差最小。因此,离线测定甲醇结晶体δ13C值是一种相对可靠的测定甲醇δ13C值的方法,可提高校正脂肪酸甲酯碳同位素测定值的精准度。关键词:脂肪酸甲酯;甲醇;碳同位素;校正方法
脂肪酸作为一种生物标志化合物已被广泛应用于环境、地质、食品、生物、医学等研究领域[1-7]。目前,随着单体有机化合物稳定同位素分析(CSIA)技术的不断发展,气相色谱-燃烧-同位素比值质谱(GC-C-IRMS)技术实现了有机样品单体化合物的在线同位素测定,已成为一种有效、准确的CSIA技术,同时也被广泛应用到脂肪酸单体化合物碳同位素的分析和相应的研究中[8-13]。
通常,采用 GC-C-IRMS分析脂肪酸,特别是长链脂肪酸(12碳以上)时,一般不直接进行分析,须将它们先衍生为脂肪酸甲酯后才进行测定[8-13]。脂肪酸的甲酯化是为了把高沸点,不易挥发、气化的脂肪酸与甲醇反应,生成相应的脂肪酸甲酯,使其变成低沸点易挥发、气化的物质,从而降低气化温度,提高分离效果[14]。目前,脂肪酸的甲酯化方法可分为3类:酸催化法、碱催化法和三甲基硅重氮甲烷(TMS)法[14-15]。由于操作方便、快速,在脂肪酸单体化合物碳同位素研究中,多采用盐酸-甲醇酸催化的甲酯化方法。
在甲酯化过程中,由于酯化甲基碳的引入使得脂肪酸碳同位素组分改变,测定的脂肪酸甲酯碳同位素值必须进行数学校正,扣除酯化甲基的碳同位素值,才能计算获得研究所需要的脂肪酸碳同位素值。因此,得到准确的甲酯化使用的甲醇碳同位素值,将有助于提高校正后的脂肪酸碳同位素值的精准度。但是,目前对于测定甲醇碳同位素值的研究甚少,Hammer等[16]通过离线测定得到脂肪酸及其甲酯化后的脂肪酸甲酯δ13C值,然后利用质量平衡方程计算得到甲醇δ13C值为-49.7±2.5‰(n=8),但此方法重现性较差,没有得到精准的甲醇δ13C值。
已有研究者对挥发性有机化合物(VOCs)碳同位素值测定方法进行研究,Jochmann等[17]采用顶空进样方式,提高了GC-C-IRMS分析VOCs碳同位素值的灵敏度。黄代宽等[18]设计了冷阱注样-密闭石英管燃烧法制备甲酸、乙酸标准的同位素样品,避免了制备过程中因挥发所导致的同位素分馏,并在Finnigan MAT-252气体同位素比值质谱仪上对其碳同位素值进行测定,同时与GC-C-IRMS测定的碳同位素值进行对比。研究结果表明,离线测定甲酸、乙酸碳同位素值的方法具有极高的重现性,精密度上优于后者。由于甲醇也是一种VOCs,借鉴前人对VOCs碳同位素值测定方法的研究,本工作提出了3种不同方法测定甲醇碳同位素值:1)甲醇与钠反应制备甲醇钠固体,离线测定甲醇钠固体碳同位素值;2)液氮冷却石英管注样法制备甲醇结晶体,离线测定甲醇结晶体碳同位素值;3)GCC-IRMS顶空进样测定甲醇碳同位素值。
通过分析3种不同方法测定的甲醇δ13C值,将其分别对离线测定的甲酯化后脂肪酸甲酯δ13C值进行校正,并将计算得到的脂肪酸δ13C值与离线测定的脂肪酸δ13C值进行误差分析,从而得出测定甲醇碳同位素值的可靠方法,进而提高校正脂肪酸甲酯碳同位素测定值的精准度。
1 试验部分
1.1 样品和主要试剂、仪器
脂肪酸标准单体化合 物 (C16:0、C18:0、C20:0、C24:0、C30:0):美国 NU-CHEK 公司产品。
甲醇、甲苯(高效液相色谱级):美国Fisher公司产品;正己烷、乙酰氯(液相色谱级):德国Merck公司产品;氯化钠(分析纯):天津市北方天医化学试剂厂产品。
气相色谱-燃烧-同位素比值质谱仪(GC-CIRMS):由Thermo Trace Ultra气相色谱仪和燃烧装置在线连接的Thermo Delta V同位素比值质谱仪组成;MAT-251型气体同位素比值质谱仪:美国Thermo Finnigan公司产品。
1.2 试验方法
1.2.1 脂肪酸甲酯标准溶液的制备 分别取约3mg脂肪酸标准单体化合物(C16:0、C18:0、C20:0、C24:0、C30:0)于4mL小瓶中,加入2mL 盐酸-甲醇后,在60℃下酯化12h,然后在酯化后的样品中加入2mL 5%NaCl溶液,用1.5mL正己烷萃取3次,最后用氮气吹干,甲苯定容至3mL,制备为脂肪酸甲酯标准溶液。
1.2.2 固体甲醇钠的制备 称取一定量的钠金属置于2mL小瓶,加入过量的甲醇至完全反应,然后在氮气下吹至粘稠的一醇化物CH3ONa·CH3OH,再将此一醇化物在150℃下加热,即可得到固体甲醇钠。
1.2.3 甲醇结晶体样品的制备 采用液氮冷却石英管注样法制备甲醇结晶体样品,首先在石英管内加入氧化铜、铜丝和铂丝,再用液氮冷却石英管3~5min后,注入6μL甲醇溶液,冷却5min使其完全凝固为结晶体,然后抽真空后用液化气焊割炬将石英管开口端密封,可有效避免样品制备过程中因挥发导致的碳同位素分馏。
1.2.4 脂肪酸和脂肪酸甲酯碳同位素值的测定
分别取约1mg脂肪酸标准单体化合物(C16:0、C18:0、C20:0、C24:0、C30:0)和1mL 制备的脂肪酸甲酯标准溶液的吹干样品,置于石英管内,加入氧化铜、铜丝和铂丝,抽真空后用液化气焊割炬将石英管开口端密封,置于马弗炉内,850℃下恒温灼烧4h,充分氧化。样品炉冷却至室温后,在真空系统中用酒精-液氮冷阱收集纯化CO2气体,最后用MAT-251型同位素质谱仪测定CO2的碳同位素。
质谱条件:离子源发射电流0.8mA,离子源真空6×10-5Pa,源磁铁0.313T,高电压9.99kV。
碳同位素组成的表达式为:
δ13C(‰)=[(Rsa-Rst)/Rst]×1 000
式中:Rsa为样品的碳同位素比值(13C/12C);Rst为标准的碳同位素比值(13C/12C)。
碳同位素组成相对于V-PDB标准。样品的测定精度用国家标准炉黑(GBW04407)控制,每批样品至少带1个工作标准,标准样品的重复分析误差小于0.2‰。同位素分析在中国科学院地球环境研究所同位素实验室完成。
1.2.5 甲醇碳同位素值的测定
1)离线测定甲醇钠固体碳同位素值
称取约8mg固体甲醇钠于石英管内,加入氧化铜、铜丝和铂丝,抽真空后用液化气焊割炬将石英管开口端密封,置于马弗炉内,850℃下恒温灼烧4h,充分氧化。样品炉冷却至室温后,在真空系统中用酒精-液氮冷阱收集纯化CO2气体,最后用MAT-251型同位素质谱仪测定CO2的碳同位素。标准样品的重复分析误差小于0.2‰。
2)离线测定甲醇结晶体的碳同位素值
将密封后石英管中的甲醇结晶体样品置于马弗炉内,850℃下恒温灼烧4h,充分氧化。样品炉冷却至室温后,在真空系统中用酒精-液氮冷阱收集纯化CO2气体,最后用MAT-251型同位素质谱仪测定CO2的碳同位素。标准样品的重复分析误差小于0.2‰。
3)GC-C-IRMS顶空测定甲醇的碳同位素值
取约1mL甲醇溶液置于1.5mL小瓶中,放置1h后采用顶空进样方式,进样量1μL。
色谱条件:色谱柱HP-1MS型毛细管柱(60 m×0.32mm×0.25μm),样口温度290℃,载气(He)流速1.0mL/min,分流比100∶1。
甲醇样品经色谱柱后,在氧化炉980℃条件下转化为CO2气体,进入同位素比值质谱测定碳同位素值。
质谱条件:离子源发射电流1.5mA,离子源真空1.2×10-4Pa,高电压3.09kV。
每6个分析样品之间加测一个实验室工作标准(C21、C25、C27、C29、C31和 C33共6个正构烷烃化合物),以监控实验过程中碳同位素的重现性和准确性,分析误差小于0.3‰。同位素分析在中国科学院地球环境研究所同位素实验室完成。
2 结果与讨论
2.1 离线测定的脂肪酸和脂肪酸甲酯δ13 C值的比较
通过离线测定脂肪酸单体化合物(C16:0、C18:0、C20:0、C24:0、C30:0)及其甲酯 化 后 的 脂肪酸甲酯δ13C值,比较两者之间的差异,分析甲酯化对脂肪酸碳同位素分馏的影响。图1比较了离线测定的脂肪酸和脂肪酸甲酯δ13C值,后者相对于前者均偏负(0.69‰~1.16‰),有着明显的差异,远远超过离线测定δ13C值的误差分析范围(<0.2‰)。因此,本研究使用的甲醇对脂肪酸甲酯化造成脂肪酸碳同位素的明显分馏。

图1 离线测定的脂肪酸和脂肪酸甲酯δ13C值的比较Fig.1 Comparisons ofδ13C values of fatty acids and FAMEs by off-line analysis
在甲酯化过程中,化学反应过程和甲醇的甲基碳引入脂肪酸都有可能造成脂肪酸碳同位素分馏。初步推测,甲酯化造成脂肪酸碳同位素明显分馏可能有两个原因:1)甲醇的甲基碳引入脂肪酸中碳同位素组分的改变;2)脂肪酸甲酯化反应过程中动力学同位素效应产生的同位素分馏。已有研究表明:如果在酯化反应过程中加入过量的甲醇,通常为定量反应,此过程不存在动力学同位素分馏效应[19]。本研究在制备脂肪酸甲酯标准溶液过程中,用2mL盐酸-甲醇分别对约3 mg脂肪酸标准单体化合物进行甲酯化,甲醇足够过量,并且在60℃下加热反应12h的酯化条件保证了脂肪酸完全酯化[15]。因此,甲酯化反应过程中不存在动力学同位素分馏。从而推断,酯化甲基碳的引入是造成脂肪酸碳同位素分馏的主要原因。
2.2 3种不同方法测定的甲醇δ13 C值校正脂肪酸甲酯δ13C值的对比
由于甲醇甲基碳的引入造成脂肪酸碳同位素的明显分馏,所以,有必要对甲酯化后的脂肪酸甲酯δ13C值进行数学校正,以得到所需的脂肪酸δ13C值。一个给定的脂肪酸甲酯的碳同位素组成是脂肪酸中每个碳和酯化甲基碳共同贡献的结果,而酯化甲基碳同位素组成应该与酯化使用的甲醇一致。只有扣除酯化甲基碳同位素的贡献,才能获得脂肪酸碳同位素的组成[20]。Duan等[21]和 Dungait等[22]利用质量平衡方程对脂肪酸甲酯碳同位素值进行了校正,校正公式如下:式中:n、δ13CFA分别为脂肪酸的碳数和碳同位素组成;δ13CFAME为脂肪酸甲酯的碳同位素组成;δ13CCH3OH为酯化使用的甲醇的碳同位素组成。
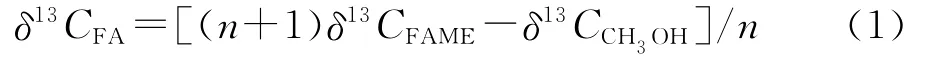
对于甲醇碳同位素组成的测定,采用以下3种不同方法:1)甲醇与钠反应制备甲醇钠固体,离线测定甲醇钠固体碳同位素值;2)液氮冷却石英管注样法制备甲醇结晶体,离线测定甲醇结晶体碳同位素值;3)GC-C-IRMS顶空进样测定甲醇碳同位素值。测定的甲醇δ13C值列于表1。离线测定甲醇钠固体δ13C值为-51.79‰ ±0.814‰(n=5);离线测定甲醇结晶体δ13C值为-50.17‰ ± 0.086‰(n=5),GC-C-IRMS顶空进样测定甲醇δ13C值为-50.59‰ ±0.185‰(n=5),3种方法测定的甲醇δ13C值之间有着明显的差异。为了分析这3种方法测定甲醇δ13C值的准确性,分别将此3种方法测定的甲醇δ13C值与离线测定的脂肪酸甲酯δ13C值代入公式(1)进行校正,计算得到的脂肪酸δ13C值与离线测定的脂肪酸δ13C值进行误差分析,结果列于表2。

表2 3种不同方法测定的甲醇δ13C值校正脂肪酸甲酯δ13C值的对比Table 2 Comparisons of three different determination methods ofδ13C values of the methanol to correctδ13C values of FAMEs
由表2可以看出,误差2(0.04‰~0.16‰)和误差3(0.06‰~0.18‰)较小,且几乎相等,均在离线测定δ13C值的误差分析范围(<0.2‰)之内,而误差1(0.12‰~0.25‰)相对于误差2和误差3较大,其中脂肪酸C18和C24的误差1分别为0.25‰、0.23‰,超过离线测定δ13C值的误差分析范围。由此可以初步认为,离线测定的甲醇结晶体δ13C值和GC-C-IRMS顶空进样测定的甲醇δ13C值都接近于理论值,而离线测定的甲醇钠固体δ13C值相对于理论值误差较大。
在制备甲醇钠固体过程中,本研究参考董红健[23]研制的制备固体甲醇钠方法,在金属钠中加入过量甲醇,反应完全后将产物浓缩至分离出一醇化物CH3ONa·CH3OH,再将此一醇化物在150℃下加热,即可制备得到固体甲醇钠,但此方法很难得到纯度100%的甲醇钠固体。另外离线测定5个平行实验制备的甲醇钠固体样品的δ13C值标准偏差为0.814‰,重现性较差,这也有可能是CH3ONa·CH3OH在制备甲醇钠固体过程中碳同位素分馏大小的不同所导致的。因此,没有制备得到纯度100%的甲醇钠固体以及化学反应过程中动力学同位素效应都有可能产生甲醇碳同位素的分馏。由此推断,离线测定的甲醇钠固体δ13C值相对于理论值误差较大的原因是在制备甲醇钠固体过程中产生较大的碳同位素分馏。
在采用液氮冷却石英管注样法制备甲醇结晶体过程中,预先用液氮冷却石英管3~5min,再往石英管中注入6μL甲醇,冷冻5min,凝固为结晶体后抽真空,用液化气焊炬将石英管密封。由于注入的甲醇量很少以及甲醇易挥发的物理性质,在注入石英管过程中,有少量甲醇挥发,从而使制备的甲醇结晶体产生微弱的碳同位素分馏,导致用离线测定的甲醇结晶体δ13C值校正后的脂肪酸δ13C值与离线测定的脂肪酸δ13C值有微小误差。
GC-C-IRMS顶空进样方式是挥发性、半挥发性有机物理想的进样技术,Slater等[24]实验证实,气相(顶空)中的δ13C值代表了液相中的δ13C值,两者的同位素差异均在误差分析范围之内。因此,甲醇顶空进样方式几乎不产生碳同位素分馏。但已有研究表明:GC和IRMS的测定条件都有可能影响GC-C-IRMS对稳定同位素的分析[25-26]。因此认为,GC-C-IRMS顶空进样方式测定的甲醇δ13C值对脂肪酸甲酯δ13C值校正后,计算得到的脂肪酸δ13C值与离线测定的脂肪酸δ13C值有微小误差的原因是GC-CIRMS系统本身测定条件影响的。
2.3 离线测定的甲醇结晶体δ13 C值和GC-CIRMS顶空进样测定的甲醇δ13C值比较
以上研究表明:离线测定的甲醇结晶体δ13C值和GC-C-IRMS顶空进样测定的甲醇δ13C值都接近于理论值。为了验证这两种方法测定的甲醇δ13C值哪个更接近于理论值,首先使用独立样本T检验研究这两种方法测定的甲醇δ13C值是否存在显著差异,结果列于表3。若这两种方法测定的甲醇δ13C值不存在显著差异,说明两者的甲醇δ13C值都接近于理论值;若存在显著差异,说明其中的一种方法测定的甲醇δ13C值更接近于理论值。
如表3所示,甲醇δ13C值的T统计值为4.683,对应双尾相伴概率为0.002,小于显著性水平0.05,因此认为这两个样本的均值有显著差异。说明离线测定的甲醇结晶体δ13C值和GC-C-IRMS顶空进样测定的甲醇δ13C值有显著差异,其中一种方法测定的甲醇δ13C值更接近于理论值。

表3 两种不同方法测定的甲醇δ13C值的独立样本T检验Table 3 Independent-samples T test onδ13C values of the methanol by the two different determination methods
为了分析离线测定的甲醇结晶体δ13C值和GC-C-IRMS顶空进样测定的甲醇δ13C值哪个更接近于理论值,对两者校正后的脂肪酸δ13C值与离线测定的脂肪酸δ13C值的误差进行比较,示于图2。由图2可知,误差2小于误差3,表明离线测定的甲醇结晶体δ13C值更接近于理论值。并且由表1显示,离线测定的甲醇结晶体δ13C 值标准偏差(0.086‰,n=5)小于 GC-CIRMS顶空测定的甲醇的δ13C值标准偏差(0.185‰,n=5),说明离线测定甲醇结晶体δ13C值的方法重现性优于GC-C-IRMS顶空进样测定。因此,离线测定甲醇结晶体δ13C值优于其他两种方法,是一种相对可靠的测定甲醇碳同位素值的方法。

图2 误差2和误差3的比较Fig.2 Comparisons between error two and error three
3 结论
通过分析3种不同方法测定的甲醇δ13C值,将其分别对离线测定的甲酯化后的脂肪酸甲酯δ13C值进行校正,并将计算得到的脂肪酸δ13C值与离线测定的脂肪酸δ13C值进行误差分析,可以得到以下结论:
1)离线测定的甲醇结晶体δ13C值和GC-CIRMS顶空进样测定的甲醇δ13C值对脂肪酸甲酯校正后,计算得到的脂肪酸δ13C值与离线测定的 脂 肪 酸δ13C 值 误 差 较 小 (0.04‰ ~0.18‰),且几乎相等,而用离线测定的甲醇钠固体δ13C值计算得到的脂肪酸δ13C值与离线测定的脂肪酸δ13C值误差较大(0.12‰~0.25‰)。
2)离线测定的甲醇结晶体δ13C值最接近于理论值,并且此方法测定的甲醇δ13C值标准偏差为0.086‰(n=5),重现性优于其他两种方法。所以,离线测定甲醇结晶体δ13C值是一种相对可靠的测定甲醇碳同位素值的方法,进而提高了校正脂肪酸甲酯碳同位素测定值的精准度。
[1]BALLENTINE D C,MACKO S A,TUREKIAN V C,et al.Compound specific isotope analysis of fatty acids and polycycfic aromatic hydrocarbons in aerosols:Impfications for biomass burning[J].Org Geochem,1996,25:97-104.
[2]TOLOSA I,VESCOVALI I,LEBLOND N,et al.Distribution of pigments and fatty acid biomarkers in particulate matter from the frontal structure of the Alboran Sea(SW Mediterranean Sea)[J].Marine Chemistry,2004,88:103-125.
[3]STEFANOVA M,DISNAR J R.Composition and early diagenesis of fatty acids in lacustrine sediments,lake Aydat (France)[J].Organic Geochemistry,2000,31:41-55.
[4]BOND B,FERNANDEZ D R,VANDERJAGT D J,et al.Fatty acid,amino acid and trace mineral analysis of three complementary foods from Jos,Nigeria[J].Journal of Food Composition and A-nalysis,2005,18:675-690.
[5]WOODBURY S E,EVERSHED R P,ROSSELL J B.δ13C analyses of vegetable oil fatty acid components,determined by gas chromatography-combustion-isotope ratio mass spectrometry,after saponification or regiospecific hydrolysis[J].Journal of Chromatography A,1998,805:249-257.
[6]FANG J,BARCELONA M J,ABRAJANO T,et al.Isotopic composition of fatty acids of extremely piezophilic bacteria from the Mariana Trench at 11,000m[J].Marine Chemistry,2002,80:1-9.
[7]BRENNAN J T.Use of stable isotopes to study fatty acid and lipoprotein metabolism in man[J].Prostaglandins,Leukotrienes and Essential Fatty Acid,1997,57:467-472.
[8]RUESS L,CHAMBERLAIN P M.The fat that matters:Soil food web analysis using fatty acids and their carbon stable isotope signature[J].Soil Biology & Biochemistry,2010,42:1 898-1 910.
[9]KANGANI C O,KELLY D E,DELANY J P.New method for GC/FID and GC-C-IRMS analysis of plasma free fatty acid concentration and isotopic enrichment[J].Journal of Chromatography B,2008,873:95-101.
[10]CROSSMAN Z M,WANG Z P,INESON P.Investigation of the effect of ammonium sulfate on populations of ambient methane oxidising bacteria by13C-labelling and GC/C/IRMS analysis of phospholipid fatty acids[J].Soil Biology & Biochemistry,2006,38:983-990.
[11]金青哲,施峰华,谢 峰,等.碳同位素比值法检测棕榈油掺入玉米油的研究[J].中国油脂,2009,34(1):73-75.
[12]段 毅,宋金明,张 辉.南沙海区生物单体脂类碳同 位 素 研 究 [J].中 国 科 学,2003,3(9):889-894.
[13]王 娜,诸乃彤,刘 锐,等.鱼油原料中DHA、EPA的碳稳定同位素测定的方法[J].食品研究与开发,2010,31(10):147-152.
[14]范亚苇,邓泽元,余永红,等.不同脂肪酸甲酯化方法对共轭亚油酸分析的影响[J].中国油脂,2007,32(1):52-55.
[15]寇秀颖,于国萍.脂肪和脂肪酸甲酯化方法的研究[J].食品研究与开发,2005,26(2):46-47.
[16]HAMMER B T,FOGEL M L,HOERING T C.Stable carbon isotope ratios of fatty acids in seagrass and redhead ducks[J].Chemical Geology,1998,152:29-41.
[17]JOCHMANN M A,BLESSING M,HADERLEIN S B,et al.A new approach to determine method detection limits for compound-specific isotope analysis of volatile organic compounds[J].Rapid Commun Mass Spectrom,2006,20:3 639-3 648.
[18]黄代宽,李心清,安 宁,等.挥发性有机化合物标准样品的碳同位素δ13C测定:以甲酸、乙酸为例[J].质谱学报,2008,29(5):301-305.
[19]RIELEY G.Derivatization of organic compounds prior to gas chromatographic-combustion-isotope ratio mass spectrometric analysis:Identif ication of isotope fractionation processes[J].Analyst,1994,19:915-919.
[20]段 毅,文启彬,罗斌杰,等.南沙海洋和甘南沼泽现代沉积物中单个脂肪酸碳同位素组成及其成因[J].地球化学,1995,24(3):270-275.
[21]DUAN Y,WEN Q B,ZHENG G D,et al.Isotopic composition and probable origin of individual fatty acids in modern sediments from Ruoergai Marsh and Nansha Sea,China[J].Org Geochem,1997,27:583-589.
[22]DUNGAIT J A J,DOCHERTY G,STRAKER V,et al.Interspecific variation in bulk tissue,fatty acid and monosaccharideδ13C values of leaves from a mesotrophic grassland plant community[J].Phytochemistry,2008,69:2 041-2 051.
[23]董红健.固体甲醇钠的研制[J].精细化工中间体,2003,3(1):40-46.
[24]SLATER G F,DEMPSTER H S,SHERWOOD LOLLAR B,et al.Headspace analysis:A new application for isotopic characterization of dissolved organic contaminants[J].Environ Sci Technol,1999,32:190-194.
[25]MERRITT D A,HAYES J M.Factors controlling precision and accuracy in isotope-ratio-monitoring mass spectrometry[J].Anal Chem,1994,66:2 336-2 347.
[26]LIU W,WANG Z,CUI L,et al.Variation of compound-specific hydrogen isotope ratios under changing temperature program in gas chromatography/thermal conversion/isotope ratio mass spectrometry[J].Rapid Commun Mass Spectrom,2012,26:1 746-1 752.
Comparative Study on Correction Methods of Carbon Isotope Measured Values of the Fatty Acid Methyl Esters
YAO Yuan1,2,ZHAO Jiang-tao2,CAO Yun-ning2,WANG Zheng2,LIU Wei-guo1,2
(1.School of Human Settlement and Civil Engineering,Xi’an Jiaotong University,Xi’an710049,China;2.State Key Laboratory of Loess and Quaternary Geology,Institute of Earth Environment,Chinese Academy of Sciences,Xi’an710075,China)
Methyl esterification of fatty acids is required prior to gas chromatography-combustion-isotope ratio mass spectrometry(GC-C-IRMS)analysis,but each fatty acid methyl ester(FAME)contains a methyl group from derivatization that is not present in the original fatty acid.So it is necessary to correct theδ13C value of each FAME for theδ13C value of the extra methyl carbon.In order to obtain the accurateδ13C value of the methanol used to methylate the fatty acids,and then improve the accuracy of the correctedδ13C values of fat-ty acids,this paper analyse theδ13C values of the methanol as determined by three different methods:1)Theδ13C values of sodium methoxide solid from chemical reaction between the methanol and sodium are determined by off-line method;2)Theδ13C values of methanol crystal as prepared by a special method that liquid nitrogen cools down quartz tube are determined by off-line method;3)Theδ13C values of the methanol are determined by GC-CIRMS with headspace sampling.Besides,theδ13C values of the fatty acids and FAMEs are also determined by off-line method,and theδ13C values of the methanol as determined by three different methods correct theδ13C values of each FAME respectively,and then this paper compare the calculatedδ13C values of the fatty acids with that of the fatty acids as determined by off-line method.The results show that the averageδ13C value of the methanol crystals as determined by off-line method is -50.17‰,and the standard deviation is 0.086‰(n=5).Reproducibility of these values is the best,and the calculatedδ13C values that theδ13C values of the FAMEs are corrected by theδ13C values of the methanol are the most similar with theδ13C values of the fatty acids as determined by off-line method.So it is a reliable method that methanol crystals are determined by off-line method,and then its accuracy is improved that theδ13C value of the methanol correct carbon isotope measured values of FAMEs.
fatty acid methyl ester(FAME);methanol;carbon isotope;correction methods
O 657.63
A
1004-2997(2012)06-0334-08
2012-07-12;
2012-10-16
国家自然科学基金项目(40873011)资助
姚 远(1986~),男,陕西人,硕士研究生,环境工程专业。E-mail:yaoyuan_1212@126.com
刘卫国(1958~),男,陕西人,研究员,从事稳定同位素地球化学研究。E-mail:liuwg@loess.llqg.ac.cn

