HPLC法测定甲磺酸伊马替尼片的含量
赵海桥,刘存领,付 建,苏贵勇
(1.山东方明药业集团股份有限公司,山东东明274500;2.山东大学药学院,山东济南250012; 3.中国药科大学药学院,江苏南京210009)
甲磺酸伊马替尼用于治疗慢性粒细胞白血病(CML)急变期、加速期或α-干扰素治疗失败后的慢性期患者;不能手术切除或发生转移的恶性胃肠道间质肿瘤(GIST)患者。进口药品注册标准JX20040087采用梯度洗脱测定甲磺酸伊马替尼片的含量,需要至少两元泵的液相才能测定,限制了该方法的普遍使用性。本文建立的方法,只需普通的液相就能测定,方法简便,结果可靠。
1 仪器与试药
1.1 仪器 日本岛津SPD-10A高效液相色谱仪。
1.2 试药 甲磺酸伊马替尼对照品(山东方明药业集团股份有限公司,1102001);甲醇、辛烷磺酸钠为色谱纯;水为纯化水;其他试剂均为分析纯;甲磺酸伊马替尼片(山东方明药业集团股份有限公司;批号:1106001、1106002、1106003;规格:0.1 g)。
2 方法与结果[1]
2.1 色谱条件 色谱柱为Kromasil C18(4.6 mm×250 mm,5 μm),以含0.04%辛烷磺酸钠的20 mmol·L-1磷酸二氢钠溶液(磷酸调至pH 2.5)-甲醇(40∶60)为流动相,流速为1 mL ·min-1,检测波长为268 nm,柱温为30℃,进样量为20 μL。
2.2 对照品溶液的制备 取甲磺酸伊马替尼对照品约24 mg,精密称定,置100 mL容量瓶中,加甲醇溶解并稀释至刻度,作为对照品溶液。
2.3 供试品溶液的制备 取甲磺酸伊马替尼片20片,精密称定,研细,精密称取粉末适量(约相当于伊马替尼20 mg),置100 mL容量瓶中,加甲醇适量,超声20 min,用甲醇稀释至刻度,摇匀,滤过,作为供试品溶液。
2.4 阴性对照溶液的制备 根据甲磺酸伊马替尼片的制剂配方,制备不含甲磺酸伊马替尼的阴性对照粉末。精密称取阴性对照粉末适量(约相当于伊马替尼20 mg的量),按照“2.3”项下方法制备阴性对照溶液。
2.5 专属性试验 辅料干扰试验:分别对阴性对照溶液、对照品溶液和供试品溶液进样分析,辅料不干扰甲磺酸伊马替尼的测定。
破坏试验:取甲磺酸伊马替尼片适量(约相当于伊马替尼20 mg)置100 mL容量瓶中,照下述方法试验:①加1.0 mol·L-1盐酸溶液2 mL并放置8 h作为酸破坏样品;②加1.0 mol·L-1氢氧化钠溶液2 mL并放置8 h作为碱破坏样品;③加3%过氧化氢溶液2 mL并放置8 h作为氧化破坏样品;④置4 500 lx光照度下8 h作为光照降解样品;同时做空白及辅料空白试验。结果表明:甲磺酸伊马替尼对酸、碱、氧化剂及光照均较稳定,各降解产物分离度良好。
2.6 线性关系考察 精密称取甲磺酸伊马替尼对照品约50.11 mg,精密称定,置100 mL容量瓶中,加甲醇溶解并稀释至刻度,作为溶液①,精密量取溶液①2.0、1.0、1.0、1.0 mL,分别置5、5、10、20 mL容量瓶中,用甲醇稀释至刻度,摇匀,作为溶液②、③、④、⑤,按上述液相条件,分别进样20 μL,记录色谱图峰面积。以甲磺酸伊马替尼峰面积A为纵坐标,浓度C为横坐标计算得回归方程为:A=561.32C+ 894.552 7,r=0.999 9。结果表明甲磺酸伊马替尼在25.055~501.1 μg·mL-1浓度范围内线性关系良好。
2.7 精密度试验 精密量取对照溶液20 μL,按上述液相条件,连续进样6次,RSD为1.0%。结果表明,精密度良好。
2.8 重复性试验 取同一批号(1106001)样品适量5份,精密量取,按样品测定项下的方法,测定甲磺酸伊马替尼片的含量,RSD为0.84%,重复性良好。
2.9 稳定性试验 取重复性实验中的第1份溶液,室温下在0、2、4、6、8 h测定,结果表明,本品的供试品溶液在室温8 h内稳定,计算得:RSD=1.1%,n=5。
2.10 方法准确度试验 在阴性对照粉末中分别加入适量的甲磺酸伊马替尼对照品,按照“2.3”项下方法制备供试品溶液,在相当于供试品溶液80%、100%和120%浓度水平下,分别考察加样回收率。每个浓度制备3份。测定3个浓度下的平均回收率分别为99.88%、100.12%、100.95%;RSD (n=3)分别为0.36%、0.88%、0.74%。
2.11 样品测定 对批号为1106001,1106002,1106003的甲磺酸伊马替尼片样品,按照“2.3”项下方法制备供试品溶液,每批样品制备3份,按外标法计算含量,测得结果与进口药品注册标准比较,结果见表1。
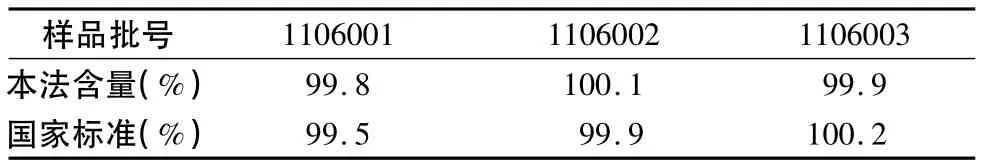
表1 样品含量测定结果比较表(n=3)
3 结果与讨论
试验表明,本测定方法简单,测定结果准确可靠,重现性好,可用于甲磺酸伊马替尼的含量测定。
流动相的选择:参考进口注册标准,减少辛烷磺酸钠用量的同时使用磷酸二氢钠,且在该流动相条件下,甲磺酸伊马替尼的保留时间较为理想,理论塔板数高[2]。
[1] 国家药典委员会.中华人民共和国药典2010年版(二部)[S].北京:中国医药科技出版社,2010:附录ⅤD.
[2] 亢玮,王文义,王友国.HPLC法测定阿昔莫司片的含量[J].齐鲁药事,2012,31(3):153-154.

