AP/SiO2/Fe2O3 纳米复合材料的制备与表征
邓竞科,陈人杰,李国平,罗运军
(北京理工大学材料学院,北京100081)
引 言
在复合固体推进剂中,AP是最常用的氧化剂,其热分解性能与固体推进剂的总体性能有密切关系[1-2]。而影响AP 性能最主要的因素是粒度及粒度分布。过渡金属氧化物(如Fe2O3)是催化AP热分解常用的催化剂[3-5]。为了提高催化剂的催化性能,一种有效的方法是将催化剂制备为纳米粒子。但由于纳米粒子极易发生团聚,不易与推进剂的其他组分均匀混合,难以发挥纳米粒子粒径小、比表面大的优异特性,影响了它的实际使用效果。将纳米粒子进行有效的复合,可提高纳米粒子的分散性,充分发挥其表面特性。目前,制备纳米复合材料的方法主要有高能研磨混合法、溶胶-凝胶法、溶剂-非溶剂法等。其中,溶胶-凝胶法由于操作简单可控,可以在纳米尺度上进行组分的混合,能精确控制材料粒子的成分和结构,可制备均一、粒径小、形状特殊的材料等[6-7],因而应用广泛。
本研究采用溶胶-凝胶法制备SiO2/Fe2O3二元凝胶骨架,使Fe2O3以纳米级分布于凝胶骨架中,同时将AP导入凝胶孔洞中,制备了纳米AP/SiO2/Fe2O3复合材料,不仅有效解决了纳米粒子团聚的问题,同时也减小了AP 的粒度,提高其热分解性能。用XRD 和SEM 对其形貌和微结构进行表征。
1 实 验
1.1 材料及仪器
正硅酸乙酯(TEOS),分析纯,天津化学试剂公司;N,N-二甲基甲酰胺(DMF),分析纯,北京化学试剂公司;环氧丙烷(PO),分析纯,北京化学试剂公司;氯化铁(FeCl3·6H2O),分析纯,北京化学试剂公司;AP,工业品,大连高氯酸钾厂。
Nicolet-8700 型FTIR红外光谱仪;X′Pert PRO MPDX 射线衍射仪,荷兰PANalytice公司;S4800 Field-Emission Scanning Electron Microscope 扫描电镜,日本日立公司;METTLER TOLEDO TGA/DSC 同步热分析仪,瑞士Mettler-Toledo公司,升温速率为10℃/min,氮气流量40mL/min,氧化铝陶瓷试样池。
1.2 AP/SiO2/Fe2O3 纳米复合材料的制备
把一定量FeCl3·6H2O 溶解在DMF 中,加入PO 作为催化剂,搅拌一段时间后,按比例加入TEOS和水,另加入一定量的PO 进一步促进溶胶的形成,把溶胶密封后放入60℃水培箱中,待凝胶形成后,再老化48h。然后用大量水置换凝胶中的DMF,置换完全后按一定比例加入AP 并老化,最后经冷冻干燥除去水,获得AP/SiO2/Fe2O3纳米复合材料。
2 结果与讨论
2.1 扫描电镜分析
图1为SiO2/Fe2O3纳米复合凝胶和AP/SiO2/Fe2O3纳米复合材料的SEM 照片。

图1 SiO2/Fe2O3 复合凝胶及AP/SiO2/Fe2O3纳米复合材料的SEM 照片Fig.1 SEM image of SiO2/Fe2O3composite hydrogel and AP/SiO2/Fe2O3nanocomposite
从图1(a)可以看出,凝胶骨架由SiO2(白色小球)和Fe2O3(黑色小球)共同组成,具有三维网络的多孔结构。两种小球粒径都在25~50nm,Fe2O3以纳米级均匀地分布于凝胶骨架中。从图1(b)中可以看出,AP/SiO2/Fe2O3纳米复合材料中,部分AP覆盖在凝胶骨架表面,其表面孔径比纯凝胶骨架孔径略大。对图1 的SiO2/Fe2O3凝胶和AP/SiO2/Fe2O3纳米复合材料表面的孔径进行统计,结果见图2,复合材料表面上孔的数量小于复合凝胶的孔数,而平均孔径大于复合凝胶的平均孔径。一方面是因为AP填充在凝胶骨架的孔道内,减少了孔的总数;另一方面,用粉末添加法[8]制备AP/SiO2复合材料,凝胶骨架经过破碎再修复这个过程,AP起到“稀释”作用,导致凝胶颗粒形成较大的孔道。
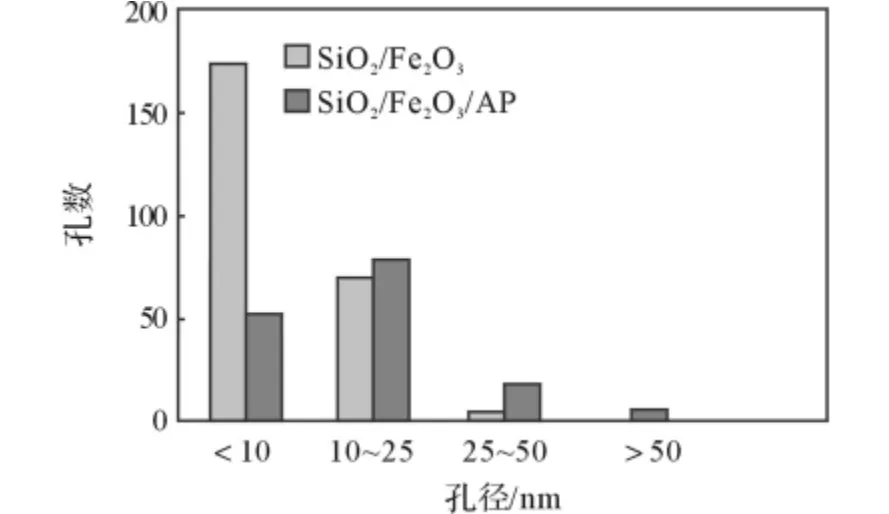
图2 SiO2/Fe2O3 复合凝胶和AP/SiO2/Fe2O3纳米复合材料的孔径Fig.2 Pore diameter of SiO2/Fe2O3composite hydrogel and AP/SiO2/Fe2O3nanocomposite
2.2 XRD 分析
图3 为α-Fe2O3和经400℃高温处理SiO2/Fe2O3复合凝胶的XRD图谱。

图3 α-Fe2O3 和经高温处理后SiO2/Fe2O3 的XRD 图Fig.3 XRD patterns ofα-Fe2O3and SiO2/Fe2O3nanocomposite
曲线(a)上出现的结晶衍射峰为α-Fe2O3的特征衍射峰,通过Scherrer公式[9]计算出的晶粒度为54nm。曲线(b)上在33.15°、35.78°、66.24°也出现了α-Fe2O3晶体的衍射峰,经计算其平均晶粒度为9.7nm,由此可见,把Fe2O3引入SiO2凝胶骨架中,可以有效防止纳米晶体的团聚。
图4分别为原料AP 和AP/SiO2/Fe2O3纳米复合材料的XRD图谱。由图4可以看出,复合材料中AP的衍射峰位置没有移动,说明在溶胶-凝胶过程前后AP的晶型没有发生变化,同时,复合材料中AP的衍射峰强度有所减弱,有宽化现象。这是因为粒子粒径很小,改变了其对X 射线的衍射性质。根据Scherrer公式计算可知,当AP 的质量分数分别为83%、85%、87%、89%和91%时,AP的晶粒度分别为82、151、193、247nm,表明凝胶内AP的平均晶粒度都较小,这是因为AP 在复合凝胶骨架的孔洞中结晶,凝胶孔洞的大小限制了AP 晶体的大小。AP含量高的复合材料,其单位体积内含有的AP数量也相应增多,导致孔洞孔径增加,填充在其中的AP的晶粒度也增大。从图1可见,其表面的AP粒径更小,是因为一部分AP包覆了凝胶骨架表面的粒子,因此其粒径与构成凝胶骨架的Fe2O3、SiO2粒子相差不大。
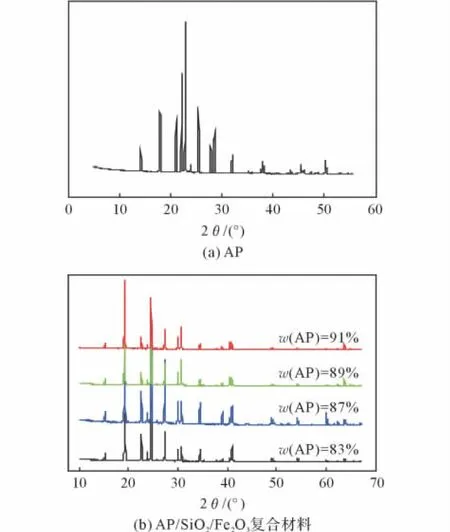
图4 AP及不同AP含量的AP/SiO2/Fe2O3 纳米复合材料的XRD图谱Fig.4 XRD pattern of AP and AP/SiO2/Fe2O3 nanocomposites with different content of AP
2.3 AP/SiO2/Fe2O3 纳米复合材料的热分解性能
分别对原料AP 以及不同AP 含量的AP/SiO2/Fe2O3纳米复合材料进行DSC 测试,结果如图5所示。由图5可看出,纯AP 的热分解过程大致可分为3个阶段:248℃左右出现一个明显的吸热峰,对应的是AP 由斜方晶型向立方晶型的可逆转变;296℃附近的放热峰对应AP 的低温分解阶段,包括AP 的离解与升华;在400~420℃内出现大面积的放热峰,对应AP的高温分解阶段,此阶段AP完全分解,放出大量热。
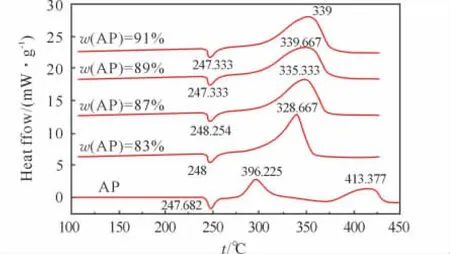
图5 纯AP及不同AP含量的AP/SiO2/Fe2O3纳米复合材料的DSC曲线Fig.5 DSC curves of AP and AP/SiO2/Fe2O3 nanocomposites with different AP content
AP/SiO2/Fe2O3复合材料的热分解过程与AP存在较大差别,不同AP 含量的复合材料的热分解都不存在低温分解阶段,而且随着AP含量的降低,其高温分解峰温分别降低了74.377、73.71、78.044、84.77℃,经过计算,其分解热比纯AP 增加700~1 000J/g。
上述结果表明,将AP引入SiO2/Fe2O3复合凝胶骨架中,在一定程度上影响了其热分解过程,主要表现为低温分解峰的消失、高温分解峰温的降低以及分解热的增加。AP的低温分解阶段主要是其表面活性点上电子的转移反应,生成NH3和HClO4气体。粒度大的AP 具有较为规则的晶体形状,其表面少量的微小晶体缺陷对于NH3和HClO4气体的吸附力相对较弱,在较低温度下即可发生解吸,继续发生反应[10],而凝胶孔洞中的纳米级AP具有很大的比表面积,对气体的吸附能力较强,覆盖了其表面的活性点,以至于无法明显观察到第一阶段的反应。随着温度的升高,AP 的气相反应加剧,凝胶骨架上的纳米Fe2O3具有较大的比表面积,表面原子所占比例很高,且表面具有大量的悬空键和不饱和键,处于不饱和状态,具有很高的表面能及大量的活性点和晶格缺陷,这些纳米Fe2O3以及凝胶的多孔结构会大量吸附气相反应中产生的气体,促进反应正向进行,使反应趋于完全;同时,AP的粒度减小也是改善其热分解性能的关键因素,粒度减小,比表面积增大,反应活性增强。这两种因素的协同作用表现为高温分解峰温降低,并且分解热增加。
3 结 论
(1)采用溶胶-凝胶法,以SiO2/Fe2O3为骨架,AP进入凝胶孔洞中制备了AP/SiO2/Fe2O3纳米复合材料,其中AP晶体粒度为80~250nm。
(2)Fe2O3能够均匀地分散在凝胶骨架中,经过400℃热处理后,SiO2/Fe2O3复合凝胶中Fe2O3的晶体粒度(9.7nm)较原料α-Fe2O3(54nm)小很多,二元凝胶骨架能有效防止纳米Fe2O3的团聚。
(3)AP/SiO2/Fe2O3纳米复合材料能有效促进AP 的热分解,使其高温分解峰温最多降低84.77℃,分解热最多提高987.1J/g。
[1]Singh G,Kapoor I P S,Dubey S.Kinetics of thermal decomposition of ammonium perchlorate with nanocrystals of binary transition metal ferrites[J].Propellants,Explosives,Pyrotechnics,2009,34:72-77.
[2]王敬念,李晓东,杨荣杰.Fe2O3/CNTs纳米粒子的制备及其对高氯酸铵燃速的催化作用[J].火炸药学报,2006,29(2):44-47.
WANG Jing-nian,LI Xiao-dong,YANG Rong-jie.Preparation of ferric oxide/carbon nanotubes composite nano-particles and catalysis on burning rate of ammonium perchlorate[J].Chinese Journal of Explosives and Propellants,2006,29(2):44-47.
[3]杨毅,李凤生,谈玲华.纳米α-Fe2O3的制备及其催化高氯酸铵热分解[J].兵工学报,2004,25(1):82-85.
YANG Yi,LI Feng-sheng,TAN Ling-hua.Preparation of nanometer sizeα-Fe2O3and its catalysis on the thermal decomposition of ammonium perchlorate[J].Acta Armamentar,2004,25(1):82-85.
[4]Kapoor I P S,Srivasta P,Singh G .Nanocrystalline transition metal oxides as catalysts in the thermal decomposition of ammonium perchlorate[J].Propellants,Explosives,Pyrotechnics,2009,34:351-356.
[5]Prajakta R P,Krishnamurthy V N,Satyawati S J.Effect of nano-copper oxide and copper chromite on the thermal decomposition of ammonium perchlorate[J].Propellants,Explosives,Pyrotechnics,2008,33(4):266-270.
[6]Tillotson T M ,Gash A E,Simpson R L,et al.Nanostructured energetic materials using sol-gel methodologies[J].Journal of Non-Crystalline Solids,2001,285:338-345.
[7]Simpson R.Nanoscale chemestry yields better explosive[J].Science and Technology Review,2000:19-21.
[8]Simpson R L,Lee R S,Tillotson T M,et al.Sol-gel manufactured energetic materials:US,66 666 935[P],2003.
[9]张立德,弁季美.纳米材料和纳米结构[M].北京:科学出版社,2001:147-148.
[10]樊学忠,李吉祯,付小龙,等.不同粒度高氯酸铵的热分解研究[J].化学学报,2009,67(1):39-44.
FAN Xue-zhong,LI Ji-zhen,FU Xiao-long,et al.Thermal decompositions of ammonium perchlorate of various granularities[J].Acta Chimica Sinica,2009,67(1):39-44.

