多西他赛、奥沙利铂联合卡培他滨新辅助化疗对进展期胃癌的疗效
王长明,沈丕杰,卫子然,朱振新,蔡清萍,颜荣林(第二军医大学长征医院胃肠外科,上海200003)
胃癌是我国常见的消化道恶性肿瘤,发病率和病死率均居恶性肿瘤前列,其世界调整死亡率(standardized mortality rate)在男、女性均居首位(分别为0.03%和0.013%),并且呈逐年上升趋势(年均增长值为1.3%,其中男1.4%,女1.1%)[1]。在我国,进展期胃癌所占比例较高,约占住院病人的60%,5年生存率为30%~50%,治疗效果差[2]。根治性手术是进展期胃癌治疗的主要手段,但大部分病人术后易复发,而术后化疗对此类病人术后生存期的提高作用有限[3]。在术前化疗治疗头颈、乳腺、膀胱等部位恶性肿瘤取得良好效果的基础上,胃癌的术前化疗也越来越受到重视。但目前,关于胃癌新辅助化疗的方案、疗程等的选择仍然存在争议。现将第二军医大学长征医院胃肠外科近3年进行的多西他赛、奥沙利铂联合卡培他滨(DOX方案)新辅助化疗的病例进行汇总分析,报道如下。
1 资 料
1.1 入组标准 病人符合下列入组标准:(1)术前均经胃镜病理学证实为胃癌病人;(2)术前分期为ⅡB期、Ⅲ期,主要参考内镜超声(endoscopic ultrasonography,EUS)、CT等检查,分期依据日本胃癌学会(JGCA)(2010年第14版)进行;(3)均为初治病人;(4)化疗前Karnofsky评分均在60分以上,均进行血常规、血生化、心电图等检查,排除化疗禁忌;(5)新辅助化疗的目的、方案及副作用均告知病人家属,同意后入组。本研究经本院伦理委员会讨论同意。
1.2 一般资料 2008-06-01至2011-05-31,本院就诊的进展期胃癌病人中共入组186例。男125例,女61例,年龄37~83岁(中位年龄57岁);ⅡB期109例,Ⅲ期77例;胃底贲门/胃食管结合部癌53例,胃体癌48例,胃窦/幽门癌77例,另有8例肿瘤范围巨大,跨越两个分区以上;中分化腺癌41例,低分化腺癌52例,未分化腺癌31例,黏液腺癌15例,印戒细胞癌47例。
1.3 药品 多西他赛注射液(商品名 艾素,规格0.5ml∶20mg),注射用奥沙利铂(商品名艾恒,规格:50mg/支,江苏恒瑞医药股份有限公司);卡培他滨片(商品名 希罗达,上海罗氏制药有限公司,规格:0.5g/片)。
2 方 法
2.1 新辅助化疗方案 多西他赛+奥沙利铂+卡培他滨,3周方案:多西他赛注射液75mg/m2,静脉滴注,第1天;注射用奥沙利铂130mg/m2,静脉滴注,第2天;卡培他滨片,1 000mg/m2,口服,bid,第1天至第14天;每3周重复。如果出现Ⅲ、Ⅳ级血液系统不良反应,或Ⅱ、Ⅲ、Ⅳ级非血液系统不良反应,则减少化疗药物的使用剂量至初始剂量的80%,或延长化疗周期至4周。
2.2 手术时机 一般选择第三次新辅助化疗结束后的2~3周将病人收治入院,重新进行评估后手术治疗。对于不良反应严重,病人难以耐受者则于第二次新辅助化疗后即进行重新评估和手术治疗;对于症状未改善甚至加重的病人,在下一次化疗前及时复查CT、EUS等进行重新评估,进而决定是否选择手术或其他治疗方案。
2.3 疗效和不良反应判定标准 应用2~3个疗程后,按照实体瘤Recist标准[4]收集临床症状改善情况和EUS、CT等检查资料进行评估。分为完全缓解、部分缓解、疾病稳定和疾病进展;有效率为完全缓解率加部分缓解率。手术标本中无肿瘤病灶残留或仅有原位癌残留,则可判定为病理性完全缓解(pathological complete response,pCR)。化疗不良反应按照WHO抗癌药物常见不良反应分级标准分为0~Ⅳ级。
3 结 果
3.1 近期疗效 入组的186例病人全部完成2~3个疗程的新辅助化疗,总疗程数为478,平均2.57个疗程,全部可评价疗效。其中完全缓解7例(3.8%);部分缓解119例(64.0%);疾病稳定53例(28.5%);疾病进展7例(3.8%);有效率为67.8%。且DOX方案新辅助化疗的疗效与年龄、性别、病理分型以及恶性肿瘤的TNM分期之间无明显相关性,具体见表1。
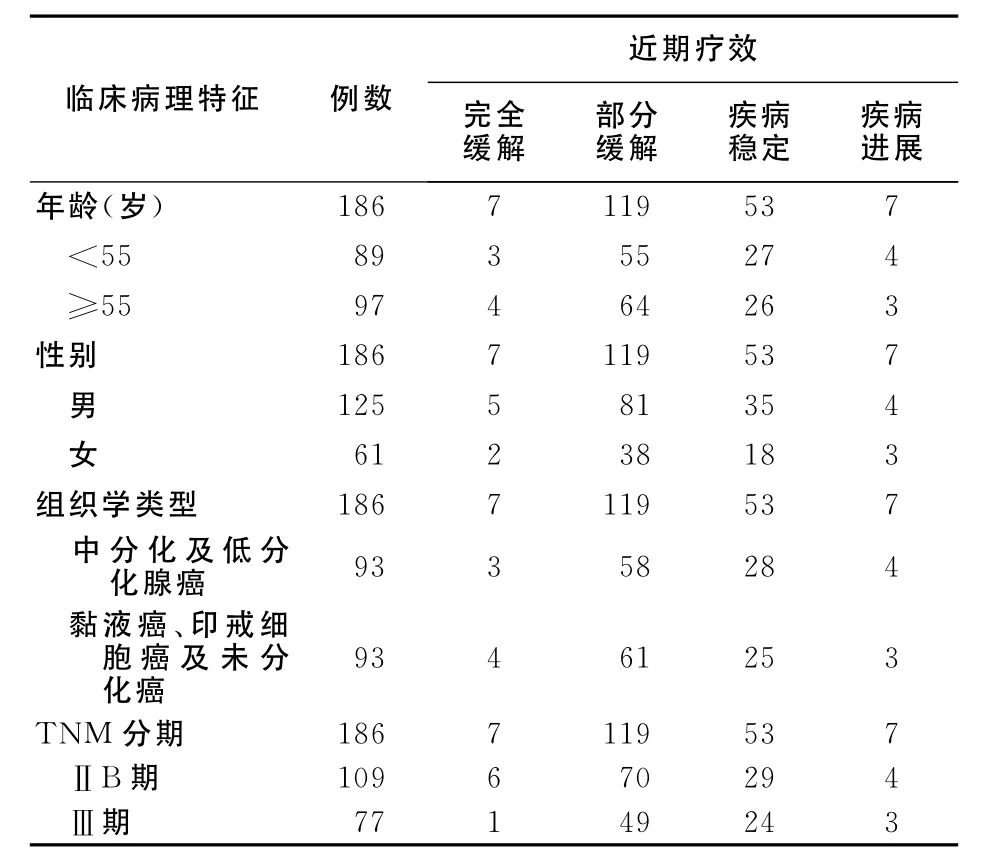
表1 DOX方案新辅助化疗对进展期胃癌的临床疗效Table 1 Clinical therapeutic effect of neoadjuvant chemotherapy of DOX regimen in treatment of advanced gastric cancer(例)
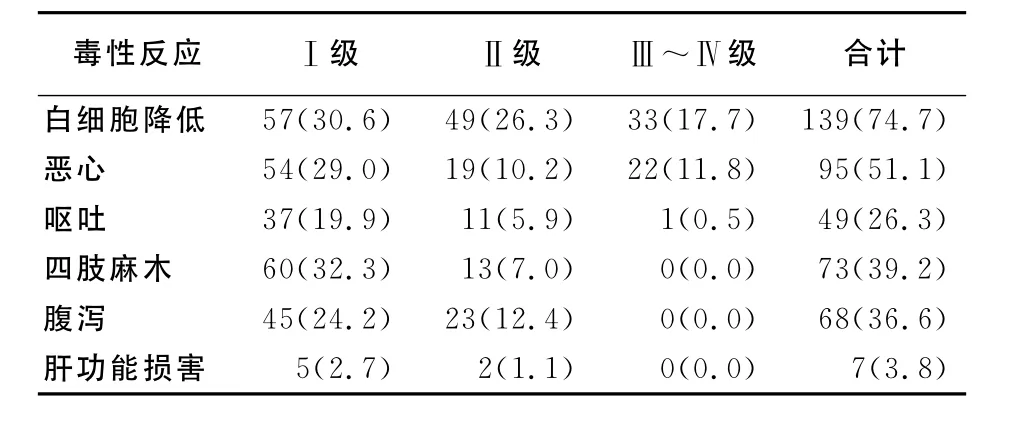
表2 DOX方案新辅助化疗不良反应发生率Table 2 Incidence of adverse drug reactions of neoadjuvant chemotherapy of DOX regimen[例(%)]
3.2 不良反应 总体化疗不良反应发生率较高,以骨髓抑制和胃肠道反应为主。Ⅲ~Ⅳ级白细胞降低者33例(17.7%);胃肠道不良反应发生率亦较高,Ⅲ~Ⅳ级23例(12.4%);周围神经毒性发生率亦较高,但基本为Ⅰ~Ⅱ级,具体见表2。经应用粒细胞集落刺激因子升高白细胞、5-羟色氨酸-3受体拮抗剂止吐等对症治疗,绝大多数病人可耐受。其中一例老年女性病人,两次新辅助化疗后白细胞一度降到0.3×109/L,继发感染,高热,体温达到39.5℃,经连续大剂量注射粒细胞集落刺激因子和抗感染治疗1周后恢复正常,3周后该病人于重新评估后顺利行根治性全胃切除术,术后恢复良好。
3.3 手术治疗及术后病理情况 186例病人中,13例病人放弃手术治疗,其中因新辅助化疗后疾病进展者5例,因化疗效果良好拒绝手术而选择继续化疗者5例,由家庭经济困难等其他原因者3例;其余173例病人均接受了手术治疗。手术切除者141例(81.5%),其中达到R0切除者139例(80.3%),达到D2根治性切除者104例(60.1%)。远端胃切除术66例(38.2%),近端胃切除术32例(18.5%),全胃切除术43例(24.9%)。其余32例中,23例行剖腹探查术(13.3%),9例行胃或空肠造口术(5.2%)。术后淋巴结清扫数目平均为(17.33± 4.32)枚,淋巴结转移(3.47±1.43)枚。
3.4 术后并发症 术后并发症发生率较低,共8例,占4.6%。没有非计划性二次手术病例,围手术期死亡率为0。术后腹腔/吻合口出血2例,近端胃切除病人胃排空障碍1例,肠梗阻2例,切口感染1例,肺部感染1例,经保守治疗后得到控制;十二指肠残端漏1例,经充分引流、抗感染、肠内+肠外营养支持治疗3周后愈合良好。
4 讨 论
随着医疗和科技水平的提高,对恶性肿瘤的诊治水平逐渐提高,对肿瘤综合治疗的理念不断加强,新辅助化疗的概念越来越为人们所接受。目前胃癌的治疗方式逐渐形成了以手术为主,化疗、放疗、生物靶向治疗、免疫治疗、中医中药治疗等为辅的综合治疗。而化疗虽然作为辅助治疗,但是其作用越来越受到重视,化疗的概念也由术后辅助化疗拓展为“围手术期化疗”,即包括术前、术中和术后化疗。
新辅助化疗是指在恶性肿瘤局部治疗、手术或放疗前给予的全身或局部化疗,也称术前化疗(preoperative chemotherapy)。它以提高根治性切除率为目的,其主要意义在于:快速改善肿瘤相关症状;减少微转移灶;通过缩小肿瘤体积和降低肿瘤分期提高手术切除率;确定特定病人对化疗的敏感性,指导选择术后辅助化疗方案。胃癌新辅助化疗的适用范围,目前普遍认为主要包括Ⅱ~Ⅲ期的进展期胃癌病人。对于分期较早的胃癌直接选择手术治疗可能更为合适,而对于出现远处转移或腹腔广泛转移的Ⅳ期胃癌病人进行的化疗则只能称为姑息性化疗;若姑息性化疗效果显著,出现转移灶消失,从而能进行根治性切除的,则称为转化性化疗。
胃癌的新辅助化疗研究很多,其中较有说服力的新辅助化疗临床研究即MAGIC试验[5],它将503例病人随机分为两组:围手术期化疗+手术组(CSC组,250例),单纯手术组(S组,253例)。化疗方案为表柔比星、顺铂和氟尿嘧啶(ECF方案)。结果发现CSC组R0切除率为79%,而S组为69%;CSC组的5年生存率明显提高(36%vs 23%)。说明以该方案进行围手术期化疗可以显著改善可切除胃癌和低位食管腺癌病人的无进展生存和总生存期。这项研究奠定了新辅助化疗在可切除胃癌病人中的标准治疗地位,ECF及其改良方案也成为各项新辅助化疗研究的参考。
当前,胃癌新辅助化疗的研究中,选择三药联合方案的研究较多[6,7],最佳方案尚未有一致看法。V325试验[8]表明多西他赛+顺铂+氟尿嘧啶(DCF方案)较顺铂+氟尿嘧啶(CF方案)治疗晚期胃癌的中位生存期明显延长(9.2个月vs 8.6个月,P=0.02),两年生存率明显提高(18%vs 9%),说明在晚期胃癌联合化疗中加入多西他赛是有效的、可行的。为了对抗肿瘤耐药性,较好地抑制和杀灭肿瘤细胞,达到更好的降级、降期的目的,考虑到化疗药物的疗效以及相互协同作用,本研究选择多西他赛、奥沙利铂联合卡培他滨的三药联合方案。奥沙利铂是第三代铂类抗肿瘤药物,其对DNA复制和转录的阻断作用强于顺铂,不良反应低于顺铂和卡铂,因此成为目前最为常用的铂类抗肿瘤药物。卡培他滨是氟尿嘧啶的前体药物,在体内经三种酶代谢转化为氟尿嘧啶后发挥抗肿瘤作用,由于其代谢最后一步所需要的胸苷磷酸化酶在肿瘤组织中的浓度远高于正常组织,使该药在肿瘤组织中大量转化为氟尿嘧啶而发挥抗肿瘤作用。紫杉类单药作为微管稳定剂及细胞周期抑制剂用于晚期胃癌,具有良好的活性。此外,有研究显示,紫杉类药物与奥沙利铂联合应用对干扰胃腺癌细胞的增殖和诱导其调亡方面有协同作用[9]。因而认为DOX方案可能具有较好的疗效。
本研究结果表明,DOX方案的有效率达到了67.8%,173例进行手术的病人中,肿瘤成功切除的有141例(81.5%),其中R0切除者139例(80.4%),略高于MAGIC试验中CSC组的R0切除率(79%),达到了较理想的治疗效果。新近发表的有关胃癌新辅助化疗的研究中,Li等[10]以奥沙利铂+亚叶酸钙+氟尿嘧啶(FOLFOX方案)对局部进展期胃癌进行新辅助化疗,其有效率达70%(23/ 36),新辅助化疗组的R0切除率达86%。DCF方案的治疗效果差别较大,其有效率可达58.6%~76%,R0切除率一般处于54%~91%,一些临床回顾性研究显示,进展期食管和胃癌新辅助化疗后手术切除率甚至可以达到100%[11,12]。但是,这些研究样本量均较小(新辅助化疗组病例数分别为36、43和29),无法完全代表该研究方案的优劣。本研究的结果显示,DOX方案较研究报道的其他三药联合新辅助化疗方案具有非劣性。DOX方案化疗相关的不良反应仍然以骨髓抑制和胃肠道反应为主,Ⅲ~Ⅳ级不良反应发生率虽然较高,但通过应用粒细胞集落刺激因子和抑酸、止吐、补液等对症处理,病人基本可迅速恢复,不影响下次化疗及手术,在本研究中,该方案所引起的不良反应是可以耐受的。但是需要警惕重度不良反应的发生,并于疗程第5天至第7天复查血常规,适时应用粒细胞集落刺激因子等药物,以避免Ⅲ~Ⅳ级血液系统不良反应所导致的严重后果。
在本组病例中,新辅助化疗后的病人术后并发症发生率为4.6%,与一般胃癌术后并发症发生率相当。术后并发症的发生与新辅助化疗无明确相关性。从术中情况看,此类病人往往组织较脆弱,创面易渗血、渗液,手术难度略有增加,但并不影响术后吻合口、伤口愈合,不增加并发症的发生率。
总之,DOX新辅助化疗方案对进展期胃癌具有较好的疗效,不良反应发生率在可接受范围,而且并不增加术后并发症的发生率。
目前针对进展期胃癌的新辅助化疗,仍然有很多问题存在争议。例如,新辅助化疗做几次最佳?若化疗效果显著,则手术切除范围是按化疗前进行还是按化疗后的进行?术后化疗方案的选择,是继续原方案三药联合还是改用两药?若化疗后疾病进展是否仍需进行手术治疗?对于新辅助化疗无效的病人采用了新辅助化疗是否不合理?这些问题都有待于进一步探索和研究。
[1] 孙秀娣,牧 人,周有尚,等.中国胃癌死亡率20年变化情况分析及其发展趋势预测[J].中华肿瘤杂志,2004,26(1):4-9.
Sun XiuDi,Mu Ren,Zhou YouShang,et al.Analysis of mortality rate of stomach cancer and its trend in the last twenty years in China[J].Chin J Oncol,2004,26(1):4-9.In Chinese with English abstract.
[2] 季加孚.胃肠道肿瘤的新辅助治疗——胃癌的新辅助化疗[J].中国实用外科杂志,2005,25(5):261-263.
Ji JiaFu.Neoadjuvant chemotherapy of gastrointestinal cancer—neoadjuvant chemotherapy of gastric cancer[J].Chin J Pract Surg,2005,25(5):261-263.In Chinese.
[3] Mezhir J J,Tang L H,Coit D G.Neoadjuvant therapy of locally advanced gastric cancer[J].J Surg Oncol,2010,101(4):305-314.
[4] Eisenhauer E A,Therasse P,Bogaerts J,et al.New response evaluation criteria in solid tumours:revised RECIST guideline(version 1.1)[J].Eur J Cancer,2009,45(2):228-247.
[5] Cunningham D,Allum W H,Stenning S P,et al.Perioperative chemotherapy versus surgery alone for resectable gastroesophageal cancer[J].N Engl J Med,2006,355(1):11-20.
[6] Sym S J,Chang H M,Ryu M H,et al.Neoadjuvant docetaxel,capecitabine and cisplatin(DXP)in patients with unresectable locally advanced or metastatic gastric cancer[J].Ann Surg Oncol,2010,17(4):1024-1032.
[7] 曲建军,石毅然,刘法荣,等.紫杉醇联合FOLFOX4方案新辅助化疗在进展期胃癌中的临床应用[J].中华胃肠外科杂志,2010,13(9):664-667.
Qu JianJun,Shi YiRan,Liu FaRong,et al.A clinical study of 5-fluorouracil/leucovorin combined with paclitaxel and oxaliplatin as neoadjuvant chemotherapy for advanced gastric cancer[J].Chin J Gastrointest Surg,2010,13(9):664-667.In Chinese with English abstract.
[8] Van Cutsem E,Moiseyenko V M,Tjulandin S,et al.PhaseⅢstudy of docetaxel and cisplatin plus fluorouracil compared with cisplatin and fluorouracil as first-line therapy for advanced gastric cancer:a report of the V325study group[J].J Clin Oncol,2006,24(31):4991-4997.
[9] Park Y H,Ryoo B Y,Choi S J,et al.A phaseⅡstudy of capecitabine and docetaxel combination chemotherapy in patients with advanced gastric cancer[J].Br J Cancer,2004,90(7):1329-1333.
[10] Li ZiYu,Koh C E,Bu ZhaoDe,et al.Neoadjuvant chemotherapy with FOLFOX:improved outcomes in Chinese patients with locally advanced gastric cancer[J].J Surg Oncol,2012,105(8):793-799.
[11] Ferri L E,Ades S,Alcindor T,et al.Perioperative docetaxel,cisplatin,and 5-fluorouracil(DCF)for locally advanced esophageal and gastric adenocarcinoma:a multicenter phaseⅡtrial[J].Ann Oncol,2012,23(6):1512-1517.
[12] Sun X C,Lin J,Ju A H.Treatment of Borrmann typeⅣgastric cancer with a neoadjuvant chemotherapy combination of docetaxel,cisplatin and 5-fluorouracil/leucovorin[J].J Int Med Res,2011,39(6):2096-2102.

