多指标正交试验法优选决明子蒽醌类成分的提取方法
王莹,王青,张伟东,王鹏远,顾宜,王晓娟*
(1.陕西中医学院药学院,陕西咸阳712046;2.第四军医大学第三附属医院药剂科,陕西西安710032)
决明子Cassiae Semen,又名草决明,为豆科植物决明Cassia obtusifolia L.或小决明Cassia tora L.的干燥成熟种子,全国大部分地区都有栽培,主产安徽、广西、浙江和四川等地。其味甘、苦、咸,性微寒,归肝、肾、大肠经,具有清肝明目、润肠通便之功效。主治目赤涩痛,羞明多泪,头痛眩晕,目暗不明,大便秘结[1]。目前研究报道的决明子提取方法主要是以大黄酚或大黄素的提取率为评价指标进行研究[2-4],未见同时以游离蒽醌、蒽醌苷类含有量为指标的研究。由于大黄酚或大黄素作为评价指标的局限性,本实验以橙黄决明素、大黄酸、黄决明素、决明素、芦荟大黄素、1-去甲基决明素、大黄酚、大黄素甲醚8种游离蒽醌,决明子苷、2-葡萄糖基橙黄决明素、2-葡萄糖基决明素、2-葡萄糖基黄决明素4种蒽醌苷类及12种蒽醌总含有量为评判指标来筛选决明子药材的最佳提取方法,为决明子中蒽醌类成分提取的样品处理方法提供科学依据。
1 仪器与试药
1.1 仪器LC—2010A高效液相色谱仪(日本岛津制作所);DL—720超声仪(浙江石浦海天电子仪器厂);BT125D分析天平(北京赛多利斯科学仪器有限公司)。
1.2 试药决明子购自湖北荆州(经陕西中医学院雷国莲教授鉴定为豆科植物决明Cassia obtusifolia L.的干燥成熟种子);对照品决明子苷、2-葡萄糖基橙黄决明素、2-葡萄糖基决明素、2-葡萄糖黄决明素、橙黄决明素、大黄酸、黄决明素、决明素、芦荟大黄素、大黄酚、1-去甲基决明素、大黄素甲醚购自西安昊轩生物科技有限公司(纯度均大于98%);乙腈、甲醇(色谱纯,美国Fisher公司),水为实验室自制三蒸水;其它试剂均为分析纯。
2 方法与结果
2.1 色谱条件[5-7]Diamonsil C18(2)柱(150 mm×4.6 mm,5 μm);流动相为乙腈-0.1%甲酸水溶液梯度洗脱;体积流量1 mL/min;检测波长280 nm;柱温25℃;进样量10 μL。梯度洗脱条件见表1。

表1 梯度洗脱程序Tab.1 Program of gradient elution
2.2 混合对照品溶液的配制分别精密称取决明子苷2.64 mg、2-葡萄糖基橙黄决明素1.80 mg、2-葡萄糖基决明素2.02 mg、2-葡萄糖基黄决明素2.08 mg、橙黄决明素2.16 mg、大黄酸1.94 mg、黄决明素2.06 mg、决明素2.02 mg、芦荟大黄素1.00 mg、1-去甲基决明素1.98 mg、大黄酚2.44 mg及大黄素甲醚2.95 mg至10 mL量瓶中,用甲醇溶解并定容至刻度,摇匀,即为对照品贮备溶液。
分别精密量取上述对照品贮备溶液2.5、4.0、1.0、1.5、3.0、5.0、0.5、0.5、2.0、0.5、0.5、0.5 mL于25 mL量瓶中,加甲醇定容至刻度,即为混合对照品贮备液。各对照品的质量浓度分别为决明子苷26.4 μg/mL、2-葡萄糖基橙黄决明素28.8 μg/mL、2-葡萄糖基决明素8.08 μg/mL、2-葡萄糖基黄决明素12.48 μg/mL、橙黄决明素25.92 μg/mL、大黄酸38.8 μg/mL、黄决明素4.12 μg/mL、决明素4.04 μg/mL、芦荟大黄素8.0 μg/mL、1-去甲基决明素3.96 μg/mL、大黄酚4.88 μg/mL、大黄素甲醚5.9 μg/mL。
2.3 供试品溶液的制备取决明子药材粉末(过三号筛)约0.5 g,精密称定。置圆底烧瓶中,按正交设计的9种工艺进行回流提取,过滤,合并滤液至50 mL量瓶中,用乙醇定容至刻度,摇匀,过0.45 μm微孔滤膜,取续滤液,即得。按2.1项下的色谱条件进行测定,色谱图见图1。
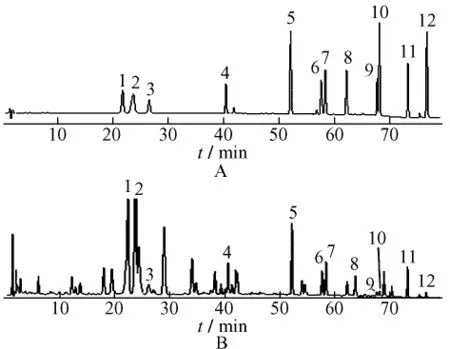
图1 混合对照品(A),决明子(B)的HPLC图Fig.1 HPLC chromatograms of 12 reference substances(A)and sample of Cassiae Semen(B)
2.4 标准曲线的绘制精密吸取上述混合对照品贮备液0.5、1.0、2.0、4.0、6.0、10.0 mL,分别置于10 mL量瓶中,加甲醇定容至刻度。分别过0.45 μm微孔滤膜,按2.1项下的色谱条件进样,色谱图见图1。以峰面积为纵坐标(Y),各对应指标成分的质量浓度为横坐标(X),绘制标准曲线,得其回归方程和相关系数,结果见表2。
2.5 精密度实验精密吸取混合对照品贮备液稀释5倍后的溶液,按2.1项下的色谱条件进行测定,连续进样6次,记录峰面积。结果决明子苷、2-葡萄糖基橙黄决明素、2-葡萄糖基决明素、2-葡萄糖黄决明素、橙黄决明素、大黄酸、黄决明素、决明素、芦荟大黄素、1-去甲基决明素、大黄酚、大黄素甲醚峰面积的RSD分别为0.58%、0.50%、0.93%、0.29%、0.61%、0.30%、0.94%、0.82%、0.75%、0.62%、0.39%、0.23%。
2.6 稳定性实验精密吸取同一供试品溶液(试验号:1),按2.1项下的色谱条件分别在0、2、4、8、12、24 h测定,记录峰面积。结果决明子苷、2-葡萄糖基橙黄决明素、2-葡萄糖基决明素、2-葡萄糖黄决明素、橙黄决明素、大黄酸、黄决明素、决明素、芦荟大黄素、1-去甲基决明素、大黄酚、大黄素甲醚峰面积的RSD分别为0.58%、0.98%、0.47%、0.55%、0.71%、0.73%、0.52%、0.96%、0.69%、0.74%、0.91%、0.90%。

表2 12个对照品的回归方程、相关系数和线性范围Tab.2 Regression equations,correlation coefficients and linearity ranges of the 12 reference substances
2.7 重复性实验精密称取决明子药材粉末0.5 g(试验号:1),平行6份,制备供试品溶液,按2.1项下的色谱条件进行测定,记录峰面积。结果决明子苷、2-葡萄糖基橙黄决明素、2-葡萄糖基决明素、2-葡萄糖黄决明素、橙黄决明素、大黄酸、黄决明素、决明素、芦荟大黄素、1-去甲基决明素、大黄酚、大黄素甲醚峰面积的RSD分别为0.27%、0.61%、0.46%、0.92%、0.79%、0.73%、0.68%、0.80%、0.68%、0.34%、0.74%、0.77%。
2.8 加样回收率实验取已知量的决明子药材粉末6份(试验号:1),每份约0.25 g,精密称定。分别精密加入决明子苷、2-葡萄糖基橙黄决明素、2-葡萄糖基决明素、2-葡萄糖黄决明素、橙黄决明素、大黄酸、黄决明素、决明素、芦荟大黄素、1-去甲基决明素、大黄酚、大黄素甲醚的对照品贮备液各2.0、3.0、0.3、0.7、2.0、3.0、0.3、0.1、0.5、0.2、0.3、0.1 mL,制备供试品溶液,按2.1项下的色谱条件进行测定,计算回收率。结果决明子苷、2-葡萄糖基橙黄决明素、2-葡萄糖基决明素、2-葡萄糖黄决明素、橙黄决明素、大黄酸、黄决明素、决明素、芦荟大黄素、1-去甲基决明素、大黄酚、大黄素甲醚的平均回收率分别为100.53%、101.22%、99.11%、102.56%、100.90%、99.73%、98.25%、101.11%、98.23%、96.41%、101.56%、100.67%,RSD分别为1.79%、2.08%、1.33%、1.97%、1.18%、1.81%、1.87%、2.31%、1.71%、2.61%、1.46%、2.05%。
2.9 正交试验与结果根据单因素预实验,选取影响提取工艺的主要因素乙醇质量分数(A)、提取时间(B)、溶剂倍量(C)和提取次数(D)进行L9(34)正交设计试验,因素水平见表3。

表3 因素水平Tab.3 Factors and levels
以游离蒽醌、蒽醌苷类及12种蒽醌总质量分数为指标,选用L9(34)正交试验表进行实验,结果及方差分析见表4、5。由极差分析结果可知,影响游离蒽醌提取因素的重要性为A>C>B>D;蒽醌苷类为A>B>C>D;总质量分数为A>B>D>C,且三者中因素A均具有显著性差异,因素B只在总质量分数提取时有显著性差异,而因素C、D均无显著性差异,对蒽醌类成分的提取影响较小。综合以上分析结果,最佳提取方法为A2B3C1D2或A2B3C1D1,从实验操作简便性和成本方面考虑,最终确定决明子中蒽醌类成分的最佳提取方法为A2B3C1D1,即50倍70%的乙醇回流提取1次,提取时间2 h。
2.10 验证实验精密称取决明子粉末(过三号筛)约0.5 g共6份,按照上述优选的提取工艺进行提取。按2.1项下的色谱条件进行测定,结果见表6。
3 讨论
本实验比较了甲醇-水、甲醇-0.1%磷酸水、乙腈-0.1%磷酸水、乙腈-0.1%甲酸水梯度洗脱系统对各种成分的影响,结果发现乙腈-0.1%甲酸水梯度洗脱时,12种蒽醌类化合物可以达到完全分离,可准确定量。
预实验同时考察了甲醇,乙醇作为溶剂,超声提取,回流提取对提取工艺的影响,最终确定用乙醇回流提取做正交试验。通过正交试验和方差分析可知乙醇质量分数和提取时间为主要影响因素,最佳提取方法为A2B3C1D2或A2B3C1D1,因素D不具有显著性差异,从实验操作简便性和成本方面考虑,提取次数选为1次。固液比50倍为正交试验设计的最低倍量,同时也考虑了更低倍量的溶剂,结果显示50倍量提取效果依然最佳。故最终确定决明子蒽醌类的提取工艺为A2B3C1D1,即50倍量70%的乙醇提取1次,提取时间2 h。

表4 正交试验结果Tab.4 Results of orthogonal test
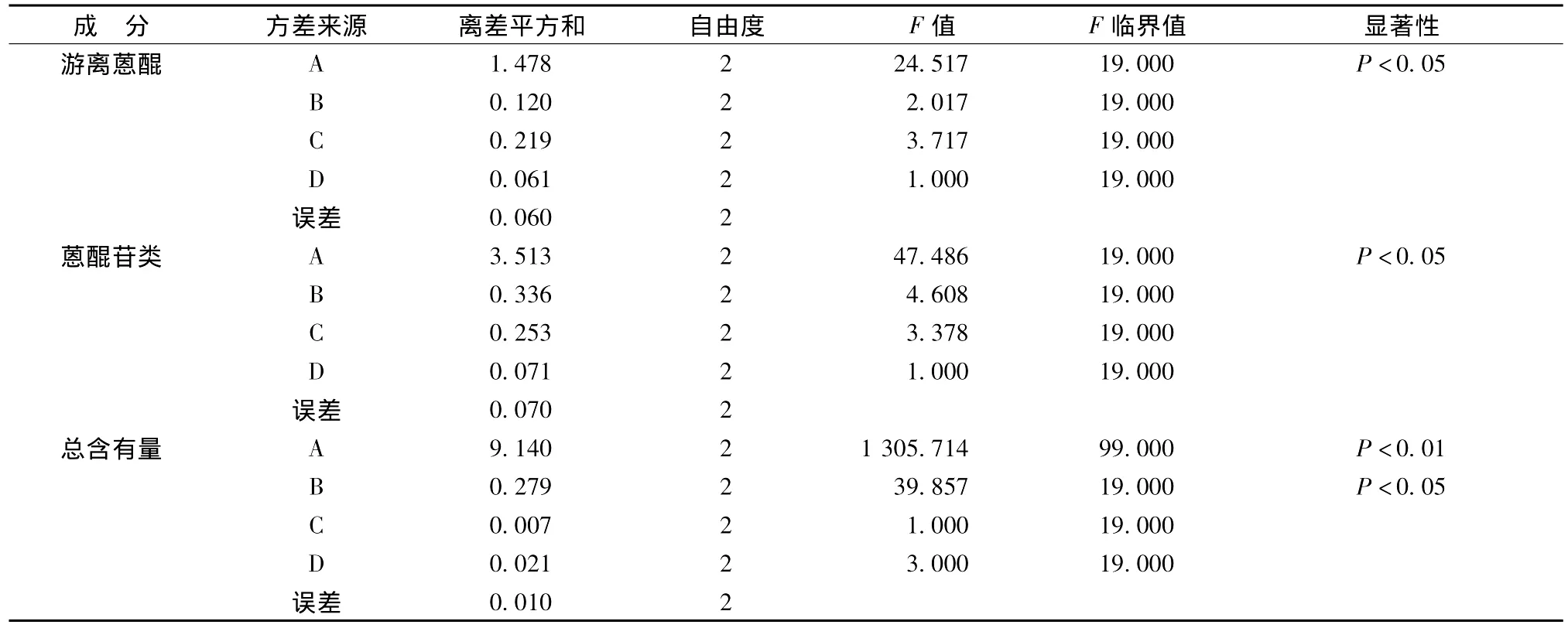
表5 方差分析Tab.5 Analysis of variance
按优选的提取工艺A2B3C1D1进行验证实验,所得6次实验的游离蒽醌、蒽醌苷类及12种蒽醌总含有量的RSD分别为0.72%,0.66%,0.57%,说明该提取方法稳定、重复性好。多年来国内外学者在决明子的化学成分方面做了大量研究,结果表明,决明子中含蒽醌类、萘骈吡喃酮类、脂肪酸类、氨基酸和无机元素等,主要有效成分为蒽醌类[8],决明子中蒽醌类成分多种多样,单一的评价指标不能全面准确的评价提取方法。本实验采用多指标成分定量分析优选决明子提取方法,为决明子药材研究中样品处理过程提供了更全面、科学、高效的方法。

表6 验证实验结果(n=6)Tab.6 Verifying test results(n=6)
[1]国家药典委员会.中华人民共和国药典:2010年版一部[S].北京:中国医药科技出版社,2010:135-136.
[2]陆赛卫,袁华.正交试验法优选决明子的提取工艺[J].山东医学高等专科学校学报,2010,32(2):105-107.
[3]黄琼华.正交试验法优选决明子提取工艺[J].海峡药学,2004,16(4):14-16.
[4]张立明,权洪峰,郑传莉,等.正交设计优化决明子中蒽醌提取工艺研究[J].宁夏医科大学学报,2011,33(1):93-95.
[5]张毅,黄小平,翁代群.HPLC测定不同产地决明子中蒽醌类成分[J].中国中药杂志,2008,33(23):2797-2799.
[6]王宾豪,杨荣平,张晓梅.高效液相色谱法测定决明子中蒽醌类成分的含量[J].时珍国医国药,2008,19(1):135-136.
[7]胡轶娟,朱军,万丽.决明子HPLC指纹图谱研究[J].中国中医药科技,2008,15(5):365-367.
[8]郝延军,桑育黎,赵余庆.决明子的研究进展[J].中草药,2001,32(9):858-859.

