高效液相色谱法中不同pH值对黄酮及有机酸分离效果的探讨
曹 越 罗颂平 苏薇薇 彭 维
1.广州中医药大学科技处,广东广州 510405;2.广州中医药大学第一附属医院妇科,广东广州 510405 3.中山大学生命科学学院,广东广州 510275
黄酮类与有机酸类化合物常同时存在于中药药材及中药组方中,是植物中重要的天然产物,目前有关此两类化合物的研究[1]越来越多。黄酮类化合物(flavonoids)[2]是一类存在于自然界的、具有2-苯基色原酮(flavone)结构的化合物。在植物体内分布广泛,具有多1种生物活性,具有消炎镇痛[3]、防治心血管疾病[4]、抗氧化[5]、抗癌[6]等方面也有显著效果。有机酸类 (Organic acids)[7]是分子结构中含有羧基(-COOH)的化合物。在中草药的叶、根、特别是果实中广泛分布,为许多中草药的有效成分,有一定的特殊的生物活性,例如金银花中有机酸有抗血栓作用[8],绿原酸具有抗氧化作用[9],大青叶中的有机酸具有抗炎解热的作用[10]。常用中药益母草、玉米须、灵芝、金银花、山楂、薄荷、刺五加等都富含黄酮化合物和有机酸类化合物,因此对于研究此2种化合物同时存在的植物的分析方法应用较为广泛。
HPLC作为黄酮类及有机酸类物质分析检测的常用方法,却未见有研究流动相pH值对其分离效果及保留时间影响的报道。为此,本实验考察了流动相pH值的微小变化对上述两种物质的保留时间的影响,旨在为以上述两类化学成分为主的植物的分析分离研究提供依据 。
我们通过实验可证明pH值的变化对黄酮类与有机酸类化合物的分离效果影响非常显著,含有此两类化合物的物质对pH值的变化是非常敏感的。
1 材料与仪器
1.1 仪器与试剂
戴安Dionex公司高效液相色谱仪(ASI-100自动进样器、ATH-58柱温箱、P680四元梯度泵、PDA-100检测器);乙腈(色谱纯,美国BJ),磷酸、甲醇均为分析纯,水为超纯水。
1.2 样品制备
取富含黄酮类成份的植物桑寄生及含有有机酸成分的续断粉末,按1:1质量比混合,以95%乙醇超声提取2次,将醇提药渣以蒸馏水100℃水浴加热回流提取2次,用布氏漏斗减压抽滤,滤液用旋转蒸发仪减压蒸干,加入甲醇溶解,用0.45μm的微孔滤膜滤过。
1.3 KH2PO4-H3PO4缓冲溶液的制备
将6.8g KH2PO4加入1000ml去离子水中,加磷酸数滴调节到相应 pH。(根据《中华人民共和国药典》2005年版一部 附录KH2PO4-H3PO4缓冲溶液的制备方法制备)。pH采用pH计测定。
2 方法与结果
2.1 色谱条件
色谱柱:Agilent HC-C18 Analytical 4.6mm×250mm 5-Micron P.N.518905-902;检测波长:220nm;流速:1mL/min;柱温:25℃;分析时间85 min;进样量10μL。流动相:乙腈(A)-(0.05mol/L)KH2PO4-H3PO4缓冲溶液 (B),线性洗脱梯度,洗脱程序如下:0~65min乙腈10%→28%,65-85min乙腈28%→52%。
2.2 不同pH流动相比较
分别比较流动相为乙腈(A)-(0.05mol/L)KH2PO4-H3PO4缓冲溶液 pH=3.5,pH=3.0,pH=2.5 的分离效果,见图 1、2、4,并以 pH=3.0为例,显示各主要色谱峰的PAD图,见图3。
通过不同流动相不同pH值的色谱图及叠加图比较,可看出不同酸度,较为明显影响黄酮和有机酸的分离,不同pH值下的各色谱峰的保留时间都不同,pH值为3.5时,最前端有机酸前移较多,与前一色谱峰无法分离,最后一个有机酸缺失,pH值为2.5时,前3个主要色谱峰无法有效分离,且第2及第3个有机酸黄酮出峰的先后顺序发生颠倒,pH值为3.0时5个色谱峰得到有效分离,且峰形理想,根据色谱峰的PAD图,出峰顺序为有机酸、有机酸、黄酮、黄酮、有机酸(图3)。因此优选pH值在3左右为流动相较为合适的pH值。?
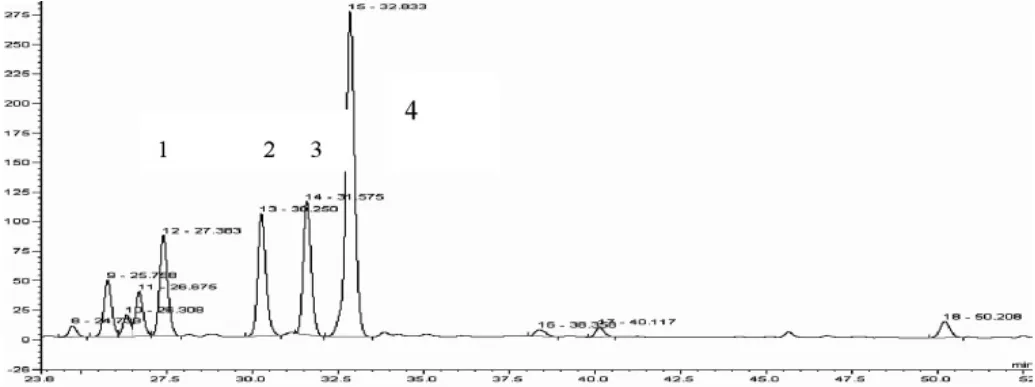
图1 乙腈-KH2PO4-H3PO4缓冲溶液pH=3.5为流动相,检测波长为355nm的HPLC图

图2 乙腈-KH2PO4-H3PO4缓冲溶液pH=3.0为流动相,检测波长为355nm的HPLC图

图3 乙腈-KH2PO4-H3PO4缓冲溶液pH=3.0为流动相主要色谱峰的PAD图
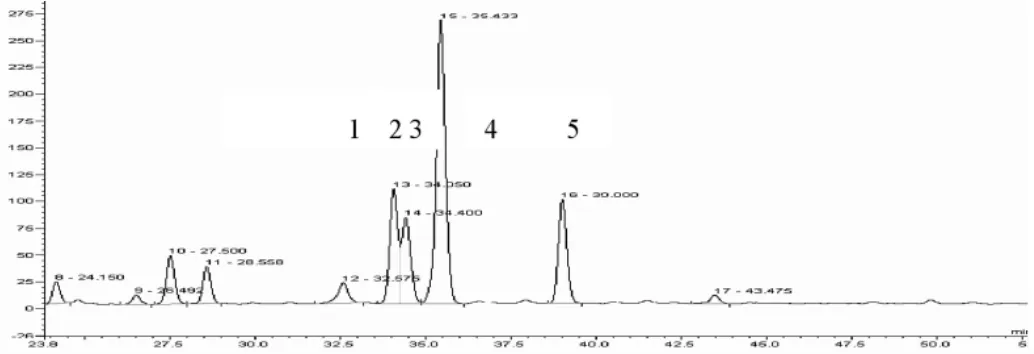
图4 乙腈-KH2PO4-H3PO4缓冲溶液pH=2.5为流动相,检测波长为355nm的HPLC图
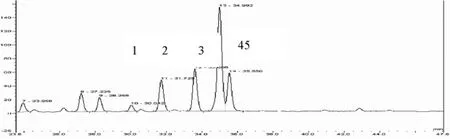
图5 乙腈-KH2PO4-H3PO4缓冲溶液pH=3.1为流动相,检测波长为355nm的HPLC图比较
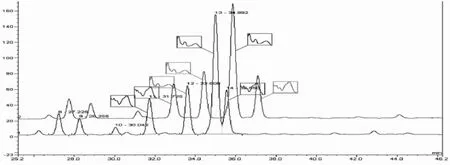
图6 乙腈-KH2PO4-H3PO4缓冲溶液pH=3.0与pH=3.1为流动相HPLC图比较及两特征色谱峰的紫外光谱图
2.3 色谱条件pH值的确定
比较流动相为乙腈 (A)-(0.05mol/L)KH2PO4-H3PO4缓冲溶液pH=3.1,见图5,pH=3.0的分离效果,并显示pH=3.0及pH=3.5重叠图的各主要色谱峰的PAD图,见图6。
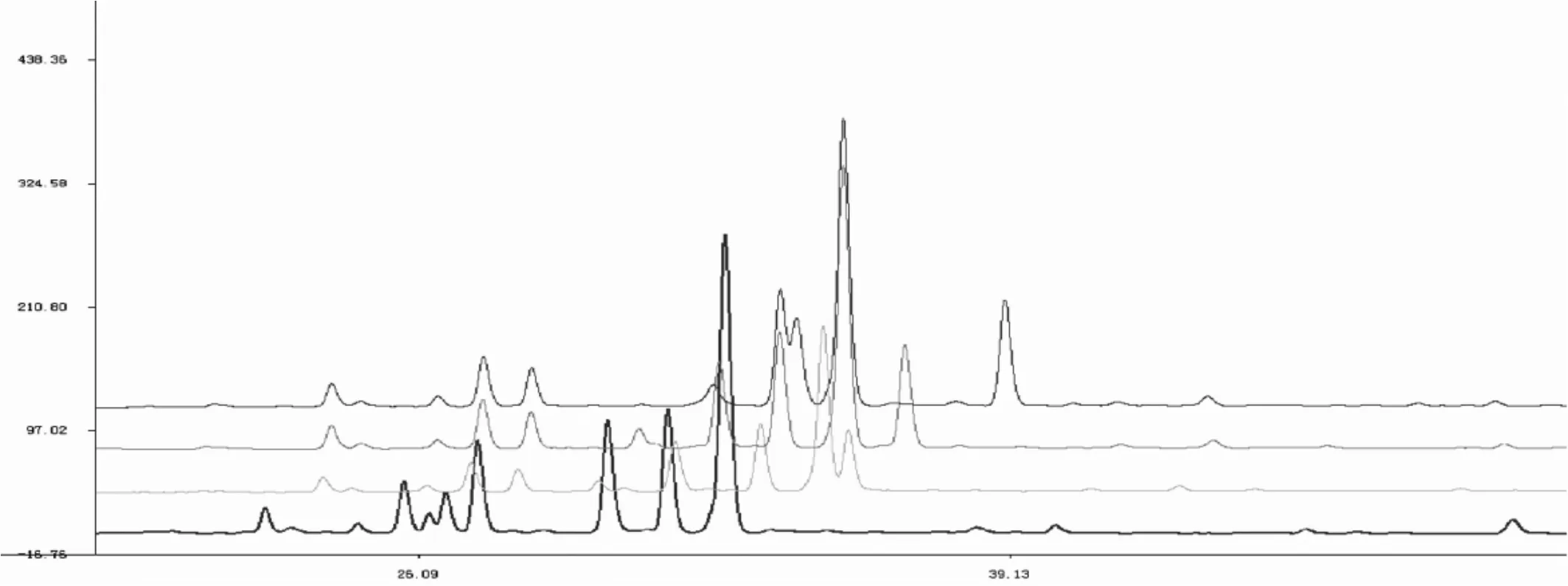
图7 不同pH乙腈-KH2PO4-H3PO4缓冲溶液为流动相,检测波长为355nm的HPLC图谱比较(从下到上以此为pH3.5,pH3.1,pH3.0,pH2.5)
从上图可看出,HPLC色谱图中黄酮类成分与有机酸对流动相的pH要求较严格,pH的稍稍波动在色谱图中有较明显的反映,pH=3.1比pH=3.0出峰提前,在pH=3.1时,第4个色谱峰黄酮苷与第5个色谱峰有机酸的分离度仅1.23,在pH=3.0时,分离度可达2.70,pH=3.0的色谱峰形比较好,且分离度较高。因此流动相选择pH=3.0。
3 结语
在应用高效液相色谱进行物质分析时,可在无机流动相中加入酸、碱或缓冲溶液,以使流动相的pH值控制一定数值,抑制溶质的离子化,减少谱带拖尾、改善峰形,提高分离的选择性。pH值的变化对本系统的分析结果产生很大影响,黄酮、有机酸色谱峰的出峰时间、峰形、分离度等方面受pH影响较大,根据使用色谱柱的填料不同,本系统在pH3.0附近要进行微调,以达到黄酮苷与有机酸完全分离。
流动相pH值的调节是分析过程中至关重要的一个环节,本文通过比较黄酮与有机酸这两大类物质分析效果的不同,指出准确调节流动相pH值的关键所在,有助于提高分析结果的准确性。pH值是影响色谱行为的主要因素之一,是流动相组成优化的最易调节和实现的因素。因此要重视准确调节流动相pH值重要性,这有利于我们更好的分析了解物质的色谱行为,有计划的进行分离条件的选择,减少不必要的错误的实验尝试。
[1]张纪宁,杨洁.黄酮类化合物的生物活性研究进展[J].伊犁师范学院学报,2009,6(2):29-31.
[2]谭秦莉,刘冬,李玉宝,等.总黄酮化合物药理作用研究进展[J].安徽中医学院学报,2009,28(3):62-64.
[3]丘鲁婴,毛春芹,陆兔林.三棱总黄酮镇痛作用研究[J].时珍国医国药,2002,1l(4):291.
[4]Marezin N,Papapetropoulos A,John D C,et al.Tyrosinekinaseinhibitors supprese endotoxin and IL-Iβinduced nonsynthesis in aortic smooth mutscle cells[J].Am J physiol,1993,265(3pt2):1014.
[5]胡琴,齐云,许利平,等.葛根黄酮的体外抗氧化活性研究[J].中药药理与临床,2007,23(6):29-31.
[6]唐丽华,徐向毅.珍珠菜总黄酮苷的抗肿瘤作用及机制研究[J].上海中医药杂志,2007,41(5):74-76.
[7]赵波.中草药中有机酸类成分的提取分离及测定方法研究进展[J].承德医学院学报,2009,26(2):190-193.
[8]樊宏伟,李英斌.金银花中有机酸类成分抗血栓作用研究[J].中药药理与临床,2007,23(3):33-36.
[9]Ricarda N,Anthony JM,Cathie M.Engineering plants with increased levels of the antioxidant chlorogenic acid[J].Nature Biotechnology,2004,22(6):746-754
[10]吴启南,王立新.大青叶中有机酸药理作用研究[J].南京中医药大学学报,2008,24(3):187-189.

