固定床催化4-苯基丁酸分子内酰化反应合成α-四氢萘酮
卞妮妮,毛建新,赵晓倩,丁龙华,郑小明
(浙江省应用化学重点实验室 浙江大学催化研究所, 浙江 杭州 310007)
固定床催化4-苯基丁酸分子内酰化反应合成α-四氢萘酮
卞妮妮,毛建新,赵晓倩,丁龙华,郑小明
(浙江省应用化学重点实验室 浙江大学催化研究所, 浙江 杭州 310007)
在固定床连续流动条件下,以4-苯基丁酸为原料,经分子内酰化反应合成α-四氢萘酮,考察了不同催化剂,反应温度和焙烧温度对催化剂性能的影响。结果表明,在900 ℃焙烧处理后的H-Beta分子筛对该反应具有较好的催化活性和稳定性,在220 ℃连续反应10 h,4-苯基丁酸的平均转化率达98.0%,α-四氢萘酮的平均得率为81.2%。
4-苯基丁酸 α-四氢萘酮 H-Beta分子筛 分子内酰化反应
α-四氢萘酮是一种重要的化工产品及合成中间体[1,2],可以通过多种途径合成。如在过量的无水AlCl3催化[3]作用下,苯和γ-丁内酯一步反应生成α-四氢萘酮,这一反应效果虽好,但后续处理污染严重;采用偶联的方法[4]先合成4-苯基-3-丁烯酸,再经加氢转化为4-苯基丁酸,最后在酸催化作用下发生分子内酰化反应生成α-四氢萘酮,目前该酸催化反应所使用的酸催化剂有三氟乙酸酐和五氧化二磷[4]等,这类催化剂是一次性使用,反应后还会带来大量废酸排放问题;另外,一些金属盐类的路易斯酸如三氟磺酸盐M(OTf)3(M为Bi,Ga和In等元素)也有较好的催化效果[5],但这类催化剂成本较高,且目前尚不明确其重复使用情况。为了克服上述问题,固体酸催化反应合成α-四氢萘酮的研究得到了人们的重视。1995年,Gunnewegh等[6]首先报道了液固相体系Beta分子筛有较好的催化效果;2008年,Hiroki等[7]发现类似的催化体系在微波作用下可以进一步促进反应的进行;最近,邱俊等[8]报道了H-Beta分子筛(Si和Al的物质的量之比为10)经柠檬酸改性后,在液固相体系中对于4-苯基丁酸分子内酰化生成α-四氢萘酮具有较高的催化活性。由于通常在固定床催化条件下的反应有利于生产过程的连续化,且可通过调整反应物与催化剂的接触时间来调控反应程度,有利于催化剂失活后的再生。本工作探讨了固定床催化条件下4-苯基丁酸分子内酰化生成α-四氢萘酮的反应规律,并比较了不同固体酸催化剂的催化效果,考察了反应条件的影响以及催化剂的稳定性。
1 实验部分
1.1 催化剂制备
以等体积浸渍法制备负载型杂多酸催化剂。称取一定量的层析硅胶,将不同量的杂多酸溶于适量的水后,分别滴加到硅胶(粒径0.075~0.150 mm)中,边滴边搅拌,加热、炒干后,置于110 ℃烘箱内干燥过夜,然后放入马弗炉中于250 ℃下焙烧4 h,冷却后保存备用。分子筛催化剂使用前在空气气氛中经过一定温度(通常为500 ℃)焙烧4 h。催化剂H-Beta(Si和Al的物质的量之比为12.5)和H-ZSM-5(Si和Al的物质的量之比为25)等分子筛为南开大学催化剂厂生产的产品。
1.2 催化剂评价
将1 g固体催化剂(粒径0.180~0.425 mm)装入反应管中,在高纯氮气气氛中(流速为10 mL/min)于一定温度下活化2 h,然后冷却至设定的反应温度。按1 g 4-苯基丁酸溶于10 mL 1,2-二氯苯的比例制备反应混合液,用恒流泵将混合液以一定的进样速率(0.12 mL/min)送入催化剂床层的上部,混合液体经气化后流经催化剂床层,产物在反应管的出口处冷凝成液体,每隔一段时间取样,产物的定性主要通过GC-MS分析法以及标准样品对照法来确定,通过GC-5190气相色谱(FID 检测器,5%FFAP-AW DMCS(颗粒粒径0.18~0.28 mm,柱长3 m)分析产物的组成。
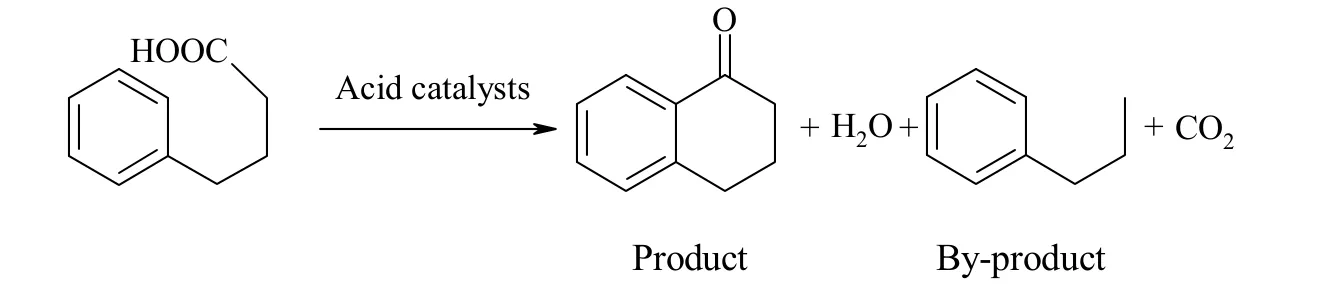
2 结果与讨论
2.1 不同催化剂的活性比较
不同固体酸催化4-苯基丁酸分子内酰化反应性能结果见图1。由图可知,在H-Beta和H4SiW12O40/SiO2(H4SiW12O40/SiO2质量分数为25%)的作用下,4-苯基丁酸能全部转化,且4-苯基丁酸转化率曲线基本重合,而H-ZSM5催化下4-苯基丁酸的转化率不断下降,120 min后转化率从初始的100%逐渐下降至48%左右。以H-Beta为催化剂,随着反应时间的增加,α-四氢萘酮得率也逐渐增加,120 min后趋于稳定;在H-ZSM5催化作用下,反应初期α-四氢萘酮的得率较高(52%),随着反应时间的增加逐渐下降,80 min后下降至5%左右;以H4SiW12O40/SiO2为催化剂,反应过程中主要检测到副产物正丙苯,而且只有当反应进行到160 min后才有少量的目标产物α-四氢萘酮生成。这是由于反应起始时较高的催化剂酸性促使4-苯基丁酸脱羧而形成副产物正丙苯,随着反应的进行,催化剂的酸性逐渐降低(这是由于反应过程中有积炭形成,催化剂的酸性中心部分受到覆盖),目标产物的选择性才逐渐升高。由于杂多酸的酸性高于H-Beta分子筛,因此以杂多酸为催化剂进行反应时生成副产物的量要远远高于H-Beta分子筛。H-ZSM5的催化活性随着反应时间的增加逐渐降低,其主要原因是H-ZSM5分子筛的孔道较小(0.53 nm×0.56 nm),反应物分子(约为1.0 nm×0.43 nm×0.31 nm)和产物分子(α-四氢萘酮分子约为0.66 nm×0.49 nm×0.18 nm)[9]不容易及时离开孔道,从而进一步发生副反应,如反应过程中产生积炭覆盖在催化剂的表面活性点或堵塞了分子筛的孔道,导致反应物分子不能进入分子筛的孔道完成反应,从而使转化率和得率逐渐降低;Beta分子筛由于孔径较大(0.64 nm×0.76 nm)[9],受孔道限制作用较小。可以看出此反应需要合适的孔道和适中的酸性,因此,H-Beta分子筛对此反应具有较好的催化活性。

图1 不同催化剂作用下4-苯基丁酸转化率及α-四氢萘酮的得率Fig.1 Effect of various catalysts on conversion of 4-phenylbutyric acid and yield of α-tetralone Reaction conditions: WHSV 9.03 h-1; catalyst 1.0 g; reaction temperature 220 ℃
2.2 反应温度、催化剂焙烧温度的影响以及催化剂的稳定性
以500 ℃下焙烧4 h的H-Beta分子筛为催化剂,考察反应温度对α-四氢萘酮得率的影响结果见图2。由图可知,反应140 min后,在不同温度下α-四氢萘酮的得率都趋近于90%,但在140 min以内,α-四氢萘酮的得率却随着反应温度的增加而降低,说明在反应初期温度高,生成副产物的量多,目标产物的选择性低。因此,适当降低反应温度有利于目标产物的生成。

图2 反应温度对α-四氢萘酮得率的影响Fig.2 Effect of reaction temperature on yield of α-tetralone Reaction conditions: WHSV 9.03 h-1; catalyst 1.0 g.
图3为焙烧温度对α-四氢萘酮得率的影响。由图可知,催化剂的焙烧温度对生成α-四氢萘酮得率的影响较大。催化剂经过300 ℃焙烧,反应60 min后,α-四氢萘酮的得率稳定在60%左右;经过500 ℃焙烧的催化剂,反应140 min以后,生成α-四氢萘酮的得率才趋于稳定;经过900 ℃焙烧的催化剂,反应60 min后,α-四氢萘酮的得率稳定在80%左右。这是由于当焙烧温度在300~900 ℃,H-Beta分子筛的主要结构没有发生变化,当焙烧温度从500 ℃上升到900 ℃,分子筛的结晶度稍有下降,而且表面酸强度和表面酸性明显下降[10]。经过900 ℃焙烧的催化剂主要以L酸中心为主[11],由此可以推断,此反应起主要催化作用的是L酸中心,虽然B酸中心在反应中也起到了一定的协同作用,但B酸中心的增加会导致副产物的增多,不利于目标产物的生成。
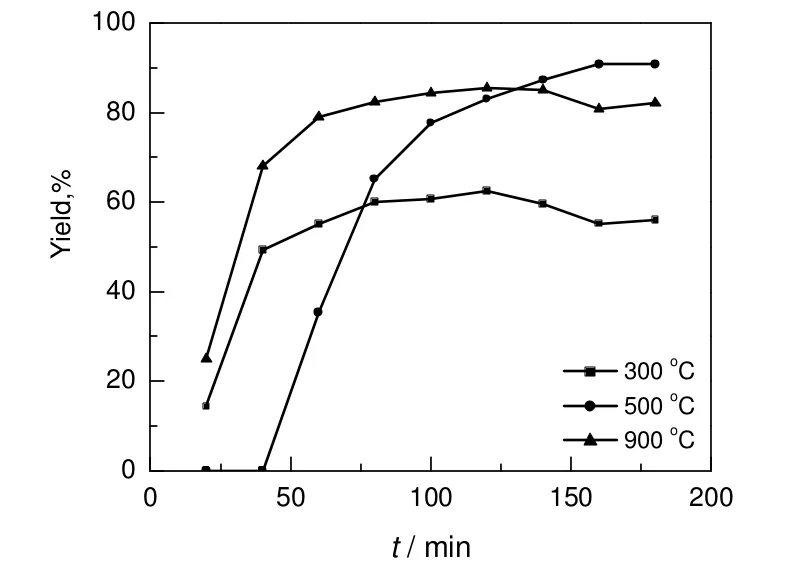
图3 焙烧温度对α-四氢萘酮得率的影响Fig.3 Effect of calcination temperature on yield of α-tetralone
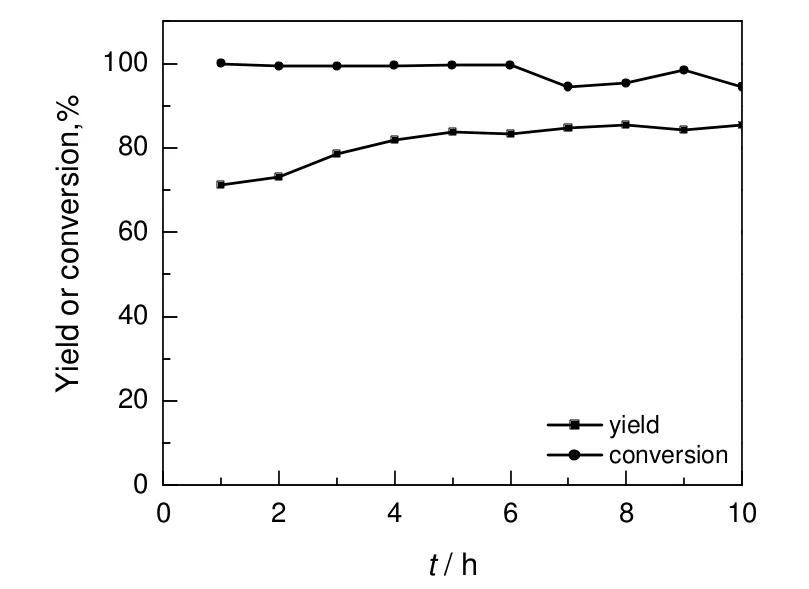
图4 催化剂连续运行的稳定性情况Fig.4 Stability of catalyst
由上述结果可知,H-Beta分子筛在900 ℃焙烧之后对此反应具有较好的催化活性和稳定性。进一步的稳定性实验结果(图4)表明,连续反应10 h,催化剂仍然能够保持较好的催化活性和选择性,4-苯基丁酸的平均转化率可达98.0%,α-四氢萘酮的平均得率为81.2%。
3 结 论
a)以固体酸为催化剂,在固定床连续流动条件下,4-苯基丁酸经分子内酰化反应合成α-四氢萘酮,催化剂的酸性过强或反应温度过高都将导致更多脱羧副产物正丙苯的生成,适当降低催化剂的酸性或反应温度将有利于目标产物选择性的提高。
b)经900 ℃焙烧后的H-Beta分子筛,对4-苯基丁酸经分子内酰化反应合成了α-四氢萘酮具有较好的催化活性和稳定性,连续反应10 h,该催化剂仍保持较好的催化活性,4-苯基丁酸的平均转化率为98.0%,α-四氢萘酮的平均得率为81.2%。
[1]Yuranov I, Kiwi-Minsker L, Renken A. One-step vapour-phase synthesis of 2-methyl-1-naphthol from 1-tetralone[J]. Applied Catalysis A:General, 2002, 226(1-2): 193-198.
[2]Vukics K, Fodor T, Fischer J, et al. Improved industrial synthesis of antidepressant sertraline[J]. Organic Process Research and Development,2002, 6(1): 82-85.
[3]Olson C E, Bader A R. α-Tetralone [1(2H)-Naphthalenone, 3,4-dihydro-][J]. Organic Synthesis, 1963. 4: 898.
[4]Vercouillie J, Abarbri M, Parrain J L, et al. Synthesis of 1-tetralone derivatives using a stille cross coupling/friedel crafts acylation sequence[J].Synthetic Communications, 2004, 34(20): 3751-3762.
[5]Cui D M, Kawamura M, Shimada S, et al. Synthesis of 1-tetralones by intramolecular Friedel-Crafts reaction of 4-arylbutyric acids using Lewis acid catalysts[J]. Tetrahedron Letters, 2003, 44(21): 4007-4010.
[6]Gunnewegh E A, Downing R S, Bekkum H . On the potential of zeolites to catalyse aromatic acylation with carboxylic acids[J]. Studies in Surface Science and Catalysis, 1995, 97: 447-452.
[7]Hiroki K, Hatori M, Yamashita H, et al. Efficient synthesis of 1-tetralones from 4-arylbutyric acids by combined use of solid acid catalysts and microwave irradiation[J]. Chemistry Letters, 2008, 37(3): 320-321.
[8]邱 俊, 王建刚, 孙 杰. 改性沸石H-Beta催化4-苯基丁酸分子内付克反应合成1-萘满酮. 应用化学, 2011, 28(2): 194-198.Qiu Jun, Wang Jiangang, Sun Jie. Synthesis of 1-tetralones by intramolecular Friedel-Crafts reaction of 4-phenylbutyric acids using modified zeoliteH-BEA[J]. Chinese Journal of Applied Chemistry, 2011. 28(2): 194-198.
[9]Bejblova M, Prochazkova D, Cejka J. Acylation reactions over zeolites and mesoporous catalysts[J], Chemsuschem, 2009,2(6): 486-499.
[10]Rao P, Leon C, Ueyama K, et al. Synthesis of BETA by dry gel conversion and its characterization[J]. Microporous and Mesoporous Materials,1998, 21(4-6): 305-313.
[11]王金龙. Hβ分子筛催化苯甲醚乙酰化反应的研究[D]. 天津: 天津大学化学工程与技术系, 2009.
Synthesis ofα-Tetralone by Intramolecular Acylation of 4-Phenylbutyric Acid in a Fixed Bed Reactor
Bian Nini, Mao Jianxin, Zhao Xiaoqian, Ding Longhua, Zheng Xiaoming
(Key Lab of Applied Chemistry of Zhejiang Province, Institute of Catalysis, Zhejiang University, Hangzhou 310007, China)
The effect of different catalysts, reaction temperature and calcination temperature on the performance of the catalyst for synthesis ofα-tetralone by intramolecular acylation of 4-phenylbutyric acids in fixed bed were investigated. The results showed that H-Beta zeolite which was calcined at 900 ℃ exhibited high activity and stability in the reaction. The average conversion of 4-phenylbutyric acid was 98.0% and the average yield ofα-tetralone was 81.2% after reaction 10 h at 220 ℃.
4-phenylbutyric acid;α-tetralone; H-Beta zeolite; intramolecular acylation
TQ426.6;TQ612.3 文献标识码:A
1001—7631 ( 2012 ) 02—0180—04
2012-01-09;
2012-03-12
卞妮妮(1987-),女,硕士研究生;毛建新(1967-),男,副教授,通讯联系人。E-mail: jxmao@zju.edu.cn
浙江省功能化多孔材料和绿色替代技术创新团队项目(2012R10014-04)

