培养基组成对铜绿假单胞菌NY3产鼠李糖脂性能和结构的影响
孙 超,郭 斐
鼠李糖脂是一种无毒且应用广泛的生物表面活性剂,具有乳化、起泡、杀菌、驱油等性能,同时可作为食品添加剂的表面活性剂,有着广泛的应用前景。鼠李糖脂在石油工业中主要应用于三次采油和石油污染土壤修复;在农业中主要应用于土壤性能的改良,保护植物以及作无污染杀菌剂使用;在环境修复中主要应用于修复重金属污染,实验证明鼠李糖脂对土壤中多种重金属离子的洗脱能力强于普通的化学表面活性剂。
我们分离筛选出的铜绿假单胞菌NY3[1]能利用不同碳源和氮源发酵产鼠李糖脂。通过改变培养基中的碳源和氮源,利用NY3菌发酵产生出结构性能不同的鼠李糖脂,为有目的控制NY3菌株发酵生产鼠李糖脂奠定了基础。
1 材料与方法
1.1 实验材料
1.1.1 菌种
铜绿假单胞菌NY3,本实验室分离鉴定[2]。
1.1.2 培养基
NY3种子液培养基:牛肉膏3.0 g,蛋白胨10.0 g,NaCl 5.0 g,pH=7.0~7.2,蒸馏水定容至1 000 ml,121℃高压蒸汽灭菌30 min。
无机盐培养基:NH4NO31.004 g(或含氮量相当的表2中所列出的其他氮源),磷酸盐缓冲液30 mL (K2HPO442 g,NaH2PO428 g,pH7.5,蒸馏水定容至1 000 ml),MgSO4溶液0.5 mL(24.64 g/L),CaCl2溶液0.1 mL(CaCl2·2H2O 14.72 g/L),微量元素1.5 mL(FeSO4·7H2O 4.5 g/L、ZnSO4·7H2O 0.148 g/L、MnSO4·4H2O 0.3 g/L、CoCl2·6H2O 0.024 g/L、NiCl2·6H2O 0.024 g/L、CuCl2·6H2O 0.017 g/L、Na2MoO4·2H2O 0.109 g/L、H3BO30.062 g/L),置于1L容量瓶中,调节pH为9.0,蒸馏水定容至刻度。
鼠李糖脂发酵培养基:100 ml无机盐培养基,加入5 ml菜籽油(或重量百分比为4.8%的表1中列出的其他碳源),121℃高压蒸汽灭菌30 min。
1.2 鼠李糖脂的发酵和提纯
将NY3菌接种于100 ml NY3种子液培养基,置30℃摇床(170 r/min)好氧培养24 h,得NY3种子液。以1%接种量将其接种于100 ml鼠李糖脂培养基中,于30℃摇床(170 r/min)好氧培养72h,得含鼠李糖脂发酵液。再于10 000 r/min转速、4℃离心10 min。用浓HCl调上清液pH=2,静置4℃冰箱中过夜,即得发酵液。收集离心沉淀,在pH=2条件下洗涤沉淀,用1 mol/L的NaOH溶解,调pH= 7,冷冻干燥得到微生物表面活性剂粗品,用CH2Cl2抽提后减压蒸干,溶于0.01 mol/L的NaOH溶液,再用Whatman No.4滤纸过滤,调滤液pH=2,于10 000 r/min转速离心30 min,收集沉淀,真空干燥,即得鼠李糖脂纯品[3]。
1.3 分析方法
1.3.1 发酵液性能分析方法
pH值测定:用pHS-3C酸度计测定。
排油圈直径测定:取直径10 cm培养皿一个,加20 ml水后,在中心加0.5 ml橄榄油,在油膜中心加0.1 ml发酵液,中心油膜被挤向四周形成一个圆,其直径与表面活性剂的含量和活性成正比,测量排油圈直径大小。
乳化性能测定:取10 ml刻度比色管,加5 ml航空煤油和5 ml发酵液,摇动混合30 s,静置数分钟,重复三次,读取乳化层体积并观察其稳定性。
表面张力测定:使用最大气泡法进行测量。
1.3.2 鼠李糖脂性能分析方法
含糖量测定:蒽酮 -硫酸法[4],在试管中加0.2%的蒽酮-浓硫酸4 mL为显色剂,沿试管壁滴加样品1 mL,冷却后沸水浴加热20 min,于30 min内在553 nm处测定OD值。
红外光谱测定:将提纯的鼠李糖脂与KBr粉末压片,放入红外光谱仪中扫描,得到红外光谱图。
不饱和键含量测定:利用碘量法[5]进行测定。
2 结果与讨论
2.1 碳源对NY3菌发酵产表面活性剂特性的影响
大量实验表明[1],NY3菌能利用多种碳源发酵产鼠李糖脂。以硝酸铵为氮源,按照1.2中的实验方法制得发酵液和鼠李糖脂后以1.3的分析方法测定其各项性能,结果如表1所示。
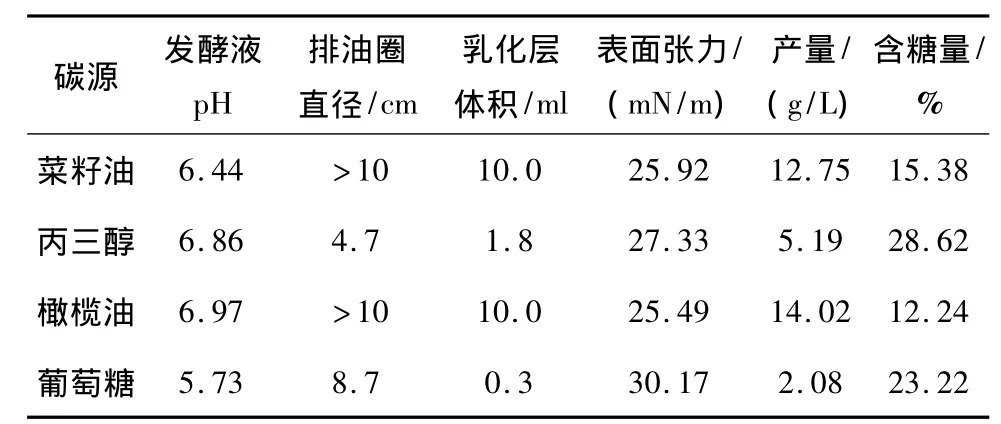
表1 不同碳源制得发酵液和鼠李糖脂性能测定结果
表1结果表明,发酵碳源不同,发酵液的性能有较大差别。以菜籽油和橄榄油为碳源时,发酵液具有极好的排油和乳化性能,且其表面张力分别降到25.92、25.49 mN/m,纯鼠李糖脂含糖量分别为15.38%、12.24%,相对较低。而以丙三醇和葡萄糖为碳源时,NY3发酵液具有较好的排油性能和较差的乳化性能,发酵液的表面张力分别降到27.33、 30.17 mN/m,纯鼠李糖脂含糖量达到28.62%、23.22%,这说明它们具有更好的水溶性。
按照1.3.2的分析方法测定纯化后鼠李糖脂的红外光谱,结果如图1所示。

图1 不同碳源NY3发酵产的鼠李糖脂红外光谱
图1中3 437 cm-1吸收带由鼠李糖环上OH的伸缩振动吸收引起;2 920 cm-1、2 850 cm-1是由脂链中甲基和亚甲基C-H对称与不对称伸缩振动产生的吸收峰;1 750 cm-1为 C=O吸收带,1 055 cm-1为C-O-C伸缩振动吸收带,说明分子中有五圆环内酯结构和糖苷键存在;3 007 cm-1处有一明显小峰,应为不饱和双键C=C吸收峰,说明分子中有不饱和键。按照前期有关NY3发酵产表面活性剂的研究结果[1]和图1中的红外谱图结果,NY3菌用不同碳源发酵所产表面活性剂为鼠李糖脂类化合物。可用3 437 cm-1峰面积和2 920 cm-1~2 850 cm-1处面积比衡量鼠李糖脂中糖含量,该比值越大,糖含量相对越高。利用Origin8软件计算该比值,结果发现,菜籽油、丙三醇、橄榄油、葡萄糖分别为碳源时,该比值为 1.322、18.778、0.706、6.528,因此,丙三醇为碳源所产鼠李糖脂糖含量最高,橄榄油为碳源所产鼠李糖脂糖含量最低。鼠李糖脂含糖量高其水溶性好,含糖量小则排油效果好,因此,红外光谱测定结果和发酵液性能测定结果是一致的。
2.2 氮源对NY3菌发酵产表面活性剂特性的影响
以菜籽油为碳源,NY3在不同氮源条件下生产的鼠李糖脂也具有不同的特性和结构,试验选取了4种具有代表性的氮源,为降低加入种子液给发酵液带来的影响,接种量减小为0.5%,氮源的量增大到原来的1.5倍,其测定结果如表2。

表2 不同氮源制得发酵液和鼠李糖脂性能测定结果
表2结果表明,硝酸铵和硝酸钠为氮源时,NY3发酵液有极好的排油和乳化性能,表面张力降到25.92、24.64 mN/m,纯鼠李糖脂含糖量为15.38%、17.16%;而以氯化铵为氮源时,NY3发酵液的排油性能和乳化性能很差,表面张力为66.93 mN/m,接近蒸馏水的,纯鼠李糖脂含糖量为10.77%;蛋白胨为氮源时,NY3发酵液有较好的排油和乳化性能,发酵液的表面张力为27.07 mN/m,纯鼠李糖脂含糖量为15.26%。
按照1.3.2的分析方法,测定纯化后鼠李糖脂的红外光谱(图2)。
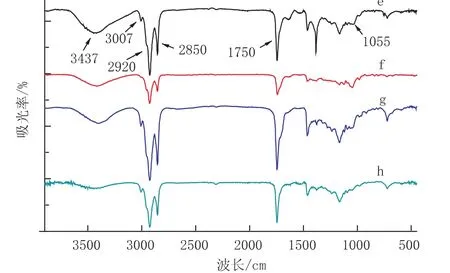
图2 不同氮源NY3发酵产的鼠李糖脂红外光谱
如图2所示,NY3在4种不同氮源培养基发酵产鼠李糖脂的吸收峰都相同或是有少许移位,总体差异并不大,因此,仍为鼠李糖脂类。较为明显的差别为羟基的吸收峰和C=C的吸收峰,其中氮源为硝酸盐时,没有出现明显的不饱和键(包括硝酸钾等),而有铵盐、硝酸铵、蛋白胨等为氮源时,不饱和键就会很明显。
用3 437 cm-1峰面积和 2 920 cm-1~2 850 cm-1处面积比衡量鼠李糖脂含糖量。硝酸铵、硝酸钠、氯化铵、蛋白胨为氮源时,该比值分别为1.322、1.471、0.519、0.534。因此,氮源对NY3产鼠李糖脂含糖量影响不大。氮源为氯化铵生产的鼠李糖脂含糖量最低,为10.77%,且具有破乳性能。氨氮为氮源产鼠李糖脂含不饱和键,有抗氧化性。按照1.3中的碘量法测定4种氮源所产鼠李糖脂的不饱和键含 量,分别为 14.02、0、10.93、13.64 mmol/g。
3 结论
铜绿假单胞菌NY3能利用多种碳源和氮源发酵产鼠李糖脂,且碳源、氮源不同,鼠李糖脂化学组成和产量有明显的差别,使得发酵液的乳化、排油等性能及其表面张力有较大差异。通过研究获得以下结论:
(1)菜籽油和橄榄油为碳源,所产鼠李糖脂含糖量低,发酵液有好的排油性能,且表面张力较低;丙三醇和葡萄糖为碳源,所产鼠李糖脂含糖量高,其水溶性好;菜籽油、橄榄油、丙三醇、葡萄糖为碳源得鼠李糖脂产量分别为 12.78、5.19、14.02、2.08 g/L。
(2)硝酸铵和硝酸钠为氮源,NY3发酵液有极好的排油和乳化性能,表面张力下降显著,提纯的鼠李糖脂含糖量为15.38%、17.16%;氯化铵为氮源,NY3发酵液的排油性能和乳化性能很差,表面张力接近蒸馏水的,提纯的鼠李糖脂含糖量较低;蛋白胨为氮源,NY3发酵液具有较好的排油和乳化性能,表面张力降到27.07 mN/m,提纯的鼠李糖脂含糖量为15.26%。硝酸铵、硝酸钠、氯化铵、蛋白胨为氮源得鼠李糖脂产量分别为12.75、12.36、2.65、9.48 g/L。
(3)氨氮为氮源产鼠李糖脂含不饱和键,有抗氧化性。硝酸铵、氯化铵、蛋白胨为氮源时,不饱和键含量为14.02、10.93、13.64 mmol/g。
[1]刘超.铜绿假单胞菌NY3产表面活性剂发酵条件优化及表面活性剂性能研究[D].陕西:西安建筑科技大学,2011.
[2]惠艳.优良菌种降解烃类污染物相互作用关系研究[D].陕西,西安建筑科技大学,2009.
[3]马满英,施周,刘有势等.预处理酸沉淀冷冻干燥法提取鼠李糖脂新工艺[J],湖南大学学报,2008,35(1):75-78.
[4]卢国满,刘红玉等.鼠李糖快速分析方法及其影响因素研究[J],微生物学通报,2006,33(4):106-111.
[5]国家环境保护总局《空气和废气监测分析方法》编委会.空气和废气监测分析方法[M].第四版增补版.北京:中国环境科学出版社,2008:421-422.

