填充柱色谱法精确测定乙醇/水体系中的醇水含量
唐 妮,魏俊富,2,张 环,2,杜 津
(1.天津工业大学环境与化学工程学院,天津 300387;2.天津工业大学中空纤维膜材料与膜过程省部共建国家重点实验室培育基地,天津 300387)
填充柱色谱法精确测定乙醇/水体系中的醇水含量
唐 妮1,魏俊富1,2,张 环1,2,杜 津1
(1.天津工业大学环境与化学工程学院,天津 300387;2.天津工业大学中空纤维膜材料与膜过程省部共建国家重点实验室培育基地,天津 300387)
利用填充柱气相色谱法测定乙醇/水体系中乙醇的含量,通过考察色谱柱、气化室温度、检测器温度、柱温及载气等色谱条件,获得了最佳色谱检测条件:汽化室温度160℃、检测器温度160℃、柱温140℃、载气流速50 mL/min.以相对校正因子结合峰面积归一法定量测定乙醇/水体系中乙醇,该方法的标准偏差为0.052 4~0.033 2.
填充柱色谱;乙醇/水体系;色谱检测
乙醇是带有一个羟基的饱和一元醇,无色透明,易挥发,易燃烧,能与水、甲醇、乙醚和氯仿等以任何比例混溶.乙醇在国防工业、医疗卫生、有机合成、食品工业、涂料、香料、工农业生产中都有广泛的用途[1-2].尤其是从20世纪70年代发生了能源危机以来,国内外开始以农作物作为原料发酵生产无水乙醇,部分乙醇代替汽油作为内燃机的燃料[3].燃料乙醇制备过程中需要将乙醇和水进行分离,高效低能耗的醇水分离技术能够大大提高乙醇的产量同时降低生产成本.醇水分离过程中,分离体系中乙醇及水含量是一项重要的指标需要进行测定,以便对生产工艺过程进行监控.目前为止,乙醇含量的测定有物理方法和化学方法.物理方法有密度瓶法、酒精计法、折射计测定法、气相色谱法;化学方法有重铬酸钾比色法、莫尔氏盐法、碘量滴定法[4-6].在乙醇/水体系中一般用酒精计法、折射计测定法、气相色谱法测定乙醇的含量[7-8].酒精计法简易迅速,但抗干扰性差、结果准确度较差、误差大;折射计测定法在测定时存在较多不确定因子,时效性、抗干扰性差;气相色谱法测定乙醇及水的含量简单、准确[9-11],对组分的定量方法常用的有面积百分比法、归一化法、内标法、外标法等.面积百分比法只适用于分析响应因子十分接近的组分的含量;在乙醇/水体系中内标法及外标法相对较复杂;在吸附剂对醇水的吸附分离过程中发现[12],定量测定分离体系中含有90%以上乙醇/水混合物中乙醇及水含量时,需对相对定量校正因子进行测定,而且相对定量校正因子不再是常量而是随体系中组分浓度变化,定量分析过程需要重新建立计算方程.为此本文采用填充柱气相色谱法精确测定乙醇/水体系中的醇水含量,通过考察色谱柱、柱温、气化室温度、检测器温度及载气等色谱条件,优化分析操作条件,对90%以上乙醇/水混合体系中相对校正因子进行了测定,同时采用峰面积归一化法对乙醇及水含量进行定量计算,建立一种应用填充柱气相色谱法测定乙醇/水体系中高含量乙醇的分析方法.
1 实验部分
1.1 仪器与试剂
仪器:配有GC2000色谱数据工作站的GC9800气相色谱仪(检测器为热导检测器TCD),上海科创色谱仪器有限公司生产;Porapak Q填充柱(2 m×3 mm),北京华博远科技制造有限公司生产;白酒填充柱(Chromorsorb W 2 m×3 mm),北京华博远科技制造有限公司生产;分析天平(TG326A),上海良平仪器仪表有限公司生产.
试剂:无水乙醇,色谱纯,天津市北方天医化学试剂厂生产;水(去离子水),实验室超纯水设备自制.
1.2 实验方法
(1)配制标样溶液.准确称取水4、8、12、16、20、24 g,再分别加入无水乙醇至100 g,配制成6种标样.
(2)填充柱的选择.用配置好的相同浓度的乙醇/水标样溶液,分别在Porapak Q填充柱和白酒填充柱条件下的气相色谱中进样2 μL,比较色谱图中锋形变化考察不同色谱柱对目标物的分离效果.
(3)温度条件.在Porapak Q填充柱的气相色谱中,取2 μL标样溶液,分别选用气化室温度为130、140、150、160、170℃;检测器温度为 130、140、150、160、170℃;恒定柱温130、140、150、160、170℃下进样测试、分析.
(4)载气流速.在Porapak Q填充柱的气相色谱中,取2 μL标样溶液,在载气(N2)流速为40、50、60 mL/min下进样测试、分析.
2 结果与讨论
2.1 气相色谱条件的选择
2.1.1 填充柱的选择
用相同浓度的乙醇/水溶液标准溶液来考察不同色谱柱对目标物的分离效果,如图1和图2所示.

通过比较图1和图2发现:乙醇在白酒专用填充柱上目标物出现半峰宽较宽、峰较矮、且有基线漂移现象、响应值低,可能是由于填充柱固定相涂层较厚的缘故;在Porapak Q填充柱上色谱峰峰形尖锐对称,响应值高且基线平稳.因此本实验选择Porapak Q填充柱作为气相色谱分析柱.
2.1.2 温度的选择
(1)气化室温度的选择.实验分别考察了气化室温度为130、140、150、160、170℃对乙醇色谱峰的影响情况,如表1所示.表1表明:随着气化室温度的升高,待测物峰面积逐步增大;当气化室温度到160℃以后随着气化室温度的升高,待测物峰面积基本不变,气化室温度为160℃时峰形最好.

表1 气相色谱气化室、检测器、柱温的选择对峰面积及峰高的影响Tab.1 Effect of gas chromatography gasify room temperature,detection temperature and column temperature on selection of peak area and peak height
(2)检测器温度的选择.实验分别考察了检测器温度为130、140、150、160、170℃对乙醇色谱峰的影响,如表1所示.表1显示:随着检测器温度的升高,待测物峰高逐步变高、峰面积逐渐增大,当温度升至160℃后,检测器温度对两者影响不大.考虑到Porapak Q色谱柱的最高使用温度为220℃,故最终选择检测器温度为160℃.
(3)柱温的选择.实验分别考察了色谱柱恒定柱温为130、140、150、160、170℃对乙醇色谱峰的影响,如表1所示.表1表明:柱温对目标物峰高及峰面积几乎无影响,但是随着柱温的升高,乙醇色谱峰分离效果越差、响应值低.综合考虑,选择140℃作为柱温.
2.1.3 载气流速的选择
考察载气(N2)的流速为40、50、60 mL/min对色谱峰的影响,如图3所示.

由图3可见,随着载气流速的增加,待测物出峰所需时间少.载气流速为60 mL/min时,水和乙醇出峰时间在1 min以内,时间太短不利于操作实用.载气流速为40 mL/min时水和乙醇出峰所需时间则过长,因此选择载气流速50 mL/min作为最佳载气流速.
2.2 校正因子的定量方法
2.2.1 校正因子
由于实验中需要测量的组分只有乙醇与水,校正因子在一定条件下并不是常数.因此采用面积归一法可以得到乙醇和水面积的百分比,测定质量定量校正因子.

实验中,用色谱级乙醇及去离子水配制一定已知浓度乙醇的标准溶液,在气相色谱的条件下进行分析测量,得到水和乙醇的色谱峰面积百分比,由式(4)可以计算出相对校正因子f乙醇,水.
2.2.2 校正因子的定量方法
将配制的乙醇/水溶液标样,在最佳测定条件下进行分析,以乙醇的峰面积百分比为横坐标,f乙醇/水为纵坐标,绘制乙醇相对水校正因子随乙醇峰面积百分比变化曲线,如图4所示.

图4是配置70%~99%范围内一定量已知的乙醇/水溶液通过气相色谱测量出气相中乙醇峰面积的量,绘制出乙醇相对水校正因子随乙醇峰面积百分比变化曲线.气相中乙醇峰面积的量用Boltzmann曲线进行拟合,得到不同乙醇峰面积条件下,乙醇相对校正因子与函数关系式为:

式中:X为乙醇质量分数(%);相关系数r=0.998 9;其余参数见表2.
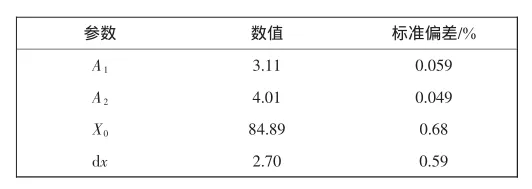
表2 式中参数Tab.2 Values of parameters in formula

相对校正因子对一定的测定体系和一定的测定方法,比如乙醇相对水的体系是不变的.但由图4可知,只有当乙醇含量较低时相对校正因子才是常量,当乙醇的质量分数在70%~99%范围内时,相对校正因子是存在变化的.选择Boltzmann模型去拟合乙醇相对水的校正因子随乙醇峰面积比的变化曲线,得到了较高相关性,证明可以用拟合公式根据峰面积百分比计算出校正因子,再根据式(4)可以计算出实际乙醇的含量.
2.3 精密度的测定
用气相色谱对配制乙醇含量为92%、88%、80%的标样进样5次测量,测定结果及标准偏差,结果如表3所示.
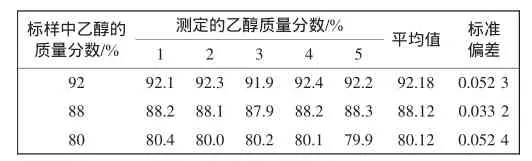
表3 精密度检测结果Tab.3 Precision of method
由表3可见,标准偏差为0.052 4~0.033 2(标准偏差越小,效果越好),其他测试乙醇/水体系中醇水含量标准偏差一般为0.3~0.5,因此,说明用填充柱气相色谱法测定乙醇/水体系中醇水含量精确度较高.
3 结论
用气相色谱法测定溶液中乙醇的含量,色谱检测条件如下:汽化室温度160℃、检测器的类型热导检测器(TCD)、检测器温度160℃、柱温140℃、载气N2、载气流速50 mL/min.获得乙醇相对水校正因子随乙醇峰面积百分比变化曲线,用峰面积归一法定量测定乙醇/水体系中乙醇.并通过精密度测定发现,该方法的标准偏差为0.052 4~0.033 2,表明此方法准确度较高、分析结果可靠、选择性好.
[1] 化学工业部北京橡胶工业研究设计院.GB/T4499-1997硫化橡胶中防老剂的检定薄层色谱法[S].北京:中国标准出版社,1998.
[2] LADISCH M R,DYCK K.Dehydration of ethanol:New approach gives positive enemy balance[J].Science,1979,205:898-900.
[3]CHANG H,YUAN X G,ZENG A W.Experiments on adsorption capability by biomass of ethanol dehydration[C]//International Symposium on Nautral Resource Process ing-Science and Technology.Tianjin:ISNRP,2003.
[4]何文绚,SHANKS Robert,游叶明.有机橡胶助剂的全分析[J].光谱学与光谱分析,2010,30(3):654-658.
[5] 王卉卉,叶曦雯,于世涛,等.橡胶及橡胶制品中4种酚类防腐剂的高效液相色谱法测定[J].分析测试学报,2010,29(3):226-231.
[6] CULLERE L,ESCUDERO A,CACHO J,et al.Gas chromatography-ol-factometry and chemical quantitative study of the aroma of six premium quality Spanish aged redwines[J].Agr Food Chem,2004(6):1653-1660.
[7] MASAZUMI Ko jima,HIROAKI Nakagam.Development of co-ntrolled release matrix pellets by annealing with micronized water-insoluble or enteric polymers[J].J Controlled Release,2002,82:335-343.
[8] United States Enrironmental Protection Agency.Methods for theDeterminationforMetalsinEnvironmental[S].UnitedStates:Noyes Publications,1996.
[9] Methods for the Determination for Metals in Environmental Samples Supplement I,EPA-6000/R-94/111,NIST,USA,1994(5).
[10]朱丽霞.用气相色谱法测定工业冷却废水中微量甲醇,乙醇,丙酮,醋酸甲酯,醋酸乙烯的含量 [J].福建环境,2002,19(4):42-44.
[11]KISHIMOTO T,WANIKAWA A,KAGAMI N,et al.Analysis of hop-de-rived terpenoids in beer evaluation of their behavior using the stir bar-sorptive extraction method with GCMS[J].J Agr Food Chem,2005,53(12):4701-4707.
[12] SONG Y,ZHOU J.Theoretical analysis of the retention behavior of alco-hols in gas chromatography[J].Bioorg Med Chem,2005(13):3169-3173.
[13]常 华.乙醇/水两组分体系在生物质上的气相吸附过程研究[D].天津:天津大学,2006.
Determination of ethanol in ethanol/water system by filling column gas
chromatography
TANG Ni1,WEI Jun-fu1,2,ZHANG Huan1,2,DU Jin1
(1.School of Environment and Chemistry,Tianjin Polytechnic University,Tianjin 300387,China;2.State Key Laboratory of Hollow Fiber Membrane Materials and Membrane Processes,Tianjin 300387,China)
A packed column gas chromatography method was established for the determination of ethanol in ethanol/water system and the best conditions was obtained by investigating the factors influenced the measure of ethanol in ethanol/water system,such as chromatographic column,gasification chamber temperature,detector temperature,column temperature and carrier gas.The optimum detection conditions:gasification chamber temperature is 160℃,detector temperature is 160℃,column temperature is 140℃,when carrier gas reached 50 mL/min,the chromatographic detection could reach best.The ethanol in ethanol/water system was quantified by the relative correction factor and peak area normalization method.The relatively standard deviati of method was 0.052 4-0.033 2.
packed column chromatography;ethanol/water system;chromatographic detection
O657.71
A
1671-024X(2012)03-0044-04
2012-02-21
国家自然科学基金资助项目(51078264);天津市应用基础及前沿技术研究计划项目(09JCZDJC23200)
唐 妮(1986—),女,硕士研究生.
魏俊富(1963—),男,博士,教授,博士生导师.E-mail:jfwei@t jpu.edu.cn

