杯[4]芳烃衍生物的合成及其晶体结构
胡晓钧,彭永标,吴 昊
(沈阳大学 区域污染环境生态修复教育部重点实验室,辽宁 沈阳 110044)
杯[4]芳烃衍生物的合成及其晶体结构
胡晓钧,彭永标,吴 昊
(沈阳大学 区域污染环境生态修复教育部重点实验室,辽宁 沈阳 110044)
通过向杯[4]芳烃下沿引入不同基团,合成得到四种杯[4]芳烃衍生物(2,3,4和5),并采用NMR、ESI-MS和EA对所合成的化合物进行结构表征.同时培养得到化合物2,3和4的单晶,解析出晶体结构,发现在化合物3和4的晶体中同时存在杯[4]芳烃的两种主要构象:锥型和部分锥型.通过分析研究,把产生这种现象的原因归结为:当下沿的保护基团具有适度大的尺寸时,就能够阻止苯环的翻转,并且提供足够的空间.当杯芳烃从溶液中析出时,第四个苯环随机地定位,从而使得两种构象并存于同一晶体中.
杯[4]芳烃;构象;晶体结构;构象异构体
杯芳烃[1-2](图1)是由对位取代的苯酚与甲醛反应得到的齐聚物,被认为是继冠醚、环糊精之后的新一代大环主体分子化合物的代表.杯芳烃具有多样性的空间结构.与环糊精的刚性结构以及冠醚的平面二维结构不同,杯芳烃分子的杯环属柔性骨架,作为连接桥的亚甲基与苯环间以旋转势垒很小的C—C单键相连接,分子内热运动会使得苯环单元绕以相邻的两个桥联亚甲基形成的轴发生翻转,从而导致多种构象并存.如杯[4]芳烃在溶液中一般可呈现锥型(cone)、部分锥型(partial cone)、1,2-交替型(1,2-alternative)和1,3-交替型(1,3-alternative)四种构象[3].在热运动下不同构象之间存在着动态平衡,并受到取代基团以及介质环境和温度的影响.例如,四羟基杯[4]芳烃下沿的四个酚羟基能形成稳定结构的分子内氢键,导致锥型构象在多数有机溶剂如氯仿、甲苯中占绝对优势[4].当下沿的酚羟基被尺寸较小的基团所取代时,分子内的环形氢键随之消失,苯环可以自由翻转,各种构象之间存在动态的转化.而当取代基团的尺寸大于或等于丙基时,这种翻转因为位阻的存在被限定,构象与构象之间的转化随之被禁止[5].在晶体中,由于杯芳烃分子构象被固定,不存在构象之间的转换,因此往往只表现出几种构象中较为稳定的一种构象.

图1 化合物结构式Fig.1 The molecular structure
近期,在对杯[4]芳烃的超分子化学性质研究过程中合成得到一种下沿由两种不同基团保护的杯[4]芳烃衍生物4,并培养得到其单晶,解析出其晶体结构.但令我们感到意外的是,发现在此种杯芳烃衍生物单晶中出现了两种杯[4]芳烃的主要构象:锥式和部分锥式构象.为了探求产生这种现象的原因,合成了一系列此类化合物(图1),并培养出单晶,解析出它们的晶体结构.
1 材料与方法
1.1 实验材料
母体5,17-二溴-25,27-二甲氧基-26,28-二羟基杯[4]芳烃(1)按照文献方法合成[6].对-叔丁基酚,甲醛,二苯醚等实验所需化学试剂和药品购于国药集团化学试剂有限公司(均为分析纯).实验用水为去离子水.
1.2 实验仪器
1H-NMR谱图采用JEOL JNM-ECA-600核磁共振波谱仪测定,质谱采用Bruker 1100和Finnigan LTQ质谱仪测定,元素分析采用EAI CE-440元素分析仪测定,晶体数据采用Bruker P4晶体衍射仪收集,并采用SHELXTL程序解析出晶体结构.
1.3 杯芳烃衍生物的合成
5,17-二溴-25,2726,28-四甲氧基杯[4]芳烃(2):将0.98 g(1.6 mmol)化合物1、1 g氢化钠、10 m L二甲基甲酰胺和100 m L四氢呋喃混合搅拌,缓慢加入10 g碘甲烷,加热回流4 h后,冷却至室温.蒸去溶剂,加入氯仿和稀盐酸,搅拌溶剂,分得下层有机相,干燥.蒸去大部分氯仿,加入甲醇,析出白色沉淀,过滤得白色粉末0.88 g,产率86%.1H-NMR (600 MHz,CDCl3)∶6.45~7.40 (m,10H,Ar H),2.92~4.32 (m,20H,Ar CH2Ar and Ar OCH3).MS(ESI,m/z):[M+Na]+,659.3(65%),661.3(100%),663.3(55%).
5,17-二溴-25,27–二甲氧基-26,28-二丙氧基杯[4]芳烃(3):将1.1 g(1.8 mmol)化合物1、1.5 g氢化钠、5 m L二甲基甲酰胺和100 m L四氢呋喃混合搅拌,缓慢加入7 g碘丙烷,加热回流24 h后,冷却至室温.蒸去溶剂,加入氯仿和稀盐酸,搅拌溶剂,分得下层有机相,干燥.蒸去大部分氯仿,加入甲醇,析出白色沉淀,过滤得白色粉末1 g,产 率 81%.1H-NMR (CDCl3)cone conformation:δ1.07(t,J7.6,6 H),1.83(m,4H),3.15(d,J13.1,4H),3.66 (t,J6.9,4 H),3.89 (s,6H),4.31 (d,J13.1,4H),6.38(s,4H),6.99(t,J7.6,2H),7.14(d,J7.6,4 H);partial-cone conformation:δ1.14(t,J7.6,6 H),1.88(m,4H),2.96(s,3 H),3.08(d,J13.7,2H),3.54 (m,2H),3.58(d,J13.1,2H),3.65(d,J13.1,2H),3.73(s,3H),3.79 (m,2H),4.01 (d,J13.7,2 H),6.47(br s,2H),6.91(t,1 H),6.92(t,1H),7.07(d,J7.6,2H),7.09(br s,2H),7.25(d,J7.6,2 H).MS(ESI/MeOH)717.4(M+Na).
5,17-二溴-25,27-二甲氧基-26,28-二丁氧基杯[4]芳烃(4):将1 g(1.64 mmol)化合物1、1.5 g氢化钠、5 m L二甲基甲酰胺和100 m L四氢呋喃混合搅拌,缓慢加入12 g溴丁烷,加热回流24 h后,冷却至室温.蒸去溶剂,加入氯仿和稀盐酸,搅拌溶剂,分得下层有机相,干燥.蒸去大部分氯仿,加入甲醇,析出白色沉淀,过滤得白色粉末0.87 g,产 率 74%.1H-NMR (CDCl3) cone conformation:δ1.00(m,6 H),1.61(m,4H),1.85(m,4H),3.15(d,J13.1,4 H),3.70(t,J6.5,4 H),3.88(s,6 H),4.31(d,J13.1,4H),6.37(s,4 H),6.99(t,J7.6,2 H),7.14(d,J7.6,4H);partial-cone conformation:δ1.00(m,6 H),1.52(m,4 H),1.82(m,4 H),2.95(s,3 H),3.08(d,J13.8,2 H),3.59(d,J13.1,2 H),3.59(m,2 H),3.66(d,J13.1,2H),3.74(s,3 H),3.81(m,2 H),4.01(d,J13.8,2 H),6.47 (br s,2 H),6.91 (t,1 H),6.92(t,1 H),7.07(d,J7.6,2 H),7.09(br s,2 H),7.25 (d,J7.6,2 H).MS (ESI/MeOH)745.3(M+Na).Anal.Calcd.for C38H42Br2O4:C,63.17;H,5.86;Found:C,62.93;H,5.58.
5,17-二溴-25,27-二甲氧基-26,28-二己氧基杯[4]芳烃(5):将1 g(1.64 mmol)化合物1、1.5 g氢化钠、5 m L二甲基甲酰胺和100 m L四氢呋喃混合搅拌,缓慢加入6.18 g溴己烷,加热回流24 h后,冷却至室温.蒸去溶剂,加入氯仿和稀盐酸,搅拌溶剂,分得下层有机相,干燥.蒸去大部分氯仿,加入甲醇,析出白色沉淀,过滤得白色粉末0.93 g,产 率 73%.1H-MR (CDCl3)cone conformation:δ0.91(br s,6 H),1.36 (br s,8H),1.49(m,4H),1.82 (m,4H),3.15(d,J13.1,4 H),3.69 (t,J5.9,4H),3.89(s,6 H),4.31(d,J13.2,4H),6.37 (s,4H),6.99(t,J7.2,2H),7.15(d,J7.3,4H);partial-one conformation:δ0.91(br s,6H),1.36 (br s,8H),1.58 (m,4H),1.86(m,4H),2.95(s,3H),3.08(d,J13.8,2H),3.57 (m,2H),3.59(d,2 H),3.65(d,J13.4,2 H),3.73 (s,3 H),3.80(m,2H),4.01(d,J13.8,2H),6.47(br s,2H),6.90(t,1 H),6.92(t,1 H),7.07(d,J6.8,2H),7.09(br s,2H),7.25(d,2H).MS(ESI/MeOH)801.4(M+Na).
5,17-溴-25,27–二甲氧基-26-甲酰基-28-基杯[4]芳烃(6):将0.9 g(0.9 mol)化合物1溶于25 L吡啶,在冰水浴中搅拌下,缓慢加入5 L苯甲酰氯,反应72 h后,停止搅拌.过滤得到白色沉淀,用蒸馏水和甲醇清洗数次.将白色粉末用层析柱分离,以石油醚/丙酮为流动相,收集前一组分,用氯仿/甲醇重结晶得白色粉末0.2 g,产率31%.
5,17-溴-5,27-甲氧基-6,28-甲酰基杯[4]芳烃(7):上面反应后,柱分离收集第二组分,用氯仿/甲醇重结晶得白色粉末0.35 g,产率48%.1H-MR(CDCl3):δ2.83~4.03(m,14 H),6.31~7.22(m,7 H),7.26~4.43 (m,13 H).MS(ESI/MeOH)841.1(M+Na).
1.4 杯芳烃衍生物单晶培养
通过在氯仿/甲醇混合液中,缓慢挥发溶剂的方法,分别培养得到化合物2、3、4的单经X射线衍射得到以下晶体结构数据:七种化合物在CCDC 的 注 册 号 码 分 别 是:2(274950),3(286075),4(263620).
2 结果与讨论
首先培养得到化合物4的晶体,并解析其单晶结构.X射线衍射的结果表明,在化合物4的晶体中存在着两种不同的杯[4]芳烃构象异构体:锥式和部分锥式,两种构象异构体出现的概率之比为1∶1,也就是说两者在晶体中有相同的稳定性.如果把两种构象叠加在一起,就得到了图2所示图形.
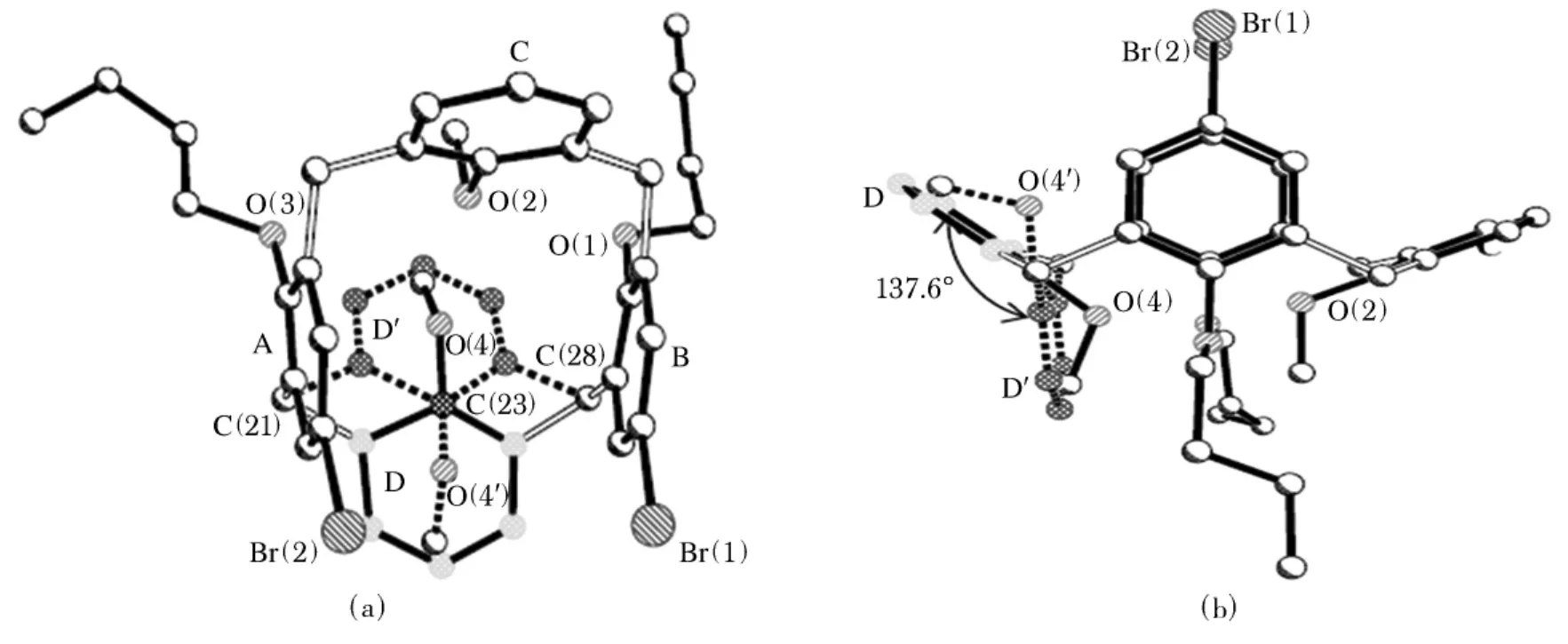
图2 化合物4两种晶体构象的叠加图Fig.2 The overlapped molecular structure of the cone and partial-cone conformational isomers of 4 in solid state
从图2中可以看出,锥式构象和部分锥式构象中的三个苯环(A、B和C)几乎完全重合,而唯一的区别就在第四个苯环(D和D′)的位置.两个相对的苯环A和B处于两个几乎相互平行的平面,平面之间的夹角为12.8°.在锥式构象中,苯环C与苯环D的夹角为65.6°,而在部分锥式构象中苯环C与苯环D′的夹角为107.9°,苯环D与D′之间的夹角为137.6°.细致观察可以发现,苯环D的C(23)与苯环D′的C(23)正好重合,就好像是苯环D绕由C(21)、C(23)和C(28)构成的虚拟轴旋转137.6°到达苯环D′.
归结产生两种主要构象同时出现在同一杯芳烃单晶中这一新现象的原因,我们做如下分析.在图2中,锥式构象中的第四个苯环D及其所接甲氧基与部分锥式构象中的苯环D′及其所接甲氧基几乎处在同样的空间位置,这就使得锥式构象和部分锥式构象在分子的尺寸和形状上几乎没有太大的差异.而且由于杯芳烃下沿的两个正丁基的尺寸较大,从而抑制住苯环A和苯环B跨越桥联亚甲基平均平面的翻转,并使得自身分子与相邻分子保持一定空间距离,为第四个苯环D的自由定位提供了足够的空间,因而可以按照溶液中的构象比例析出.通过分析化合物4在氯仿中的核磁共振氢谱,得知化合物4在溶液中也存在着两种构象(锥式和部分锥式),两种构象的比例也是1∶1,这也印证了我们的推论.
为了证明对这一新现象归因的正确性,将下沿的两个正丁基用尺寸稍小的正丙基取代,从而制得化合物3.化合物3在氯仿中的核磁共振氢谱显示了和化合物4同样的结果,即化合物3在溶液同样存在锥式和部分锥式两种构象(表1),并且二者的比例接近1∶1,说明尺寸稍小一些的丙基在溶液中也能阻止苯环A和苯环B的翻转.利用挥发溶剂的方法培养出化合物3的晶体,并解出其单晶结构.单晶衍射测试的结果与我们的预期相吻合,在化合物3的单晶中也存在着锥式和部分锥式两种构象,但两者比例接近7∶3.
比较图3和图2可以看出,化合物3和化合物4在单晶中的两种构象的形状非常相似,两种构象的第四个苯环及所接甲氧基也同样处在几乎相同的空间位置,并且苯环D与苯环D′之间的夹角比化合物4中的稍小,为136.6°.唯一较明显的区别就是下沿的取代基差异,化合物4中为正丁基,而化合物3中为正丙基.这也进一步证实本研究对这一新现象归纳原因的正确性.虽然,在溶液中,由于含甲氧基的苯环可较自由地翻转,使锥式和部分锥式两种构象按近似1∶1的比例存在;而在晶体中由于杯芳烃下沿的两个正丙基的有适度大的尺寸,从而抑制住苯环A和苯环B跨越桥联亚甲基平均平面的翻转,并使得自身分子与相邻分子保持一定空间距离,但正丙基的尺寸所能提供的空间只能满足第四个苯环以70%概率处在正立位置D,即锥式构象,而以30%的概率处在翻转位置D′,即部分锥式构象.

图3 化合物3两种晶体构象的叠加图Fig.3 The overlapped molecular structure of the cone and partial-cone conformational isomers of 3 in solid state
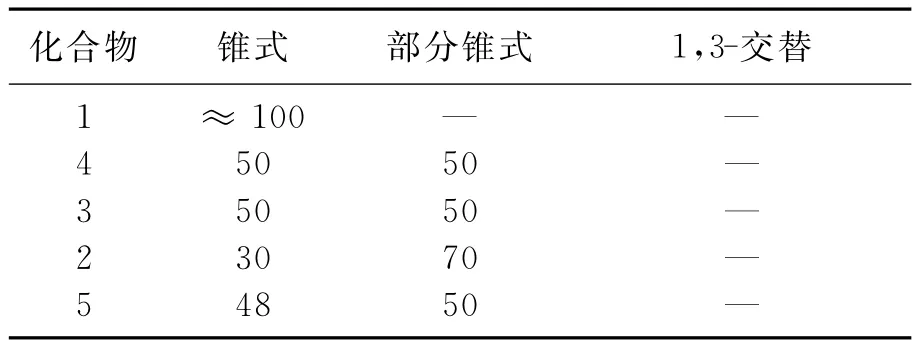
表1 几种化合物在溶液中的存在构象比例Table 1 Distribution of conformational isomers of the calix[4]arene derivatives in solution %
当把下沿的取代基从丙基进一步减小到甲基,就得到了化合物2.同样也培养得到化合物2的晶体,并解出其单晶结构.同样和预期的结果相符,在化合物2的单晶中没有出现两种主要构象共存的现象,只有一种部分锥式构象被观察到.这也证实了我们的推测,由于甲基的尺寸较小,不能阻止苯环的翻转,也就不可能为第四个苯环随机性地定位提供有效的空间,为了能最紧密堆积,所以化合物2在从溶液中析出时只采用了稳定的部分锥式构象.而化合物2的核磁共振氢谱则表明,化合物2在溶液中同样存在两种构象(锥式和部分锥式).图4显示了化合物2的晶体构象,与3和4不同,为了使分子内空间位阻最小,两个带有溴原子的苯环处于反式位置,苯环平面之间的夹角为47.9°.而另外两个相对苯环则处在顺式位置,两个苯环平面几乎平行,呈13.5°夹角.四个甲氧基为减小空间位阻而伸向空腔外测.
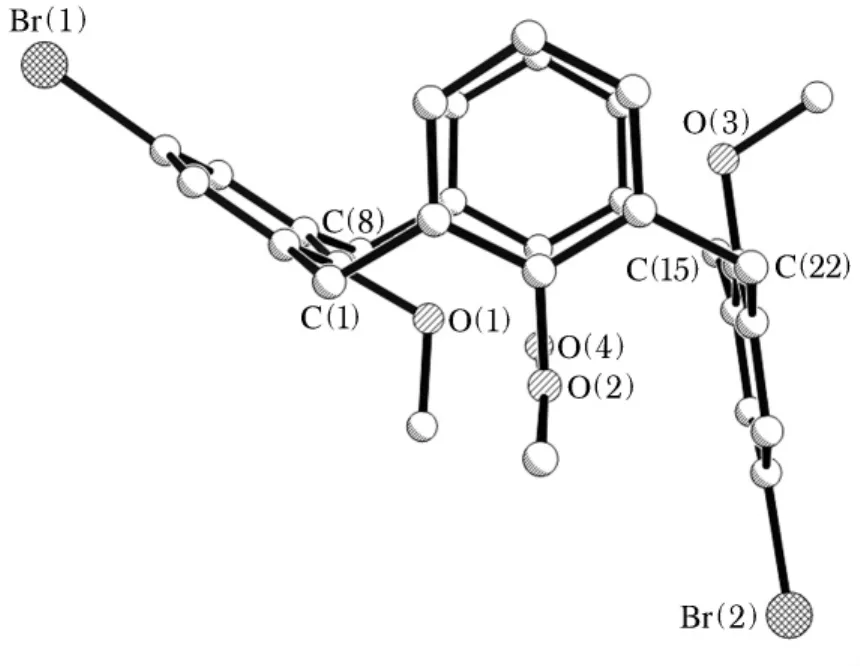
图4 化合物2的晶体构象图Fig.4 The molecular structure of 2 in solid state
为了再一次证明我们的推论和归因的正确性,将下沿的取代基由正丁基改换为较大的正己基,就得到化合物5.培养出化合物5的晶体外形很规整,但遗憾的是虽然做了X射线衍射测试,可能是由于正己基长链的柔性引起的不确定性太大,没能解出其单晶结构.但是化合物.5在溶液中的核磁共振氢谱告诉我们,同样存在着锥式和部分锥式两种构象,而且两者比例也是接近1∶1.并且在化合物3、4和5三者的核磁共振氢谱上,苯环氢、桥联亚甲基氢和甲氧基氢的化学位移值及积分值都非常接近,而高场部分的峰形的不同是由于不同长度烷基取代基而引起的差异(图5).化合物5下沿接的取代基为长度更长的正己基,也能够为第四个苯环的随机性定位提供足够的空间,因此有理由相信在化合物5的晶体中同样存在着锥式和部分锥式两种构象.
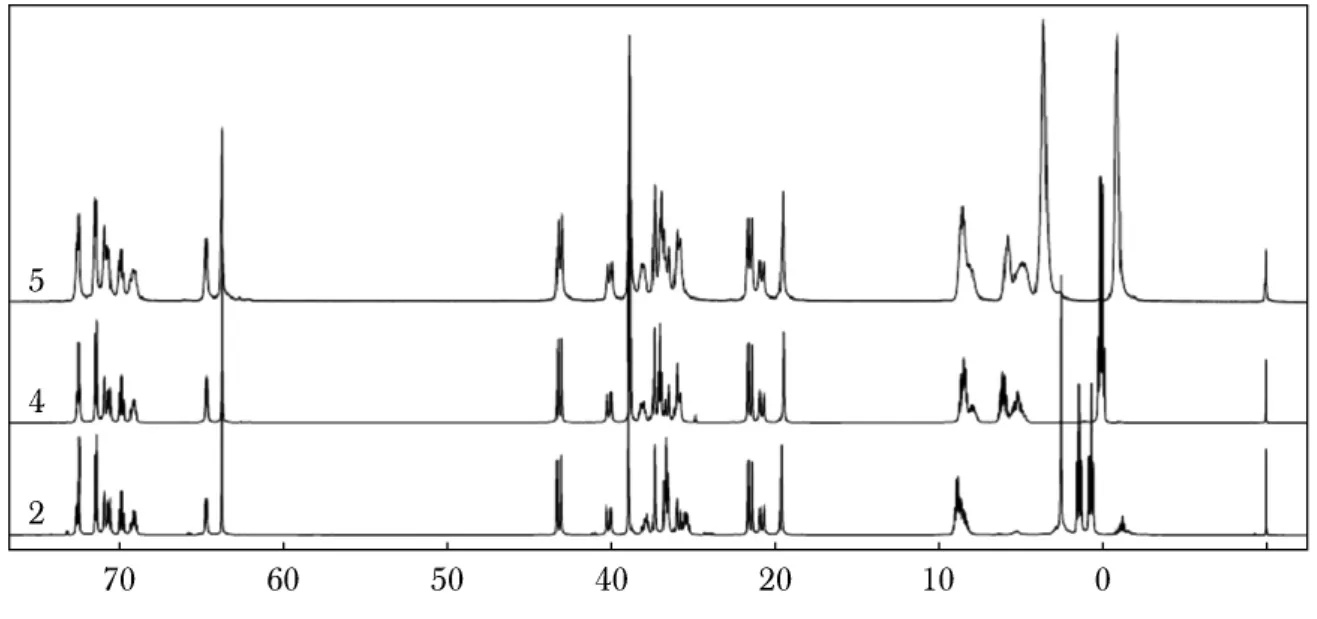
图5 化合物3、4和5的核磁共振氢谱Fig.5 The 1 H-NMR spectra of 3,4 and 5 in CDCl3
3 结 论
通过更换不同取代基团,合成了4种新的杯[4]芳烃衍生物,并培养出其中3种新化合物的晶体,解出其单晶结构.其中发现一种新的现象:两种不同的杯[4]芳烃主要构象并存于晶体中.通过实验数据分析,我们把产生这种现象的原因归结为:当下沿的保护基团具有适度大的尺寸时,就能够阻止苯环的翻转,并且提供足够的空间,在杯芳烃从溶液中析出时,让第四个苯环随机地定位,从而使得两种构象并存于同一晶体中.
[1] Gutsche C D.Calixarenes,Monograph in Supramolecular Chemistry[M].London:The Royal Society of Chemistry,1989:124.
[2] Gutsche C D.Calixarenes,a Versatile Class of Macrocyclic Compounds[M].Dordrecht:Kluwer,1991:55.
[3] Iqbal M,Mangiafico T and Gutsche C D.Calixarenes 21:The conformations and structures of the products of aroylation of the,calix[4]arenes[J].Tetrahedron,1987,43(21):4917-4930.
[4] Gutsche C D,Levine J A.Calixarenes.6.Synthesis of a functionalizable calix[4]arene in a conformationally rigid cone conformation[J].Journal of the American Chemistry Society,1982,104(9):2652-2653.
[5] Koji I,Koji A,Seiji S.Conformations and structures of tetra-O-alkyl-p-tert-butylcalix [4]arenas. How is the conformation of calix[4]arenes immobilized?[J].Journal of Organic Chemistry,1991,56(16):4955-4962.
[6] Van Loon J D,Arduini A,Coppi L,et al.Selective functionalization of calix[4]arenes at the upper rim [J].Journal of Organic Chemistry,1990,55(21):5639-5646.
Syntheses and Crystal Structures of Calix[4]Arenas Derivatives
HUXiaojun,PENGYongbiao,WUHao
(Key Laboratory of Regional Environment and Eco-Remediation (Ministry of Education),Shenyang University,Shenyang 110044,China)
A novel phenomenon about calix[4]arenes was observed that there were two discrete conformational isomers observed in single crystals of tetra-O-alkylated calix[4]arenes.Four calix[4]arene derivatives(2,3,4 and 5)were synthesized with 1 as the precursor,and their single crystals were prepared to disclose reasons for this novel phenomenon.It was found that the introduced alkyl groups inhibited the oxygen-through-the-annulus rotation of phenyl rings,and there was enough space for the forth phenyl ring to randomly position in cone conformation or upside down in partial-cone conformation,leading to the coexistence of two discrete conformational isomers in single crystals of calix[4]arenes.
calix[4]arene;conformation;crystal structure;conformational isomer
O 62
A
1008-9225(2012)02-0035-05
2011-12-18
国家科技支撑计划课题(2011BAJ06B02).
胡晓钧(1977-),男,浙江淳安人,沈阳大学教授,博士后研究人员.
王 颖】

