双有机溶剂中黑曲霉脂肪酶催化阿魏酸的酯化反应*
刘焕珍,王明兹,郭英佳,郑丽妃,Guo Zheng,Xu Xuebing,陈必链
1(福建师范大学工业微生物教育部工程研究中心,福建福州,350108)2(福建师范大学生命科学学院,福建 福州,350108)3(Faculty of Science,University of Aarhus,Aarhus,Denmark)
双有机溶剂中黑曲霉脂肪酶催化阿魏酸的酯化反应*
刘焕珍1,2,王明兹1,2,郭英佳2,郑丽妃2,Guo Zheng3,Xu Xuebing3,陈必链1,2
1(福建师范大学工业微生物教育部工程研究中心,福建福州,350108)2(福建师范大学生命科学学院,福建 福州,350108)3(Faculty of Science,University of Aarhus,Aarhus,Denmark)
在双有机溶剂体系中,用黑曲霉脂肪酶催化合成阿魏酸油醇酯,考察酶浓度、温度和底物摩尔比等因素对酯化反应的影响。结果表明:在异辛烷/丁酮体系中,当反应温度为60℃,阿魏酸和油醇的摩尔比为1∶8,即阿魏酸浓度为0.39 mg/mL和油醇浓度为4.3 mg/mL,脂肪酶浓度为0.2 g/mL时,转化率为97.6%;而在环己烷/丁酮体系中,当反应温度为60℃,阿魏酸和油醇的摩尔比为1∶8,即阿魏酸浓度为0.49 mg/mL和油醇浓度为5.37 mg/mL,脂肪酶浓度为 0.25 g/mL 时,转化率为 91.0%。
脂肪酶,酯化,有机溶剂,阿魏酸,油醇
阿魏酸(ferulic acid,FA),其化学名称为4-羟基-3-甲氧基苯丙烯酸,属于酚酸的一种,具有顺式和反式两种异构体。谷物、水果、蔬菜和咖啡中富含游离态和结合态的阿魏酸[1]。阿魏酸低毒性,易被人体吸收和代谢,具有多种生理功能,包括抗氧化、抗菌、抗炎症、抗血栓和抗癌等,对冠状动脉疾病具有治疗效果,能降低胆固醇和增加精子活力,被广泛用于食品和化妆品中[2]。
由于阿魏酸的亲水特性限制了它在脂肪和油类体系中的应用,通过酯化作用,也就是将醇与阿魏酸的羧基进行酯化产生阿魏酸酯可以克服这个缺陷。酶催化阿魏酸进行酯交换反应已有研究报道,如用不同来源的脂肪酶:Novozyme 435、Candida rugosa、Chromobacterium viscosum 和 Pseudomonas sp.等催化乙烯阿魏酸与羟基类固醇和p-熊果苷进行酯交换反应[3];用Novozyme 435催化亚麻籽油与肉桂酸或阿魏酸发生酯交换反应[4];以离子液体为反应介质,采用化学催化剂和脂肪酶作为催化剂以阿魏酸为底物合成阿魏酸单甘油酯和阿魏酸双甘油酯[5]。本文作者研究了在异辛烷/丁酮双溶剂体系中,Novozym 435脂肪酶催化合成阿魏酸油醇酯[6],本文继续该研究工作,研究黑曲霉脂肪酶在异辛烷/丁酮或环己烷/丁酮溶剂体系中催化阿魏酸与油醇的酯化反应,并优化了反应条件。
1 材料与方法
1.1 药品与仪器
黑曲霉脂肪酶,深圳绿微康生物工程有限公司,酶活力为8000单位每克酶粉(水解活力);分析纯反式阿魏酸和4 Å分子,天津市光复精细化工研究所;分析纯油醇,Sigma公司;色谱纯甲醇,上海国药集团;封口膜,英国Alcan Group公司。其他试剂均为市售分析纯。
美国安捷伦1100高效液相色谱仪,瑞士Mettler Toledo电子分析天平,湘仪台式离心机,上海智诚恒温培养摇床。
1.2 方法
1.2.1 酶催化酯化反应
将一定量阿魏酸溶于丁酮,一定量油醇溶于待测溶剂,分别取前者1 mL,后者9 mL于50 mL具塞三角烧瓶中,加入一定量脂肪酶,并用封口膜将瓶口封好,置于恒温摇床上,转速为150 r/min,12 h后加一定量4 Å分子筛,每48 h取1次样,每次取100 μL。进行阿魏酸和油醇摩尔比实验时,固定阿魏酸的量,将3.9 mg或4.9 mg阿魏酸溶于1 mL的丁酮中,按一定比例增加油醇的量,即 5.4、21.5、43、64.4 mg 或6.7、26.8、53.7、80.5 mg 油醇溶于 9 mL 的异辛烷或环己烷中,使酸醇摩尔比分别为 1∶1、1∶4、1∶8、1∶12。每个实验做3次重复,实验结果取其平均值。
1.2.2 阿魏酸转化率的测定
将100 μL样品溶于900 μL甲醇中,储于 -20℃冰箱待分析。采用高效液相色谱方法分析阿魏酸油醇酯的含量,色谱柱为Hypersil ODS-C18 reversed-phase column(5 μm,250 ×4.0 mm,Agilent),上样量为20 μL,流速为1 mL/min,洗脱液:A液为95%甲醇,B液为5%水,柱温为35℃,检测器为紫外可变波长检测器。用各组分的HPLC峰面积比表征产物与底物相对含量比(n/n)。

2 结果与讨论
2.1 有机溶剂混合物的影响
阿魏酸在丁酮的溶解度较大,但丁酮是亲水性的有机溶剂,能够剥夺酶表面的必需水,使酶的构象发生改变[7],从而降低了脂肪酶的活性。因此,将疏水性的有机溶剂和丁酮组成双溶剂作为反应介质,一方面可以减少酶活的损失,另一方面又可以适当地增加阿魏酸的溶解度。本文采用正辛烷、异辛烷、正庚烷、环己烷和丁酮构成双溶剂体系,丁酮的用量为10%。不同的双有机溶剂体系对阿魏酸和油醇酯化反应的影响见图1。
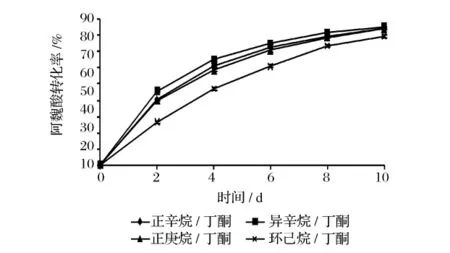
图1 不同的双有机溶剂对阿魏酸转化率的影响
由图1可知,随着反应的进行,阿魏酸转化率逐渐提高。到第10天时,在正辛烷/丁酮、异辛烷/丁酮、正庚烷/丁酮、环己烷/丁酮溶剂体系中,转化率分别为 84.0%、85.4%、84.3%、79.1%。脂肪酶的催化活性与溶剂的疏水性参数log P值间有一定的相关性,正辛烷、异辛烷、正庚烷、环己烷的log P值分别为 4.5、4.5、4.0、3.2。Lee 等人[8]研究溶剂对酶促合成对甲氧基肉桂酸辛醇酯的影响,在丙酮、叔丁醇、甲苯、正己烷、庚烷、异辛烷等几种溶剂中,发现在log P值最高的异辛烷中,对甲氧基肉桂酸的转化率最高。而熊健等的实验结果证实随着溶剂log P值的降低,转化率逐渐升高[9]。本实验还观察到在异辛烷/丁酮体系中阿魏酸的转化率较高,而在环己烷/丁酮体系中阿魏酸的溶解度较大,因此选择异辛烷或环己烷与丁酮构成双溶剂体系进行后续的研究。
2.2 酶浓度的影响
在异辛烷/丁酮体系、环己烷/丁酮体系中,酶浓度对阿魏酸酯化反应的影响分别见图2A和2B。
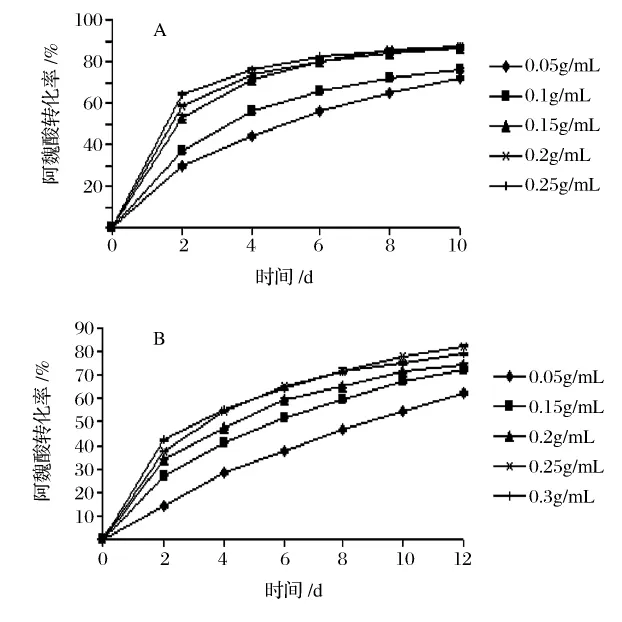
图2 在异辛烷/丁酮体系(A)和环己烷/丁酮体系(B)中酶浓度对阿魏酸转化率的影响
由图2A可知,在异辛烷/丁酮体系中,当酶浓度从0.05 g/mL升至0.2 g/mL时,阿魏酸的转化率从72.1%增至 87.1%,当脂肪酶的浓度为 0.2 g/mL时,阿魏酸的转化率最大为87.1%,因此最适酶浓度为0.2 g/mL。由图2B可知,在环己烷/丁酮体系中,当酶浓度从0.05 g/mL升至0.25 g/mL,阿魏酸的转化率从62.6%增至82.5%;再增加酶浓度至0.3 g/mL时,阿魏酸的转化率反而下降。因此脂肪酶的最适浓度为0.25 g/mL。
2.3 反应温度的影响
在异辛烷/丁酮体系、环己烷/丁酮体系中,反应温度对阿魏酸酯化反应的影响分别见图3A和3B。
由图3A可知,在异辛烷/丁酮体系中,当温度从55℃升到60℃,阿魏酸的转化率从84.0%增至88.5%;当温度升高到65℃时,阿魏酸的转化率为86.1%。因此最适温度为60℃。由图3B可知,在环己烷/丁酮体系中,当温度从50℃升到60℃,阿魏酸的转化率从64.6%增至86.5%。考虑到当温度低于50℃时阿魏酸的溶解度较低,而异辛烷的沸点为99.2℃、正己烷的沸点为80.7℃,当温度高于60℃时对酶的热稳定性和有机溶剂的发挥性都有较大的影响,因此在环己烷/丁酮体系中未选择更高的温度如65℃进行试验。Novozym 435催化酯合成反应的反应温度范围也都选择在50 ~60 °C[10]。
2.4 阿魏酸和油醇摩尔比的影响
在异辛烷/丁酮体系、环己烷/丁酮体系中,底物酸醇摩尔比对脂肪酶催化阿魏酸酯化反应的影响分别见图4A和4B。
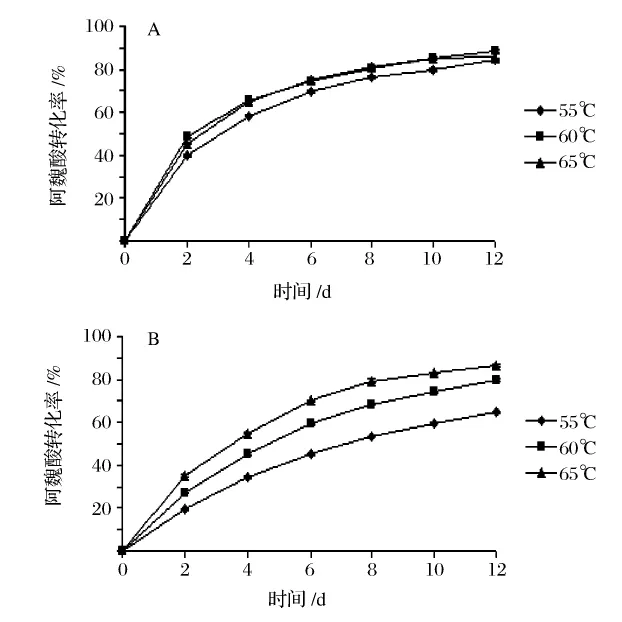
图3 在异辛烷/丁酮体系(A)和环己烷/丁酮体系(B)中反应温度对阿魏酸转化率的影响

图4 在异辛烷/丁酮体系(A)和环己烷/丁酮体系(B)中酸醇摩尔比对阿魏酸转化率的影响
由图4A可知,在异辛烷/丁酮体系中,反应12 d,阿魏酸和油醇的摩尔比为 1∶1时,转化率为24.6%;当阿魏酸和油醇的摩尔比为1∶8时,阿魏酸的转化率最大为86.1%;当酸醇摩尔比再增至1∶12时,阿魏酸的转化率略有下降为85.2%。因此酸醇最适摩尔比为1∶8。由图4B可知,在环己烷/丁酮体系中,反应12天,当阿魏酸和油醇的摩尔比为1∶1时,转化率为28.4%;酸醇摩尔比为1∶8时,阿魏酸的最大转化率为67.2%;酸醇摩尔比再增至1∶12时,阿魏酸的转化率降为64.12%。因此本实验以1∶8的酸醇摩尔比为最适底物摩尔比。
Lue[11]等人研究脂肪酶催化肉桂酸和油醇的酯化反应,以及本课题组研究在异辛烷/丁酮体系中Novozym 435脂肪酶催化阿魏酸和油醇的酯化反应[6],都未发现醇抑制酯化反应的现象。在脂肪酶催化异丁酸和正丁醇的酯化反应[12]以及丁酸和2-四氢呋喃甲醇的酯化反应时[13],过量的醇对酶都表现出抑制现象。在脂肪酶催化棕榈酸和异丙醇的酯化反应过程中,两种底物都表现底物抑制现象[14]。
2.5 优化后的反应
在异辛烷/丁酮体系、环己烷/丁酮体系中优化后的反应见图5。

图5 优化后的阿魏酸酯化反应
在异辛烷/丁酮体系中,得出优化后的反应条件为:异辛烷9 mL,丁酮1 mL,反应温度为60℃,阿魏酸和油醇的摩尔比为1∶8,阿魏酸0.39 mg/mL,油醇4.3 mg/mL,分子筛 5 mg/mL,黑曲霉脂肪酶 0.2 g/mL,摇床转速为150 r/min。反应8 d就基本达到平衡,阿魏酸的转化率为95.5%,反应12 d时转化率达到最大值为97.6%。在环己烷/丁酮体系中,得出优化后的反应条件为:环己烷9 mL,丁酮1 mL,反应温度为60℃,阿魏酸和油醇的摩尔比为1∶8,阿魏酸0.49 mg/mL,油醇 5.37 mg/mL,分子筛 5 mg/mL,黑曲霉脂肪酶0.25 g/mL,摇床转速为150 r/min,反应12天时转化率达到最大值为91.0%。
3 结论
在双有机溶剂体系中,建立了黑曲霉脂肪酶催化阿魏酸和油醇合成阿魏酸油醇酯的反应体系。考察了酶浓度、反应温度和底物摩尔比等因素对阿魏酸酯化反应的影响。在异辛烷/丁酮双有机溶剂体系中,脂肪酶的浓度和底物酸醇摩尔比对阿魏酸转化率的影响较大,反应温度对阿魏酸转化率的影响较小,在最优的反应条件下阿魏酸的转化率可达97.6%。在环己烷/丁酮双有机溶剂体系中,温度、脂肪酶浓度和底物酸醇摩尔比对阿魏酸转化率的影响较大,在最优的反应条件下阿魏酸的转化率可达91.0%。
[1] Zhao Z,Moghadasian M H.Chemistry,natural sources,dietary intake and pharmacokinetic properties of ferulic acid:A review [J].Food Chemistry,2008,109:691-702.
[2] Ou S,Kwok K C.Ferulic acid:pharmaceutical functions,preparation and applications in foods[J].Journal of the Science Food and Agriculture,2004,84:1 261-1 269.
[3] Chigorimbo-Murefu NTL,Riva S,Burton SG.Lipase-catalysed synthesis of esters of ferulic acid with natural compounds and evaluation of their antioxidant properties[J].Journal of Molecular Catalysis B:Enzymatic,2009,56(1):277-282.
[4] Choo W S,Birch E J,Stewart I.Radical scavenging activity of lipophilized products from transesterification of flaxseed oil with cinnamic acid or ferulic acid [J].Lipids,2009,44:807-815.
[5] Sun S,Yang G,Bi Y et al.Chemoenzymatic synthesis of feruloylated monoacyl-and diacyl-glycerols in ionic liquids[J].Biotechnology Letters,2009,31:1 885-1 889.
[6] 郑丽妃,刘焕珍,Guo Z,等.有机相中脂肪酶催化阿魏酸油醇酯合成的研究[J].食品工业科技,2009,30(4):285-289.
[7] Li X F,Lou W Y,Smith TJ et al.Efficient regioselective acylation of 1-β-d-arabinofuranosylcytosine catalyzed by lipase in ionic liquid containing systems[J].Green Chemistry,2006,8(6):538-544.
[8] Lee G S,Widjaja A,Ju Y H.Enzymatic synthesis of cinnamic acid derivatives[J].Biotechnology Letters,2006,28(8):581-585.
[9] 熊健,季峥,吴坚平,等.有机介质中脂肪酶催化转酯化反应拆分苯乙氰醇的研究[J].生物加工过程,2005,3(3):33-37.
[10] Katsoura M,H Polydera A.C,Katapodis P,et al.Effect of different reaction parameters on the lipase-catalyzed selective acylation of polyhydroxylated natural compounds in ionic liquids[J].Process Biochem,2007,42:1 326-1 334.
[11] Lue B M,Karboune S,Yeboah F K,et al.Lipase-catalyzed esterification of cinnamic acid and oleyl alcohol in organic solvent media[J].Journal of Chemical Technology& Biotechnology,2005,80(4):462-468.
[12] Yadav G D,Lathi P S.Kinetics and mechanism of synthesis of butyl isobutyrate over immobilised lipases [J].Biochemical Engineering Journal,2003,16(3):245-252.
[13] Yadav G D,Devi K M.Immobilized lipase-catalysed esterification and transesterification reactions in non-aqueous media for the synthesis of tetrahydrofurfuryl butyrate:comparison and kinetic modeling[J].Chemical Engineering Science,2004,59(2):373-383.
[14] Garcia T,Sanchez N,Martinez M et al.Enzymatic synthesis of fatty esters:Part I.kinetic approach[J].Enzyme and Microbial Technology,1999,25(7):584-590.
Esterification of Ferulic Acid by Aspergillus niger Lipase Catalysis in Binary Organic Solvents System
Liu Huan-zhen1,2,Wang Ming-zi1,2,Guo Ying-jia2,Zheng Li-fei2,Guo Zheng3,Xu Xue-bing3,Chen Bi-lian1,2
1(Engineering Research Center of Industrial Microbiology,Ministry of Education,Fujian Normal University,Fuzhou 350108,China)2(College of Life Sciences,Fujian Normal University,Fuzhou 350108,China)3(Faculty of Science,University of Aarhus,Aarhus,Denmark)
In binary organic solvents system,the esterification between ferulic acid and oleyl alchol was investigated,catalyzed by the native Aspergillus niger lipase.The effective factors,such as lipase concentration,temperature and the molar ratio of ferulic acid to oleyl alchol on the esterification were studied.The results indicated that in the isooctane/2-butanone solvents system,under the reaction conditions of Aspergillus niger lipase concentration 0.2 g/mL,temperature 60 ℃,the molar ratio of ferulic acid to oleyl alchol 1∶8,substrate concentration of ferulic acid 0.39 mg/mL,and oleyl alcohol 4.3 mg/mL,the conversion rate of esterification was 97.6%.Under the optimal condition in the cyclohexane/2-butanone solvents system which was:Aspergillus niger lipase concentration 0.25 g/mL,temperature 60 ℃,the molar ratio of ferulic acid to oleyl alchol 1∶8,the substrate concentrations of ferulic acid at 0.49 mg/mL and oleyl alcohol at 5.37 mg/mL,the conversion rate of esterification was 91.0% .
lipase,esterification,organic solvent,ferulic acid,oleyl alcohol
硕士(陈必链为通讯作者,Email:chenbil@fjnu.edu.cn)
*福建省科技厅重点项目(2007I0039,2008I0047),教育部留学回国人员科研启动基金资助课题
2010-08-13,改回日期:2011-02-21

