粪便Alu序列的检测在胰腺癌诊断中的价值
任艳 高军 王小玮 刘建强 顾俊骏 金晶 龚燕芳 李兆申
·论著·
粪便Alu序列的检测在胰腺癌诊断中的价值
任艳 高军 王小玮 刘建强 顾俊骏 金晶 龚燕芳 李兆申
目的检测胰腺癌患者粪便Alu序列表达量,探讨其对胰腺癌的诊断价值。方法收集41例胰腺癌、27例慢性胰腺炎及23例健康者的粪便样本,采用酚-氯仿方法抽提粪便中基因组DNA,应用实时定量PCR方法检测Alu重复序列的表达量。结果胰腺癌、慢性胰腺炎、正常健康者粪便Alu重复序列表达量分别为(5.17±0.99)、(3.79±0.94)、(0.28±0.35)ng/g,三组间差异有统计学意义(P值均<0.05)。通过接受者操作特征(ROC)曲线分析,胰腺癌的曲线下面积为74.8%,95%可信度为0.661~0.835,诊断胰腺癌的敏感性为75.6%,特异性为67.1%。结论胰腺癌患者粪便Alu序列表达量显著增加,对胰腺癌的诊断可能有一定价值。
胰腺肿瘤; Alu序列; 诊断; 实时定量PCR; 粪便
Alu重复序列是人类基因组中一族散布的、长度大约为300 bp的中等重复序列。它是短分散重复序列(short interspersed elements,SINEs,≤500 bp)中最大的一个家族,约占基因组的5%~10%,以平均间隔4 kb随机分散于整个基因组中。Alu序列插入到功能重要的基因区或其他Alu依赖性的基因功能改变区会导致多种遗传性疾病,并且可能和肿瘤的发生相关[1]。本研究旨在观察Alu序列表达与胰腺癌发生、发展的关系,探讨其临床意义。
材料与方法
一、研究对象
选取长海医院2007年9月至2010年5月住院患者68例,其中胰腺癌患者41例,慢性胰腺炎患者27例。以正常健康者23例作为对照。患者的一般情况见表1。
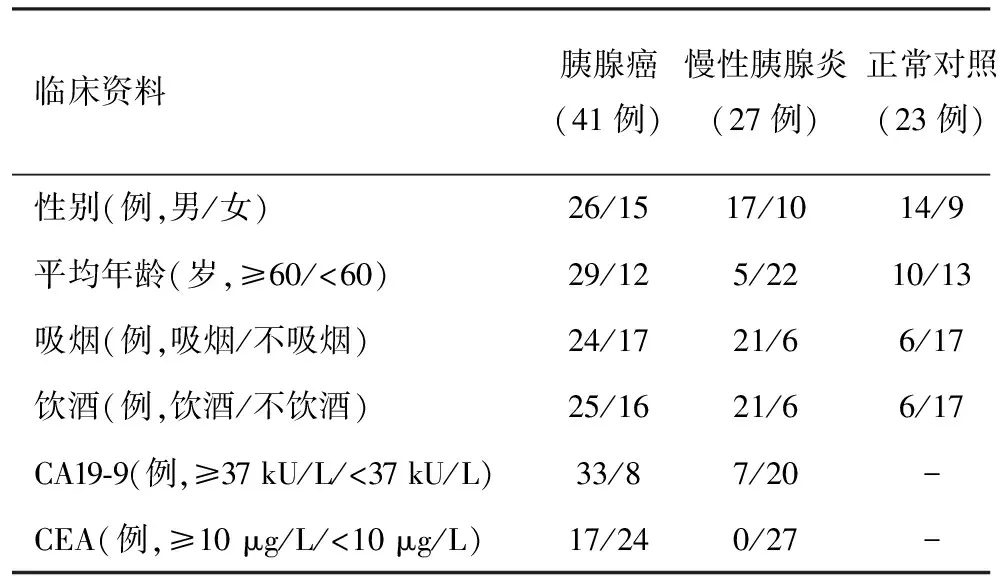
表1 各组的一般临床资料
二、粪便收集方法及DNA提取
标本收集于冻存管后即置于冰盒中,在6 h内转移至-80℃冰箱保存。从冻存管中称取200 mg粪便,先加入淀粉及TEN预处理,采用酚-氯仿方法抽提DNA,再采用qiagen纯化试剂盒纯化DNA。使用NanoDrop (ND-1000, USA) 进行DNA浓度检测和纯度鉴定,置-80℃保存。
三、实时PCR
Alu序列包括保守区域及可变区域,设计的PCR引物应完全或部分位于保守区域(至少是3′端引物,图1)。Alu上游引物:5′-ACGCCTGTAATCCCAGCACTT-3′;下游引物:5′-TCGCCCAGGCTGGAGTGCA-3′,扩增片段245 bp。粪便DNA以1∶5的比例稀释,取1 μl加入包含SYBR GREEN Supermix的25 μl反应体系。PCR反应条件:95℃ 3 min,95℃ 30 s、60℃ 30 s、72℃ 40 s,25个循环。选取30例正常粪便DNA进行混合,作为参照。
阳性标本的PCR扩增曲线呈典型的S型曲线,阴性对照是一条不规则的波浪线。Ct为循环阈值,△Ct=Ct样品- Ct内参,△△Ct=△Ct-(Ct阴性样品-Ct阴性内参),样品中目的基因初始cDNA相对表达量以2-△△Ct表示。
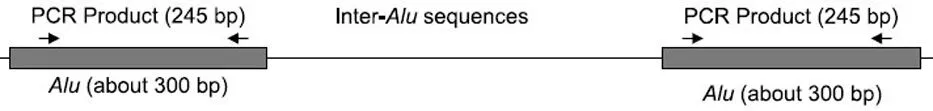
图1 PCR引物设计图
四、统计学处理
结 果
一、RT-PCR标准曲线
制作标准曲线时DNA样本以10倍体积倍比稀释,DNA量分别为2.5 ng,250 pg,25 pg,2.5 pg,250 fg,25 fg。标准曲线样品的PCR扩增曲线见图2a,标准曲线见图2b。

图2 标准样品的PCR扩增曲线(a)及标准曲线(b)
二、粪便Alu序列的表达
粪便Alu的扩增曲线及溶解曲线见图3。溶解曲线只有单峰,可排除非特异性扩增。胰腺癌患者Alu序列表达量为(5.17±0.99)ng/g,慢性胰腺炎、正常对照者的表达量分别为(3.79±0.94)、(0.28±0.35)ng/g,3组间差异有统计学意义(P值均<0.05)。通过接受者操作特征(ROC)曲线分析,胰腺癌、慢性胰腺炎和正常对照人群之间有显著差异,胰腺癌的曲线下面积(AUC)为74.8%,95%可信度为0.661~0.835,诊断胰腺癌的敏感性为75.6%,特异性为67.1%。
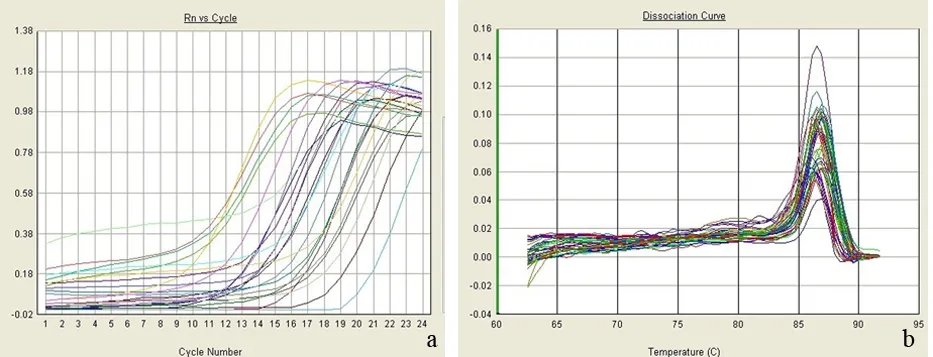
图3 粪便样品的PCR扩增曲线(a)及溶解曲线(b)
Alu序列在人类基因组中普遍存在,但未见于其他非灵长类物种[2]。目前的研究表明,Alu序列与某些恶性肿瘤的发生密切相关。Rohlfs等[3]用Southern杂交等方法对两个乳腺癌及卵巢癌家族进行研究,结果显示Alu介导的同源重组可导致BRCAl基因外显子8、9间出现5 kb的缺失,认为这种缺失和复制是导致家族性乳腺癌和卵巢癌的重要因素。Tournier等[4]报道,Alu介导的同源重组可导致BRCA2基因外显子8与外显子9的缺失。Ichimura等[5]采用相同的方法对神经胶质瘤进行研究,结果显示Alu介导的同源重组可导致神经胶质瘤特异性基因p107的缺失。Wang等[6]检测108例遗传性非息肉性结直肠癌(HNPCC)的MLHl、MSH2、MSH6等错配修复基因的突变,结果显示38%的患者存在MLHl和MSH2的点突变,19例患者出现基因缺失,其中42%发生在MLHl,58%发生在MSH2,而这些基因突变都是由Alu介导的同源重组所导致的。Hsieh等[7]在Hep3B肝癌细胞株中分离出了一个异常的CAD基因转录产物,它的外显子3被截短的转座Alu序列所代替,从而认为肝癌的发生与Alu介导的基因突变有关。Strout等[8]报道,急性髓样白血病(AML)的发生与染色体导致的基因融合有关,而部分串联重复又是其中重要的机制,通过对9例AML患者的基因融合的DNA序列进行检测,发现部分串联重复总是由Alu介导的同源重组产生。
然而,最近的两个多中心的实验研究表明,有关粪便Alu表达的研究非常少,源于粪便标本的收集及储存可能导致样本降解,并且抽提方法仍不成熟。本研究采用qiagen试剂盒提供的抽提方法并予以改良,结果表明DNA抽提结果稳定。这一无创性检查方法具有标本易采取、操作简便易行等优点,为下一步实验提供基础。我们采用实时定量PCR方法的检测范围从250 fg到2.5 ng范围。本结果显示,胰腺癌患者粪便中Alu序列表达量显著高于慢性胰腺炎及正常对照者,提示检测胰腺癌Alu序列的表达量对胰腺癌的诊断可能有一定的价值。
[1] Schmid CW. Alu: structure, origin, evolution, significance and function of one-tenth of human DNA. Prog Nucleic Acid Res Mol Biol, 1996,53:283-319.
[2] Shih C,Weinberg RA. Isolation of a transforming sequence from a human bladder carcinoma cell line. Cell, 1982,29:161-169.
[3] Rohlfs EM,Puget N,Graham ML,et al. An Alu-mediated 7.1 kb deletion of BRCA1 exons 8 and 9 in breast and ovarian cancer families that results in alternative splicing of exon 10. Genes Chromosomes Cancer, 2000,28:300-307.
[4] Tournier I, Paillerets BB,Sobol H,et al.Significant contribution of germline BRCA2 rearrangements in male breast cancer families. Cancer Res,2004,64:8143-8147.
[5] Ichimura K, Hanafusa H,Takimoto H,et al.Structure of the human retinoblastoma-related p107 gene and its intragenic deletion in a B-cell lymphoma cell line. Gene,2000,251:37-43.
[6] Wang Y,Friedl W,Lamberti C, et al.Hereditary nonpolyposis colorectal cancer: frequent occurrence of large genomic deletions in MSH2 and MLH1 genes. Int J Cancer,2003,103:636-641.
[7] Hsieh SY,Liaw SF,Lee SN, et al.Aberrant caspase-activated DNase (CAD) transcripts in human hepatoma cells. Br J Cancer, 2003,88:210-216.
[8] Strout MP,Marcucci G,Bloomfield CD,et al.The partial tandem duplication of ALL1 (MLL) is consistently generated by Alu-mediated homologous recombination in acute myeloid leukemia. Proc Natl Acad Sci USA,1998,95:2390-2395.
2011-01-14)
(本文编辑:屠振兴)
ValueofdetectionoffecalAlurepetitivesequencesinthediagnosisofpancreaticcancer
RENYan,GAOJun,WANGXiao-wei,LIUJian-qiang,GUJun-jun,JINJing,GONGYan-fang,LIZhao-shen.
DepartmentofGastroenterology,ChanghaiHospital,SecondMilitaryMedicalUniversity,Shanghai200433,China
LIZhao-shen,Email:lizhaoshen111@gmail.com
ObjectiveTo detect the Alu expression in the stool of patients with pancreatic cancer and investigate its value in the diagnosis of pancreatic cancer.MethodsStool samples were obtained from patients with pancreatic cancer (PC) (n=41), chronic pancreatitis (CP) (n=27) and healthy subjects (n=23), the DNA was extracted from the stool and the expression of Alu repetitive sequences was subjected to quantitative analysis by the real-time PCR.ResultsThe expressions of Alu repetitive sequences in PC, CP, and healthy subjects were (5.17±0.99), (3.79±0.94), (0.28±0.35) ng/g, and the difference among the three groups was statistically significant (P<0.05). The AUC of PC was 74.8% with the 95%CI0.661~0.835, and the sensitivity, specificity was 75.6% and 67.1%, respectively.ConclusionsAlu repetitive sequences are highly expressed in the stool of patients with pancreatic cancer, and it is of value in the diagnosis of pancreatic cancer.
Pancreatic neoplasms; Alu repeats; Diagnosis; Real-time PCR; Feces
10.3760/cma.j.issn.1674-1935.2011.06.001
国家科技支撑计划(2006BAI02A12)
200433 上海,第二军医大学长海医院消化内科
李兆申,Email:lizhaoshen111@gmail.com

