气相色谱分析多糖衍生化方法的研究与比较
白娣斯,张 静
(陕西师范大学食品工程与营养科学学院,陕西西安710062)
气相色谱分析多糖衍生化方法的研究与比较
白娣斯,张 静*
(陕西师范大学食品工程与营养科学学院,陕西西安710062)
采用糖腈衍生化和糖醇衍生化两种方法分析多糖组分,找出线性关系,计算摩尔比,测定加样回收率、精密度、重复性等。糖醇衍生化中,果糖经过还原可得到山梨醇和甘露醇的混合物,测定结果容易导致色谱峰的混乱,不易定性分析,并且衍生化方法反应时间较长,操作比较麻烦。糖腈乙酸酯衍生物气相色谱法具有衍生物制备简便、试剂易得等优点,并且每种糖都能得到单一的色谱峰。通过对气相色谱糖腈衍生化法和糖醇衍生化法的研究和比较,表明糖腈衍生化方法是气相色谱研究食品多糖较为合适的衍生化方法。
多糖,气相色谱,糖腈乙酰酯衍生法,糖醇醋酸盐衍生法
近年来,人们致力于研究多糖的生理活性和它的化学结构方面的关系,从更深层次探讨多糖的作用机制。有关多糖立体构型的改变、分子量变化、重复结构单位主侧链的类型以及主侧链分子比例、降解或引进基团等因素对多糖生理活性影响的研究己有相关报道[1-3]。气相色谱是多糖结构分析中最重要的手段之一,测定糖类具有选择性好、样品用量少、分辨率强、灵敏度高、分析速度快以及可用于定性及定量分析等优点[4]。气相色谱要求试样具有良好的挥发性和热稳定性。中药多糖为生物大分子物质,由于含大量羟基不能在高温下直接挥发,不适用于气相色谱,因而在研究中药多糖中需要将大分子多糖降解为单糖或寡糖,并且将其衍生成易挥发,且热稳定的衍生物。本实验研究了两种衍生化方法,通过对多糖的定性定量分析以及重复性、回收率的测定,比较这两种衍生化方法的优劣,从而建立一种较好的适用于中药多糖的气相色谱衍生化方法。
1 材料与方法
1.1 材料与仪器
样品 南瓜皮粗多糖APP以及用CTAB法分离得到的南瓜皮多糖APP1和APP2;D-果糖 Shanghai Green Rird Technology Devel.Ltd.;D-半乳糖 上海恒信化学试剂有限公司;D-甘露糖、D-木糖 中国医药(集团)上海化学试剂公司;D-核糖 北京鼎国生物技术发展中心;葡萄糖 天津市科密欧化学试剂开发中心;吡啶、盐酸羟胺、硼氢化钠、乙酸、三氟乙酸等试剂 均为分析纯。
TDL80-2B飞鸽牌系列离心机 上海安婷科学仪器厂制造;Trace GC气相色谱仪 美国菲尼根;RE-52AA旋转蒸发器,ACQ-600超声波发生器,LXJ -ⅡB型低速大容量多管离心机,Christ ALPH1-4真空冷冻干燥机。
1.2 标准单糖糖腈衍生化[5]
准确称取各种标准单糖10mg,分别加入10mg的盐酸羟胺,用0.5mL的吡啶溶解后封管,在90℃水浴中反应30min,冷却至室温加入0.5mL无水醋酸酐封管后于90℃水浴中反应30min,反应物直接进行气相色谱分析。
1.3 标准单糖糖醇衍生化[5]
准确称取各种标准单糖10mg,加入30mg硼氢化钠,加入2mL水振荡后,在室温下放置至少1.5h,使糖还原成相应的糖醇,滴入醋酸分解过量的硼氢化钠,至无气泡产生为止。溶液在60℃下减压浓缩至干,加入0.1%(V/V)盐酸甲醇溶液2mL,振荡后加压蒸发至干,重复四次以除去硼酸根,剩余物在105℃烘箱中加热15min除去水分。加入0.5mL吡啶和0.5mL醋酸酐,封管后在沸水浴中反应1h,反应物进行气相色谱分析。
1.4 标准曲线
1.4.1 糖腈衍生化法标准曲线 准确称取500mg肌醇六乙酰酯,用无水吡啶溶解并定容于50mL容量瓶中作为内标。精确称取各标准单糖阿拉伯糖、鼠李糖、核糖、木糖、甘露糖、半乳糖、葡萄糖各10、15、20、25、30mg,用无水吡啶溶解并定容于5mL容量瓶中,分别吸取各标准单糖0.6mL于具塞试管中,分别加入内标溶液0.1mL和10mg的盐酸羟胺,各管以无水吡啶补至1.0mL,溶解后封管,在90℃水浴中反应30min,冷却至室温加入0.5mL无水醋酸酐封管后于90℃水浴中反应30min进行乙酰化,冷却后用氯仿萃取3次,合并氯仿层,减压抽干后加入1mL氯仿溶解进行气相色谱分析。以每种单糖进样前浓度为横坐标,单糖与内标的峰面积比为纵坐标作线性回归,计算出回归方程与相关系数。
1.4.2 糖醇衍生化法标准曲线 准确称取500mg肌醇六乙酰酯,用无水吡啶溶解并定容于50mL容量瓶中作为内标。精确称取各标准单糖阿拉伯糖、鼠李糖、核糖、木糖、甘露糖、半乳糖、葡萄糖各10、15、20、25、30mg,用蒸馏水溶解并定容于5mL容量瓶中,分别吸取各标准单糖0.6mL于具塞试管中,分别加入3.6、5.4、7.2、9.0、10.8mg NaBH4还原,加入1.4mL蒸馏水,使其体积均为2mL。在室温下放置至少1.5h,使糖还原成相应的糖醇,滴入醋酸分解过量的硼氢化钠,至无气泡产生为止。溶液在60℃下减压浓缩至干,加入甲醇2mL,振荡后加压蒸发至干,重复四次以除去硼酸根,剩余物在105℃烘箱中加热15min除去水分。加入0.5mL吡啶和0.5mL醋酸酐,封管后在沸水浴中反应1h,反应物进行气相色谱分析。以每种单糖进样前浓度为横坐标,单糖与内标的峰面积比为纵坐标作线性回归,计算出回归方程与相关系数。
1.5 肌醇六乙酰酯的制备
称取3g肌醇,加入4.5g盐酸羟胺、45mL醋酸酐和3mL吡啶,在90℃水浴中加热2h,并不断搅拌,将反应液冷却至室温后倒入50mL冰水中,使肌醇六乙酰酯析出,过滤后加20mL水洗涤,将压干后产物放入100℃烘箱中烘干备用。气相色谱检测肌醇六乙酰酯为单峰。
1.6 气相色谱条件
OV-17毛细管柱;FID检测器;升温程序:150℃(7℃/min)→190℃(15℃/min)→250℃;进样口温度280℃;检测器温度260℃;Air:H2∶N2=300∶30,载气流速10mL/min;进样量0.1μL。
1.7 多糖组分的定性分析
1.7.1 多糖的完全酸水解 取南瓜皮多糖5mg,置于安培管中,加入0.4mL蒸馏水溶解,再加入等体积的4mol/L三氟乙酸,封管,置于110℃水解3h,将水解液减压蒸干,加入1.5mL甲醇溶解,再减压蒸干,重复三次以除尽残余的三氟乙酸,得到水解后的南瓜皮多糖。
1.7.2 多糖糖腈乙酸酯衍生物的制备 将水解后的多糖加入10mg的盐酸羟胺,用0.5mL的吡啶溶解后封管,在90℃水浴中反应30min,冷却至室温加入0.5mL无水醋酸酐封管后于90℃水浴中反应30min,冷却后用氯仿萃取3次,合并氯仿层,减压抽干后加入1mL氯仿溶解进行气相色谱分析。
1.7.3 多糖糖醇醋酸盐衍生物的制备 多糖水解后,用NaBH4(15mg)还原,加入2mL蒸馏水振荡后,在室温下放置至少1.5h,使糖还原成相应的糖醇,滴入醋酸分解过量的硼氢化钠,至无气泡产生为止。溶液在60℃下减压浓缩至干,加入甲醇2mL,振荡后加压蒸发至干,重复四次以除去硼酸根,剩余物在105℃烘箱中加热15min除去水分。加入0.5mL吡啶和0.5mL醋酸酐,封管后在沸水浴中反应1h,反应物进行气相色谱分析。
1.8 多糖组成的定量分析
1.8.1 多糖的衍生化 准确称取水解后的南瓜皮多糖10mg,加入4mg的肌醇六乙酰酯作为内标物,然后分别按照两种衍生化方法制备多糖衍生物。
1.9 多糖中单糖摩尔比的计算
根据各单糖的标准曲线计算出多糖中单糖的含量,各单糖的摩尔数:
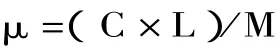
式中:C为测得的单糖的浓度,L为进样前的体积,M为该单糖的分子量。
2 结果与讨论
2.1 标准单糖衍生化方法比较
采用糖腈衍生化和糖醇衍生化两种衍生化方法进行对比,通过气相色谱对七种单糖标品的混标进行定性分析。
图1为混合标准单糖糖腈化衍生物的气相色谱图,采用这种方法衍生化后,各种单糖能完全在石英毛细管柱中很好的分离,几乎无杂峰产生,且这种衍生化方法制备简单,能够有效克服由于糖的异构化而造成的多峰现象,每种糖都能得到单一的色谱峰,有利于进行气相色谱的定性和定量分析。
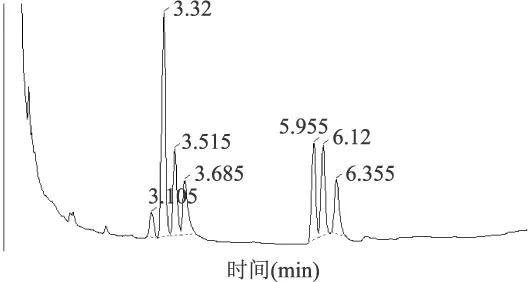
图1 混合标准单糖的糖腈乙酰酯衍生物的气相色谱图
如图2所示,采用糖醇乙酰化法研究混合标准单糖时,糖醇乙酰化衍生物在色谱柱中没有有效的分离,经过多次实验,在气相色谱图中果糖出现两个峰,葡萄糖和半乳糖的保留时间重合,在实验中很难根据标准单糖的色谱峰作定性的对照。
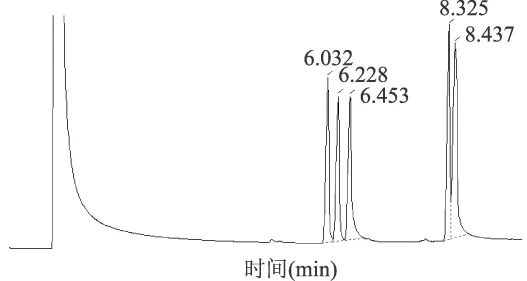
图2 混合标准单糖的糖醇醋酸盐衍生法的气相色谱图
2.2 南瓜多糖中单糖组成的定性分析结果
本实验采用糖腈衍生化方法完成了7种单糖(阿拉伯糖、鼠李糖、葡萄糖和半乳糖、果糖、木糖、苷露糖)在毛细管柱中的分离,南瓜多糖中单糖种类的定性采用与标准单糖的色谱保留时间相对照的方法。
2.3 南瓜多糖中单糖组成的定量分析结果
南瓜多糖中各种单糖组成的定量采用糖腈衍生化方法依照1.4.1中所作标准曲线的回归方程求得,回归方程和相关系数如表1所示。

表1 标准单糖测定的线性回归方程和相关系数
由回归方程求出南瓜皮多糖APP、APP1、APP2中各种单糖的含量、摩尔数及摩尔比如表2所示。采用糖腈衍生化方法测定南瓜皮粗多糖APP由鼠李糖、阿拉伯糖、葡萄糖和半乳糖组成,摩尔比为0.3256∶0.1936∶0.3150∶0.3529;用CTAB法得到的APP1由鼠李糖、果糖、葡萄糖和半乳糖组成,摩尔比为0.5934∶0.7194∶0.2612:0.3312;以及 APP2由鼠李糖、阿拉伯糖、葡萄糖和半乳糖组成,摩尔比依次为0.3667∶0.1824∶0.1891∶0.3638。实验结果表明,糖腈衍生化既能确定多糖的组成,也能确定多糖的摩尔比;而糖醇衍生化则不能确定多糖的组成及摩尔比,因此糖腈衍生化为较好方法。
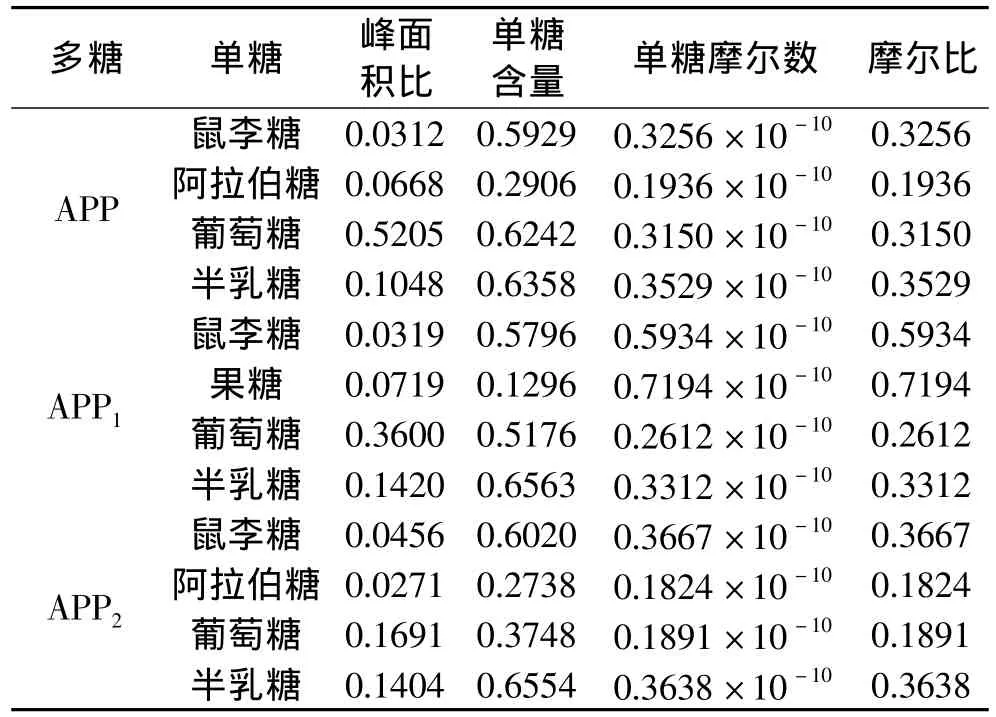
表2 南瓜多糖组分分析结果
2.4 南瓜多糖加样回收率的测定和精密度实验
在多糖样品中定量加入标准单糖,采用糖腈衍生化方法操作后测定回收率,样品进行了重复(6次)实验,计算6次平行测定的相对标准偏差(RSD)和回收率,结果见表3。从表中可以看出,用糖腈衍生化方法测定回收率较高,重复性较好,而糖醇衍生化不能准确定量,较糖腈衍生化差。
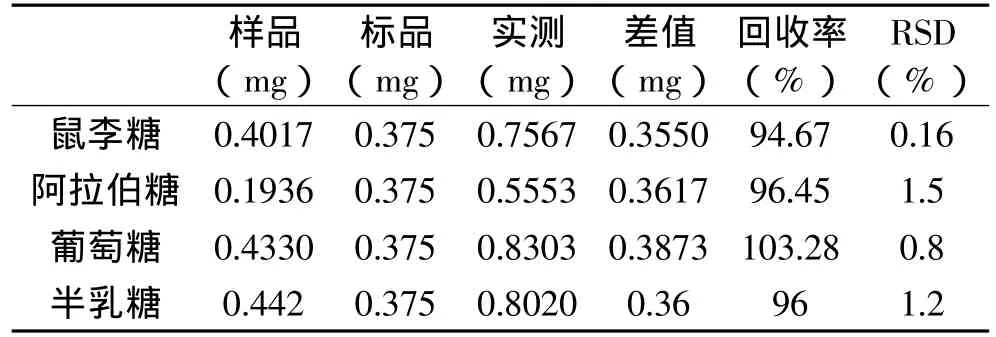
表3 方法的精密度和回收率(n=6)
3 结论
3.1 制备糖醇乙酸酯衍生物时,果糖经过还原可得到山梨醇和甘露醇的混合物,测定结果容易导致色谱峰的混乱,不易定性分析,并且衍生化方法反应时间较长,操作比较麻烦。
3.2 糖腈乙酸酯衍生物气相色谱法具有衍生物制备简便、试剂易得等优点,并且每种单糖都能得到单一的色谱峰。
3.3 采用糖腈衍生化方法对南瓜多糖APP、APP1、APP2中各种单糖的组成进行定性和定量分析,结果表明,采用糖腈衍生化方法可准确地得到南瓜多糖的单糖组成及单糖的含量、摩尔分数以及摩尔比,而糖醇衍生化方法则不能,因此,糖腈衍生化方法是用气相色谱研究食品多糖的较为合适的衍生化方法。
[1]杨怀谨.多糖研究进展[J].中国中医药信息杂志,2003,9(10):70-71.
[2] Schepetkinia, Quinnmt. Botanical, polysacchsrides:macrophage immunomodulation and the therapeutic potentiallntemational[J].Immunopharmacology,2006(6):317-333.
[3]Wangjy,Kasperdl,Tzianabos A.Biological chemistry of immunomodulation by zwitterionic polysaceharides[ J]. Carbohydrate Research,2003,338:2531.
[4]陶乐平,丁在富,张部昌.气相色谱在多糖结构测定中的应用[J].色谱,1994,5(12):1-7.
[5]张惟杰.糖复合物生化研究技术[M].浙江大学出版社,2006:38-40.
Study and comparison of two derivatization methods of polysaccharides by GC
BAI Di-si,ZHANG Jing*
(Department of Food Engineering and Nutrient Science,Shaanxi Normal University,Xi’an 710062,China)
Two methods of derivatization:glyc-nitrile derivatization and furfury alcohol derivatization in gas chromatography(GC)were used to analyze the composition of the polysaccharides,find the linear correlation,calculate the molar ratio and determine recovery of the sample,precision and the repeatability.ln the method of furfury alcohol derivatization,fructose was deoxidized to the mixture of sorbitol and mannitol,and the results could cause the chaos of the chromatographic peaks,made it hard to determine the amounts of the components of the polysaccharides,meanwhile,the reaction of derivatization lasted a long time,manipulation was also troublesome. While using glyc-nitrile derivatization to prepare the derivative,its manipulation was easier,and the reagent was easy to get,every monosaccharide got a single peak.From the study and comparison of the two methods of derivatization,we can see that the method of glyc-nitrile derivatization is the more suitable derivatization method.
polysaccharides;GC;glyc-nitrile derivatization;furfury alcohol derivatization
TS201.2+3
A
1002-0306(2011)02-0322-04
2009-10-12 *通讯联系人
白娣斯,女,硕士研究生,主要从事天然产物有效成分的化学研究。
国家自然科学基金(10874108);陕西省自然科学基础研究计划(SJ08A16)。

