添加甘氨酸对天冬醇胺/葡萄糖模拟体系中丙烯醇胺形成的抑制作用
刘 洁,张海霞,胡小松,陈 芳,*
(1.河南工业大学粮油食品学院,河南郑州450052;2.中国农业大学食品科学与营养工程学院,北京100083)
添加甘氨酸对天冬醇胺/葡萄糖模拟体系中丙烯醇胺形成的抑制作用
刘 洁1,张海霞2,胡小松2,陈 芳2,*
(1.河南工业大学粮油食品学院,河南郑州450052;2.中国农业大学食品科学与营养工程学院,北京100083)
美拉德反应目前被认为是形成丙烯酰胺的重要途径,极探讨了甘氨酸在葡萄糖/天冬酰胺模拟体系中抑制丙烯酰胺形成的规律。模拟体系分别在90、100、110、120℃下反应4h,丙烯酰胺的生成、褐变度的增加、产物的减少以及对天冬酰胺和甘氨酸降解动力学的分析表明,甘氨酸的添加能够显著降低美拉德反应生成的丙烯酰胺,且在该反应体系中甘氨酸与天冬酰胺之间存在竞争关系。
丙烯酰胺,甘氨酸,美拉德反应,模拟体系
食品安全关系到人类健康、国家安危以及社会发展。近年来,食品中有毒有害残留和污染物逐渐受到关注,尤其是食品加工过程中产生的有害物成为世界各国的研究热点。2002年4月,由瑞典国家食物管理局和斯德哥尔摩大学联合宣称,在食品中含有对人体具有潜在致癌性的丙烯酰胺,尤其是以薯条为代表的富含碳水化合物的高温油炸食品中含量最为丰富[1]。这一结论立即引起世界卫生组织、联合国粮农组织以及世界各国食品界的广泛关注,在2002年4月的《Nature》杂志连续刊登了两篇关于丙烯酰胺形成机制的文章,并认为加热条件下发生Maillard反应是导致丙烯酰胺的主要途径[2-3]。许多研究都证实食品加工过程中添加甘氨酸对丙烯酰胺有抑制作用[4-6],因此本文建立了天冬酰胺/葡萄糖/甘氨酸的模拟体系,研究在不同温度和时间下进行加热,甘氨酸对丙烯酰胺形成的具体影响。
1 材料与方法
1.1 材料与仪器
丙烯酰胺(AA)标准品(>99.9%) Sigma公司;甲醇 色谱纯,美国Fisher公司;D-葡萄糖(Glc)分析纯,北京化学试剂公司;L-天冬酰胺(Asn)北京科吴达生物技术发展有限公司;L-甘氨酸(Gly)美国Amresco公司。
高效液相色谱(HPLC)系统K-1001型输液泵、K-1500溶剂混合器、K-2501型可变波长紫外检测器 德国Knaur公司;AT-150型柱温箱 奥德赛斯公司;868型酸度计 美国奥立龙公司;EY-300A分析天平 日本松下电器;HH-1智能型数显恒温油浴槽 金坛市正基仪器有限公司;T6新世纪紫外可见分光光度计 北京普析通用仪器有限公司;2000D型超纯水器 北京长风仪器仪表公司。
1.2 实验方法
1.2.1 Asn/Glc/Gly模拟体系的建立 准确量取1mL Glc溶液(0.5mol/L)、1mL Asn溶液(0.5mol/L)和1mL Gly溶液(5%)置于20mL的具塞刻度试管中,然后用0.2mol/L的磷酸缓冲液(pH=7.5)补充到8mL,振荡均匀,加入沸石,加上自制冷凝装置。将试管置于油浴锅中,分别于90、100、110、120℃下反应4h,每隔0.5h取样。每个实验做3次重复。
1.2.2 还原糖的测定方法 采用HPLC法测定还原糖含量。色谱柱为 Waters Sugar park-I(6.5×300mm,5μm),柱温90℃,流动相为50mg/L乙二胺四乙酸二钠盐水溶液,流速为0.5mL/min,RI-2301示差检测器,进样量20μL。分别取100、500、1000、2500、5000μg/mL的还原糖混标,在上述色谱条件下用BF-2002液谱工作站绘制标准曲线。
1.2.3 Asn和 Gly的测定方法 准确量取样品200μL,分别置于1.5mL离心管中,加入三乙胺乙腈溶液(14%)100μL,异硫氰酸苯酯乙腈溶液(1.2%)100μL,混匀,室温放置 70min后,加入正己烷400μL,振摇后静置10min,取下层溶液,用0.45μm膜过滤,进行HPLC测定。HPLC条件为:Venusil-AA氨基酸分析柱(4.6mm×250mm,5μm);柱温40℃;流动相A/流动相B=98/2;流速1mL/min;流动相A:称取15.2g醋酸钠,加水1850mL,溶解后用冰醋酸调pH至6.5,然后加乙腈140mL,混匀;流动相 B为80%乙腈;紫外检测器检测波长为254nm;进样量1μL。准确称取Gly和Asn各100mg,用0.1mol/L的HCl溶解并定容至100mL容量瓶中。将上述溶液配制成 150、300、600、800、1000μg/mL的混标,经0.45μm膜过滤,按照上述方法衍生后测定,用BF-2002液谱工作站绘制标准曲线。
1.2.4 丙烯酰胺的测定方法 采用HPLC法直接测定,条件为ODS HYPERSIL柱(250×4.6mm,5μm);进样量20μL;流动相为水∶甲醇(98∶2);检测波长为205nm;流速为0.7mL/min;柱温30℃。分别取50、100、250、500、750、1000、1750、3500、7000g/L的标品溶液,按上述条件分析并绘制标准曲线。
1.2.5 褐变度 Asn/Glc/Gly体系反应完成后,用T6新世纪紫外可见分光光度计测定反应体系溶液在420nm下的吸光度值A420。
2 结果与分析
2.1 Asn/Glc/Gly模拟体系中AA的形成规律
尽管随反应时间的延长,AA生成量呈上升趋势(图1),但图2显示了Asn/Glc/Gly体系AA生成量比Asn/Glc体系[7]中AA生成量降低的百分比。可以看出,在100、110、120℃反应4h后,Asn/Glc/Gly体系中AA的生成量比Asn/Glc体系[7]中AA的生成量分别减少了71.8%、83.9%、90.6%,说明Gly能够显著抑制美拉德反应生成的AA。方差分析表明,100、110、120℃ 三者之间差异不显著(α>0.05),90℃与其它三个温度则差异显著(α<0.05)。统计分析表明90℃下Asn/Glc/Gly体系和Asn/Glc体系的AA含量无显著差异(α>0.05)。
2.2 Asn/Glc/Gly模拟体系的褐变度与AA生成量之间的关系
Asn/Glc/Gly模拟体系反应4h后,测定了其在420nm的吸光度,如图3所示。与Asn/Glc[7]体系相比较其吸光度增加,AA含量下降,进一步说明了Gly参与了美拉德反应,并抑制了AA的生成。

图1 Asn/Glc/Gly模拟体系的AA含量变化趋势

图2 Gly对Asn/Glc/Gly模拟体系AA抑制趋势

图3 Asn/Glc/Gly在体系420nm下的吸光度变化
零级和一级动力学方程都可以很好地拟合Asn/Glc/Gly模拟体系中AA与A420之间的关系,相关系数分别在0.80和0.92以上。这表明我们可以根据A420的值,通过这两个方程来预测Asn/Glc/Gly模拟体系中AA的含量,相关数据如表1、表2。方差分析表明,90、100、110℃三者之间差异显著(α <0.05),110℃与120℃之间差异不显著(α>0.05)。

表1 Asn/Glc/Gly模拟体系中AA生成量与A420之间线性相关数据

表2 Asn/Glc/Gly模拟体系中AA生成量与A420之间相关性数据(一级动力学方程)
2.3 Asn/Glc/Gly模拟体系中Glc、Gly和Asn的变化规律
对Asn/Glc/Gly模拟体系中的Glc、Asn、Gly进行定量分析,结果见图4~图6。可以看出,随着加热温度和时间的增加,Glc呈逐渐下降趋势,同时伴随着果糖(Fru)的生成。Gly与Asn也均表现出下降趋势,说明这三个化合物均参与了美拉德反应。
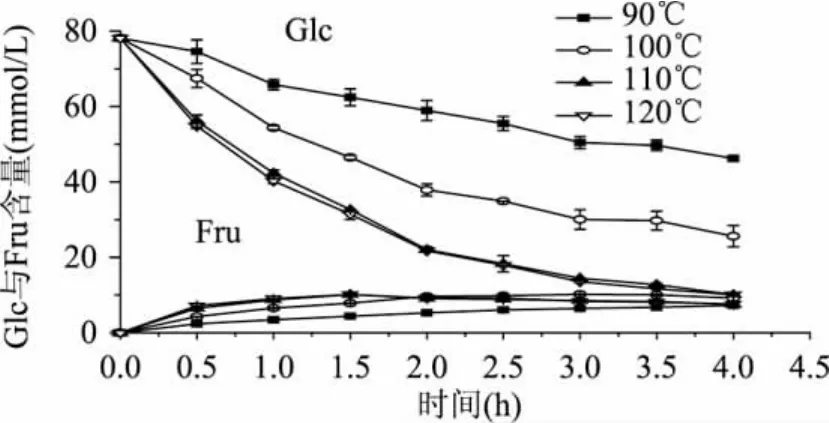
图4 Asn/Glc/Gly体系Glc与Fru的含量变化趋势
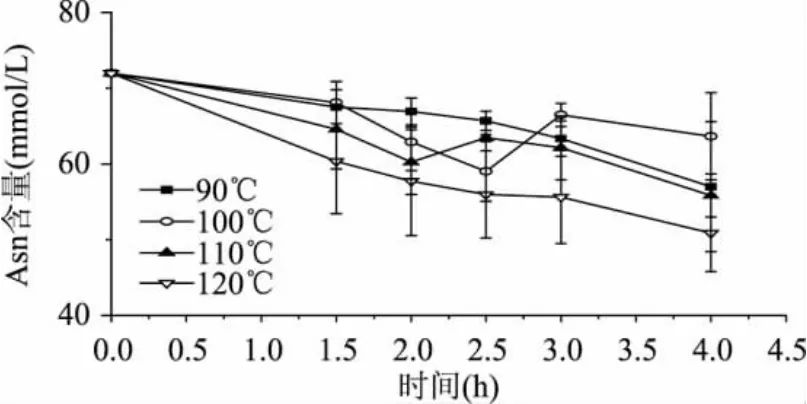
图5 Asn/Glc/Gly体系的Asn含量变化趋势
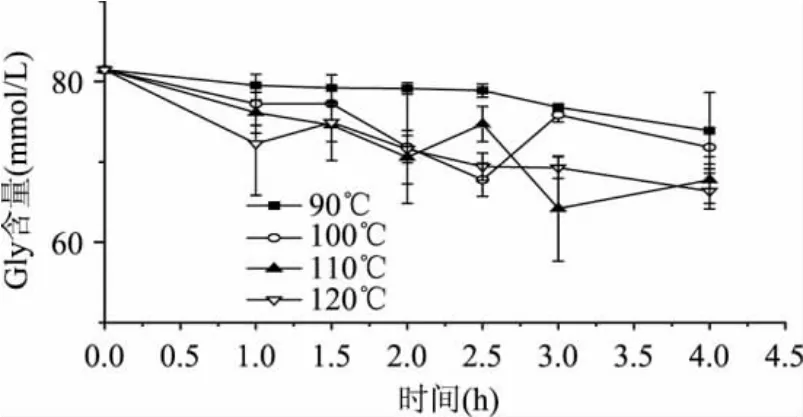
图6 Asn/Glc/Gly体系的Gly含量变化趋势
温度对Glc、Gly和Asn的变化有显著影响。方差分析表明,对Glc的变化趋势100、110、120℃之间差异不显著(α>0.05),90℃与其它温度之间差异显著(α<0.05)。对Asn的变化趋势90℃与100℃之间差异不显著(α>0.05),100℃与110、120℃之间差异显著(α<0.05)。对Gly的变化趋势110、120℃之间差异不显著(α>0.05),110℃和120℃分别与90℃和100℃之间差异显著(α<0.05)。
2.4 Asn/Glc/Gly模拟体系中Gly与Asn一级动力学反应模型
分别以 ln([Gly]t/[Gly]0)与 ln([Asn]t/[Asn]0)为y轴,反应时间t为x轴作图则可以得到一条直线,其斜率即为k。根据ln(C/C0)=-kt可以求出各温度下的k值,结果见表3、表4。回归分析表明,各温度下Gly、Asn的变化与t之间呈显著的直线回归(α<0.05)关系,相关系数都在0.79~0.93之间,这说明在Asn/Glc/Gly模拟体系下,一级动力学模型可以很好地反映Gly与Asn的降解动态。

表3 Asn/Glc/Gly模拟体系中Asn变化的一级动力学参数

表4 Asn/Glc/Gly模拟体系中Gly变化的一级动力学参数
2.5 Asn/Glc/Gly模拟体系中Gly与Asn竞争反应模型
由以上可知,Asn与Gly的降解动态都符合一级动力学模型。本研究以Asn一级动力学模型参数为基础,可以作出不同温度下ln([Gly]t/[Gly]0)对ln([Asn]t/[Asn]0)的关系图,经回归分析,发现二者之间呈显著的直线回归关系(α<0.05),相关系数都在0.91~0.95之间。Asn/Glc/Gly模拟体系各个温度下Gly的竞争模型分析结果见表5。

表5 Asn/Glc/Gly模拟体系Gly的竞争模型动力学参数
比较通过一级动力学模型推算出来的kGly和竞争模型推算出来的k′Gly,发现两者非常接近,并无显著性差异(α>0.05)。可见竞争模型能够很好地解释Asn/Glc/Gly模拟体系中Gly的变化过程,说明在Asn/Glc/Gly模拟体系中,Gly、Asn是竞争着和 Glc发生反应的。
3 结论
通过对Asn/Glc/Gly模拟体系的研究发现,Gly能够显著抑制美拉德反应生成的AA;Asn,Glc,Gly三个化合物均参与了美拉德反应;可以根据褐变度A420的值预测Asn/Glc/Gly模拟体系中AA的含量。另外一级动力学模型较好地反映了90、120℃下Asn/Glc/Gly模拟体系中Gly、Asn的降解动态,竞争模型拟合结果显示Gly与Asn均能与Glc发生反应,且两反应之间存在竞争关系。
[1]Swedish NFA.Information About Acrylamide in Food.Swedish National Food Administration,April 24,2002.http://www.slv.se/engdefault.asp.
[2]Mottram D S,Wedzicha B L,Dodson A T.Acrylamide is formed in the maillard reaction[J].Nature,2002,419:448-449.
[3]Stadler R H,Blank I,Varga N,et al.Acrylamide from Maillard reaction products[J].Nature,2002,419:449-450.
[4]Fink M,Andersson R,Rosén J,et al.Effect of Added Asparagine and Glycine on Acrylamide Content in Yeast-Leavened bread[J].Cereal Chem,2006,83(2):218-222.
[5]Low M Y,Koutsidis G,Parker J K,et al.Effect of Citric Acid and Glycine Addition on Acrylamide and Flavor in a Potato Model System[J].J Agric Food Chem,2006,54:5976-5983.
[6]Kim C T,Hwang E-S,Lee H J.Reducing acrylamide in fried snack products by adding amino acids[J].Journal of Food Science,2005,70(5):354-358.
[7]张海霞,陈芳,袁媛,等.Asn/Glc模拟体系中丙烯酰胺形成规律的研究[J].食品工业科技,2007,28(12):108-109.
Inhibition of acrylamide formation in asparagine/glucose model systems by glycine addition
LIU Jie1,ZHANG Hai-xia2,HU Xiao-song2,CHEN Fang2,*
(1.College of Food Science and Engineering,Henan University of Technology,Zhengzhou 450052,China;2.College of Food Science and Nutritional Engineering,China Agricultural University,Beijing 100083,China)
Maillard reaction was proved as the main pathway to form acrylamide.In order to study the mechanism of inhibition of acrylamide formation in asparagine/glucose model systems by glycine addition,the model systems were heated in 90~120℃ for 4 hours.The formation of acrylamide,decrease of asparagine,glucose and glycine,increase of absorbance at 420nm and the kinetic analysis on glycine and asparagine degradation were discussed in the glucose/asparagine/glycine model reaction systems.It concluded that glycine significantly inhibited the formation of acrylamide.Glycine and asparagine competed with each other in the model systems.
acrylamide;glycine;Maillard reaction;model system
TS201.2
A
1002-0306(2011)06-0073-03
2009-04-17 *通讯联系人
刘洁(1979-),女,博士,讲师,研究方向:食品安全。
国家自然科学基金(31071554);国家十一五支撑计划课题(2009BADB9B07)。

