不同初始条件下乙醇-空气预混合气层流燃烧火焰结构分析
张志远,郑建军,黄佐华,马向平,韩 树
(1装甲兵工程学院机械工程系,北京100072;2西安交通大学动力工程多相流国家重点实验室,陕西西安710049)
燃料乙醇可用剩余粮食、能源作物和秸秆等生物资源制成,属于可再生燃料。乙醇又是含氧燃料,内燃机燃用乙醇可以实现无烟排放,并能大幅度降低CO排放。因此,无论从降低对石油的依赖度还是从实现内燃机的洁净燃烧方面,乙醇都是有较好应用前景的内燃机替代燃料。乙醇燃料可以采用掺烧方式100%替代汽油燃料,因此其作为内燃机替代燃料的应用研究已开展得相当广泛,并获得了许多燃用乙醇或乙醇-汽油混合燃料的内燃机性能和排放的研究成果。但对于乙醇和乙醇-汽油混合燃料燃烧特性的内在机理认识还不清楚,有必要对内燃机燃用乙醇燃料以及乙醇-汽油混合燃料燃烧方面开展系统深入的基础研究和应用研究,为内燃机技术的不断发展提供理论和技术支撑[1]。
乙醇燃料的预混层流燃烧特性实验研究和利用乙醇化学反应动力学机理的模拟计算是乙醇基础燃烧研究的2个重要方面。在乙醇燃料预混层流燃烧特性研究方面,文献[2-5]作者分别用不同的试验方法对乙醇-空气预混合气的层流燃烧速度进行了测定,得出了相同的层流燃烧速度随初始条件(初始压力、初始温度和气体稀释度)变化而变化的规律。为了对乙醇-空气火焰传播速度随初始条件变化的原因从火焰结构上给予解释,笔者利用Chemkin提供的火焰模拟类反应模型中的层流预混火焰传播速度计算模型,对不同初始条件下乙醇-空气混合气一维稳态层流预混火焰进行模拟计算,给出一维层流自由传播火焰中反应物、自由基、碳基中间产物和燃烧产物分布规律,分析火焰结构中的物种分布特别是中间自由基的分布与层流燃烧速度的关系,尝试从化学反应动力学角度解释乙醇-空气预混合气层流燃烧速度随初始压力、初始温度和稀释度的变化规律。
1 扩展乙醇化学反应机理的验证
在乙醇燃料的燃烧中,也按C/H/O化学反应产生火焰。燃料攻击中涉及同碳氢燃料一样的自由基(H、O、OH、HO2)。醇类火焰与一般碳氢燃料火焰的区别是初始攻击时会产生更多的含氧基,而在通常的碳氢燃料燃烧中它们仅以微量出现。燃烧中间产物也是相似的,因为涉及同样的元素,所以最终的绝热产物也是一样的。文献中给出的乙醇化学反应机理有2个:一是N.M.Marinov给出的高温条件下乙醇氧化的详细化学动力学反应机理,其包含57个物种,383步反应[6];二是 Priyank Saxena给出的一个新的乙醇扩展简化机理,其包含53个物种和288步基元反应[7]。Marinov机理是一个详细化学动力学机理,通过与实验测定的层流燃烧速度和激波管测定的着火延迟期数据比较,证明了该机理的有效性。而且该机理的计算结果也与通过连续反应器和搅动床反应器测定的物种浓度数据进行了比较。但是Marinov机理不涉及NOx生成的化学反应动力学机理。本研究通过耦合Marinov机理和NO机理[8],生成一个新的包含63个物种、392步反应的扩展乙醇化学动力学反应机理。
为验证该扩展乙醇化学反应机理对于计算乙醇-空气预混合气燃烧过程的适应性,笔者首先利用Chemkin 4.0层流火焰速率计算模型和该扩展乙醇化学反应机理,计算了初始温度Tu=423 K、初始压力 Pu=0.1 MPa、当量比 φ =0.7 ~1.4 的乙醇 - 空气预混合气层流燃烧速率u1。图1给出了乙醇-空气预混合气层流燃烧速率计算结果和文献[5]中同样初始条件下实验结果的比较,可以看出:计算结果和实验结果非常吻合,表明高温下扩展乙醇化学动力学反应机理适用于计算本文实验条件下的乙醇-空气混合气预混层流燃烧过程。
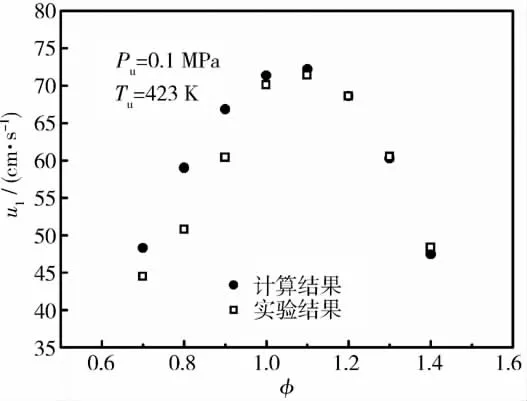
图1 乙醇-空气混合气层流燃烧速度计算结果和实验结果的比较
2 乙醇-空气混合气预混层流燃烧火焰结构分析
笔者采用Chemkin 4.0层流火焰速率计算模型和Marinov扩展乙醇化学反应机理计算不同初始条件下的乙醇-空气层流预混燃烧特性。图2-4分别给出了不同初始压力、不同初始温度和不同气体稀释度下化学计量当量比一维层流自由传播乙醇-空气的火焰结构,从图中可以看出:乙醇-空气燃烧火焰的反应物(C2H5OH和O2)、燃烧产物(CO2、CO和 H2O)、活性基(H、OH、O、HO2和 H2O2)和碳基中间产物(CH3CHO、C2H4、CH2O、CH4、C2H6、CH3、HCCO和CH2CO)的浓度随燃烧区与火焰面距离的变化曲线。乙醇-空气火焰中主要反应物和燃烧产物的摩尔分数量级为10-2~10-1,火焰中自由基的最大摩尔分数量级为10-4~10-3,因此火焰中主要物种摩尔分数由反应物组分所决定,同时燃烧化学反应过程对其也有影响。从碳基中间产物的摩尔分布曲线可以看出:碳基中间产物最大摩尔分数量级为10-5~10-3。火焰结构分析表明:在乙醇-空气混合气预混火焰中OH的摩尔分数在整个火焰反应区范围内最大,其次是H,然后是O,而HO2和H2O2基团的最大浓度值较小。在碳基中间产物中,乙醛CH3CHO是C2基与O2或其他活性组分次级反应的主要产物,其浓度最大。其次是乙烯C2H4,它不仅通过乙醇的直接裂解产生,还通过乙醇中氢原子抽离形成的CH2CH2OH的裂解产生,其摩尔浓度也较大。
2.1 不同初始压力下乙醇-空气一维层流自由传播火焰结构
图2给出了初始温度Tu=423 K、初始压力Pu分别为0.1 MPa和0.5 MPa时化学计量当量比一维层流自由传播乙醇-空气的火焰结构。可以看出:随着初始压力的增加,火焰反应区域变薄,反应物摩尔分数下降速度和生成物摩尔分数增加速度明显加快。活性基(H、OH和O)浓度下降,其中以H基最为明显。HO2和H2O2基团最大浓度的变化不明显。在给定当量比条件下,层流燃烧速度随初始压力增加而降低[5]。初始压力的增加导致H、OH和O基浓度下降是造成乙醇燃烧反应速率变慢的主要原因之一。碳基中间产物浓度最大值随初始压力的变化无明显改变。

图2 不同初始压力下乙醇-空气预混层流燃烧火焰结构比较
2.2 不同初始温度下乙醇-空气一维层流自由传播火焰结构
图3给出了初始压力 Pu=0.1MPa、初始温度Tu分别为373 K和423 K时化学计量当量比一维层流自由传播乙醇-空气的火焰结构。可以看出:初始温度的增加对反应物、燃烧产物以及碳基中间产物的浓度基本上无影响。随着初始温度的增加,浓度变化最明显的是活性基H、OH和O,在整个燃烧反应区内3种活性基浓度都有增加,这也是乙醇-空气混合气预混层流燃烧速率随初始温度增加而增加的主要原因之一。
2.3 不同气体稀释度下乙醇-空气一维层流自由传播火焰结构
图4给出了初始压力Pu=0.1 MPa、初始温度Tu=373 K、氮气稀释度φr分别为0%和15%时化学计量当量比一维层流自由传播乙醇-空气的火焰结构。可以看出:由于氮气的稀释,反应物的浓度下降,燃烧产物的浓度变化不明显。随着氮气的添加,碳基中间产物最大摩尔分数对应位置向火焰区下游移动。由于氮气稀释降低了火焰温度,导致这些碳基中间产物的生成和消耗反应向温度更高的下游位置移动。碳基中间产物中乙醛浓度最大,乙醛是乙醇燃烧中最主要的中间产物,其次是乙烯。所以乙醛的裂解和氧化机理是乙醇燃烧机理必须包含进来的重要一部分。氮气稀释气的添加降低了乙醛的浓度,从而乙醛排放降低。另一方面,氮气稀释气的添加直接导致活性基H、OH和O浓度在整个燃烧反应区内明显下降,这也是乙醇-空气混合气预混层流燃烧速率随氮气稀释度增加而减小的主要原因之一。

图3 不同初始温度下乙醇-空气预混层流燃烧火焰结构比较

图4 不同气体稀释度下乙醇-空气预混层流燃烧火焰结构比较
2.4 不同初始条件下乙醇-空气预混层流燃烧NOx排放预测
扩展的乙醇-空气化学反应机理增加了NO、NO2和N2O的反应机理,图5给出了基于该机理计算的NO、NO2和N2O的浓度分布曲线。可以看出:NO是NOx中的主要生成物,其浓度随着火焰区温度的升高而增加,最后在计算区域边界达到最高浓度。相对而言,NO2和N2O浓度比NO浓度相差1~2个数量级,N2O浓度在火焰中心区达到最大浓度,N2O受温度影响不大。具体分析初始压力、初始温度和氮气稀释度对NO生成的影响可以发现:由于NOx的生成和N2、O2、H、O、OH 和 N 的浓度有很大关系,而这些物质主要在高温区生成;因而NOx的生成与火焰温度直接相关。初始压力增加,火焰燃烧温度增加,NOx生成浓度增加。由于化学反应区域变薄,可以看出NO和N2O增加速度很快,其中NO最为显著。初始温度增加,NO浓度增加,N2O变化很小。氮气添加到乙醇-空气混合气后,稀释度增加,火焰温度降低,NOx浓度降低。其中,NO大幅度下降,而N2O和NO2变化很小。

图5 不同初始条件下乙醇-空气火焰NOx浓度分布曲线
3 结论
笔者提出了一个扩展的乙醇化学反应机理并给予了验证。利用此扩展机理进行模拟计算得到如下主要结论:主要自由基OH、H和O浓度随初始压力增加而减小;随初始温度增加而增加;随氮气稀释度的增加而减小。自由基浓度随初始条件的变化规律部分地解释了试验和计算得到的层流燃烧速度随初始条件的变化规律。
笔者的研究表明,基于一个恰当机理的乙醇-空气混合气一维稳态层流预混火焰模拟计算,一方面可以指导层流燃烧速度测定试验的进行,另一方面从化学反应动力学角度解释了乙醇-空气预混合气层流燃烧速度随初始条件的变化规律。同样的研究用于基于恰当简化机理的高碳碳氢化合物也会对高碳碳氢化合物或高碳碳氢化合物和乙醇混合燃料预混层流燃烧的研究起到积极的指导作用。
[1]黄佐华,蒋德明,王锡斌.内燃机燃烧研究及面临的挑战[J].内燃机学报,2008(S1):101-106.
[2]Gulder O L.Laminar Burning Velocities of Methanol,Isooctane and Isooctane/Methanol Blends[J].Combustion Science and Technology,1983,33(1/4):179-192.
[3]杜德兴,Law C K.甲醇、乙醇-空气混合物层流火焰传播速度的实验研究[J].工程热物理学报,1992,13(4):448-452.
[4]Liao S Y,Jiang D M,Huang Z H,et al.Determination of the Laminar Burning Velocities for Mixtures of Ethanol and Air at Elevated Temperatures[J].Applied Thermal Engineering,2007,27(2/3):374-380.
[5]张志远,黄佐华,郑建军,等.高温高压条件下乙醇-空气-稀释气预混合气层流燃烧特性研究[J].内燃机学报,2010,28(2):103 -108.
[6]Marinov N M.A Detailed Chemical Kinetic Model for High Temperature Ethanol Oxidation[J].International Journal of Chemical Kinetics,1999,31(3):183-220.
[7]Saxena P,Williams F A.Numerical and Experimental Studies of Ethanol Flames[J].Proceedings of the Combustion Institute,2007,31(1):1149-1156.
[8]Kong S C,Sun Y,Rietz R D.Modeling Diesel Spray Flame Liftoff,Sooting Tendency,and NOxEmissions Using Detailed Chemistry with Phenomenological Soot Model[J].Journal of Engineering for Gas Turbines and Power-transactions of the Asme,2007,129(1):245-251.

