用改进的耦合水平集方法从MSCT中分割左心室
王兴家 董利娜 李传富 范 亚 冯焕清*(中国科学技术大学电子科学与技术系,合肥 3007)
2(安徽中医学院第一附属医院影像中心,合肥 230031)
引言
随着多层螺旋CT(multi-slice spiral CT,MSCT)技术的快速发展,64层乃至更高层数(如128、256)的MSCT装备进了许多医院,320层的机器也已问世。它们通过多排探测器技术来提供高扫描速度、高时间分辨率的体数据,同时采用心电门控技术来同步扫描,做到每个心动周期扫描一周,能显著减少心跳的伪影;通过指定不同的同步位置,还能获得心脏不同搏动时相的体数据。例如,以0.1s间隔,取R峰及前后共10个位置为扫描起始点,各心动周期成像一次,就可获得表征一个心动周期不同搏动时相的10个CT数据集,实现所谓的“四维CT成像”。对该4D-CT数据集做进一步的处理和分析,就可能形成心、肺、冠状动脉等器官的动态图像,进行心、肺功能的更深入研究。
四维CT数据处理的第一步是针对各个时相的数据集进行心脏或肺的分割,工作量很大,必须实现自动分割,而且算法要能保证较高的分割精度,这是后续研究顺利进行的根本保证。由于左心室在心脏功能研究中的重要地位,因此本研究以它为例,介绍从4D-CT心脏数据中分割出左心室腔和心肌的方法。在MRI心脏成像领域已有不少左心室分割的研究工作,但针对MSCT的左心室分割的报道较少,已有的研究基于主动形状模型或主动表现模型,需要大量训练数据集,且不适合病变个体[1-2]。采用嵌入先验知识的改进耦合水平集(improved couple level set,ICLS)模型,从MSCT心脏数据中精确提取左心室腔和心肌。下面在介绍水平集模型的基础上,重点讨论如何针对左心室分割的特点和先验知识,分别对水平集耦合因子、水平集起始轮廓、边缘检测因子进行改进的思路,并给出采用特定心相MSCT数据集进行验证的结果。
1 原理和算法
1.1 水平集模型
水平集(level set)方法首先由Osher和Sethian提出,并用于曲线演化模型[3]。Caselles与Malladi等将该方法引入图像处理领域,提出了几何主动轮廓模型,使初始曲线向能量泛函的极小值演化[4-5],利用水平集方法,使模型能自适应被检物体的拓扑变化,且与参数无关。近年来,出现了许多基于水平集的图像分割算法[6-9]。
在水平集模型中,用C表示演化曲线,C(t)={(x,y)|φ(t,x,y)=0}是水平集函数φ(t,x,y)的零水平集,其中初始化轮廓为{(x,y)|φ0(x,y)=0}。假设I为待分割图像,为使外部能量驱动零水平集函数向目标边缘移动,构造图像梯度的递减函数为边界检测因子g,使得g在图像边缘的值近似为0。通常将g定义为
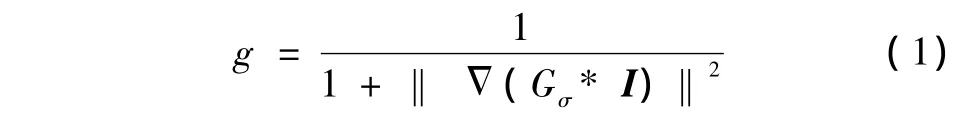
式中,Gσ是标准差为σ的高斯函数,*表示卷积运算。
边界检测因子g在图像分割中扮演极其重要的角色。从式(1)可看出,在图像梯度较大区域,g值近似为0,在灰度一致区域为正值。采用文献[7]的WRLS模型为原始水平集模型,该模型包含了额外的能量项,用于控制水平集函数和符号距离函数的位置偏差,避免计算量大且复杂的重新初始化。能量函数由惩罚项作为内部能量P(φ)和外部能量εg,λ,ν(φ)构成,有
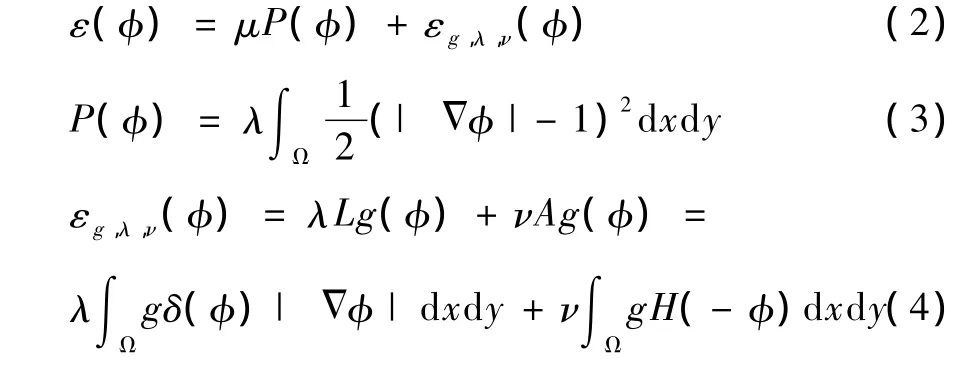
式中,λ(λ>0)和ν为常数,δ为狄拉克函数,H为海维塞德函数。
外部能量项εg,λ,ν(φ)驱动零水平集曲线向目标边界移动,同时内部能量项μP(φ)约束水平集函数趋近符号距离函数,从而保持水平集函数的平滑性。最小化能量函数,得到水平集演化方程,即
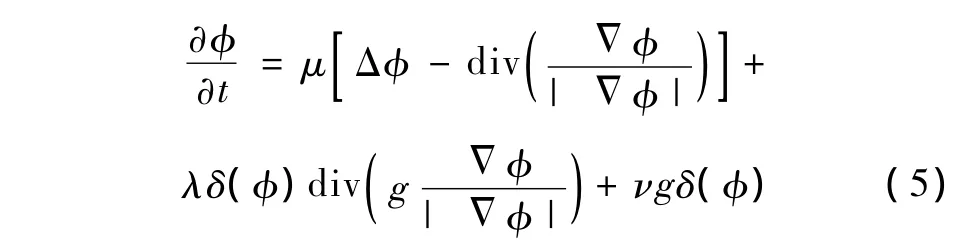
下面将针对MSCT图像的特点以及左心室的先验知识改进WRLS模型,使原始模型能适用于左心室的定位和精确分割。
1.2 水平集耦合因子
在结构上,左心室可看成由类圆形的腔和类环形的心肌构成,因此采用了不同的水平集函数φ1、φ2来表示左心室的腔和心肌。为避免两水平集函数发生重叠,定义一个耦合水平集(coupled level set,CLS)因子,它的正负和权重控制着水平集曲线的方向和演化速度,即
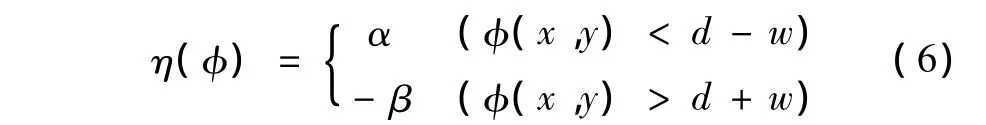
式中,d表示从左心室重心到内、外心膜的平均距离,w表示平均距离的容许范围。
在实际应用中,可根据左心室的结构和大小对d、w取值。通过耦合水平集,水平集函数在内、外心膜的对应区域演化而不相互影响。
1.3 起始轮廓的初始化
1.3.1 左心室定位
由于分辨率很高,而且Z轴分辨率与层片内的分辨率一致,即数据是各向同性的,所以MSCT数据具有结构连续性的显著特征,即相邻层片间的结构变化是连续的,结构差异不大,灰度具有较大的相似性[10]。根据结构连续特征,提出MSCT左心室的定位算法和粗轮廓提取算法,其中粗轮廓用于水平集起始函数的初始化。
设I是心脏某心相的左心室短轴MSCT的3D数据集,它包含N个层片In:Ω⊂R2→R+,n∈[1,2,…,N]。选取层片Is(s∈[1,2,…,N])作为序列I的定位模板,其中Is需满足条件:左心室腔面积在层片中较大(腔面积要比主动脉等大血管面积大),左心室腔有较光滑的边界,腔周围有较小的组织噪声。由于左心室腔的灰度值较大,边缘较明显,所以可根据阈值法和形态学操作获得左心室腔的定位初始模板。
1)利用阈值法和形态学模型,去除胸腔的肺、骨头、大血管等组织,初步获取定位模板图像中的左心室腔粗轮廓模板M,即

式中,T1和T2是去除左心室腔以外组织的低阈值和高阈值,*表示二值形态学操作,结构元素SE1用于填充左心室腔中的小孔,Bwselect用于提取阈值分割结果,max用于提取出面积最大的左心室腔。
2)通过层片与模板相乘,提取出左心室腔的粗轮廓ΓtM为
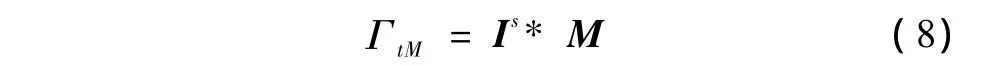
式中,*表示矩阵对应点的值相乘。
沿着左心室的短轴从腔由大变小的方向,使用初始定位模板来获取邻近层片左心室腔的粗轮廓,层片In的腔室掩板可由层片In-1得到,并利用图1所示流程更新定位模板,从而获取整个数据集中层片的左心室腔粗轮廓,完成左心室的定位。
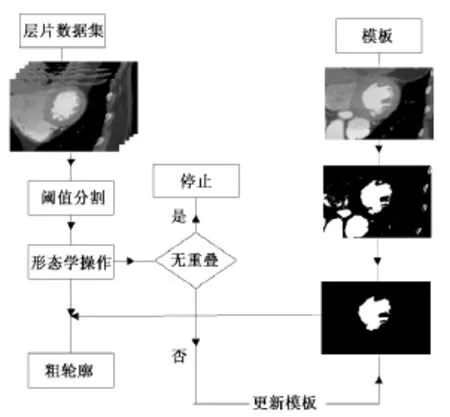
图1 左心室腔粗轮廓的获取流程Fig.1 The flowchart to extract coarse contour of LV cavity
1.3.2 起始轮廓的初始化
水平集曲线演化之前必须确定初始化轮廓的位置、面积,不合适的起始位置、形状和大小可能导致错误的分割结果。在大多数水平集模型中,初始轮廓的形状是圆形、矩形等规则形状,与待分割目标形状无任何关系。本模型则按如下方法、利用左心室腔粗轮廓来定义起始形状,有
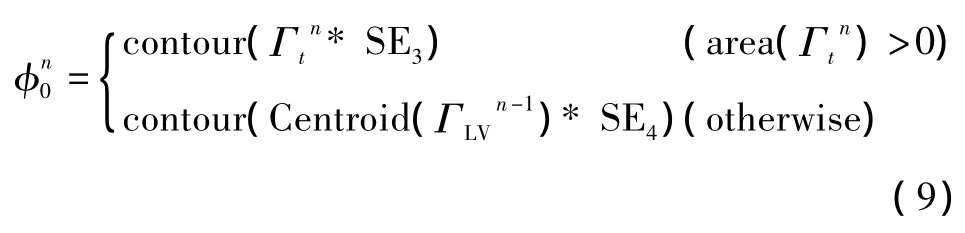
式中,Γtn是左心室的粗轮廓,area(Γtn)表示左心室腔的区域,Centroid(ΓLVn-1)表示上一层片左心室的质心,*表示二值形态学运算,结构因子SE3、SE4用于平滑区域轮廓。
利用结构连续性和前一层片的分割结果,可以精确地定位腔室和心肌的起始轮廓,而且由于起始轮廓近似于待分割目标边缘,因此有效降低了水平集演化时间。
1.4 基于先验区域的边缘检测因子
边缘检测因子又称为停止项,文献[8]将其改进为
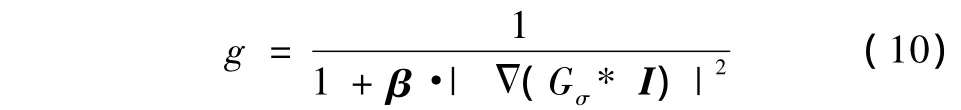
式中,β是由高斯函数Gσ和引导因子λ卷积构成的矩阵,*表示矩阵对应点的值相乘。
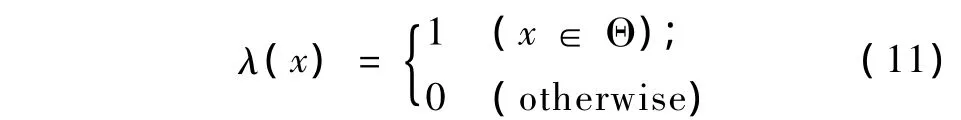
引导因子定义为式中,Θ表示给定的感兴趣区域。
引导因子可以把先验知识融合到曲线的演化当中。由式(11)可知,当曲线演化到感兴趣区域时,引导因子退化为常数,g还原成式(1)的边缘检测因子,曲线保持正常的演化。当引导因子为0时,曲线会越过不感兴趣的区域。由于MSCT图像层片间左心室的结构和位置相对不变,假设Γn-1是上一层片图像分割的左心室腔区域,则下一层片边缘和层片n-1相近。本模型中设Γn-1为感兴趣区域,则分割室腔的水平集引导函数可定义为
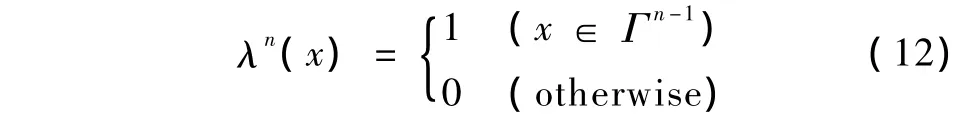
同样,可以设置心肌的感兴趣区域。通过重新设计引导函数,水平集演化方程在每个层片上都有对应的检测因子和停止函数,降低了曲线的演化泄露和曲线在目标区域内局部极值上的迭代。
1.5 改进耦合水平集模型
把融合区域先验模型的边缘检测因子、水平集耦合因子加入水平集演化方程,便可得到ICLS模型的演化方程为
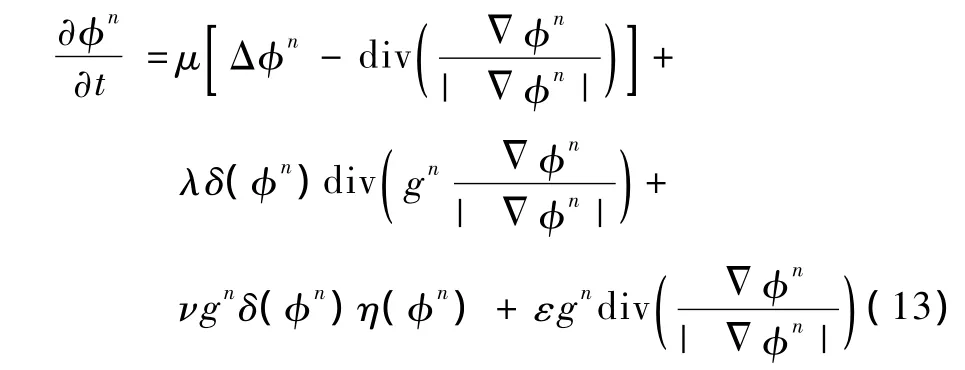
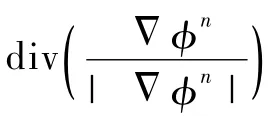
步骤1:通过式(7)和式(8),获取层片In的左心室腔粗轮廓。
步骤3:通过式(10)和式(12),更新边缘检测因子gn。
步骤5:计算|φt+1n-φtn|<θ,θ是自定义的小常数。如果对比水平集演化前后的面积差满足该条件,便停止演化,否则继续步骤4。
2 实验方法
在应用ICLS模型分割前,必须对获取的MSCT图像数据进行有效的预处理。首先对原始CT数据作非线性灰度变换,把一定范围内的灰度值映射到特定范围内,使得在该灰度范围内的图像更加便于后续图像处理[11]。此外,CT数据会受到数据采集系统的电子噪声和重建噪声等的影响。为提高分割质量,必须去除其中的局部噪声和斑点噪声,同时要保留待分割目标的边缘。采用Paris等提出的快速双边滤波器[12]来去除CT图像噪声,与传统的高斯滤波器相比,双边滤波器能较好地保持图像边缘,而高斯滤波后的左心室边缘却比较模糊(见图2)。
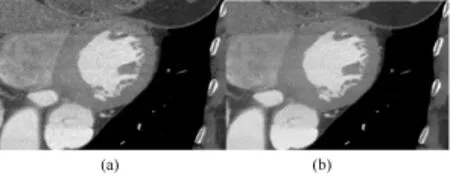
图2 滤波效果。(a)高斯滤波器;(b)双边滤波器Fig.2 Filtering results.(a)Gaussian filter;(b)bilateral filter
实验数据采自GE公司的64排螺旋CT,采用心电门控技术获取的3D心脏MSCT数据,分辨率512像素×512像素×297像素;以及来自Philips公司的256排MSCT的8例3D心脏数据集,分辨率为512像素×512像素×331像素。首先选用64排3D心脏数据集,初步验证ICLS模型的分割效果。ICLS模型的参数设置为μ=0.04,λ=5,ν=3,ε=1.5,θ=10,曲线演化步长Δt=5。为了进一步验证算法对三维数据分割的适用性和有效性,保持ICLS模型的参数不变,对8例256排MSCT三维数据集进行左心室心肌和血腔的分割与提取。
为了精确比较并评价自动分割结果与手工分割结果的相似度,用ICLS模型自动提取该数据集的短轴位[13]左心室腔和心肌,然后将自动分割的结果与手工勾勒的结果进行比较。采用如下方法[14]进行相似度(Similarity,SM)对比:设CT层片经计算机分割处理后,得到目标面积S1、手工勾勒轮廓包围的面积S2和共同包围的面积S,相似度的计算公式为
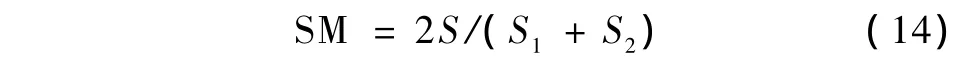
SM的范围为0~1。当S1与S2完全重合时值为1,完全不重合时值为0;当相似度数值越接近于1,表明算法的分割结果越接近于手工分割,算法的准确性就越高。
3 结果
图3是原水平集模型(WRLS)和改进耦合水平集模型(ICLS)起始轮廓的对比,后者起始轮廓已近似于待分割轮廓,并能保证左心室的精确定位。图4是两种模型在相同参数下左心室的分割结果,可见在灰度近似区域ICLS模型减少了边缘泄露。
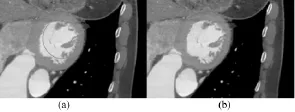
图3 起始轮廓。(a)WRLS模型;(b)ICLS模型Fig.3 The initial contour.(a)WRLS model;(b)ICLS model
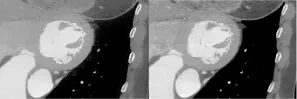
图4 分割结果。(a)WRLS模型;(b)ICLS模型Fig.4 Segmentation results.(a)WRLS model;(b)ICLS model
图5是相似度分析后的结果,其中左心室腔的平均相似度0.950 3,标准偏差0.043 5;左心室心肌的平均相似度0.920 6,标准偏差为0.026 8。在腔和包围腔的心肌之间,灰度对比度较为明显,边缘较为清晰,腔的定位和分割效果较好。心肌和邻近组织的灰度相似度很高,心肌边缘不是特别明显。不过,除极个别层片外,其他层片的分割情况都较好,自动分割与手工分割的结果基本吻合。图6显示的是对分割结果进行3D表面重建后的结果,可以看出分割结果在左心房短轴位具有很好的同一性和完整性。
表1是ICLS模型与分割对心肌的分割结果,用式(14)计算获得平均相似度。可得ICLS模型的血腔分割结果的平均相似度为0.959 2,平均标准偏差为0.019 0;心肌分割结果的平均相似度为0.906 3,平均标准偏差为0.025 6。可以看出,对于不同来源的三维左心室数据,ICLS模型同样具有较高的分割精度,对心肌的平均分割准确率可以达到95%以上,对心肌的分割准确率可以达到90%以上,说明ICLS算法具有普遍的适用性。因此,ICLS模型可以用于提取整个3D+t的MSCT心脏数据,这为后续多心相的心功能分析研究打下良好的基础。
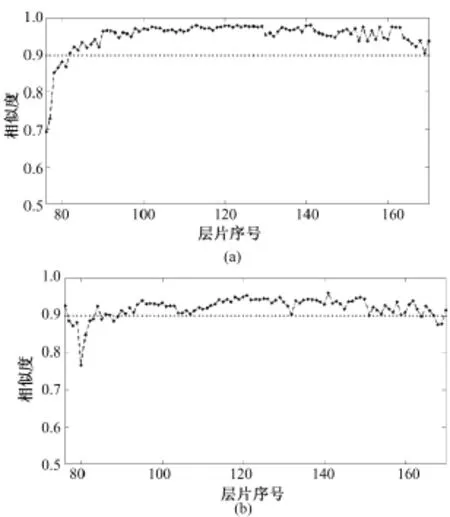
图5 分割相似度。(a)左心室腔;(b)心肌Fig.5 Similaritiy of Segmentation results.(a)LV cavity;(b)myocardium

图6 左心室三维重建结果。(a)不同角度下的心肌;(b)不同角度下的血腔Fig.6 3D surface reconstruction results of LV.(a)myocardium from different views;(b)cavity from different views
4 结论
针对MSCT图像左心室定位与分割的特定应用,本研究提出了融合左心室先验形状和结构连续性的耦合水平集模型——ICLS模型。它首先根据结构连续性和阈值法定位,提取出左心室腔的粗轮廓;然后利用左心室先验知识以及结构连续性,指导后续水平集曲线的演化。ICLS模型对MSCT数据集的实验表明,它能实现左心室腔和心肌的自动分割,与其他基于单幅梯度边缘、无耦合因子、无先验知识的水平集方法比较,结果更准确和完整,还提高了曲线演化速度并减少了边缘泄露,这为进一步分析左心室运动提供良好的数据保证。
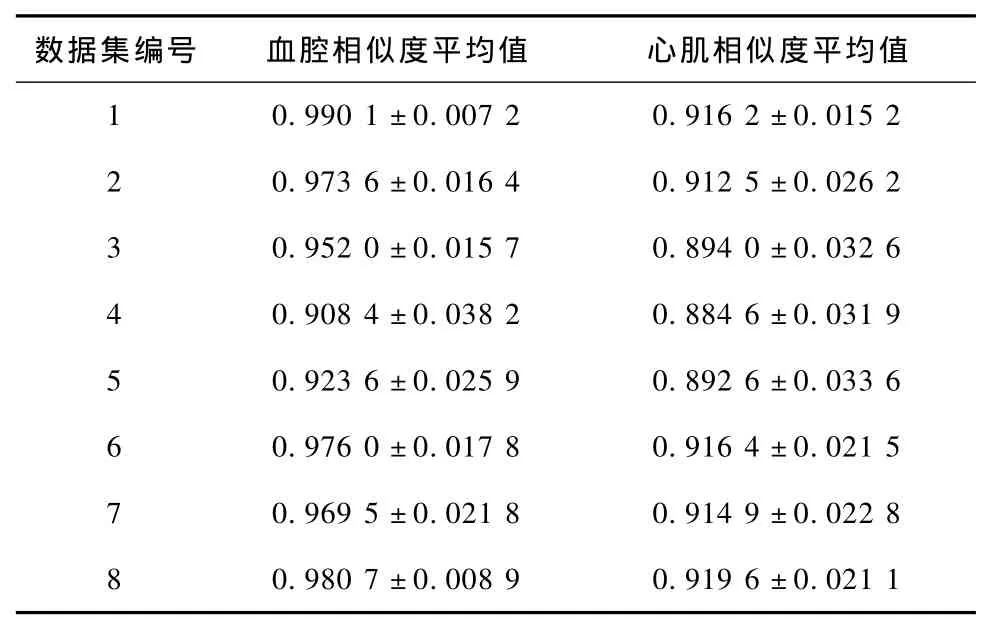
表1 ICLS模型分割结果与手工分割结果的相似度与标准偏差Tab.1 The similarity and standard deviation between ICLS model and manual segmentation results
[1]Fritz D,Kroll J,Dillmann R,et al.Automatic 4D-segmentation of the left ventricle in cardiac-CT-data[C].//Pluim JPW,Reinhardt JM.,eds.Medical Image 2007:Imaging Proceeding.Bellingham:SPIE-INT Soc Optical Engineering,2007,6512:N5123.
[2]Garreau M,Simon A,Boulmie D,et al.Assessment of left ventricular function in cardiacmsct imaging by a 4D hierarchical surface-volume matching process[J].International Journal of Biomedical Imaging,2006,1-10.
[3]OsherS,Sethian JA.Fronts propagating with curvature dependent speed:algorithms based on the Hamilton-Jacobi formulation[J].Journal of Computational Physics,1988,79:12-49.
[4]Caselles V,Catte F,Coll T,et al.A geometric method for active contours[J].Numeriche Meathematik,1993,66:1-31.
[5]Malladi R,Sethian JA,Vemuri BC.Shape modeling with front propagation:a level set approach[J].IEEE Trans Pattern Analysis and Machine Intelligence,1995,17(2):158-175.
[6]Chan T,Vese L.Active contours without edges[J].IEEE Transactions on Image Processing,2001,10(2):266-277.
[7]Li CM,Xu CY,Gui C,et al.Level set evolution without reinitialization:a new variational formulation[C].//Schmid C,Soatto S,Tomasi C.,eds.IEEE International Conference on Computer Vision and Pattern Recognition.Los Alamitos:IEEE Computer Soc,2005,1:430-436.
[8]Zhang H,Morrow P,McClean S,et al.Incorporating feature based priors into the geodesic active contour model and its application in biomedical imagery[C]//McDonald J,Markham C,Ghent J,eds.International Machine Vision and Image Processing Conference.Los Alamitos:IEEE Computer Soc,2007:67-74.
[9]Lynch M,Ghita O,Whelam PF.Left-ventricle myocardium segmentation using a coupled level set with a priori knowledge[J].Computerized Medical Imaging and Graphics,2006,30:255-262.
[10]Liu Junwei.,Feng Huanqing,Zhou Yingyue,et al.A novel automatic extraction method of lung texture tree from HRCT image[J].Acta Automatica Sinica,2009,35(4):345-349.
[11]Heinemann EG.Simultaneous brightness induction as a function of inducing and test field luminances[J].Journal of Experimental Psychology,1955,50(2):89-96.
[12]Paris S,Durand F.A fast approximation of the bilateral filter using a signal processing approach[C]//Bischof H,Leonardis A.,eds.European conference on Computer Vision.Berlin:Springer-Verlag,2006,81(1):24-52.
[13]American Heart Association Writing Group on Myocardial Segmentation and Registration for Cardiac Image.Standardized myocardial segmentation and nomenclature fortomographic imaging of the heart[J].Circulation,2002,105:539-542.
[14]周颖玥,冯焕清,李传富,等.一种从胸HRCT图像序列分割肺的自动化方法[J].北京生物医学工程,2008,27(1):6-10.
——以内蒙古伊敏煤为例

