RP-HPLC法测定雷公藤微乳中雷公藤内酯甲的含量
王志君,尤本明,孙华君,宋洪杰,刘继勇 (第二军医大学长海医院药学部,上海 200433)
雷公藤(Tripterygium)为卫茅科植物雷公藤Tripterygium wilfordii Hook.f的根、叶及花,又名黄藤、断肠草。性味辛凉,有大毒,入肝经,兼入脾肾经,其主要功能为清热解毒、祛风除湿、舒筋活血通络、消肿止痛、杀虫止痒。雷公藤多苷为雷公藤的主要活性成分,在临床上多与其他药物复方配伍应用,目前上市的雷公藤制剂主要有雷公藤片、雷公藤双层片、雷公藤多苷片等[1]。但由于其口服存在着较大的毒性反应,因此限制了其临床应用[1,2]。微乳(microemulsion,ME)是由水相、油相、表面活性剂和助表面活性剂按适当比例混和,自发形成的各向同性、透明、热力学稳定的分散体系。具有增加药物的溶解度、提高药物稳定性、促进药物透皮吸收、延长药物作用时间等优点,因此日益受到研究者的重视[3~6]。本文研究了用高效液相色谱法测定雷公藤微乳中雷公藤内酯甲含量的方法,现报道如下。
1 仪器与试剂
1.1 仪器 LC-10A vp高效液相色谱仪(日本岛津制作所,包括 LC-10ATvp泵、SPD-10Avp紫外检测器、CLASS vp色谱工作站和SCL-10Avp系统控制器);调温调湿箱(上海实验仪器厂有限公司,302A型);FA-2004电子天平(万分之一,上海天平仪器厂);电子天平(十万分之一,Sartorius);精密酸度计(上海天达仪器有限公司)。
1.2 试剂 雷公藤多苷原料药(浙江得恩德制药有限公司,雷公藤内酯甲含量0.263%);雷公藤内酯甲标准品(批号111597-200402,纯度>98%,中国药品生物制品检定所);Lecithin E200(德国Degussa公司);肉豆蔻酸异丙酯 (IPM,国药集团化学试剂有限公司);烷基葡萄糖苷(APG,中国日用化学工业研究院);1,2-丙二醇(上海制药有限公司);中性氧化铝(上海五四化学试剂有限公司);甲醇和乙腈(HPLC级,Tedia公司);水为重蒸水;其他试剂为分析纯。雷公微乳(自制,雷公藤多苷含量1.2%)。
2 方法与结果
2.1 溶液的制备
2.1.1 对照品溶液的制备 精密称取雷公藤内酯甲对照品2 mg,于10 ml量瓶中,加甲醇溶解稀释至刻度,得200 μg/ml的储备液,密封,于4℃冰箱保存。
2.1.2 供试品溶液的制备[7,8]将制备好的雷公藤多苷微乳5 g加15 ml甲醇破乳,超声30 min,将破乳的雷公藤多苷微乳加到已处理好含水分3%的中性氧化铝柱(100~200目,12 g,内径3 cm,湿法装柱,用适量三氯甲烷预洗)上,用乙酸乙酯-丙酮(3∶1)50 ml洗脱,收集洗脱液,蒸干,残渣用甲醇溶解,转移至10 ml容量瓶中,加甲醇稀释至刻度,摇匀,即得。
2.1.3 空白溶液的制备 将不含雷公藤多苷样品的空白微乳制剂5 g加15 ml甲醇破乳,超声30 min,将破乳的空白微乳按上述按2.1.2项下方法处理,得空白体系溶液。
2.2 色谱条件与系统适应性[8]色谱柱:Diamond C18柱(4.6 mm × 250 mm,5 μm);流动相:乙腈-水(90∶10);流速:1.0 ml/min;检测波长:210 nm;进样量:20 μl;柱温:室温;灵敏度:0.01 AUFS。
上述溶液分别进样20 μl,将所得色谱图进行比较。从图1可见,辅料对雷公藤多苷的测定无干扰,表明本方法专属性好。

图1 雷公藤微乳色谱图
2.3 标准曲线的绘制 分别精密量取储备液0.1、0.2、0.5、1.0、1.5 ml置于 10 ml容量瓶中,用甲醇定容,制备浓度分别为 2.0、4.0、10.0、20.0、30.0 μg/ml的标准溶液。按上述色谱条件依次进样。以测得峰面积A与其浓度C线性回归,得标准曲线方程 A=9 498.4C -1 688.2,r=0.999 9,线性范围为2.0 ~30.0 μg/ml。
2.4 日内精密度 分别取低、中、高3组浓度的混合对照品溶液各20 μl,在上述色谱条件下,重复进样3次,每次进样间隔时间为4 h,记录峰面积,计算峰面积变异系数。雷公藤内酯甲低、中、高3个浓度(2.0、10.0、20.0 μg/ml)峰面积的 RSD 分别为 0.40%、0.17% 和0.28%,表明所建立的HPLC方法重现性好。
2.5 日间精密度 分别取低、中、高3组浓度的混合对照品溶液各20 μl,在上述色谱条件下,重复进样3次,每次进样间隔时间为24 h,记录峰面积,计算峰面积变异系数。雷公藤内酯甲低、中、高3个浓度(2.0、10.0、20.0 μg/ml)峰面积的 RSD 分别为1.77%、0.84%和1.74%,表明所建立的HPLC方法重现性好,且测定时间内样品溶液稳定性良好。
2.6 稳定性试验 在供试品溶液配制后的8 h内,每隔2 h测定1次,记录峰面积值,其RSD值为0.86%(n=5),表明供试品在处理后8 h内稳定。
2.7 重复性试验 取雷公藤多苷微乳5份,按2.1.2项下操作,进样,测定峰面积并计算含量,雷公藤内酯甲的RSD为0.98%(n=5)。
2.8 回收率试验 精密量取低、中、高3个浓度的雷公藤内酯甲标准品溶液加入到浓度已知的样品溶液中,进样测定,计算回收率。结果见表1。
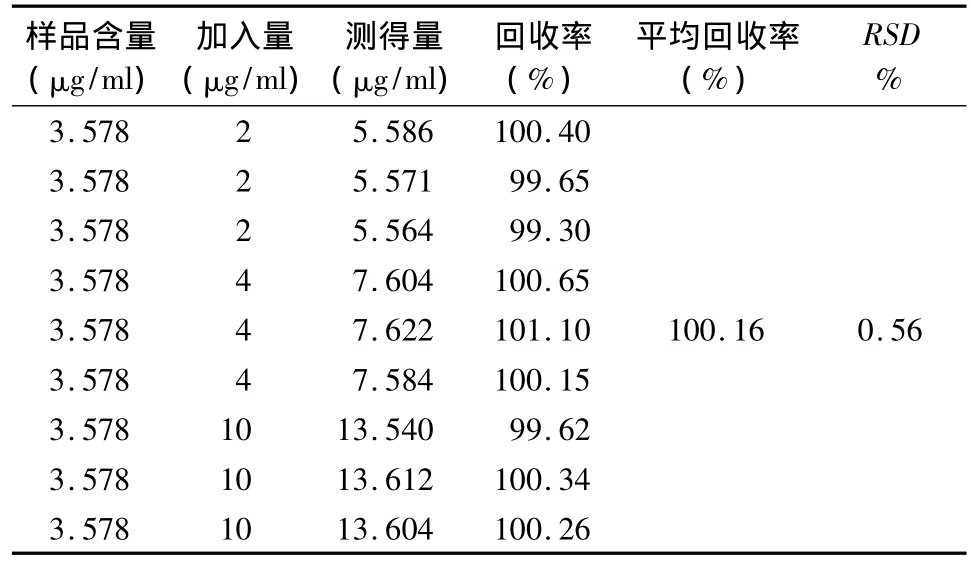
表1 雷公藤微乳回收率测定结果(n=9)
2.9 样品含量测定 取3批样品,依样品溶液处理方法制备成供试品溶液,按2.1.2项下测定。用标准曲线计算3批样品中雷公藤多苷的含量,其结果见表2。3批样品中雷公藤内酯甲的平均含量分别为标示量的(98.92±0.92)%,均在标示量的95%~105%之间,符合含量测定要求。

表2 雷公藤多苷微乳含量测定结果(n=3)
3 讨论
本实验建立了测定雷公藤微乳中雷公藤内酯甲的反相高效液相色谱方法。经方法学研究表明,所建立的HPLC方法灵敏,专属性强、准确,重现性好。
雷公藤多苷中成分复杂,雷公藤内酯甲的含量仅为0.263%。含量测定时一般要先进行柱处理,除去部分杂质纯化样品,减少杂质对目标峰的影响,利于样品的分离测定。
测定微乳药物含量时一般需先破乳,再以适当的溶剂提取分离后测定。而本研究中雷公藤多苷微乳中的肉豆蔻酸异丙酯溶于甲醇,故根据各成分的溶解特性,采用甲醇破乳,破乳后溶液呈澄清透明,无需提取分离,可直接过柱分离后进样测定,实验中发现采用乙腈、乙醚等破乳时均不能形成澄清透明溶液。
[1]徐央丽.雷公藤的研究进展[J].现代中西医结合杂志,2008,17(12):1914.
[2]金美子.雷公藤研究进展[J].中国社区医师,2007,21:34.
[3]寇 欣.微乳给药系统的研究进展[J].天津药学,2005,17(6):52.
[4]Peltola S,Saarinen-Savolainen P.Microemulsions for topical delivery of estradiol[J].Int J Pharm,2003,254(2):99.
[5]Rhee YS,Choi JG.Transdermal delivery of ketoprofen using microemulsions[J].Int J Pharm,2001,228(1-2):161.
[6]王高森,侯世祥,毛生俊等.丹参酮ⅡA微乳的制备与质量评价[J].华西药学杂志,2007,22(3):279.
[7]谢 谊,王实强,刘可柔.反相高效液相色谱法测定雷公藤多甙片中雷公藤酯甲的含量研究[J].湖南中医杂志,2007,23(1):79.
[8]刘法千,鲍立曾,熊仕强.HPLC法测定雷公藤多苷中雷公藤内酯甲的含量[J].中国药品标准,2007,8(4):38.

