微生物转化法生产香兰素的研究进展
罗诚浩,喻 林,魏 敏,宋旭艳,陈义坤,陈 勇
(1.湖北中烟工业有限责任公司技术中心,湖北 武汉 430040;2.湖北大学 中药生物技术省重点实验室,湖北 武汉 430062)
香兰素(Vanillin)又名香草醛,化学名3-甲氧基-4-羟基苯甲醛,是甜菜、香草豆、安息香胶、秘鲁香脂、妥卢香脂等的香味成分。香兰素既是一种重要的香料,广泛用作化妆品、食品的香精和定香剂,也是一种重要的抗癫痫药,同时,对细菌、酵母菌、霉菌等也有较强的抑制作用,可用于治疗皮肤病[1],而作为一种催欲剂已不再为人所知[2]。
香兰素是目前世界上产量最大的合成香料,也是医药工业重要的原料和中间体。随着其应用范围的日益扩大,香兰素的合成已成为研究热点。香兰素的合成方法主要有化学合成法和微生物转化法。化学合成法产率高、成本低,一直占据着香兰素生产的主导地位,但其原料愈创木酚等有毒,环境污染较严重。微生物转化法因反应条件温和、能保持食品的天然性而越来越受关注,许多天然物质如阿魏酸、丁香酚、异丁香酚、葡萄糖、木质素、香草酸、芳香族氨基酸、姜黄素、辣椒素等都可作为微生物转化法生产香兰素的前体,一些农副产品如麦糠、甜菜浆等也可经由连续的酶促反应来生产香兰素[3]。作者在此对微生物转化法生产香兰素的研究进展进行了较详细的评述。
1 以阿魏酸为底物的微生物转化法
阿魏酸,化学名3-(4-羟基-3-甲氧苯基)-2-丙烯酸,是麦麸中含量最高的酚酸,可达其干重的0.5%~1%。主要通过酯键与多糖和木质素交联或自身酯化或醚化形成结合态的阿魏酸。阿魏酸是合成香兰素的前体物质,微生物主要通过以下4条途径将阿魏酸转化为香兰素,即非氧化脱羧反应、侧链还原反应、不依赖辅酶A的去乙酰反应、依赖辅酶A的去乙酰反应,见图1、图2[4]。
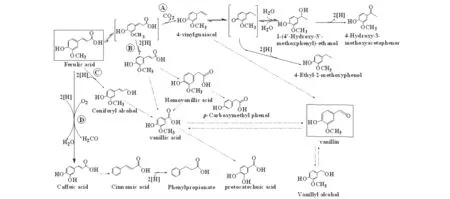
图1 阿魏酸生产香兰素的非氧化脱羧反应(A)和侧链还原反应(B、C、D)

图2 阿魏酸生产香兰素的不依赖辅酶A的去乙酰反应(A)和依赖辅酶A的去乙酰反应(B)
在由阿魏酸生产香兰素时,可先利用一些微生物分泌的酯酶将阿魏酸从植物细胞壁中游离出来,然后再将阿魏酸转化成香兰素。目前已经分离、提纯了多种阿魏酸酯酶(如FAEⅠ、FAEⅡ、FAEⅢ等),它们可以断裂阿魏酸与糖之间连接的酯键,从而释放出游离的阿魏酸[5,6]。近几年以阿魏酸为底物通过微生物转化法生产香兰素的文献总结见表1。

表1 近几年以阿魏酸为底物生产香兰素的研究状况
虽然有些微生物具有较高的转化效率,但发酵工艺还不能满足工业化生产的要求。随着基因工程的发展,利用重组菌株来生产香兰素颇具吸引力。目前以阿魏酸为底物、以依赖辅酶A的去乙酰反应途径生产香兰素所涉及酶的基因已从拟无枝酸菌(Amycolatopsissp.strain HR167)、西塘氏链霉菌(Streptomycessetonii)、荧光假单胞菌(P.fluorescensstrain AN103)、恶臭假单胞菌(P.putidastrain WCS358)、丁香假单胞菌(Pseudomonassp.strain HR199)等微生物中克隆出来,并在大肠杆菌(Escherichiacoli)中得到了表达[17],但如何提高这些酶在大肠杆菌中的表达效率仍有待深入研究。
2 以丁香酚或异丁香酚为底物的微生物转化法
丁香酚(化学名4-丙烯基-2-甲氧基苯酚)为无色或微黄色液体,有丁香香气,味辛辣,露置空气中逐渐变为棕色,具有局部阵痛、防腐的作用,主要存在于丁香油、丁香罗勒油、月桂叶油中。丁香酚的同分异构体异丁香酚(化学名4-丙烯基-2-甲氧基苯酚)为无色或淡黄色液体,有柔和焦糖辛香式丁香香气,为丁香酚的替代品,除用于医药外,还可作为合成香料的原料,也可用于配制康乃馨香型日用香精,也可作为食用香精,主要存在于依兰、肉豆蔻、丁香等的精油中[18]。丁香酚和异丁香酚均可经化学法或微生物转化法生产香兰素。
目前,有关丁香酚的微生物代谢途径报道逐渐增多,而异丁香酚的微生物代谢途径尚未见报道。1977年,Tadasa[19]首次报道棒杆菌(Corynebacteriumsp.)能将丁香酚降解为阿魏酸、香兰素、香草酸和原儿茶酸,然后再通过邻位开裂继续降解。茄病链孢霉菌也可将丁香酚转化为香兰素和4-乙烯愈创木酚,转化过程中可能产生阿魏酸[20]。Pseudomonassp.HR199能将丁香酚转化为松柏醛、松柏醇、阿魏酸、香兰素,且相关基因已得到克隆和鉴定[21,22]。Pseudomonassp.HR199对丁香酚的代谢路径及其关键酶见图3[18]。
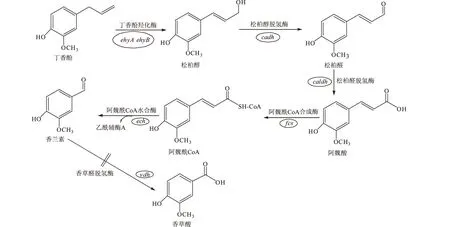
图3 基因工程菌Pseudomonas sp.HR199转化丁香酚生成香兰素的代谢途径
丁香酚、异丁香酚对微生物的生长或其酶活性有抑制作用,导致微生物转化丁香酚、异丁香酚生成香兰素的能力均较低[18]。为了提高香兰素产量,Shimoni等[23]利用离子交换树脂XAD-2吸附异丁香酚,有效地避免了异丁香酚对枯草芽孢杆菌(Bacillussubtilis)B2细胞的生长抑制。Rabenhorst等[22]在分离获得Pseudomonassp.HR199(DSM7.62或DSM7.63)后发现,该菌能转化丁香酚生成一系列甲氧基苯酚类芳香族化合物,但并不积累香兰素,通过在香兰素脱氢酶的基因中插入一个omega因子使其活性下降,从而积累香兰素。近几年以丁香酚或异丁香酚为底物通过微生物转化法生产香兰素的文献总结见表2。

表2 近几年以丁香酚或异丁香酚为底物生产香兰素的研究状况
3 以葡萄糖为底物的微生物转化法
葡萄糖原料充足,生产成本较低。Li等[30]采用基因工程方法对大肠杆菌(Escherichiacoli)K L7/pK L5126A或 K L7/pK L5197A进行基因重组,使菌体利用葡萄糖通过磷酸戊糖途径和莽草酸途径合成3-脱氢莽草酸;然后利用3-脱氢莽草酸脱水酶使3-脱氢莽草酸转化为原儿茶酸;原儿茶酸在儿茶酚O-O甲基转移酶的作用下转化为香兰素酸;再利用从脉孢菌(Neurosporacrassa)中提纯的芳基乙醛脱氢酶将香兰素酸转化成香兰素。该方法菌种生长周期短、繁殖量大,反应条件温和,原料丰富易得,但也存在香兰素产量低、产物分离复杂、不能满足工业化生产要求等问题[31]。
4 以木质素为底物的微生物转化法
木质素是自然资源最丰富的芳香化合物之一,广泛存在于废木材、禾秸、泥炭、纸浆废液和酒糟中,以其通过化学氧化法生产香兰素早有报道,但以其为底物通过微生物转化法生产香兰素却鲜有报道。Priefert等[32]发现白腐菌能降解木质素,释放出香兰素、香草酸、脱氧二香兰素、松柏醛、阿魏酸、肉桂醛、羟基肉桂酸、愈创木酚-β-松柏醇醚和愈创木酚等。由于利用真菌分解木质素得到的香兰素含量甚微,故目前采用该法生产香兰素还未进入实用阶段[33]。
5 以香草酸为底物的微生物转化法
香草酸是微生物降解木质素和阿魏酸过程中积累的重要中间产物。如荧光假单胞杆菌BF13在5 h可将95%的阿魏酸转化成香草酸,然后再还原成香兰素[22]。香草酸在漆酶和过氧化物酶的作用下所产生的脱羧反应会降低香兰素的产率。防止脱羧反应的方法是在加入香草酸前添加纤维二糖,这样可以使香草酸按还原途径代谢而提高香兰素的产量,纤维二糖的作用机理是诱导醌氧化还原酶的形成,从而抑制漆酶和过氧化物酶引起的香草酸脱羧[33]。
王明君等[34]筛选到1株可以转化香草酸生成香兰素的朱红密孔菌(Pycnoporuscinnabarinus)SW20203,通过优化培养基和转化条件后,可以将 1.682 g·L-1的香草酸转化生成 0.875 g·L-1香兰素,摩尔转化率为57.5%。在25 L罐中进行放大试验,香兰素产量为0.818 g·L-1,摩尔转化率为53.7%。从转化液中提取得到纯度为95%的香兰素结晶,提取率为63.9%。Li等从诺卡氏菌分离纯化了羧酸还原酶并将其作用于香草酸,能高效生产香兰素,但此酶需ATP和NADPH作为辅酶,价格昂贵,其应用受到限制[35]。
6 微生物转化法与化学合成法的比较(表3)
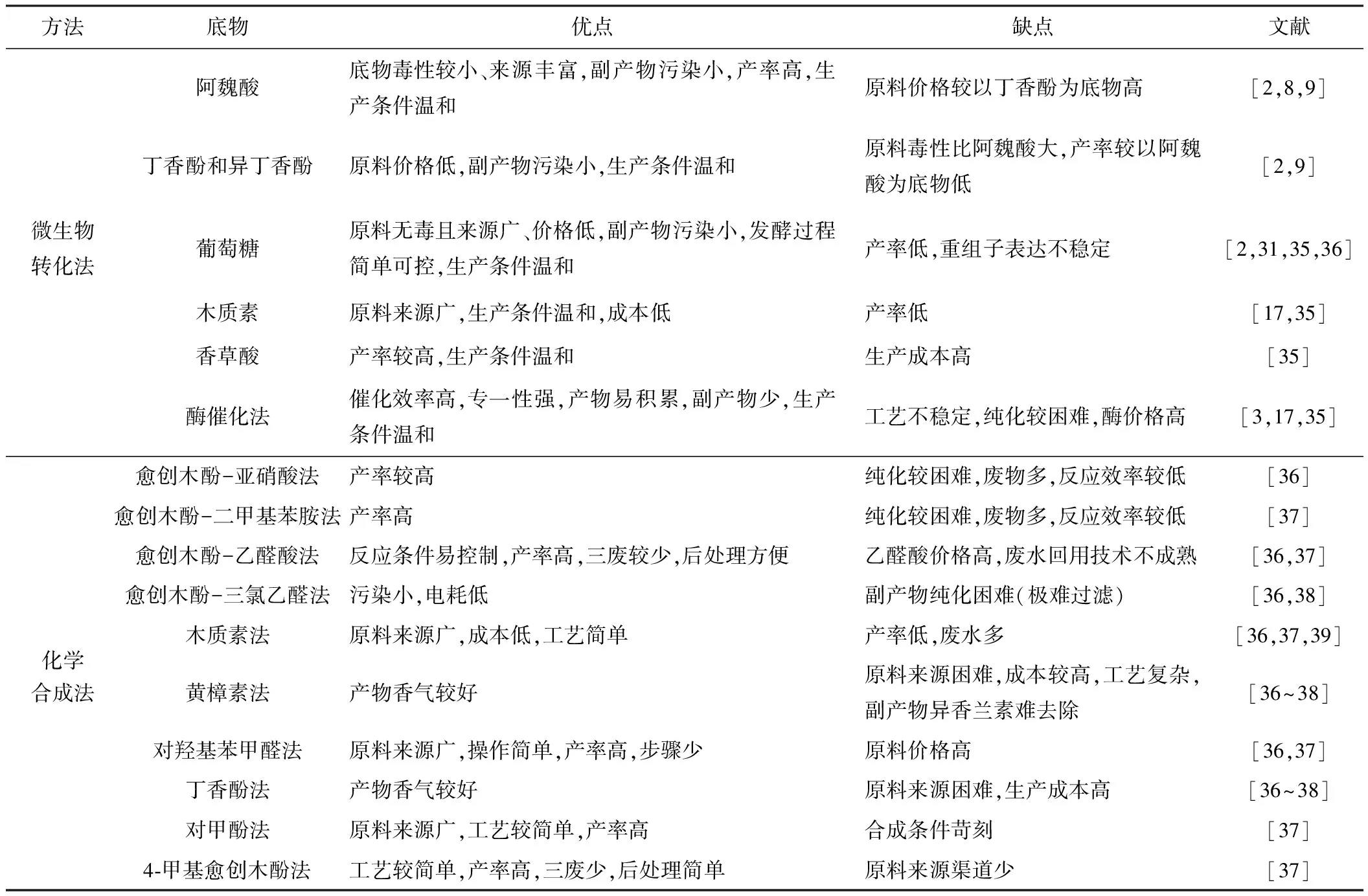
表3 微生物转化法和化学合成法生产香兰素的比较
7 展望
微生物转化法生产香兰素是一项新兴技术,具有反应条件温和、污染小等优点。以北方特产的米糠、甜菜等原料作为发酵底物,采用微生物转化法生产天然香兰素,还可以进一步降低生产成本,虽然目前还处于技术开发阶段,但仍显示了良好的发展前景[35]。另外,采用基因工程方法对大肠杆菌进行基因重组也是一种很有发展前景的香兰素生产方法,但就目前的技术来看,保证大肠杆菌重组子的稳定表达仍然是此项技术的难点[5,40]。结合我国的资源优势,认为现阶段开发以异丁香酚、阿魏酸为底物的微生物转化法生产香兰素技术将更具有可行性与应用前景。
[1] 姜欣,彭黎旭.香兰素微生物发酵法研究进展[J].华南热带农业大学学报,2007,13(4):34-38.
[2] Lawler L J,著,庄馥萃,译.香荚兰的药疗作用[J].亚热带植物通讯,1991,20(1):64.
[3] 李永红,郑璞,孙志浩.生物技术方法生产香草醛研究进展[J].工业微生物,2004,34(4):46-57.
[4] 赵建芬,张广,陈惠音.以阿魏酸为底物生物合成香兰素[J].韶关学院学报(自然科学版),2007,28(9):81-85.
[5] 范韵敏,李夏兰,方柏山.阿魏酸酯酶产生菌的培养条件优化[J].华侨大学学报(自然科学版),2010,31(4):426-429.
[6] 王谦,李夏兰,程珊影,等.生物酶降解米糠释放阿魏酸工艺条件优化[J].华侨大学学报(自然科学版),2011,32(1):62-66.
[7] 张莉力,迟玉杰.微生物转化阿魏酸生产香兰素的研究[J].现代食品科技,2005,21(2):47-49.
[8] 董长颖,赵丽香.香兰素的生物转化研究[J].吉林农业科技学院学报,2005,14(1):1-4.
[9] 周庆礼,黄艳凤,韩英素,等.微生物转化法生产香兰素[J].食品与发酵工业,2004,30(3):18-20.
[10] 张兆斌,曾义勇,华栋梁,等.微生物转化制备天然香兰素新工艺[A].第七届中国香料香精学术研讨会论文集[C].杭州:中国香料香精化妆品工业协会,2008.
[11] 王洪亮.微生物转化生产香兰素[D].西安:陕西科技大学,2008.
[12] Muheim A,Lerch K.Towards a high-yield bioconversion of ferulic acid to vanillin[J].Appl Microbiol Biotechnol,1999,51(4):456-461.
[13] Cheetham P S J,Gradley M L,Sime J T.Flavour/aroma materials and their preparation[P].WO 2000 050 622,2000-08-31.
[14] Rabenhorst J,Hopp R.Process for the preparation of vanillin and microorganisms suitable therefor[P].USP 6 133 003,2000-10-17.
[15] Muheim A,Muller B,Munch T,et al.Microbiological process for producing vanillin[P].USP 6 235 507,2001-05-22.
[16] 郑璞,郑丽蓉,孙志浩,等.黑曲霉CGMCC0774和朱红密孔菌CGMCC1115两步转化阿魏酸制备生物香兰素[J].生物加工过程,2005,3(3):69-73.
[17] 赵建芬,陈惠音,张广.香兰素的生物合成[J].现代食品科技,2006,22(4):251-254.
[18] 赵丽青.微生物法转化异丁香酚生成香草醛的研究[D].无锡:江南大学,2006.
[19] Tadasa K.Degradation of eugenol by a microorganism[J].Agric Biol Chem,1977,41(6):925-929.
[20] Nazareth S,Mavinkurve S.Degradation of ferulic acid via 4-vinylguaiacol byFusariumsolani(Mart.) Sacc[J].Canadian Journal of Microbiology,1986,32(6):494-497.
[21] Rabenhorst J.Production of methoxyphenol-type natural aroma chemicals biotransformation of eugenol with a newPseudomonassp.[J].Appl Microbiol Biotechnol,1996,46(5-6):470-474.
[22] Rabenhorst J,Hopp R.Process for the preparation of vanillin[P].EP 0 405 197,1991-01-02.
[23] Shimoni E,Ravid U,Shoham Y.Isolation of aBacillussp.capable of transforming isoeugenol to vanillin[J].Biotechnology,2000,78(1):1-9.
[24] 赵丽青,朱蕾蕾,孙志浩,等.转化异丁香酚生成香草醛纺锤芽孢杆菌的筛选[J].微生物学通报,2006,33(1):72-77.
[25] 孙志浩,郑璞,赵丽青.微生物转化异丁香酚制备香草醛的菌种和方法[P].CN 1 712 518,2005-12-28.
[26] Overhage J,Priefert H,Rabenhorst J,et al.Biotransformation of eugenol to vanillin by a mutant ofPseudomonassp.strain HR199 corstructed by disruption of the vanillin dehydrogenase (vdh)gene[J].Appl Microbiol Biotechnol,1999,52(6):820-828.
[27] Furukawa H,Morita H,Yoshida T,et al.Conversion of isoeugenol into vanillic acid byPseudomonasputida158 cells exhibiting high isoeugenol-degrading activity[J].Bioscience and Bioengineering,2003,96(4):401-403.
[28] 孙敏,姚日升,高文霞.异丁香酚的生物转化及香兰素的合成[J].生物加工过程,2006,4(2):33-36.
[29] Chatterjee T,De B K,Bhattacharyya D K.Microbial conversion of isoeugenol to vanillin byRhodococcusrhodochrous[J].Indian Journal of Chemistry,1999,38B(5):538-541.
[30] Li K,Frost J W.Synthesis of vanillin from glucose[J].American Chemical Society,1998,120(40):10545-10546.
[31] 朱慧霞,邓胜松,张洪斌,等.香兰素生物合成法的研究进展[J].精细化工,2004,21(2):125-128.
[32] Priefert H,Rabenhorst J,Steinbüchel A.Biotechnological production of vanillin[J].Appl Microbiol Biotechnol,2001,56(3-4):296-314.
[33] 欧仕益,李爱军,包惠燕,等.生物法生产香兰素研究进展[J].广州食品工业科技,2004,20(2):119-121.
[34] 王明君,郑璞,孙志浩,等.微生物转化香草酸生产香草醛[J].食品与发酵工业,2004,30(2):43-47.
[35] 许美玲,王芳,谭天伟.香兰素生物合成技术进展及展望[J].现代化工,2007,27(Z1):142-147.
[36] 郑波涛.香兰素的合成工艺进展[J].化工之友,2007,(9):51-53.
[37] 吴方宁,丁兴梅,丁敏,等.香兰素的合成及技术展望[J].化工技术与开发,2006,35(2):6-11.
[38] 赵元,丁绍民,宋华付.香兰素生产工艺研究进展[J].化工进展,2001,20(3):13-16.
[39] 李辉,尹笃林.香兰素合成技术研究进展[J].吉首大学学报(自然科学版),2001,22(1):90-93.
[40] 赵建芬,张广.荧光假单胞菌香兰素脱氢酶基因的克隆及表达[J].微生物学杂志,2007,27(6):51-54.

