13C3-三硬脂酸甘油酯的合成与表征
吴航宇,林 琳,李 蕾,陈大舟
(1.北京化工大学理学院,北京 100029;2.中国计量科学研究院化学计量与分析科学研究所,北京 100013)
稳定同位素试剂广泛应用于生命科学、食品安全、资源环境、新型材料、军事与安全等科学研究领域[1-2],是同位素示踪技术的重要试剂。
传统的酯化反应所采用的催化剂为酸或碱[3],得到的硬脂酸甘油酯通常是一酯、二酯和三酯的混合物,需要繁琐的提纯过程,不适合价格昂贵的13C标记化合物的合成。为此,本工作拟采用Lipozyme酶作为催化剂,利用酶的高选择性直接合成三酯,同时在反应体系中不会引入其他溶剂[4-6],所得产物无需纯化。
1 主要仪器与试剂
傅立叶VECTDR22型红外光谱仪(KBr压片)、AV 600核磁共振仪(溶剂为 CDCl3):德国Bruker公司;PYRIS I型差示扫描量热仪(氮气保护):美国Perkinelmer公司;MAT 900XL型双聚焦高分辨质谱仪:配电子轰击(EI)离子源,美国THERMO FINNIGAN公司。
13C3-甘油(13C同位素丰度为 99%):美国Cambridge Isotope Laboratories公司;硬脂酸(99%):美国 Alfa Aesar公司;Lipozyme 酶 :美国Sigma公司;三硬脂酸甘油酯标准品:北京西中化工厂。
2 实验方法
2.1 13 C3-三硬脂酸甘油酯的合成
13C3-三硬脂酸甘油酯的合成路线示于图1[5]。

图1 13 C3-三硬脂酸甘油酯的合成路线
将13C3-甘油和硬脂酸按一定摩尔比混合置于50 mL圆底烧瓶中,放入恒温水浴加热磁力搅拌器中,开启搅拌使反应物混合均匀并加热,待反应物完全熔融,保持15 min,加入催化剂Lipozyme酶,采用抽真空的方式去除产物中的水,恒温水浴反应一定时间,不经过提纯,热过滤将产物与酶分离,即得到产物13C3-三硬脂酸甘油酯。烘干、称重,计算产率。
由于13C同位素产品价格昂贵,本实验通过对未标记三硬脂酸甘油酯的合成条件进行探索,分别考察反应时间、反应温度、反应物比例、催化剂用量和反应方式对三硬脂酸甘油酯纯度的影响,确定最佳合成条件。此后,将原料替换成13C同位素产品,在最佳条件下合成13C3-三硬脂酸甘油酯。
2.2 结构表征方法
采用差示扫描量热分析(DSC)确定产物熔点,分别采用质谱、核磁共振和傅里叶变换红外光谱(FT-IR)对产物进行表征。
DSC分析条件:升温范围40~120℃,升温速率10 ℃/min,载气(N 2)流速1.2 mL/min。
质谱条件:电子轰击(EI)离子源,电子能量70 eV,传输线温度275℃,离子源温度200℃,激活电压1.5 V,质量扫描范围(m/z)35~700。
核磁共振分析条件:液体高分辨NMR 600 MHz,优质核磁管(φ5 mm:0.6 mL或 4 cm),CDCl3溶剂。
FT-IR分析条件:测定波数范围为 500~3 000 cm-1,参比物为空气,扫描次数32或16,分辨率8或4 cm-1。
3 结果与讨论
3.1 合成条件优化
3.1.1 反应时间
反应时间对三硬脂酸甘油酯纯度的影响示于图2。由图2可知,三硬脂酸甘油酯的纯度随时间延长而逐渐增大,10 h后反应基本达到平衡。为避免催化剂Lipozyme酶长时间处在高温下及副产物的生成,确定最佳反应时间为25 h。产物纯度为98.4%。
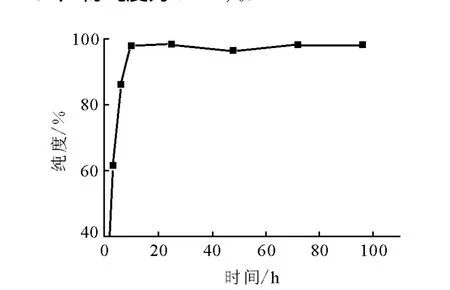
图2 反应时间对三硬脂酸甘油酯纯度的影响
3.1.2 反应温度
反应物硬脂酸的熔点为68~72℃,为了保证反应物的熔融状态,条件实验中选择反应温度为75、80和85℃。此温度下合成的对三硬脂酸甘油酯的纯度示于图3。催化反应速率随着温度升高而加速,在75~80℃时,三硬脂酸甘油酯的纯度随温度升高呈增大趋势;酶在高温下会失活,80~85℃时,三硬脂酸甘油酯的纯度下降。因此,确定最佳反应温度为80℃。
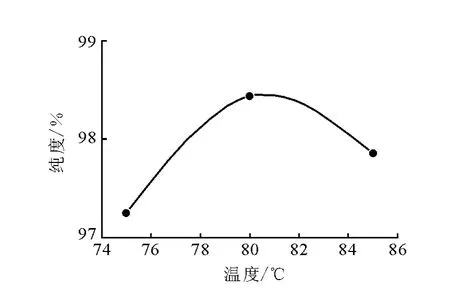
图3 反应温度对三硬脂酸甘油酯纯度的影响
3.1.3 硬脂酸与甘油的摩尔比
反应物比例对三硬脂酸甘油酯纯度的影响示于图4。由图4可知,硬脂酸与甘油摩尔比为2.8∶1时,生成的三硬脂酸甘油酯的纯度高于摩尔比为3.0∶1时的纯度。但随着甘油用量的进一步增加,这是由于甘油用量增加后,三硬脂酸甘油酯的纯度呈下降趋势,会导致副产物双甘酯、单甘酯的生成。因此,确定硬脂酸与甘油的摩尔比最佳摩尔比为2.8∶1。
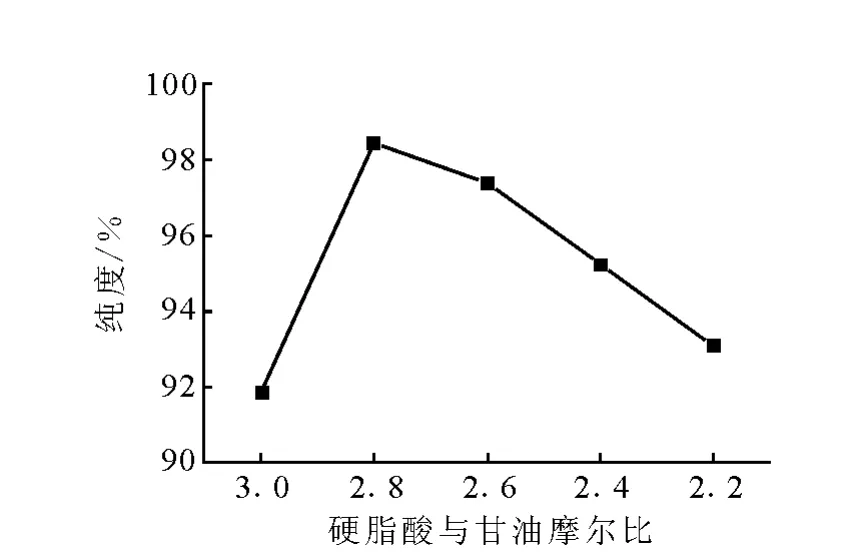
图4 反应物比例对三硬脂酸甘油酯纯度的影响
3.1.4 催化剂用量

图5 催化剂用量对三硬脂酸甘油酯纯度的影响
催化剂用量对三硬脂酸甘油酯纯度的影响示于图5。由图5可知,三硬脂酸甘油酯的纯度随着酶用量的增加而增大,当酶用量加到底物含量的3.6%时,反应基本达平衡。比较含酶量7.6%、5.6%、3.6%时产物的纯度可见,含酶量为7.6%的三硬脂酸甘油酯纯度略高(98.4%),考虑到产品质量和能源消耗,选择最佳催化剂用量为底物含量的7.6%。
3.1.5 反应方式
酯化反应是可逆反应,除去产物水可以促使反应向正向进行。采用抽真空、敞口自然蒸发及封闭反应3种反应方式分别进行5组三硬酯酸甘油酯的合成,其他条件不变,结果显示,抽真空反应方式下,产物纯度最高,为98.27%;敝口自然反应方式次之,为96.14%;封闭反应方式产物纯度最低,为91.93%。说明用抽真空的反应方式可以更有效地去除水分。因此,最佳的反应方式为抽真空。
综上所述,三硬脂酸甘油酯合成的最佳条件为:硬脂酸与甘油摩尔比为2.8∶1,催化剂Lipozyme酶用量为底物总质量的7.6%,反应时间为25 h,反应温度为80℃,反应过程中抽真空。最佳条件下,三硬脂酸甘油酯的合成产率为80%。
3.2 结构表征
3.2.1 FT-IR分析
13C3-三硬脂酸甘油酯产品和三硬脂酸甘油酯标准品的FT-IR谱图示于图6。
由图6可知,13C3-三硬脂酸甘油酯产品和三硬脂酸甘油酯标准品的主要特征峰均吻合。其中,2 926 cm-1和2 854 cm-1为脂肪族-CH-不对称振动吸收峰;1 737 cm-1为酯基的C=O的特征吸收峰;1 179 cm-1和1 113 cm-1为酯基的C-O-C特征吸收峰;1 467 cm-1为脂肪族-CH 2-剪式振动;717 cm-1为脂肪族-(CH 2)n-的平面摇摆振动。利用OPUS谱图检索软件,将产品与标准品进行比对,得到匹配度为92.3%。以上结果表明,产物为13C-三硬脂酸甘油酯。
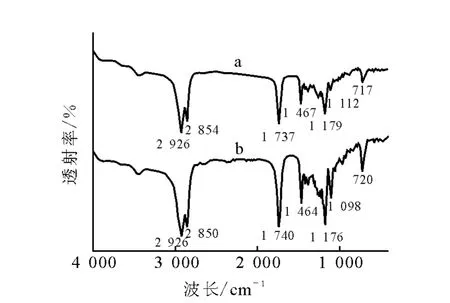
图6 13 C3-三硬脂酸甘油酯的FT-IR谱图a——合成产物;b——三硬脂酸甘油酯标准品
3.2.2 核磁共振谱(1H NMR、13CNMR)
13C3-三硬脂酸甘油酯和三硬脂酸甘油酯标准品的1H NMR谱图数据列于表1。
由于13C标记的化合物中,13C(自旋量子数I=1/2)会对同碳上的H(1J偶合)或邻碳上的H(2J偶合)存在耦合,且同碳耦合,耦合常数较大,一般大于100 Hz。由表 1可知,产物 δ=5.26,δ=4.29,δ=4.13处13C 对 H 均存在明显的裂分,且其耦合常数 J分别为 148.8 Hz,148.8 Hz和151.1 Hz。而对应的三硬脂酸甘油酯标准品 δ=5.26,δ=4.28和 δ4.14处均无相关裂分。以上结果表明,合成产物为13C3-三硬脂酸甘油酯。
13C3-三硬脂酸甘油酯和三硬脂酸甘油酯标准品的13C NMR谱图数据列于表2。

表1 13 C3-三硬脂酸甘油酯和三硬脂酸甘油酯标准品的1H NMR
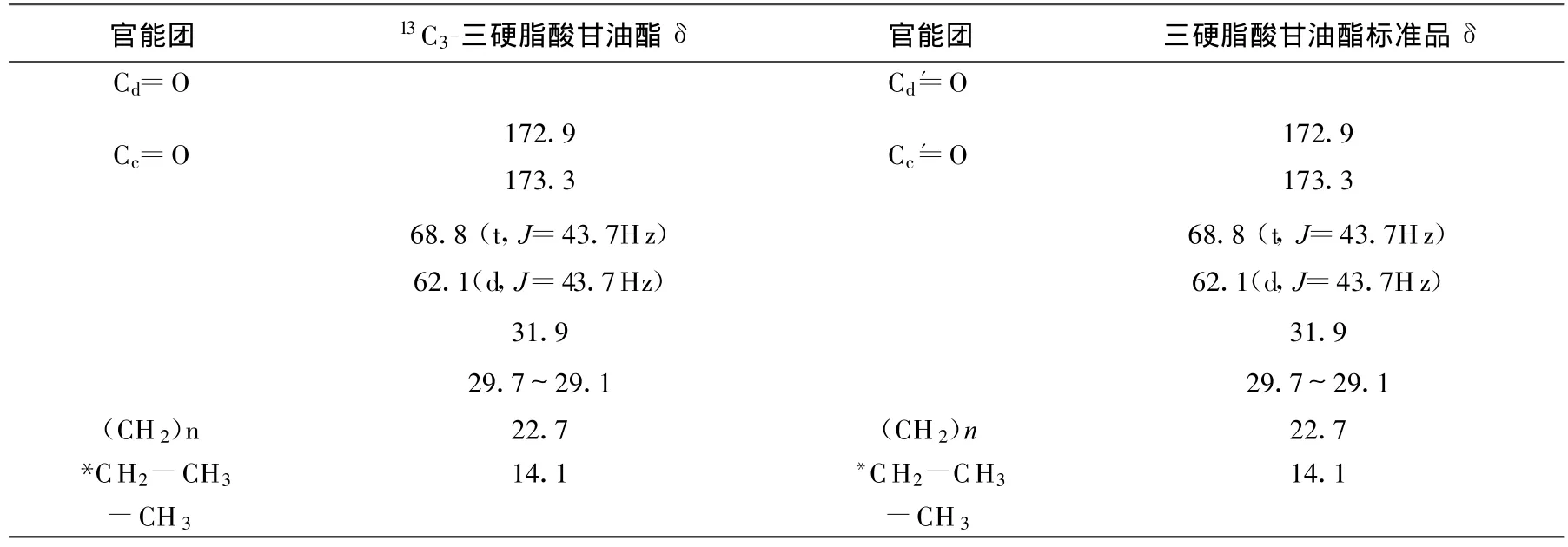
表2 13 C3-三硬脂酸甘油酯和三硬脂酸甘油酯标准品的13 C NMR
与1H NMR结果相似,在13C标记化合物的13C NMR谱图上同样存在着13C对相邻碳的耦合。由表2可知,产物在δ=68.8和δ=62.1处均存在明显的耦合。δ=68.8处对应的官能团为甘油酯中间的碳C-b,δ=62.1处对应官能团为两端的碳C-a,其中C-a化学环境相同,皆对C-b存在耦合,使得 C-b生成三重峰(J=43.7 Hz),同时C-a受C-b耦合生成双峰(J=43.7 Hz)。而在未标记的13C NMR谱图中,化学位移δ=68.8和δ=62.1处呈现的则是两个单峰。因此进一步证明合成产物为13C3-三硬脂酸甘油酯。
3.2.3 质谱(MS)
13C3-三硬脂酸甘油酯和三硬脂酸甘油酯标准品的质谱检测结果列于表3。

表3 13C3-三硬脂酸甘油酯和三硬脂酸甘油酯标准品的质谱裂解碎片离子
在质谱分析中,[RCO]+、[M-RCOO]+、[RCO+74]+以及[RCO+128]+是4类用于鉴定三硬脂酸甘油酯的碎片离子[8]。由表 3可知,13C3-三硬脂酸甘油酯上述特征离子m/z分别为 267、344、398、610,而非标记三硬脂酸甘油酯m/z分别为264、341、395和 607,两者对比,m/z相差3,这是因为有13C3同位素的存在。此结果说明合成的标记产物为13C3-三硬脂酸甘油酯。
根据质谱峰强度可计算产物13C3-三硬脂酸甘油酯中的13C丰度。计算公式为13C丰度=[I M+3/(I M+I M+3)]×100%(I为碎片离子强度),利用质量数398计算13C丰度,计算结果列于表4。由表4可见,13C丰度为99.49%。
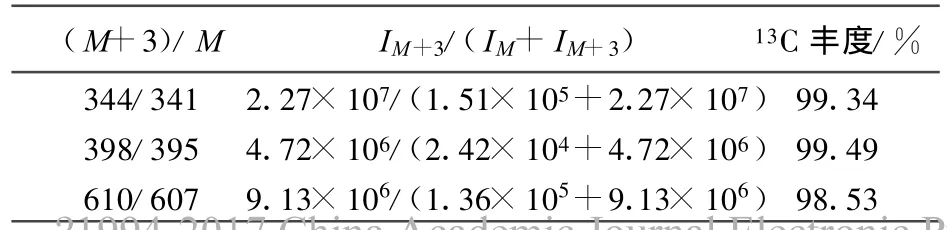
表4 根据质谱峰强度计算13 C3-三硬脂酸甘油酯中13 C的丰度
3.2.4 产物熔点测定
13C3-三硬脂酸甘油酯和三硬脂酸甘油酯标准品的差示扫描量热分析(DSC)谱图示于图7。由图7可知,合成的产物熔点为56.496℃,三硬脂酸甘油酯标准品的熔点为59.669℃,均在三硬脂酸甘油酯熔点范围53~62℃[7]内,说明合成的产物为三硬脂酸甘油酯。根据图7计算得其化学纯度>98%。
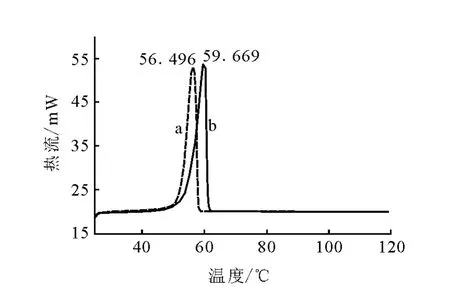
图7 13 C3-三硬脂酸甘油酯的DSC谱图a——合成产物 ;b——三硬脂酸甘油酯标准品
3 小 结
以摩尔比n(硬脂酸)∶n(13C3-甘油)=2.8∶1,采用生物Lipozyme酶作为催化剂,在无毒有机溶剂的存在下,直接酯化合成13C3-三硬脂酸甘油酯,产物无需纯化,产率可达80%。产物经差示扫描量热分析(DSC)、红外光谱(FT-IR)、核磁共振(1H NMR)、质谱(MS)分析表征,结果表明,合成产物为13C3-三硬脂酸甘油酯,且化学纯度>98%,同位素丰度>99%,均符合技术指标要求。与传统工艺比较,该合成工艺高效、经济合理,具有重要应用价值。
[1] 徐大刚,钟授富.稳定同位素的分离与应用[J].化学进展,1997,5(2):41-46.
[2] 孙雨安,刘保霞,程定玺,等.稳定同位素及其在卫生检验中的应用[J].中国卫生检验杂志,2004,12(4):387-389.
[3] Yannick Pouilloux,Sébastien Métayer,Joël Barrault.Synthesis of glycerol monooctadecanoate from octadecanoic acid and glycerol:Influence of solvent on the catalytic properties of basic oxides[J].Comptes Rendus de l'Académiedes Sciences-Series IIC-Chemistry,2000,3(7):589-594.
[4] Ergan F,Trani M,Andre'G.Production of glycerides from glycerol and fatty acid by immobilized lipase in non-aqueous media[J].Biotechnology and Bioengineering,1990,35:195-200.
[5] Selmi B,Gontier E,Ergan F,et al.Effects of fatty acid chain length and unsaturation number on triglyceride synthesis catalyzed by immobilized lipase in solvent-free medium[J].Enzyme and Microbial Technology,1998,23(3):182-186.
[6] 李蕾,林琳,俞玮瑄,等.碳-13标记甘油三酯的合成方法:中国,CN200910079434.4[P].2010-09-15.
[7] 毕艳兰.油脂化学[M].北京:化学工业出版社,2005:87-88.
[8] Kalo P,Kemppinen A.Mass spectrometric identification of triacylglycerols of enzymatically modified butterfat separated on a polarizable phenylmethylsilicone column[J].JAmOil Chem Soc,1993,70(12):1 209-1 217.

