地被菊直接体细胞胚发生的优化
蒋 凡,黄寿先,张皓磊,蒋细旺
(1.广西大学 林学院,广西 南宁530004;2.江汉大学 生命科学院,湖北 武汉430056)
1 引言
体细胞胚的诱导主要有两种途径:一是直接由叶片的叶脉及脉间表皮细胞分裂产生(直接类型):二是首先由茎段脱分化成愈伤组织,然后由这些愈伤组织的某些细胞形成体细胞胚(间接类型)[1]。由叶片的表皮细胞分裂产生体细胞胚,取材容易,诱导体细胞胚的速度快。
直接体细胞胚发生途径形成的体胚,发生频率高,无畸形胚产生,生长健壮,分化能力强,成苗率高,而且直接体细胞胚的再生植株变异频率低[2]。直接体细胞胚具有很强的接受外源DNA的能力,是理想的基因转化感受态细胞;而且胚性细胞繁殖量大,同步性好,转化后的胚性细胞可顺利发育成胚状体及完整的转基因植株。大量研究表明,直接体细胞胚发生多是单细胞起源,转化获得的转基因植株嵌合体少[3,4],因此,植物通过直接体细胞胚发生形成的体细胞胚可作为理想的遗传转化受体体系[5,6]。
蒋细旺等[7]在对地被菊“玉人面”直接体细胞胚发生研究中发现,叶片经体细胞胚诱导培养基(MS+KT 2.0mg/L+2,4-D 2.0mg/L+NAA 0.5mg/L)诱导10 d后,发现有薄层愈伤的出现,转接到体细胞胚发育培养基(MS+KT 2.0mg/L+NAA 0.5mg/L)中,13d后,发现有大量淡黄色颗粒突起,同时愈伤量会增多,到15d时发现有大量芽点出现,到17d时发现有大量芽出现,到24d时,又有一批球状颗粒突起,到30d时,能显著观察到分化出两批植株,高度相差约5mm,高度比值约3~4倍。这两批植株的出现时间相差大约7~10d。而且由上述诱导的体细胞胚再生出的苗容易玻璃化,体细胞胚发育为芽之前,叶片外植体表面上容易生根,由体细胞胚发生途径转化为器官发生途径;薄层愈伤的出现,也会有一部分体细胞胚是间接体细胞胚发生。
由于3种方式发生的时间不一致,在遗传转化时,农杆菌侵染的最佳时间也会有差异,而使转化效率低下。目前对地被菊直接体细胞胚发生中出现器官发生途径及间接体细胞胚发生途径该如何克服的研究较少。达克东[8]在苹果离体叶片培养诱导直接体细胞胚胎发生研究中发现,2,4-D是使外植体产生薄层愈伤组织的原因之一,叶片在含有2,4-D的培养基中处理时间过长是使外植体产生愈伤组织的原因之二,通过缩短胚性细胞诱导时间和减少诱导培养基中蔗糖量来减少叶片直接体细胞胚发生中的间接体细胞胚发生的百分率来得到优化。而张健[9]通过提高诱导培养基中的蔗糖浓度到(5%~10%),来提高柑桔幼胚的直接体细胞胚的诱导率来得到优化。马国华[10]在木薯嫩叶直接诱导初生体细胞胚胎发生和芽的形成的研究中,发现NAA不仅能够诱导木薯嫩叶产生体细胞胚,而且能够直接诱导芽的形成,其它几种生长素类化合物如2,4-D、dicamba或picloram等只能直接诱导体细胞胚胎发生,所不同的是这种NAA诱导的木薯体细胞胚胎发生和芽的器官发生几乎是同步进行的,但它们之间在形态上和植株再生的时间及方式上存在较大的差异。
2 材料与方法
“玉人面”‘Yurenmian’(白花)由北京林业大学陈俊愉院士提供。MS培养基为基本培养基,试验激素分别为2,4-D(2,4二氯苯氧乙酸)、KT(激动素)、NAA(萘乙酸)。
2.1 无菌苗的获得和叶片外植体的准备
按蒋细旺等[11]的方法和培养条件获得无菌苗并继代。从新增殖(4周左右)的幼苗上切取嫩叶,并去除叶缘切成约0.5cm2的叶片,以近轴面接触培养基。每培养皿接种25个外植体,重复5次。
2.2 玉人面的诱导培养时间对体细胞胚发生的影响
按蒋细旺等[7]的方法和培养条件,进行体细胞胚的诱导,即在诱导培养基MS+KT 2.0mg/L+2,4-D 2.0mg/L+NAA 0.5mg/L中,分别诱导培养3d、5d、7d、10d和15d,然后转入 MS+KT2.0mg/L+NAA0.5mg/L中培养。蔗糖浓度为30g/L,琼脂糖浓度为6g/L,pH 值为6.0,培养温度为(25±2)℃,日光灯光源,光照(2 000lx)12h·-1。一共培养25d后,计算直接体细胞胚发生率、平均每外植体分化的体细胞胚数、体细胞胚发育为芽前的生根率及玻璃化率。
2.3 不同蔗糖浓度对玉人面体细胞胚诱导的影响
外植体先在 MS+KT 2.0mg/L+2,4-D 2.0mg/L+NAA 0.5mg/L中培养5d,其中蔗糖浓度分别为10g/L、30g/L和60g/L;然后分别转入含10g/L、30g/L、60g/L蔗糖的 MS+KT 2.0mg/L+NAA 0.5mg/L培养基中培养。一共培养25d后,计算直接体细胞胚发生率、平均每外植体分化的体细胞胚数、体细胞胚发育为芽前的生根率及玻璃化率。
2.4 激素对体细胞胚诱导的影响
外植体先培养在 MS+KT 2.0mg/L+2,4-D 2.0mg/L+NAA 0.5mg/L中,蔗糖浓度为10g/L,诱导5d后;转入MS+KT+NAA,其中的KT浓度为(0、0.5、1.0、2.0、4.0mg/L),NAA 浓度为(0、0.5mg/L),共20个组合,蔗糖浓度为30g/L。共计培养25d后,计算直接体细胞胚发生率、平均每外植体分化的体细胞胚数和体细胞胚发育为芽前的生根率。
2.5 数据统计与分析
所得数据采用SAS软件进行方差分析与多重比较(LSD法,P=0.05)。
(1)体细胞胚发生率(%)=产生体细胞胚的外植体个数/外植体总数×100%。
(2)平均每外植体体细胞胚发生个数=所有外植体产生的体细胞胚个数/外植体总数×100%。
(3)体细胞胚发育为芽前的生根率=外植体生根的个数/外植体总数×100%。
3 实验结果分析
3.1 诱导培养时间对玉人面体细胞胚发生的研究
体细胞胚发生率在诱导培养7d时最高,达100%,诱导培养超过7d或少于7d体细胞胚发生率都会稍降低;每个外植体体细胞胚发生的数量在10d达到12.3个,诱导培养超过10d或少于10d每个外植体体细胞胚发生的数量不同程度的减少;仅诱导培养3d时体细胞胚发育为芽前,没有有根的生成,其它诱导培养时间有不同程度的生根;薄层愈伤量在各个培养时间均有,但程度不同。可见不同诱导培养时间对体细胞胚发生率、每个外植体体细胞胚发生的数量、生根率、薄层愈伤量影响均较大(表1)。最终筛选出7d为最优诱导培养时间,见图1。

表1 玉人面的诱导培养时间对体细胞胚发生的研究

图1 经过7d诱导培养的玉人面体细胞
3.2 不同蔗糖浓度对玉人面体细胞胚诱导及发生的调控研究
直接体细胞胚诱导阶段,若培养基的蔗糖浓度过高,经诱导后,易出现薄层愈伤,产生间接体细胞胚,体细胞胚萌发获得的苗易玻璃化;直接体细胞胚发生阶段,若培养基的蔗糖浓度过高,获得的苗容易黄化。若直接体细胞胚一直用高浓度的蔗糖,愈伤程度很大,获得的苗极度畸形,大部分是通过间接体细胞胚获得的苗。若一直用低浓度的蔗糖,体细胞胚发生率及每个外植体体细胞胚发生的数量很低。可见蔗糖浓度的变化对体细胞胚发生率、每个外植体体细胞胚发生的数量、生根率、薄层愈伤量影响也较大(见表2)。优化结果:直接体细胞胚诱导阶段用10g/L的蔗糖,体细胞胚发育阶段用30g/L的蔗糖,见图2。

表2 不同蔗糖浓度对玉人面体细胞胚诱导及发生的调控研究
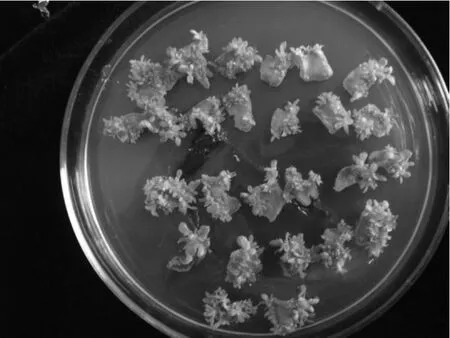
图2 用蔗糖浓液诱导培养的玉人面体细胞
3.3 激素浓度对玉人面体细胞胚发生的研究
对于加了NAA的培养基,体细胞胚发生率、每个外植体体细胞胚发生的数量及生根率均比没加NAA的培养基的要高。但加了NAA后,在体细胞胚发育成植株前易生根,容易走器官发生途径。所以在地被菊“玉人面”体细胞胚发生途径中,应去掉NAA,在体细胞胚发生前就不会有根的形成,培养25后,待芽长出后,才有根的形成。在没加NAA的五种培养基中,KT为2.0时,体细胞胚发生率及每个外植体体细胞胚发生的数量均最高。优化后的结果:直接体细胞胚发育培养基应去掉NAA,仅用2.0mg/L的KT的培养基,见图3。
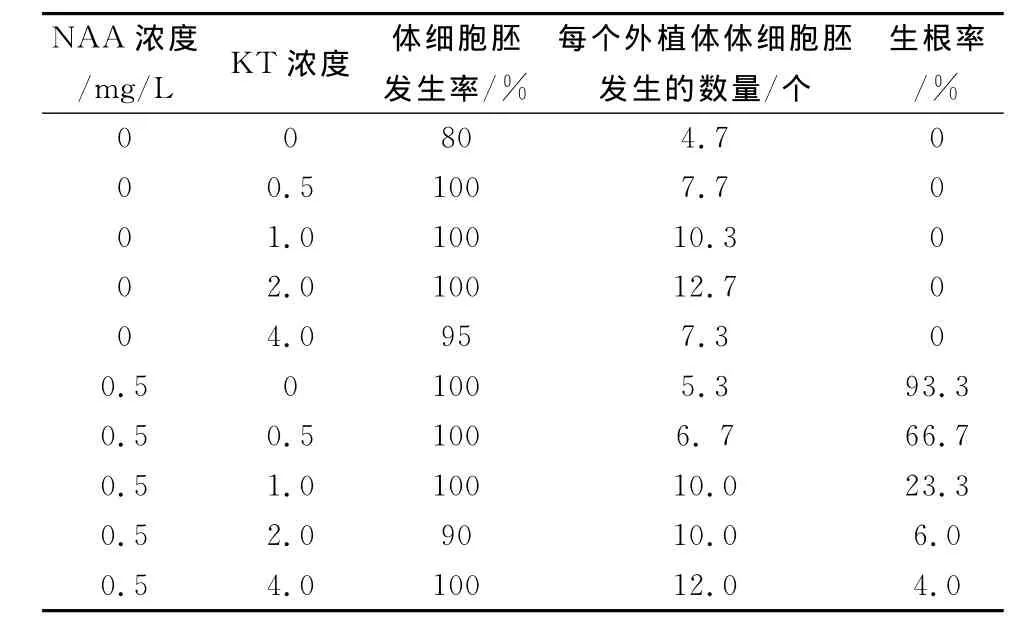
表3 激素浓度对玉人面体细胞胚发生的研究

图3 用激素浓液诱导培养的玉人面体细胞
4 结语
本文研究得到,地被菊“玉人面”的直接体细胞胚诱导最佳时间为7d,诱导7d后转入去除2,4-D的培养基中进行体细胞胚的发育。崔凯荣[12]等研究发现体胚诱导后必须去掉2,4-D。2,4-D的作用具有阶段性,在诱导阶段通常起促进作用,而在胚状体分化发育阶段一般起抑制作用。周俊彦[13]等研究也发现2,4-D对胡萝卜的体胚前期诱导有利,对后期发育抑制。2,4-D的阶段性抑制作用,目前可从三个水平上得到证实。在生理水平上,Tisserat B[14]等认为2,4-D 可能通过促进乙烯合成而抑制体胚发育。这种抑制体胚发育已为胡萝卜、枸杞、三叶草,芹菜等许多植物体胚发生所证实[15-16]。在分子水平上,韩碧文[17]等进一步研究发现,2,4-D通过抑制胚胎发育基因的程序表达来抑制体细胞胚的后期发育。在信号转导水平上,崔凯荣[18]等认为2,4-D是先与细胞内生长素结合蛋白(ABP)作用,然后通过细胞内信号传递系统,激活某些基因的表达,产生特异的mRNA,而促进体细胞胚发生;但是,一段时间后,它又可以抑制这些基因的表达,激活另一些基因的表达,从而防碍体细胞胚的进一步发育,认为2,4-D对基因表达的调控有时空特异性。本文的研究结果认为,诱导时间低于7d可能是诱导时间不够,直接体细胞胚发生相关基因没有充分诱导表达,而使直接体细胞胚发生率和每个外植体上直接体细胞胚发生的数量较低;诱导时间多于7d,在2,4-D的培养基中暴露时间过长,抑制了直接体细胞胚发育相关基因的程序表达来抑制体细胞胚的后期发育,进而使直接体细胞胚发生途径转向间接体细胞胚发生途径,导致产生薄层愈伤。
蔗糖量的增加会引起外植体愈伤组织量的增加和间接类型体细胞胚发生,适当减少培养基中蔗糖量有利于叶片直接体细胞胚诱导;在直接体细胞胚发育的过程中,提高蔗糖浓度,抑制体胚迅速发育为植株和大量根的生成,促进胚胎的发育并停留在球形胚期,调控胚胎发育。培养基中的糖除了提供培养物的碳源以外还起着调节渗透压的作用,一般在体胚诱导阶段需要较低的蔗糖浓度[19],而在体胚成熟阶段则需要较高的蔗糖浓度[20]。分子水平上,蔗糖如何调控胚胎的发育,程玉兰[21]等认为在体胚发育过程中,蔗糖浓度可导致体胚内源ABA水平的变化,表现为:60S,ABA含量稍微有下降,并趋于稳定,胚也逐渐进入静止状态,并停留在晚期子叶胚后,不再继续发育,而在胚根处产生大量的次生胚;对30S,ABA含量缓慢下降,并开始初生根的发育,但初生根的发育缓慢;在10S中,其内源ABA含量急剧下降,胚的形态建成后就迅速开始胚后发育,子叶胚迅速长成小苗,根长度伸长至胚体的几倍。显然:在体胚发育过程中,高浓度的ABA水平有利于胚性状态的维持。本研究也观察到这一现象。进一步有学者研究,刑更生[22]等认为ABA通常对DNA和RNA的合成有抑制作用,但对某些植物体细胞胚发生的特异基因表达则起调控作用,抑制体细胞胚过早萌发。但这种分子调控机制需进一步研究。
本研究在体细胞胚发育阶段去掉NAA后,在体细胞胚发育成植株前没有根的生成。有理由认为:NAA不仅能够诱导叶片产生体细胞胚,而且能够直接诱导芽的形成。这和马国华[10]的研究结果相同。
[1]Sharp W R,Sondahl M R,Caldas L S,et a1.The physiology of in vitro asexual embryogenesis[J].Hort Rev,1980(2):268~310.
[2]周丽侬,曹 静,邝哲师,等.园艺植物体胚发生及植株再生技术研究[J].热带作物学报,1998,19(2):15~19.
[3]Shinoyama H,Nomura Y,Tsuchiya T,et al.A simple and efficient method for somatic embryogenesis and plant regeneration from leaves of chrysanthemum[J].Plant Biotechnology,2004,21(1):25~33.
[4]Mandal A K A,Datta S K.Direct somatic embryogenesis and plant regeneration from ray florets of chrysanthemum[J].Biologia Plantarum,2005,49 (1):29~33.
[5]洪 波,全 征,李邱华,等.地被菊花Fall Color体细胞胚途径再生、遗传转化及转基因植株的抗寒性检测[J].中国农业科学,2006,39(7):1 443~1 450.
[6]Blanc G,Baptiste C,Oliver G,et al.Efficient Agrobacterium tumefaciens-mediated transformation of embryogenic calli and regeneration of Hevea brasiliensis Mull Arg.plants[J].Plant Cell Rep,2006(24):724~733.
[7]蒋细旺,陈发菊,陆 苗,等.地被菊直接体细胞胚发生研究[J].北京林业大学学报,2008,30(2):65~70.
[8]达克东,张 松,李雅志,等.苹果离体叶片培养直接体细胞胚胎发生研究[J].园艺学报,1996,23(3):241~245.
[9]张 健,吕柳新.柑桔幼胚培养的直接体细胞胚发生与植株再生[J].河南科技大学学报,2006,26(6):82~84.
[10]马国华,许秋生,羡蕴兰.从木薯嫩叶直接诱导初生体细胞胚胎发生和芽的形成[J].植物学报,1998,40(6):503~507.
[11]蒋细旺,刘国锋,包满珠.菊花9个品种叶片和茎段快速高效再生体系的建立[J].华中农业大学学报,2003,22(2):162~166.
[12]崔凯荣,邢更生,周公克,等.植物激素对体细胞胚胎发生的诱导与调节[J].遗传,2000,22(5):349~354.
[13]周俊彦.植物体细胞在组织培养中产生的胚状体Ⅱ.影响植物胚状体发生和发育的因素[J].植物生理学报,1982,8(1):91~99.
[14]Tisserat B,Murash ige T.Effects of ethephon,ethylene,and 2,4-dich lorophenoxyacetic acid on asexual embryogenesis in vitro[J].Plant Physiol,1977(60):437.
[15]Nadel BL,Altman A,Liv M.Regulation of somatic embryogenesis in celery cell suspension 2.Early detection of embryogenic potential and the induction of synch ronized cell cultures[J].Plant Cell T issue and Organ Culture,1990(20):119~124.
[16]Parrott WA.A uxin2stimulated somatic embryogenesis from immature cotyledons of white clover[J].Plant Cell Rep,1991(10):17~21.
[17]韩碧文,刘淑兰.植物离体体细胞胚胎发生[J].植物生理学通讯,1988(10):9~15.
[18]崔凯荣,刑更生,刘新民,等,细胞信号传导与植物体细胞胚发生[J].生命科学,2002,14(3):171~176.
[19]Gupta P K,Grob J A.Somatic embryogenesis in conifers.In:Jain SM,Gupta PK,Newon PJ(eds).Somatic Embryogenesis in woody Plants[M].The Netherlands:Kluwer.Academic Publishers,1995.
[20]Hetherington AM,Quatrano RS.Mechanisms of action of abscisic acid at a cellular level[J].New phytol,1991(119):9~32.
[21]程玉兰,黄美娟,刁丰秋,等.蔗糖调控培养对胡萝卜体细胞胚内源 ABA水平的效应[J].植物学报,1999,41(7):761~765.
[22]刑更生,崔凯荣,山 仑,等.植物体细胞胚发生的分子基础[J].遗传,1999,21(1):30~34.

