浓硫酸性质实验改进两例
魏崇启 牛永香
浓硫酸性质实验改进两例
魏崇启 牛永香
(江苏省丰县中学江苏丰县221700)
对浓硫酸性质实验:“黑面包”实验以及铜与浓硫酸的反应实验进行了改进,增强了实验的可操作性。
浓硫酸性质实验;改进
一、“黑面包”实验
浓硫酸与蔗糖的“黑面包”实验体现了浓硫酸的三大特性即吸水性、脱水性和强氧化性,因此该实验是浓硫酸性质的重要实验。但是该实验往往由于污染严重,而被多数老师变为黑板实验,或者以播放视频取代,不能给学生直观的印象,更谈不上能力的培养。经过多次实验,笔者进行改进使得该实验不但操作简单且现象明显,真正实现了绿色化。
1.实验仪器及试剂
普通试管1支、小气球1只、注射器1支、试管夹、胶头滴管、药匙、酒精灯、火柴、玻璃棒、滤纸、蔗糖、98%浓硫酸、蒸馏水、品红溶液、6moI·L-1NaOH溶液
2.实验装置(如图1)

图1
3.实验步骤
①取1支两头带有橡皮塞的弯导管,在扎气球一端塞入一小滤纸条,用胶头滴管滴几滴品红溶液将其润湿,然后套上气球用透明胶带缠紧并赶出气体备用。
②在试管中加入1g蔗糖,1~2mL浓硫酸,用胶头滴管滴入2滴蒸馏水后用螺旋铁丝迅速搅拌,然后塞上橡皮塞(预先准备的上述带玻璃弯管和螺旋铁丝的橡皮塞)。蔗糖先变黄后变黑并逐渐膨胀,气球慢慢鼓起,吸有品红溶液的滤纸条褪色。
③待吸有品红溶液的滤纸条褪色后,用酒精灯对其加热,滤纸条恢复原来的红色。
④实验结束后,等试管冷却后小心用注射器将6moI·L-1NaOH溶液注入气球,吸收生成的酸性气体以免污染环境。
⑤抽出铁丝将黑色固体带出,便于清洗试管。
4.本实验的特点
实验操作简便易行、现象明显,真正实现了实验的绿色化,有较强的趣味性,节省实验时间,适合课堂演示或学生实验。
二、铜与浓硫酸反应实验
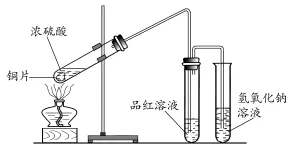
图2
在按苏教版化学必修1p92实验3(如图2)进行操作时发现,该实验有以下缺点:①因SO2在NaOH溶液中的溶解度大,所以易于产生倒吸现象。②铜片与浓硫酸反应不易控制。③产生气流较快SO2可能没来得及充分吸收就逸出而造成污染。在准备县公开课时,我对该实验做如下改进。
1.实验仪器及试剂
具支试管1支、注射器1支、酒精灯、气球1只、滤纸、玻璃导管、单孔橡皮塞2只、一端弯成螺旋状的铜丝1根、铁架台、98%浓硫酸、品红溶液、6moI·L-1NaOH溶液
2.实验装置(如图3)

图3
3.实验步骤
①取1支带有橡皮塞的玻璃导管,在扎气球一端塞入一小滤纸条,用胶头滴管滴几滴品红溶液将其润湿,然后套上气球用透明胶带缠紧并赶出气体备用。
②在具支试管中加入约2mL浓硫酸,塞上带有可抽动的铜丝的单孔橡皮塞(注意铜丝不接触浓硫酸)。用酒精灯将浓硫酸加热至接近沸腾后,将可抽动的铜丝送入浓硫酸液面下。反应开始后撤走酒精灯,当气球膨胀且吸有品红溶液的滤纸条褪色后,立即将铜丝提起。
③待吸有品红溶液的滤纸条褪色后,用酒精灯对其加热,滤纸条恢复原来的红色。
④实验结束后,小心用注射器将6moI·L-1NaOH溶液从橡胶管处注入气球,吸收生成的酸性气体。
⑤待气球变瘪后,取下玻璃导管和橡皮塞,倾去上层溶液,将试管底部的白色晶体加适量蒸馏水溶解,溶液变蓝。
4.本实验的特点
可抽动的铜丝可以控制实验,气球既起到防止倒吸的作用又可以使污染降到最低。实验节约试剂,操作简单,实验现象明显,节省实验时间,适合课堂演示或学生实验。
[1]王祖浩主编.普通高中课程标准实验教科书:化学1(必修)[M].南京:江苏教育出版社,2010:92
1008-0546(2011)11-0092-01
G633.8
B
10.3969/j.issn.1008-0546.2011.11.044

