胃转流术对2型糖尿病大鼠降糖作用及 DPP-IV分泌的影响
史逸华,王跃生,陈福军
(佳木斯大学第一附属医院普外一科,黑龙江 佳木斯 154003)
上世纪 50年代,减肥手术开始用于治疗肥胖症,最初的临床观察发现,肥胖患者术后不仅体重显著下降,而且其并发的非胰岛素依赖型糖尿病得到意想不到的治愈或改善[1]。但这一现象并未引起关注,至1998年,East Carolina大学Brody医学院的 Pories等在 Annals of Surgery杂志报道了减肥手术后的随访研究结果[2],才引起了学术界的高度重视。目前研究趋向于术后胃肠道激素分泌改变,术后消化道功能分为两个区域:(1)食物转流区:这段上消化道术后不再受食物刺激,导致分泌及合成“致糖尿病因子”减少如 DPP-IV。(2)食物流经区。本实验将对胃转流术的降糖作用及其可能机制做初步研究。
1 材料与方法
1.1 实验材料
清洁级近交系雄性 SD大鼠45只,体重 270~290克 /只,0.5%戊巴比妥钠,链尿佐菌素(Sigma公司,美国),DPP-Ⅳ酶联免疫吸附测定试剂盒,全自动血糖仪,低温离心机,柠檬酸钠-柠檬酸缓冲液(pH4.4),柠檬酸钠-柠檬酸缓冲液(pH4.4)10mL都由佳木斯大学实验室提供。
1.2 动物模型的建立
16~ 25℃,SD大鼠,按体重随机分组为造模组 25只和非造模组20只。对造模组25只制造糖尿病大鼠的模型,正常饮食1周,2d后按35mg/kg,于左下腹穿刺,腹腔内一次注射1%的 STZ溶液,一周和2周后空腹情况下取大鼠尾静脉血,快速血糖仪检测,两次均大于或等于13.6mmol/L为成功模型,稳定5d为成功模型,共有22只成模[3]。成模率88%。
1.3 实验分组
实验动物分组将非造模组随机分为假手术组(NC)和手术组(NO),造模组随机分为造模假手术组(DC)和造模+手术组 (DO)。每组 10只 (其余鼠备用 )。术前 NC、 NO、DO、 DC组之间体重、平均进食量无显著性差异。
1.4 检测方法
用全自动血糖仪检测血糖值。DPP-IV测定方法:大鼠采用断尾取血法采血,将收集于血清分离管的全血标本在室温静置30min,然后3000r/min离心离心20min,取上清即可检测,或将上清置于-20℃或-80℃冰箱保存,统一时间用DPP-Ⅳ酶联免疫吸附测定试剂盒检测。
1.5 统计学分析
2 结果
2.1 血糖
与术前相比,DO组术后第72小时空腹血糖已开始下降(P<0.05),术后各时相点 DO组的空腹血糖明显低于相应时间点 DC(P<0.05);NO组、DC组、NC组手术前后空腹血糖无明显改变,术前术后血糖变化无统计学意义(P > 0.05)。见表 1。
表1 各组血糖变化 (± s,mmol/L)

表1 各组血糖变化 (± s,mmol/L)
注:DO组与术前相比较*P<0.05;DO组与 DC组比较☆P<0.05。
组别 DO DC NO N C术前 20.84± 1.98 20.79± 1.70 4.67± 0.19 4.45± 0.12术后 72h 12.50± 0.82* 22.02± 0.64☆ 4.89± 0.17 4.57± 0.20术后1周 11.29± 0.62* 21.40±0.64☆ 4.74±0.14 4.59± 0.15术后4周 5.47± 0.47* 22.21±1.05☆ 4.54±0.19 4.37± 0.55术后8周 5.58± 0.11* 21.44±0.68☆ 4.78±0.68 4.35± 0.09
2.2 DPP-IV
与术前相比,D0组手术后第72小时空腹血清 DPP-Ⅳ已开始明显下降 (P <0.05)。N0组术后72h空腹血清 DPP-Ⅳ下降 (P<0.05);术后各时相点 DO组的空腹血清 DPP-Ⅳ明显低于相应时间点 DC组 (P<0.05),术后各时相点NO组的空腹血清 DPP-Ⅳ明显低于相应时间点 N C组(P<0.05);DC组,NC组手术前后空腹血清 DPP-Ⅳ值无明显变化。见表2。
表2 各组 DPP-IV变化 (± s,μ g/L)
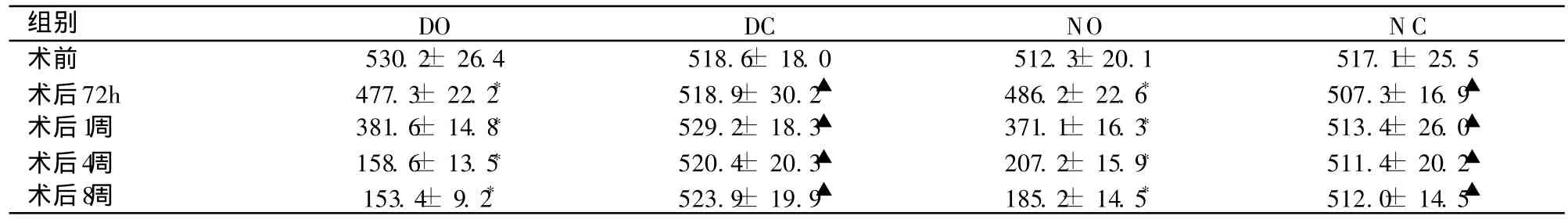
表2 各组 DPP-IV变化 (± s,μ g/L)
注:DO、NO组与术前相比较*P <0.05;DO组与 DC、NO组与 NC组比较▲P <0.05。
组别 DO DC NO N C术前 530.2± 26.4 518.6± 18.0 512.3± 20.1 517.1± 25.5术后 72h 477.3± 22.2* 518.9± 30.2▲ 486.2± 22.6* 507.3± 16.9▲术后1周 381.6± 14.8* 529.2±18.3▲ 371.1±16.3* 513.4±26.0▲术后4周 158.6± 13.5* 520.4±20.3▲ 207.2±15.9* 511.4±20.2▲术后8周 153.4±9.2* 523.9±19.9▲ 185.2±14.5* 512.0±14.5▲
3 讨论
3.1 胃转流术对2型糖尿病的治疗作用
GBP术降低血糖的机制刚开始认为是 GBP后肥胖症患者饮食减少和体重下降的结果[4],但后来对 GBP术后更长期的随访以及动物实验,否定了此观点。本实验使用 SD雄性大鼠制造非肥胖的2型糖尿病模型,GBP术后糖尿病大鼠的空腹血糖由术前的(20.84±1.98)mmol/L下降至术后第 8周的 (5.58±0.11)mmol/L(P < 0.05)。2008年黑龙江省第一例 GBP手术是由我院首次开展,患者术后2个月后停用所有药物和胰岛素,且饮食正常,血糖、胰岛素、糖基化血蛋白保持正常水平,目前随访血糖未出现反弹。
3.2 DPP-IV与 GBP后糖尿病大鼠血糖改善中的关系
目前大多数研究倾向于手术机制可能与肠-胰岛轴的分泌改变有关。正常情况下食物经过胃、十二指肠、空肠和回肠,并被消化吸收,胃转流手术的独特之处在于改变了食物的正常生理流向,手术通过阻断胃、胃肠吻合、肠肠吻合等步骤最终完成。术后消化道功能分为两个区域:(1)食物转流区:远端的胃、十二指肠及部分近段空肠,这段上消化道术后不再受食物刺激,导致分泌及合成“致糖尿病因子”减少,如DPP-IV;(2)食物流经区:近端胃、远段空肠及回肠,这段消化道提前接纳未消化或未完全消化的食物,导致降糖类分泌激素增加如 GLP- 1。目前认为以 DPP-IV和 GLP-1这 2种激素最受关注,其中以 DPP-IV为最终点,且市场上已出现了 DPP-IV的抑制剂,发展最好的 DPP-Ⅳ抑制剂有默克公司的 sitagliptin(Januvia)中文名叫捷诺维 ,于2006年10月经美国 FDA批准上市,本实验亦是根据此药得到的启发。DPP-IV[5]最初被认为是一种 T细胞活化抗原 CD26。DPP-Ⅳ在哺乳动物组织中表达较广泛,但以十二指肠,近端空肠表达为主,DPP-Ⅳ可以迅速且特异性地裂解胰高血糖素样肽-1(GLP-1),从而使其失去活性,影响 GLP-1的血糖调节等生理反应。GLP-1的主要作用有:① GLP-1刺激胰岛素分泌,抑制胰高血糖素分泌;② GLP-1改善β细胞功能;③GLP-1延缓胃排空;④GLP-1作用于胰岛 α细胞 ,呈葡萄糖浓度依赖性抑制胰高血糖素的分泌。但由于天然 GLP-1在体内很快被 DPP-Ⅳ降解,其半衰期仅有 1~ 2min,补充外源性 GLP-1,很快会被 DPP-IV降解,临床价值不大。目前上市的 DPP-IV口服抑制剂被证明可以降低 DPP-IV的含量和活性,从而提高内源性 GLP-1水平,延长其活性,使其能够在血糖升高时控制糖尿病患者的血糖水平[6]。本实验 GBP大鼠 DPP-IV由术前(530.2±26.4)μg/L至术后第8周下降为 (153.4± 9.2)μg/L(P < 0.05)。提示 DPP-IV在 GBP改善糖尿病大鼠血糖中起重要作用。NO组 DPPIV由术前的 (512.3± 20.1)μ g/L下降到术后 8周的 (185.2±14.5)μg/L(P<0.05),但手术对于 NO组大鼠血糖无影响,表明该手术不会影响正常大鼠血糖值。唯一的解释是 GLP-1可能具有血糖依赖性的肠促胰岛素分泌作用,随着血糖水平下降,GLP-1促胰岛素分泌作用减弱,故 GLP一 l的降血糖作用是自限性的,不会发生低血糖。
[1]Brolin RE.Bariatric surgery and long-term control of morbid obesity[J].JAM A,2002,288:2793-2796
[2]Shuhaiber JVitello J.Is gastric bypass associated with more complications in patients weighing> 500lb(> 227kg)[J].Obes Surg,2004,14(l):43-46
[3]张新国,杨学军,徐红,等.胃旁路手术治疗Ⅱ型糖尿病的体会[J].中华普通外科杂志,2005,20(9):599
[4]Patriti A,Facchiano E,Sanna A,et al.The enteroinsular axis and the recovery from type 2 diabetes after bariatric surgery[J].Obes Surg,2004,14(6):840-841
[5]DRUCKER DJ.Dipeptidyl peptidase-4 inhibition and the treatment of type2diabetes[J].Diabetes Care,2007,30(6):1335-1343.
[6]张立宏,王莉莉,李松.二肽基肽酶-Ⅳ抑制剂药理学作用及机制的研究进展 [J].Chinese Journal of New Drugs,2009,18(11):132-134

