交联辛烯基琥珀酸淀粉酯半干法合成工艺与改性机理研究
石海信,邓全道,刘灵芝,严凤英,方怀义
(1.钦州学院化学化工学院,广西 钦州 535000;2.钦州出入境检验检疫局,广西 钦州 535000)
交联辛烯基琥珀酸淀粉酯半干法合成工艺与改性机理研究
石海信1,邓全道2,刘灵芝2,严凤英1,方怀义1
(1.钦州学院化学化工学院,广西 钦州 535000;2.钦州出入境检验检疫局,广西 钦州 535000)
以环氧氯丙烷(ECH)和辛烯基琥珀酸酐(OSA)为改性剂,采用半干法工艺合成具有疏水亲脂性质的交联辛烯基琥珀酸淀粉酯(COSAS)。通过单因素及正交试验研究COSAS的合成工艺与反应机理,测定产品白度,并用红外光谱仪和扫描电镜对产品结构进行分析。结果表明:半干法合成COSAS的最佳工艺参数为淀粉含水量15%~18%、OSA用量3%(占淀粉干基分数)、酯化时间90min、pH9.0、温度100℃,在此工艺下制备的COSAS平均取代度为0.0175,白度值比原淀粉的稍低;红外光谱图证实了淀粉经交联酯化变性后引入了醚化交联键和辛烯基琥珀酸基团。扫描电镜显示淀粉颗粒表面受到侵蚀,部分颗粒出现凹陷、空隙和裂缝。
木薯淀粉;交联辛烯基琥珀酸淀粉酯;半干法;反应机理
传统的改性淀粉通常是在淀粉分子中引入亲水基团,加上淀粉本身的亲水性质,使产品只具有单一的亲水性。在淀粉分子中引入亲油基团可使淀粉的性质得到明显改善,从而使其在可降解包装材料、食品乳化稳定剂、阿拉伯胶替代品、微胶囊壁材等高附加值领域具有广泛应用前景。国内外对淀粉的疏水亲脂改性研究主要集中在酯化、交联、偶联改性等方面。Hu等[1]用环氧氯丙烷(epichlorohydrin,ECH)作为交联剂对淀粉进行变性处理后制备了疏水化交联淀粉(cross linked starch,CS),用作药物缓释剂;而用辛烯基琥珀酸酐(octenyl succinic anhydride,OSA)作为酯化剂对淀粉进行变性处理后得到的辛烯基琥珀酸淀粉酯(octenyl succinic anhydride modified starch,OSAS),因其分子中同时含有亲水亲油基团的独特结构特点而具有优良的乳化分散性能[2-3]。交联辛烯基琥珀酸淀粉酯(crosslinked octenyl succinic anhydride modified starch,COSAS)则是对淀粉进行交联与酯化双重变性处理后得到的一种新型疏水亲脂复合变性淀粉[4],兼有CS与OSAS的优点,从而使它具有更广泛的应用价值。
交联疏水亲脂淀粉的制备方法主要有湿法、干法等。其中湿法工艺指反应在液相中进行,工艺比较成熟,但存在着生产流程长、废水多、淀粉酯易发生水解副反应等问题[5]。干法则是在固相条件下进行反应,生产周期短、效率高,但也存在着混料不匀、对设备要求较高等缺陷[6]。近年来发展起来的半干法工艺,具有生产周期短、设备投资小,环境污染少等优点[7],正受到越来越多的关注,但目前还未有应用于生产COSAS的报道。本实验以ECH和OSA为疏水化改性剂,采用现代环保半干法工艺对木薯淀粉进行复合疏水亲脂改性,对COSAS合成工艺参数及反应机理进行研究,旨在为变性淀粉的半干法制备提供新的理论依据,推动淀粉工业的发展。
1 材料与方法
1.1 材料与试剂
木薯淀粉 广西明阳生化科技股份有限公司;OSA杭州中香化学有限公司;ECH、氢氧化钠、无水乙醇、硝酸银、盐酸等均为分析纯。
1.2 仪器与设备
DF-101D型集热式恒温磁力搅拌器、501BS型超级恒温水浴锅 上海梅香仪器有限公司;JJ-1型精密增力电动搅拌器 常州国华电器有限公司;FA2004型分析天平 上海上天精密仪器有限公司;H1650型离心机 长沙湘仪离心机仪器有限公司;PHS-3C型精密pH计 上海精密科学仪器有限公司;101-1A型数显式电热恒温干燥箱 上海沪越实验仪器有限公司;SHZ-D(III)型循环水式真空泵 郑州长城科工贸有限公司;WSD-3C型全自动白度计 北京康光仪器有限公司;S-3400N型扫描电子显微镜 日本日立公司;Nexus470型傅里叶变换红外光谱仪 美国Nicolet公司。
1.3 方法
1.3.1 交联辛烯基琥珀酸淀粉酯的制备
将淀粉配制成质量分数为40%的水乳液置于三口圆底烧瓶中,搅拌并在35℃恒温条件下,用1mol/L NaOH溶液将淀粉乳液调pH11,碱化10min后,滴加占淀粉干基质量比为0.3%的ECH,用橡皮塞塞紧瓶口,保持搅拌,连续反应3.0h后,加入占淀粉干基质量比为3%的OSA-乙醇溶液(OSA原液临用前用无水乙醇稀释4倍,下同),用1mol/L N aOH溶液调pH值为弱碱性,保持搅拌20min,抽滤预干至含水量10%~20%,粉碎过筛后将粉末置于100℃烘箱中反应一定时间,中和、洗涤、干燥、粉碎过筛即得产品。
1.3.2 交联度的测定
根据淀粉交联度与沉降积(VSE)呈线性负相关关系,以沉降积为指标来间接测定交联度,沉降积越小,交联度越大。具体测定步骤见文献[8]。
1.3.3 取代度(degree of substitution,DS)的测定
参照Ruan等[9]的方法加以改进。称量1.5g样品置于100mL烧杯中,加入100mL 95%乙醇,在磁力搅拌器上搅拌10min,加10mL 2mol/L盐酸和20mL 95%乙醇酸化30min,将样品倒入布氏漏斗,用95%乙醇抽滤洗涤至无Cl-(用硝酸银检验),将样品在50℃烘干1h,再在130℃烘干40min,置干燥器中冷却待称。精确称取酸洗后的绝干样品1.0000g并加100mL蒸馏水于250mL三角瓶中,沸水浴20min,加2滴酚酞,趁热用0.05mol/L NaOH溶液滴定至粉红色,根据下式计算取代度:
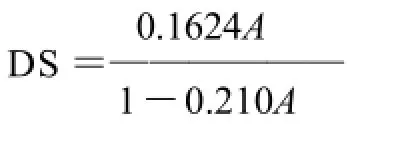
式中:A为每克辛烯基琥珀酸淀粉酯所耗用0.05mol/L NaOH标准溶液的毫摩尔数。
1.3.4 白度的测定
参照GB/T 22427.6—2008《淀粉白度测定》。
1.3.5 红外光谱分析
将干燥样品和KBr混合后制成样品块,用红外光谱仪进行全波段扫描,绘出红外光谱图。
1.3.6 淀粉颗粒形貌观察
将样品用双面胶固定在样品台上喷金,拍摄淀粉颗粒形貌照片(scanning electron microscope,SEM)。电子枪加速电压为20.0kV,放大倍数为1500倍。
2 结果与分析
2.1 单因素试验结果与改性机理分析
2.1.1 酯化时间对取代度的影响
用1mol/L NaOH溶液调节交联淀粉乳液pH8.0,OSA加入量3%,搅拌20min后,把多余水分滤除,将含水量约为15%的滤饼粉碎过筛后放入烘箱,控制温度100℃,分别考察酯化时间为30、60、90、120、150min时对取代度的影响,结果见图1a。
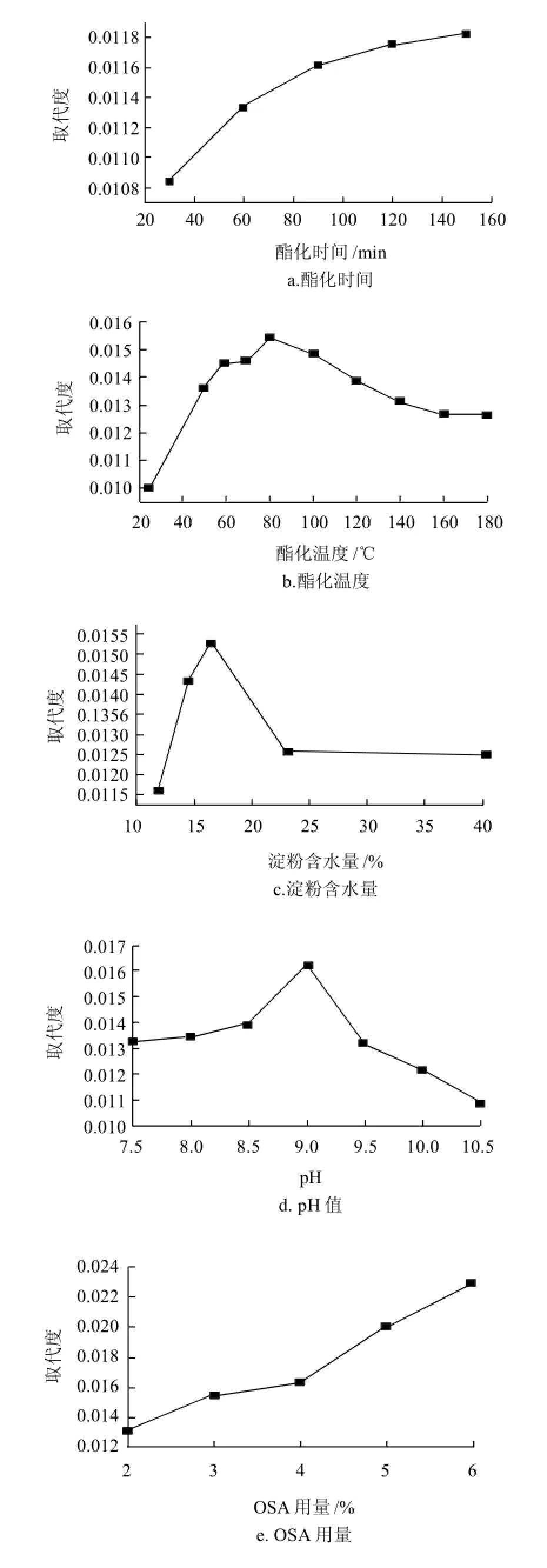

图1 各因素对取代度的影响Fig.1 Effects of modification parameters on DS
从图1a可见,酯化时间越长,产物取代度越高。这是由于在固相进行酯化反应时,副反应OSA的水解及淀粉酯的水解几乎不存在,因此反应时间越长,酯化反应进行得越充分,这是固相反应与液相反应不同的地方。从图1a还可看出,在90~150min内,随着反应时间的延长,取代度增加不是很明显,这也说明随着反应时间延长,酯化剂将逐渐消耗完毕,因此从节能及提高生产效率考虑,反应时间以90~120min为宜。
2.1.2 酯化温度对取代度的影响
用1mol/L NaOH溶液调交联淀粉乳液pH8.0,OSA用量3%,搅拌20min后,滤去多余水分,使淀粉含水量约为15%,放入烘箱反应60min,分别考察酯化温度为25、50、60、70、80、90、100、120、140、160、180℃时对取代度的影响,结果如图1b所示。
由图1b可见,温度对取代度存在着积极与消极两方面的影响。当反应温度低于80℃时,升高温度对反应有利,从80~180℃,随着温度升高,取代度逐渐降低,并以渐近线的形式逼近一个极限值。这是因为淀粉的酯化变性属固相化学反应过程,其反应历程包含扩散、反应等步骤[10],反应温度的升高一方面有利于越过反应能垒,也有助于OSA在淀粉中的扩散,使反应物接触反应,但另一方面,随着温度升高,溶剂乙醇及水挥发加快,溶剂太少难以激活反应,OSA无法渗透到淀粉颗粒内部。因此,反应温度以80~100℃为宜。
2.1.3 淀粉含水量对取代度的影响
在OSA用量3%、酯化pH8.0、酯化时间40min、酯化温度100℃条件下,淀粉含水量对取代度影响见图1c。从图1c可见,当淀粉含水量在12%~18%之间时,随着含水量的增加,取代度增加,原因是固相反应体系若不含任何水分,则淀粉颗粒难以溶胀,OSA无法渗透到颗粒内部发生反应,因此体系必须维持一定量的水分。但当淀粉含水量超过18%以后,随着含水量的增加,产物取代度反而下降,原因可能是在高温下淀粉容易局部糊化结块,而且OSA的水解,酯化反应逆反应等副反应也可能发生,因此较适宜的淀粉含水量为15%~18%。
2.1.4 pH值对取代度的影响
在OSA用量3%、酯化时间60min、酯化温度120℃、淀粉含水量约15%条件下,体系pH值对酯化反应影响见图1d。
在碱性条件下淀粉首先形成亲核试剂StO-,然后StO-与酸酐发生亲核取代反应,酸酐上的环被打开,酸酐分子双羧基的一端与淀粉上的羟基反应形成酯键,另一端则产生一个羧酸,使体系的pH值下降,故需要加入碱性催化剂才能完成酯化反应。由图1 d可知,pH7.5~9.0,随着pH值的增加,取代度相应增加,之后,继续升高pH值取代度反而下降。原因是在固相反应条件下,体系的pH值一次性调好以后便在烘箱中一直反应到结束,当pH值较低,体系仅呈极弱碱性时,反应物系的pH值会随反应的进行很快下降,由于没有足够的碱来补充,酯化反应逐渐停止,只有在较高的pH值状态下,才能维持反应体系的碱性,反应才较为彻底,达到较高的取代度。但若pH值过高,会造成淀粉局部糊化结块,并导致OSA与NaOH生成辛烯基琥珀酸氢钠或二钠以及COSAS发生水解,从而影响酯化反应效率[11],这与湿法改性机理相同。
2.1.5 OSA用量对取代度的影响
在酯化时间60min、酯化温度80℃、淀粉含水量约20%、pH9.5条件下,OSA对取代度影响如图1 e所示。
从图1e可知,OSA用量在2%~6%范围内,随着OSA用量的增加,产物取代度也相应增大。原因是随着OSA用量增加,OSA与淀粉分子发生有效碰撞机率增大,因此在生产中可根据产品用途选用适量的OSA参与反应。在食品工业中为保证所制备的变性淀粉的食用安全性,要求OSA用量不超过3%[12]。
2.1.6 NaCl用量对取代度的影响
控制淀粉含水量约为18%、酯化时间60min、酯化温度80℃,在pH9.5的液相交联反应体系中添加NaCl,考察NaCl用量分别为0%、5%、10%、15%对交联淀粉进行酯化复合变性的影响,结果见图1f。
从图1f可知,随着NaCl用量的增加,产物取代度呈下降趋势。原因可能是在固相反应条件下,淀粉本身就较难溶胀,NaCl的存在破坏淀粉粒表面极少的水化膜,进一步抑制了淀粉粒的润胀,淀粉葡萄糖单元的—OH不易舒展,与OSA活性碰撞几率变小,取代度随之下降,这与湿法改性机理不同[13]。因此在固相反应状态下,以不添加NaCl为宜,这样也可减少产物洗涤除盐的麻烦。
2.2 酯化反应正交试验设计方案及结果
通过酯化变性单因素试验得知,pH值、OSA用量、淀粉含水量、反应时间、反应温度、NaCl用量均对酯化取代度有一定影响。为了全面考察主要因素对酯化变性可能存在的交互影响作用,固定交联时间3h、交联pH11、交联温度35℃、控制淀粉含水量约为15%,以酯化时间、酯化温度、酯化pH值、OSA用量为考察对象,以DS为评价指标,选择L9(34)正交表对COSAS制备条件进行优化试验,L9(34)正交试验设计与结果见表1。

表1 酯化反应条件优化L9(34)正交试验设计及结果Table 1 Orthogonal array design and corresponding experimental results
表1极差R表明,半干法制备COSAS4个因素重要性顺序为A>C>D>B,从k值可知最优化工艺条件为A3B2C2D3,即OSA用量3%、酯化时间90min、酯化pH9.0、酯化温度100℃。
按正交试验选出的最佳工艺条件进行3次平行重复实验,所得COSAS的取代度平均值为0.01750,实验重现性良好,由此证明选出的最佳组合A3B2C2D3合理。
2.3 白度分析
原淀粉(natural starch,NS)、湿法合成的COSAS湿(按文献[14]方法由实验室自制)和半干法合成的COSAS干白度测定结果见表2。所有变性淀粉样品洗涤次数均为5次,并在50℃烘箱中烘干12h,粉碎过100目筛。

表2 原淀粉和改性淀粉的白度值Table 2 Comparison of whiteness between native starch and modified starch
由表2可见,无论是湿法变性还是半干法变性合成的COSAS,其白度值均比原淀粉略为下降,主要是因为淀粉发生交联酯化变性后引入了含不饱和键(>C=C<,>C=O)的辛烯基琥珀酸生色团,能够在紫外及可见光区域内(200~800nm)产生吸收,造成变性后的淀粉白度值略为下降。至于COSAS干的白度值比COSAS湿的要稍小些,可能是因为淀粉在较高温度固相变性时,淀粉中所含的微量蛋白质被烘焦,产生一定量的有色物质,致使半干法变性后的产品白度值降低。从差异显著性分析可知,COSAS取代度不同的数据各自间存在显著性差异。可见取代度能在一定程度上反映酯化变性对淀粉白度的影响程度。
2.4 红外光谱分析
分别将NS、CS(VSE=2.3mL)和COSAS干(DS=0.01732)作红外光谱分析,结果见图2。

图2 原淀粉和不同改性淀粉红外光谱图Fig.2 FTIR spectra of native starch and modified starch
由图2可知,木薯原淀粉主要红外光谱带集中在3440、2886、1650、1012cm-1处。当原淀粉与ECH发生交联反应时,原淀粉的部分自由羟基-OH变成了交联淀粉的醚键(-O-),其他的与原淀粉的化学键基本相同,所以CS在吸收峰波数方面与NS差别不大,但波数为3440cm-1附近表征着羟基的光谱带却有所变化。在CS的红外谱图中,交联淀粉的羟基吸收峰移向高波数区(3489cm-1),吸收峰也变宽了,说明淀粉颗粒的-OH发生缔合趋势下降。淀粉颗粒的交联本身就是一个不断破坏氢键,而以交联键取代氢键的过程[15]。COSAS除了原淀粉所具有的特征吸收峰外,与CS相似的是,-OH伸缩振动吸收峰也移到了较高波数处(3454cm-1);与NS、CS不同的是,COSAS在1731cm-1处出现了酯羰基C=O伸缩振动吸收峰,这表明经酯化变性处理的淀粉引入了新的官能团,并以酯键形式与淀粉葡萄糖上羟基相连。由于制备工艺中ECH及辛烯基琥珀酸盐均已被乙醇抽提去除,所以可断定淀粉分子与ECH及OSA发生了交联和酯化双重变性反应,在淀粉中引入了醚化交联键及辛烯基琥珀酸基团。
2.5 电镜扫描分析
分别将NS、CS以及COSAS干在扫描电镜下观察,颗粒形貌见图3。

图3 原淀粉和改性淀粉电镜扫描照片(×1500)Fig.3 Scanning electron micrographs of native starch and modified starch (×1500)
从图3可见,木薯原淀粉颗粒基本形状为大小不等的圆形或多角形,大部分颗粒表面光滑;交联淀粉的颗粒基本保持原淀粉的形态,少数淀粉颗粒表面略有凹陷或风化状;经半干法变性合成的交联辛烯基琥珀酸淀粉酯,受侵蚀颗粒数量增多,表面出现凹陷或裂痕,说明淀粉确实发生了交联酯化双重变性反应。
3 结 论
3.1 采用半干法制备交联辛烯基琥珀酸淀粉酯,先在液相进行交联反应,待淀粉发生一定程度交联后,调整并控制体系pH为弱碱性,滴加一定量的OSA,搅拌20min后抽滤并预干燥,将滤饼捣碎过筛后在固相进行酯化反应,整个交联疏水亲脂变性过程既具有湿法工艺的反应物料易混合均匀的优点,又具有干法变性效率高的效果,非常适合工业化生产。
3.2 当交联剂ECH用量0.3%、交联pH11.0、交联温度35℃条件下反应3h后进行固相酯化反应,得到半干法制备COSAS的最佳条件为淀粉含水量15%~18%、OSA用量3%、酯化时间90min、酯化pH9.0、酯化温度100℃,此时制备的COSAS平均取代度为0.0175。
3.3 白度测定表明,半干法合成的COSAS白度比原淀粉略为下降;FTIR证实了淀粉经交联酯化变性后引入了醚化交联键和辛烯基琥珀酸基团。S E M图谱表明,COSAS受侵蚀颗粒数量增多,表面出现凹陷或裂痕。
参考文献:
[1]HU Yan, ZHOU Xiaoju, LU Yong, et al. Novel biodegradable hydrogels based on pachyman and its derivatives for drug delivery[J]. International Journal of Pharmaceutics, 2009, 371(1/2)∶ 89-98.
[2]虎玉森, 蒲陆梅, 张红利, 等. 辛烯基琥珀酸马铃薯淀粉酯的制备及结构表征[J]. 食品科学, 2010, 31(2)∶ 22-24.
[3]WANG Junping, SU Lianghua, WANG Shuo. Physicochemical properties of octenyl succinic anhydride-modified potato starch with different degrees of substitution[J]. Journal of the Science of Food and Agriculture, 2010, 90(3)∶ 424-429.
[4]石海信, 谢新玲, 张友全, 等. 醚化交联玉米辛烯基琥珀酸淀粉酯的制备工艺及特性[J]. 食品科技, 2009, 34(8)∶ 214-217.
[5]刘凤茹, 张燕萍. 两种不同方法制备的硬脂酸玉米淀粉酯的性质研究[J]. 食品工业科技, 2009, 30(10)∶ 143-146.
[6]刘国琴, 陈洁, 韩立鹏, 等. 干法合成硬脂酸小麦淀粉酯的特性研究[J]. 农业机械学报, 2009, 40(8)∶ 99; 143-148.
[7]KHALIL M I, BELIAKOVA M K, ALY A A. Preparation of some starch ethers using the semi-dry state process[J]. Carbohydrate Polymers, 2001, 46(3)∶ 217-226.
[8]伍亚华, 石亚中. 交联-羧甲基淀粉糊性质研究[J]. 食品与机械, 2008, 24(6)∶ 16-19.
[9]RUAN Hui, CHEN Qihe, FU Mingliang, et al. Preparation and properties of octenyl succinic anhydride modified potato starch[J]. Food Chemistry, 2009, 114(1)∶ 81-86.
[10]周益明, 忻新泉. 低热固相合成化学[J]. 无机化学学报, 1999, 15(3)∶273-292.
[11]石海信, 谢新玲, 张友全, 等. 交联辛烯基琥珀酸淀粉酯亲核取代机理与结构表征[J]. 高校化学工程学报, 2010, 24(2)∶ 307-312.
[12]BHOSALE R, SINGHAL R. Effect of octenylsuccinylation on physicochemicaland functional properties of waxy maize and amaranth starches[J]. Carbohydrate Polymers, 2007, 68(3)∶ 447-456.
[13]侯汉学, 董海洲, 汪建民, 等. 羟丙基糯玉米淀粉POCl3交联复合变性条件的研究[J]. 中国粮油学报, 2005, 20(2)∶ 45-48.
[14]石海信, 谢新玲, 张友全, 等. 辛烯基琥珀酸交联淀粉酯合成工艺研究[J]. 中国粮油学报, 2009, 24(10)∶ 59-63.
[15]吴学森, 王伟. 淀粉含量对聚乳酸/淀粉共混物力学性能的影响[J].中国塑料, 2009, 23(2)∶ 27-31.
Semi-dry Synthesis and Modification Mechanisms of Crosslinked Octenyl Succinic Anhydride-modified Cassava Starch
SHI Hai-xin1,DENG Quan-dao2,LIU Ling-zhi2,YAN Feng-ying1,FANG Huai-yi1
(1. School of Chemistry and Chemical Engineering, Qinzhou University, Qinzhou 535000, China;2. Qinzhou Entry-Exit Inspection and Quarantine Bureau, Qinzhou 535000, China)
Cassava starch was modified with epichlorohydrin (ECH) and octenyl succinic anhydride (OSA) by a semi-dry process to synthesize hydrophobic lipophilic crosslinked octenyl succinic anhydride-modified starch (COSAS). The synthesis process was optimized by one-factor-at-a-time and orthogonal array design methods. The reaction mechanisms were elucidated. The whiteness of COSAS was determined and structural analysis was carried out using Fourier transform infrared spectrometry and scanning electron microscope (SEM). The results indicates that the optimal synthesis process parameters of COSAS were starch water content of 15%-18%, OSA amount of 3% (based on the dry weight of starch), esterification time of 90 min, pH 9.0, and reaction temperature of 100 ℃. The average degree of substitution (DS) of COSAS prepared using the optimized process parameters was 0.0175, and its whiteness was slightly lower than that of native starch. FTIR spectral analysis revealed that crosslinked bonds and groups in octenylsuccinate were introduced into starch after esterification. SEM observations also showed that the surface of COSAS was rougher than that of native starch although some particles with concaves, gaps and cracks were observed.
cassava starch;crosslinked octenyl succinic anhydride-modified starch;semi-dry process;reaction mechanism
TS235.2
A
1002-6630(2011)16-0172-06
2010-11-08
广西科学基金资助项目(桂科自0991274);广西高校重点实验室项目(HYSYS-YB07)
石海信(1962—),男,副教授,硕士,研究方向为淀粉化学品合成与应用。E-mail:shihaixin2006@163.com

