不同煤种燃烧过程中NO x 形成规律的数值模拟与分析
刘建红,任晓平,张自国
(长春工程学院能源与动力工程学院,长春 130012)
0 引言
NOx是一种危害人体健康,破坏大气环境的污染物,燃煤电站锅炉是NOx的主要排放源。2000年全国电站锅炉NOx的平均排放质量浓度为750 mg/Nm3,NOx排放总量为258.02万t,2010年NOx排放总量比2000年增长336万t左右。按照我国2004年火电厂大气污染物排放标准规定,1 000 t/h以上的固态排渣煤粉锅炉NOx排放标准为450 mg/Nm3。根据调查(按2002年为6%计算)固态排渣煤粉炉NOx的平均排放量为600~1 200 mg/Nm3[1]。随着国家对环保的日益重视,我国对火电厂的污染物排放控制也将更加严格。所以,对煤燃烧过程中NOx的生成机理以及其控制方法开展研究,对促进国民经济的发展和改善生态环境具有重要的现实意义。
锅炉内的煤粉燃烧是一个复杂的物理、化学过程,它涉及到多相流动、传热传质和燃烧等多个学科。加深了解煤粉燃烧过程中NOx的生成机理,对控制燃烧过程中的NOx排放至关重要。在煤粉燃烧过程中产生的NOx主要有3种,即热力型、快速型和燃料型NOx。本文通过查阅大量的文献,发现电厂中生成快速型NOx很少,可以忽略不计,所以本文采用数值模拟方法研究不同煤种燃烧过程中NOx的生成,分析煤燃烧过程中NOx的形成机理及其影响因素,综述现代电厂中采用的低NOx燃烧的控制技术。
1 数学模型
数值模拟的第一步是由燃烧过程所遵循的基本定律:质量守恒定律、牛顿第二定律、能量转换和守恒定律、组分转换定律等,构造基本守恒方程,即连续方程、动量方程、能量方程、组分方程等。对于所有的流动问题进行数值计算,都需要求解连续性方程和动量守恒方程。当流动是湍流时,还要求解附加的输运方程。对于包含传热的流动,需要求解能量守恒方程。对于包含组分混合和化学反应的流动,需要求解组分守恒方程来求解混合分数的守恒方程。
1.1 连续性方程

式中:ρ——质量密度,kg/m3;
t——时间,s;
V——速度矢量,m/s。
1.2 动量守恒方程

式中:μ——动力粘度系数,Pa·s;
p——燃烧炉内压力场,Pa。
1.3 能量守恒方程
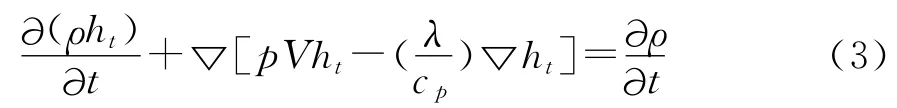
式中:ht——比焓,J/kg;
λ——导热系数,w/(m·k);cp——定压比热,J/(Kg·k)。
由于燃烧炉的气体流动属于湍流流动,故采用κ-ε湍流流动模型进行计算。
1.4 化学组分守恒方程
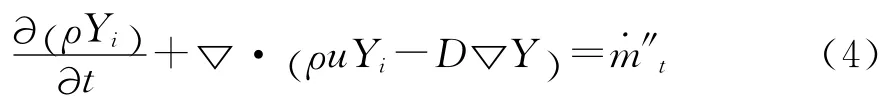
式中:Yi——质量分数;
u——扩散速度;D——扩散系数;˙m″——质量通量。
2 几何模型和数值计算方法
2.1 几何模型
本文参照一维沉降炉[2]实际尺寸建立几何模型如图1所示,直径50 mm,高度1.2 m的二维图形,网格为10万左右的规则网格。边界条件为速度入口、压力出口和壁面边界条件,空气和煤粉从速度入口进入,然后从压力出口流出。

图1 几何模型
2.2 数值计算方法
本文对高挥发分煤(coal-hv)、中挥发分煤(coal-mv),低挥发分煤(coal-lv)3种煤种在燃烧温度分别为1 527℃、1 627℃的高温沉降炉内燃烧的NOx生成进行数值模拟研究,采用κ-ε模型模拟气相湍流输运及气相湍流燃烧。采用离散传播法计算辐射换热。对煤粉的挥发分释放采用双平行反应模型,对颗粒的湍流扩散采用随机轨道模型,对焦炭的燃烧采用扩散动力模型。对气相控制方程组采用SIMPLER算法,差分格式使用混合上风格式。颗粒相的计算采用拉氏方法,气相—颗粒相间的耦合采用PSIC算法实现。
在NOx的生成模型中,对于热力NOx的生成采用Zeldovich机理[3]进行计算,对燃料NOx的生成,采用 De′Soete[4]提出的总体反应速率模型进行计算。计算中主要考虑湍流脉动对燃料NOx生成速率的影响,即考虑湍流脉动对反应速率RHCN→NO和RNO→N2的影响。采用β函数型概率密度函数(β-pdf)来求出RHCN→NO和RNO→N2的时平均值RHCN→NO和RNO→N2。
3 计算结果的分析与讨论
3.1 燃料型NO x研究
图2分别是高挥发分煤(coal-hv)、中挥发分煤(coal-mv),低挥发分煤(coal-lv)在燃烧温度为1 527℃下燃烧生成NOx质量浓度比较,通过模拟可以发现高质量浓度的NOx几乎都是在距离入口0~0.2 m的范围内生成的,经过计算得出,hv的质量浓度范围为0~0.046%,mv的质量浓度范围为0~0.064%,lv的质量浓度范围为0~0.039%,所以中挥发分煤(coal-mv)生成的NOx最多。
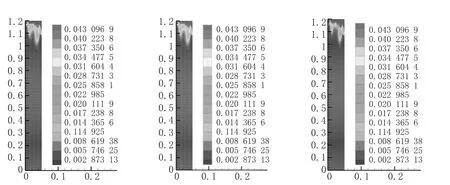
图2 hv,mv,lv在1 527℃燃烧时生成的NO x的质量含量比较
煤在燃烧过程中首先经过热解反应,在热解的初期,煤迅速脱除挥发分,其中包括碳氢化合物、焦油等。煤中的N一部分随挥发分释放出来,另一部分残留在焦炭中,并随焦炭的燃烧释放出来。挥发分-N经过一系列反应生成NO、N2和N2O,这时进行的是气气同相反应;固—态的焦炭与烟气中的氧气进行反应,焦炭-N经过一系列反应生成NOx、N2和N2O,这时进行的是固—气的异相反应。图2为煤中含有的N元素进行均相和异相的氧化和还原反应的最终结果。
由于电厂中生成的快速型NOx很少,可以忽略不计,煤粉燃烧排放的NOx中约有95%来源于燃料型NOx[5],因此研究燃料型NOx的生成和还原机理,对控制NOx排放显得尤其重要[6]。煤粉中氮元素的质量浓度一般都在0.8%~2%左右,与煤的等级没有明显的相关性。燃料型NOx的生成机理非常复杂,因为燃料型NOx的生成和还原过程不仅和煤种特性、结构、燃料中的N受热分解后在挥发分和焦炭中所占的比例、成分和分布有关,而且大量的反应过程还和燃烧条件,如运行温度和氧气质量浓度等密切相关。
图3分别是高挥发分煤(coal-hv)、中挥发分煤(coal-mv),低挥发分煤 (coal-lv)在燃烧温度为 1 800 K的炉膛温度比较,经过计算得出,hv的炉膛温度范围为1 527~3 020℃,mv的温度范围为1 527~3 229℃,lv的温度范围为1 527~2 965℃。比较图2的结果,可以得出燃料型NOx的形成与燃烧温度关系不大,因为燃料型NOx的生成量,取决于系列反应中燃料N是氧化成NOx还是被还原成N2。研究表明,燃料型NOx质量浓度,在还原性气氛中较少,在氧化性气氛中较高,并随着燃料量的增加而明显地增加。综上所述,影响燃料型NOx生成的影响因素有:
(1)燃料N含量增加,则中间产物增加,NOx的生成量随之增加。
(2)热分解温度提高,释放出的中间产物增多,NOx质量浓度增加。
(3)煤燃烧是部分扩散火焰,在常规燃烧条件下,NOx的生成量随着空气过剩系数α的增大而增加。
(4)燃烧区中,若氧气充足,释放出的N停留时间越长,则生成NOx越多;反之,若氧气缺乏,延长在燃烧区中的停留时间,使NOx与中间产物反应充分,因而使NOx量减少。因此,使用低N含量燃料,实施缺氧燃烧,延长燃烧产物在还原区的停留时间,可以有效地控制燃料型NOx的生成[1]。

图3 hv,mv,lv在入口温度1 527℃燃烧时炉膛温度比较
3.2 热力型NO x研究
图4为不同煤种生成NOx的生成速率比较,图5为不同温度生成NOx的生成速率比较,图4的数值模拟计算结果为:在燃烧温度为1 527℃时,hv的热力型NOx生成速率的范围为-125~475,lv热力型NOx生成速率的范围为的-84~365。图5的数值模拟计算结果为:在燃烧温度为1 527℃时,hv的热力型NOx生成速率的范围为-125~475,1 627℃时的热力型NOx生成速率的范围为2 102~44 042。因此可以得出结论:热力型NOx的形成很大程度上依赖于温度而不是燃料的种类,温度升高100℃,温度型NOx形成速率就翻倍,且基本上成指数关系。
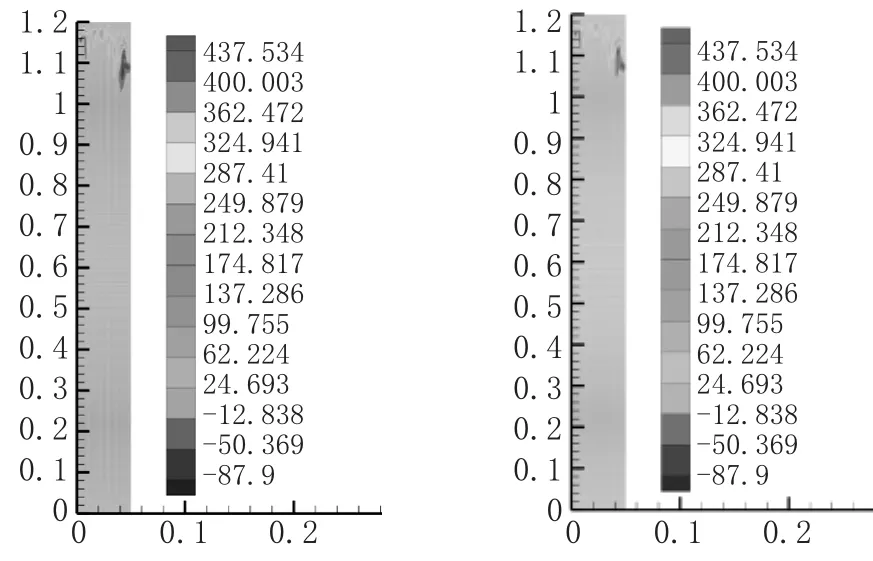
图4 hv,lv在燃烧温度为1 527℃热力型NO x的生成速率比较

图5 hv在燃烧温度为1 527℃,1 627℃热力型NO x生成速率比较
热力型NOx是由空气中的N2在高温下氧化生成的。其形成机理是由前苏联科学家捷里道维奇提出的,被称为广义Zeldovich机理[3],其生成的多少主要依赖于燃烧区域的温度水平和氧质量浓度,影响因素有:
(1)温度对热力型NOx的生成有决定性的影响。由于生成NOx的活化能(565 kJ)非常大,反应速度与温度变化密切相关。当燃烧温度低于1 500℃,热力型NOx生成量非常少;温度超过1 500℃,反应速度将剧增,NOx生成量随温度升高而急剧增加。因此,适当降低燃烧区域的温度,避免出现局部温度峰值,可以显著减少NOx的生成量。
(2)缩短燃烧产物滞留高温区的时间。实际燃烧中,高温火焰内的氧原子已经超过平衡质量浓度,为空气中N的氧化提供了条件。若反应混合物滞留时间长,会使NOx质量浓度迅速增加。因此,控制燃烧产物在高温区的滞留时间,可以减少NOx的生成和控制最终的烟气成分。
(3)反应混合物中氧质量浓度。NOx的生成量与氧质量浓度的关系存在一个峰值。理论上当空气过剩系数α=1时,NOx的质量浓度最高。当α<1时,NOx的质量浓度随氧的质量浓度增加而提高,因为氧原子的数量增加;当α>1时,NOx的质量浓度随氧的质量浓度增加而降低,这是由于氧的稀释使燃烧温度下降[1]。
3.3 控制NO x排放的技术措施
电厂中控制NOx排放的技术措施可以分为一次措施和二次措施。所谓一次措施是通过各种技术手段降低燃烧过程中的NOx生成量;二次措施是将已经生成的NOx通过某种技术手段从烟气中脱除掉。由此发展起了2大类降低NOx的技术,即低NOx燃烧技术和烟气处理NOx技术。具体的技术措施见图6。
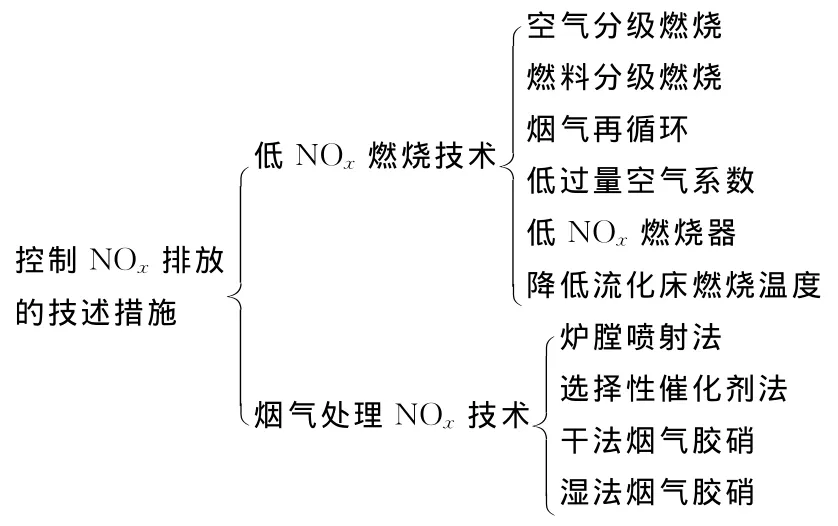
图6 控制NO x排放的技术措施
4 结语
燃煤过程对大气造成的污染正日益引起人们的关注,控制NOx的排放是煤燃烧利用研究中亟需解决的课题。本文采用数值模拟方法,研究了不同煤种在不同温度下燃烧生成NOx的影响,并探讨了降低NOx的途径,对促进国民经济的发展和改善生态环境具有重要的现实意义。
[1]刘峰,左宁心.大型煤粉锅NOx的生成机理及其控制方法[J].中国科技信,2008,23:75-79.
[2]张聚伟.高温条件下NO-焦炭反应动力学的研究[D].哈尔滨:哈尔滨工业大学,2009:28-31.
[3]Zeldovich YB.The oxidation of nitrogen in combustion and explosions[J].Acta Physicochem USSR,1946,21:577-628
[4]DeSoete G G.Overall Reaction Rates of NO and N2Formation from Fuel Nitrogen.Proc 15th Symposium (International)on Combustion[J].The Combustion Institute,Pittsburgh,PA,1975:1093-1102.
[5]刘海峰,刘银河,刘艳华,等.煤热解过程中含氮气相产物转化规律的实验研究[J].燃料化学学报,2008,36:134-138.
[6]Anker Jensen,Jan Erik Johnsson.Modelling of NOxE-missions from Pressurized Fluidized Bed Combustion Parameter Study[J].Chemical Enoineering Science,1997,52(11):1715-1731.

