人参皂苷对糖尿病大鼠肾组织基质金属蛋白酶9及Ⅳ型胶原表达的影响
苏建明 倪海祥 黄 琦 朱 锋
浙江省中医院(浙江杭州310006)
糖尿病肾病(DN)特征性的病理改变是细胞外基质(ECM)在肾小球、肾小管积聚导致肾小球硬化和肾间质纤维化[1],而ECM的堆积是由于ECM产生过多和降解减少所致。基质金属蛋白酶及其组织抑制因子表达和活性的改变,与ECM堆积关系密切。基质金属蛋白酶9(MMP-9)参与血管基底膜主要结构成分-Ⅳ型胶原(Col-Ⅳ)的降解,与DN的关系密切[2-3]。本实验采用免疫组织化学方法对糖尿病时肾组织MMP-9和Col-Ⅳ表达改变进行研究,并用人参皂苷进行干预,以探讨期防治DN的作用和可能机制。
1 材料与方法
1.1 实验材料 动物:健康雄性SPF级SD大鼠100只,12周龄,体质量(300±20)g,购自中国科学院上海实验动物中心,由浙江中医药大学SPF动物房饲养。试药:人参皂苷,由浙江省中医院制剂科提供;链脲佐菌素(STZ),美国Sigma公司;一抗,鼠抗人(MMP-9 和 Col-Ⅳ)抗体;二抗,羊抗鼠抗体;MMP-2、Col-Ⅳ,均购自北京中山生物制品有限公司。
1.2 模型制备 随机留取正常对照组18只,其余随机36只大鼠禁食过夜后,按70mg/kg,左下腹腔内一次性注射1%STZ溶液 (pH 4.5的0.1mol/L柠檬酸钠-柠檬酸缓冲液在冰浴中新鲜配制)。注射后72h,用血糖仪测定尾尖血血糖,血糖≥16.7mmol/L的大鼠判定为糖尿病大鼠。
1.3 分组与给药 将模型大鼠随机分为模型组(18只)和人参皂苷组(18只)。人参皂苷组灌胃人参皂苷0.5g/kg(溶于10%纤维素钠溶液),模型组和正常对照组灌胃等量生理盐水。每日2次。
1.4 标本采集 每周用血糖仪测尾尖血血糖,称体质量,并计算水和食物的摄入量。至实验第2、4、8周时每组各取6只大鼠留取尿液,苯巴比妥麻醉后行股动脉放血处死,留取股动脉血并取右肾称质量。右肾与体质量的比值作为肾脏肥大程度的指标。尿液用于测定尿肌酐、尿白蛋白测定,并用尿白蛋白与尿肌酐比值作为临床肾损害的指标。股动脉血用于测定血糖、C肽、肌酐。
1.5 标本处理与免疫组化染色 大鼠肾脏经10%甲醛固定,梯度乙醇逐步脱水、浸蜡、石蜡包埋、切片(厚2μm)。石蜡切片经二甲苯脱蜡后作PAS染色、HE染色以及MMP-2、Col-Ⅳ免疫组化染色,E法。一抗均为鼠抗人(MMP-9和Col-Ⅳ)抗体,二抗为羊抗鼠抗体,MMP-9的工作滴度为1∶80,Col-Ⅳ工作滴度为1∶100。每次实验均设PAS(空白对照)和正常兔血清取代一抗(阴性对照)。光镜观察肾组织病变与MMP-9、Col-Ⅳ的分布,免疫组化染色以细胞浆膜或间质有棕黄色颗粒或线状沉积为阳性,否则为阴性。MMP-9、Col-Ⅳ定量均采HPIAS-21000型高清晰度彩色病理图文报告分析系统在高倍镜下计算其阳性面积百分比(%),每张切片选取10个视野,求平均值。
1.6 统计学处理 应用SPSS 13.0统计软件。计量资料以(x±s)表示,多样本均数的两两比较采用单因素方差分析,如果方差齐采用LSD,方差不齐采用Tamhane’sT2。P<0.05为差异有统计学意义。
2 结 果
2.1 一般情况 STZ注射72h后,大鼠的血糖均≥16.7mmol/L,并逐渐出现多饮、多尿、多食,体质量增长缓慢等糖尿病症状。与正常对照组相比,血糖、肾脏肥大指数均升高,体质量、C肽显著下降,尿白蛋白排泄量有升高,但无统计学意义。人参皂苷治疗对体质量、肾脏肥大、尿白蛋白排泄有改善作用,但与模型组相比,差异无统计学意义(P>0.05),见表 1;但其对血糖、血脂作用明显,与模型组比较,差异有统计学意义(P<0.05),与国内外相关研究结论一致[4-6]。见表2。
2.2 病理组织变化 HE染色下肾脏结构清楚,细胞核呈蓝色,胞浆呈粉红色。PAS染色下正常对照组未见明显的肾小球系膜增生及基底膜增厚,模型组8周时可见肾小球系膜轻度增生、肾小管轻度颗粒样变、基底膜轻度增厚,但未见肾小球结节样增生和动脉玻璃样变性等典型的糖尿病肾脏改变,人参皂苷组上述病变程度更轻。模型大鼠肾组织MMP-9的组织定位MMP-9抗原免疫组化染色示棕黄色或深棕黄色,主要表达在大鼠肾小球系膜细胞、内皮细胞、包曼氏囊壁层上皮细胞、肾小管上皮细胞,偶见浸润的巨噬细胞和中性粒细胞表达。
表1 各组大鼠一般情况比较 (±s)
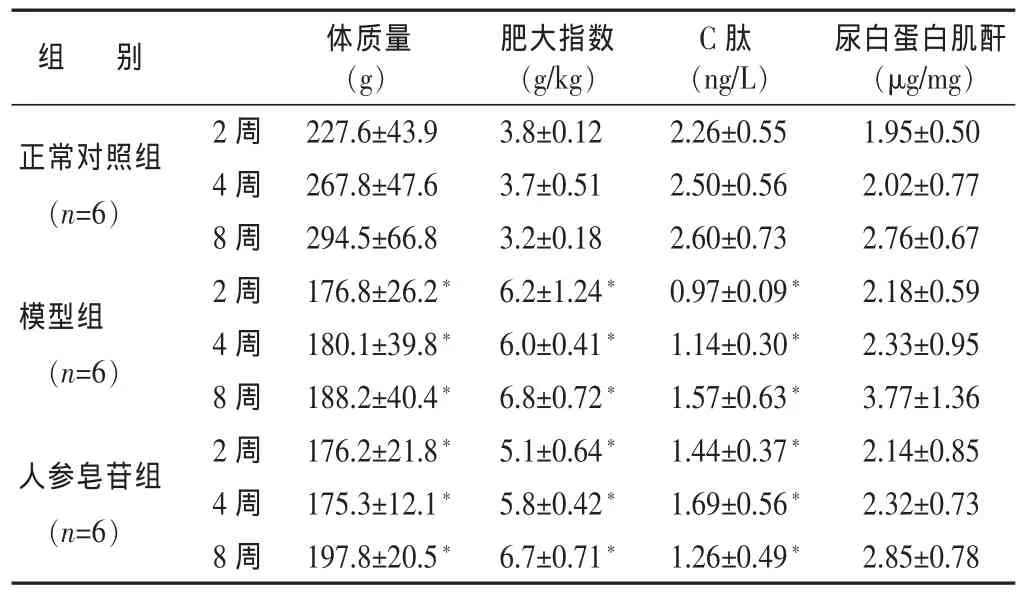
表1 各组大鼠一般情况比较 (±s)
与正常对照组比较,*P<0.05,**P<0.01;与模型组比较,△P<0.05,△△P<0.01。 下同。
组 别C肽正常对照组(n=6)2周4周体质量(g)227.6±43.9 267.8±47.6肥大指数(g/kg)3.8±0.12 3.7±0.51(ng/L)2.26±0.55 2.50±0.56 8 周 294.5±66.8 3.2±0.182.60±0.73 0.97±0.09*尿白蛋白肌酐(μg/mg)1.95±0.50 2.02±0.77 2.76±0.67 2.18±0.59模型组(n=6)2 周 176.8±26.2* 6.2±1.24*4 周 180.1±39.8* 6.0±0.41* 1.14±0.30* 2.33±0.95 8 周 188.2±40.4* 6.8±0.72* 1.57±0.63* 3.77±1.36人参皂苷组(n=6)2 周 176.2±21.8* 5.1±0.64* 1.44±0.37* 2.14±0.85 4 周 175.3±12.1* 5.8±0.42* 1.69±0.56* 2.32±0.73 8周197.8±20.5*6.7±0.71*1.26±0.49*2.85±0.78
表2 各组大鼠血清糖脂代谢指标比较 (mmol/L,±s)
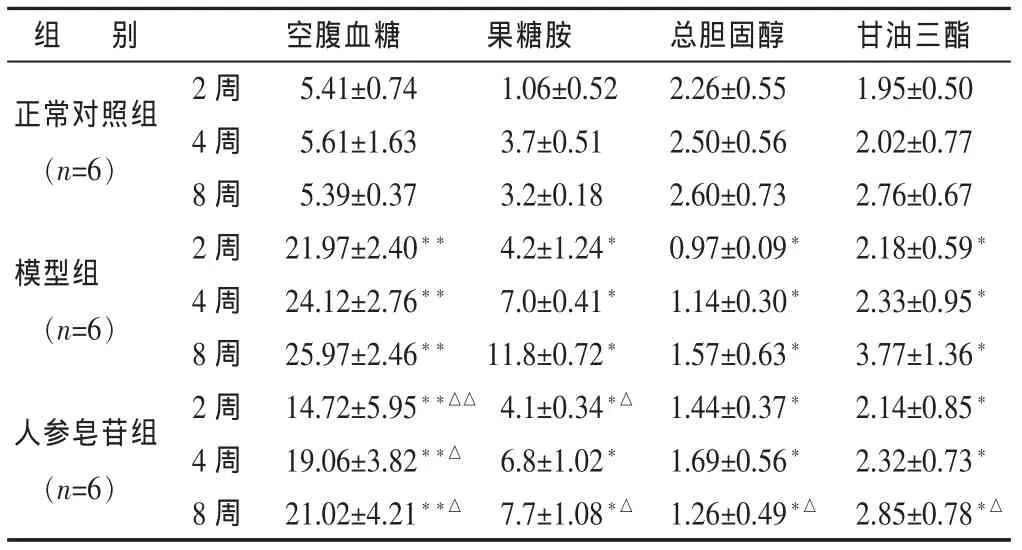
表2 各组大鼠血清糖脂代谢指标比较 (mmol/L,±s)
人参皂苷组(n=6)4 周 19.06±3.82**△ 6.8±1.02* 1.69±0.56* 2.32±0.73*8周21.02±4.21**△7.7±1.08*△1.26±0.49*△2.85±0.78*△
2.3 各组大鼠肾组织MMP-9、Col-Ⅳ表达比较 见表3。糖尿病大鼠肾小球MMP-9在2、4、8周时较对照组明显下降 (P<0.05),人参皂苷组肾小球 MMP-9高于糖尿病组,在 4、8周时差异有统计学意义 (P<0.05)。组内比较发现模型组大鼠在4、8周时肾小球MMP-9较2周时低(P<0.05),而人参皂苷组则在4、8周时肾小球MMP-9较2周时高(P<0.05)。各时期模型组肾间质MMP-9与正常对照组相比,有升高但差异无统计学意义(P>0.05),人参皂苷组较模型组肾间质MMP-9有下降,第8周时差异有统计学意义 (P<0.05)。糖尿病大鼠肾小球Col-Ⅳ的表达在 2、4、8 周时均较正常组升高(P 均<0.05),而肾间质 Col-Ⅳ的表达在8周时较正常组明显升高(P<0.05)。人参皂苷组肾小球Col-Ⅳ的表达则较模型组下降,在4、8周时差异有统计学意义(P<0.05),肾间质 Col-Ⅳ的表达也较模型组下降,在 8周时差异有统计学意义(P<0.05)。
表3 各组大鼠肾小球MMP-9、Col-Ⅳ表达比较 (%,±s)
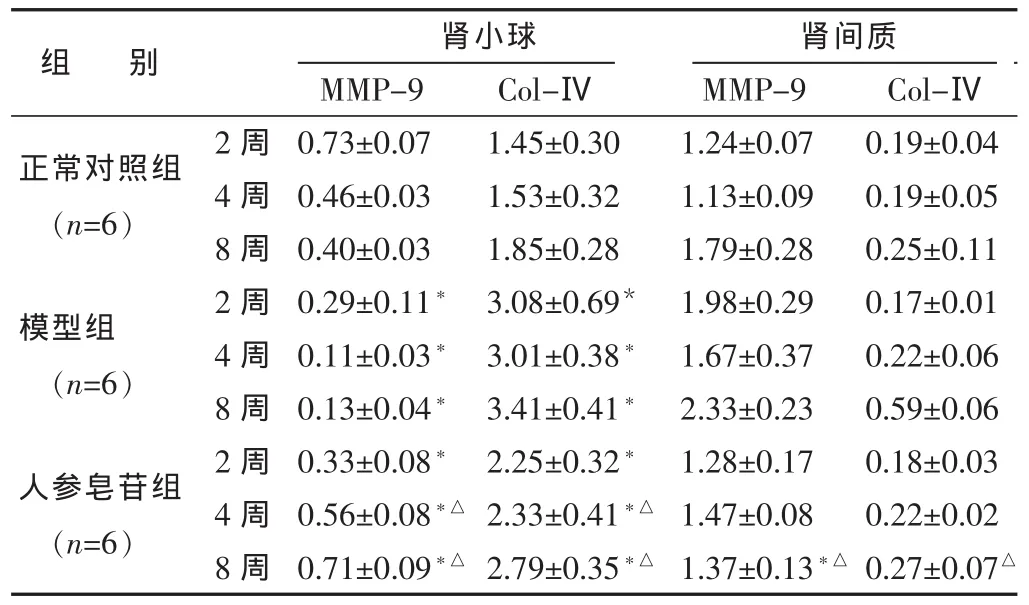
表3 各组大鼠肾小球MMP-9、Col-Ⅳ表达比较 (%,±s)
组 别 肾小球 肾间质MMP-9 Col-Ⅳ MMP-9 Col-Ⅳ正常对照组(n=6)2周4周0.73±0.07 0.46±0.03 1.45±0.30 1.53±0.32模型组(n=6)人参皂苷组(n=6)8 周 0.40±0.03 2 周 0.29±0.11*4 周 0.11±0.03*8 周 0.13±0.04*2 周 0.33±0.08*4 周 0.56±0.08*△1.85±0.28 3.08±0.69*3.01±0.38*3.41±0.41*2.25±0.32*2.33±0.41*△8周0.71±0.09*△2.79±0.35*△1.24±0.07 0.19±0.04 1.13±0.09 0.19±0.05 1.79±0.28 0.25±0.11 1.98±0.29 0.17±0.01 1.67±0.37 0.22±0.06 2.33±0.23 0.59±0.06 1.28±0.17 0.18±0.03 1.47±0.08 0.22±0.02 1.37±0.13*△ 0.27±0.07△
3 讨 论
本研究用STZ制成糖尿病大鼠模型,并用人参皂苷治疗,用免疫组化方法检测肾小球及肾间质MMP-9和Col-Ⅳ表达的变化。发现糖尿病时肾小球MMP-9的表达下降,Col-Ⅳ表达上升,且随病程进展愈加明显。本研究发现糖尿病大鼠模型中MMP-9在肾小球中的表达是降低的,这与其他相关研究[7]结果一致。但同时发现糖尿病大鼠肾间质MMP-9的表达增加,而与Col-Ⅳ表达成正比。可能的是在肾小球中,高血糖所致的诸多因素导致MMP-9的表达下降在先,从而引起Col-Ⅳ的降解减少,Col-Ⅳ的积累增加,导致肾小球硬化的发生。
人参为临床上治疗糖尿病的常用中药,具有大补元气,补脾益肺,生津止渴,安神益智之功效。既合“消渴”的基本病机“阴虚为本”,亦治久病及肾之下焦虚寒、阴阳两虚。本研究观察了人参皂苷对2型糖尿病实验大鼠相关指标2周、4周、8周的影响,提示人参皂苷对肾脏的保护作用也可能通过减少ECM的形成起到保护肾细胞的作用。
由于各方面条件的限制,本研究例数尚少,此外,MMPs的表达调节大致可以分为基因水平的调节,酶原活化调节,活化后调节等调节方式[7-10]。相关药物能否作用于在这几个环节从而调节MMPs的表达尚待进一步研究。由于人参皂苷成分较多,其疗效是多耙向的,故其治疗2型糖尿病的机制相对较复杂,确切机制尚不明确,有待于在进一步的研究中筛选提取方式,阐释其作用机理,寻找答案。
[1] 朱禧星.现代糖尿病学[M].上海:上海医科大学出版社,2000:311-327.
[2] Schaefer L,Ham X,August C,et al.Differential regulation of glomenrulargelatinaseB (MMP-9)and tissue inhibitorofmetalloproteinase-1(TIMP-1) in obese Zucker rats[J].Diabetologin,1997,40(3):1035-1043.
[3] Nakamure T,Fukui M,Ebihara L,et al.Abnormal gene expression of matrixmetalloproteinases and their inhibitor in glomerular from diabetes ratas[J].RenalPhysiolBiochem,1994,17 (6 ):316-325.
[4] Attele AS, Zhou YP, Xie JT,et al.Antidiabetic effectsof Panax ginseng berry extractand the identification of an effective component[J].Diabetes, 2002 , 51 (6):1851-1858.
[5] 陈冬梅,睢诚,曲绍春,等.人参果皂苷注射液对实验性高血糖的影响[J].吉林大学学报,2007,9(5):647-650.
[6] 胡翠华,徐华丽,于晓风,等.人参二醇组皂苷对实验性2型糖尿病大鼠血糖及血脂代谢的影响[J].吉林大学学报,2006,32(6):1004-1008.
[7] Dong FQ,LiH ,CaiW M,etal.Efectsof pioglitazoneon expressionsof matrixmetallopro-teinases2 and9 in kidneysofdiabetic rats[J].Chin Med JEngl,2004,117(7):1040-1044.
[8] Ayala JE,Boustead JN,Chapman SC,etal.Insulin-mediated activation of activator protein-1 through themitogen-activated protein kinase pathway stimul-ates colla gen-a se1 gene transcription in the MES13mesangial cell line[J].JMol Endocrinol,2004,33(1):263-80.
[9] 冯梅,陈云波,王奇,等.人参皂苷Rg1对Aβ25-35诱导的星形胶质细胞核因子κB活化及炎症反应的影响[J].中国老年学杂志,2006,26(10):1382-1384.
[10] Kurata H,ThantA A,Matsuo S,etal.Constitutiveactivation of MAP kinase kinase (M EK1) is critical and sufficient for the activation of MMP22[J].Exp CellRes,2000,254 (1):180-188.

