不同厂家红霉素软膏微生物限度检查方法验证研究
李传响
不同厂家红霉素软膏微生物限度检查方法验证研究
李传响
目的建立红霉素软膏的微生物限度检查方法。方法 人为加入5种阳性对照菌,测定其回收率。结果根据回收率试验结果,判定红霉素软膏对细菌的抑菌作用的强弱。结论必需采用离心集菌薄膜过滤法才能清除样品的抑菌作用,该法可用于红霉素软膏的微生物限度的检查。
红霉素软膏;微生物限度;回收率
(如金黄色葡萄球菌,肺炎链球菌等),对衣原体等也有抑菌作用。笔者在反复验证多个厂家红霉素软膏微生物限度检查方法时,发现常规法,培养基稀释法均不适用于该制剂的微生物限度检查,而离心集菌薄膜过滤法均可适用。
1 资料与方法
1.1 一般资料 HTY-601型集菌仪(杭州泰林医疗机械厂);红霉素软膏(6个厂家分别编号为S1~S6);大肠埃希菌;枯草芽孢杆菌;金黄色葡萄球菌;铜绿假单胞菌;白色念珠菌;黑曲霉菌种均系中国药品生物制品检定所提供。营养琼脂,玻瑰红钠琼脂,胆盐乳糖,pH 7.0无菌氯化钠-蛋白胨等培养基均系牛牛基因生物公司生产。
1.2 方法
1.2.1 菌液制备 金黄色葡萄球菌、枯草芽孢杆菌、大肠埃希菌、铜绿假单胞菌菌液:取上述菌种的新鲜培养物接种至营养肉汤培养基10 ml中,经35℃培养24 h,再将上述各菌的营养肉汤培养物,用0.9%无菌氯化钠溶液10倍级分别稀释至10-7、10-5、10-7,10-6,使以上各菌含菌量约为 50 ~ 100 cfu/ml,备用。
1.2.2 白色念珠菌液 取该菌种新鲜培养物接种至改良马丁培养基中,经25℃ 培养36 h,再取该菌液体培养物,用0.9%无菌氯化钠溶液稀释至10-5,备用。
1.2.3 黑曲霉 取黑曲霉新鲜培养物接种至改良马丁琼脂斜面培养基,25℃ 培养7 d,再取该斜面培养物,加4 ml 0.9%无菌氯化钠溶液洗下黑曲霉孢子,吸取孢子悬液1 ml,加0.9%无菌氯化钠溶液适量稀释,用标准比浊管比浊,浊度相当后,取1 ml稀释后的孢子悬液,用0.9%无菌氯化钠溶液稀释至10-4,备用。上述各株菌的培养物均为第3代的培养物。
1.2.4 供试液制备 参照关资料文献[1~6]的方法,取本品10g,加无菌十四烷酸异丙酯20 ml及玻璃珠,充分振摇,分散均匀,再加入0.9%无菌氯化钠溶液至100 ml,充分振摇,萃取,置8℃环境中静置分层,取下层部分作为供试液。
1.2.5 回收率测定 试验组(A组):取供试液1 ml和试验菌液1 ml,注入平皿,立即倾注相应的培养基,平行制备2皿,依法测定其菌落数[1]。培养基稀释法:取供试液1 ml,分注5个平皿中,使成0.2 ml/皿;取供试液1 ml,分注2个平皿中,使成0.5 ml/皿,再依次加入试验菌。离心集菌薄膜过滤法:取供试液1 ml,加入200 ml稀释液中混合均匀后,经薄膜过滤并冲洗,冲洗量分别为200、400、500、600、800 ml,在最后一次冲洗液中加入试验菌,滤干,取出薄膜贴于琼脂培养基平板上。菌液组(B组):依法测定;供试品组(C组):取规定量的供试液,除不加阳性菌外,依法测定;稀释剂对照组(D组):用相应的稀释液替代供试品,加入试验菌,依法测定。

1.2.6 检查方法确定 常规法、培养基稀释法:先挑选金黄色葡萄球菌、枯草芽孢杆菌、白色念珠菌作为试验菌。采用常规法、培养基稀释法分别进行回收率试验,再据预测结果,确定计数方法并进行全菌种验证。薄膜过滤法[7]:经薄膜过滤法,用600 ml冲洗液冲洗后,进行菌落计数及回收率测定。
1.2.7 检查方法验证 取不同厂家的样品,按确定的方法对5株实验菌进行回收率试验。
1.2.8 控制菌检查方法确立与验证 外用消炎制剂,都不得检出金黄色葡萄球菌和铜绿假单胞菌,故以此二菌为验证菌株,以大肠埃希菌为阴性对照菌。分别作为试验组和对照组。试验组取供试液10 ml,加入适量的培养基中,按药典附录下的金黄色葡萄球菌进行检查,应检出该菌株。采用低速离心集菌薄膜过滤法时,取适量供试液,500r/min的转速进行离心5 min,取上清液10 ml,加至稀释液200 ml中混合均匀,经薄膜过滤,冲洗,在最后一次冲洗液中加入验证菌株,再加入相应的增菌液100 ml,按规定培养。阴性菌对照组,不得检出。依次采用常规法、培养基稀释法、离心薄膜过滤法。
2 结果
2.1 方法预试验结果见表1。可见样品对细菌有明显抑制作用,对真菌无抑制作用。因此,不可用常规法和培养基稀释法进行细菌计数,但常规方法适用于霉菌及酵母菌计数检查。薄膜过滤法预试结果显示,细菌的回收率都高于70%以上[8]。因此可确定用薄膜过滤法进行细菌计数检查,用常规法进行霉菌及酵母菌的计数检查。
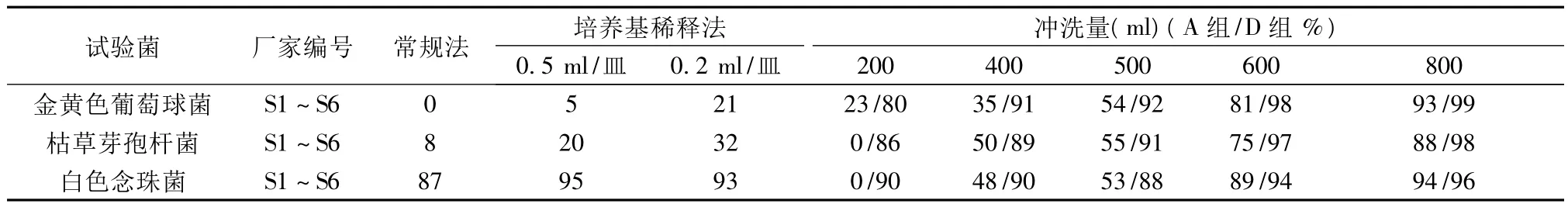
表1 常规法、培养基稀释法回收率预试验结果(%)
2.2 方法验证结果见表2。结果显示3次平行度验证的回收率均达到了70%以上,说明所用方法符合2005年版中国药典的规定。
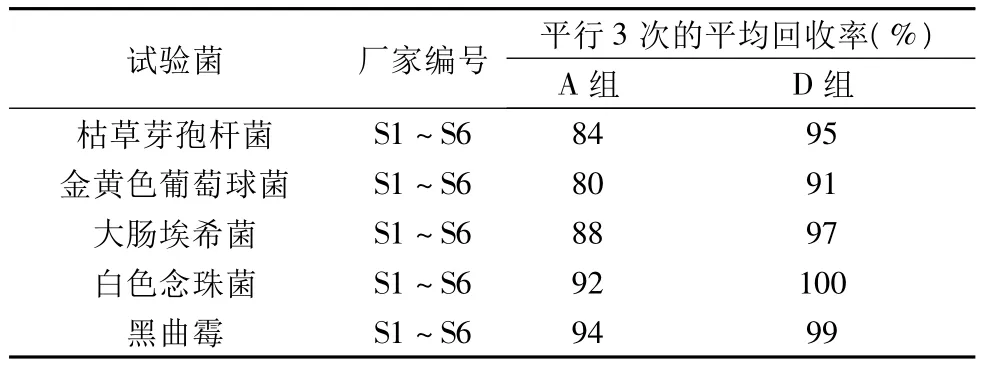
表2 不同厂家的样品验证试验结果
2.3 依据控制菌检查方法验证后,结果表明,金葡菌和铜绿菌以低速离心集菌薄膜过滤法,冲洗量以400 ml最佳冲洗量,能够有效去除该类药品的抑菌活性。
3 讨论
红霉素软膏对真菌几乎无抑制作用,因此可用常规方法进行霉菌及酵母菌检查。但对细菌有很强的抑制作用,但细菌检查以低速离心集菌薄膜过滤法,冲洗量600 ml/膜最佳。控制菌检查,采用低速离心集菌薄膜过滤法,以400 ml冲洗量为宜。薄膜过滤法时,冲洗量宜采用少量多次的梯度冲洗法,有利于供试液中微生物的回收,并先加入到一定量的稀释液中,有助于细菌分散均匀,益于过滤。因验证工作量大,为尽快掌握验证方法,先以少数敏感菌进行预试验,可以快速找准检测方法。红霉素软膏的基质全是油包水型的,不易溶解于水中,因此加入无菌十四烷酸异丙酯,无菌的玻璃珠振摇,可以有效地溶解软膏,分散均匀,同时置于8℃以下的环境中静置分层,有利于将水层分离出来做为供试液。
[1] 国家药典委员会.中华人民共和国药典(二部).北京:化学工业出版社,2005;附录XIH:附录89-98
[2] 于荣,李海妮,邢俊生.诺氟沙星软膏微生物限度检查方法的建立和验证.中国药物与临床,2009,9(9):831-833
[3] 陆益萍.3种软膏剂的微生物限度检查验证.安徽医药,2008,12(4):318-319.
[4] 马晓璇,李汶,温玉莹.2种含硫磺制剂的微生物限度检查方法验证.今日药学,2009,19(2):50-51.
[5] 袁林娜.苗药肤痔清软膏微生物限度检查方法验证试验研究.中国民族民间医药杂志,2007,(3):171-173.
[6] 吴晓敏,王燕燕.8种医院制剂微生物限度检查方法验证.中国医院药学杂,2007,27(1):93-94.
[7] 宋勤,杜平华.中成药微生物限度检查法的探讨.中国药事,2006,20(1):46-48.
[8] 李秋菲,唐振宏,张芹,等.4种大环内酯类药物微生物限度检查方法验证.中国药业,2008,17(13):20-21.
Method Validation of microbial limit Test for erythromycin oiintment
LI Chuan-xiang.Anqing Institute for Food and Drug Control,Anqing 246001,China
ObjectiveTo establish the microbial limit test method for Erythromycin Ointment.MethodsThe antimicrobial effect of Erythromycin Ointment was determined by recovery rate with 5 control strains.ResultsAccording to theResultsof the recovery rate test.Erythromycin Ointment had higher antimicrobial effects.ConclusionThe antimicrobial effect must be eliminated by centrifugation and membrane filtration.The method can be used to the microbial limit test for Erythromycin Ointment.
Erythromycin Ointment;microbial limit;Recovery rate根据2005年版中国药典规定微生物限度检查应进行验证。红霉素属于大环内酯类的抗生素,对革兰氏阳性微生物
246001安庆市食品药品检验所
·论著·

