乙醇与金属钠反应实验的新方法
赵立国 齐俊林
唐山师范学院玉田分校 河北唐山 064100
乙醇与金属钠反应实验的新方法
赵立国 齐俊林
唐山师范学院玉田分校 河北唐山 064100
乙醇与金属钠的反应实验是一个典型的常规实验。但笔者通过多年的教学实践发现,按照现行人教版高中化学教材化学第二册第151页[实验—62]的实验方法及实验装置(如图1所示)进行实验时,很难得到纯净的氢气。其主要原因是金属钠和无水乙醇用量较小,产生的氢气的量严重不足,不能将反应器内的空气排尽,从而得不到纯氢气。故对氢气进行点燃检验时,将会造成一定的安全隐患。针对这一情况,笔者进行认真的设计和研究,总结出实验的新方法,收到较好的实验效果。
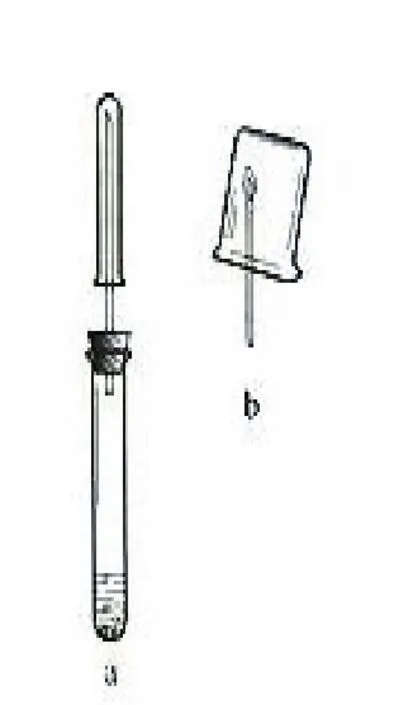
图1 教材中乙醇与金属钠反应实验装置
1 实验用品
两通管(2 cm×4 cm)1根,气球1个,3号单孔塞1只,两通旋塞阀门1个,烧杯1只,细线若干,火柴1盒。
金属钠,无水乙醇。
2 实验装置(图2)
3 仪器组件的处理与组装
1)取一个两通旋塞管,将一端用三角钢锉截去一段,然后用胶管将一小段玻璃尖嘴固定在上方。
2)装有玻璃尖嘴的两通旋塞管的另一端插入弹孔橡胶塞的孔内。
3)将一个内壁干燥的气球用细线牢固地系在两通管的一端,然后用细线将两通管下方的气球部分沿管口扎紧(其目的是使用较小的气球部分,以便节省无水乙醇的用量)。

图2 实验装置
4 实验方法及其现象
1)将一小块绿豆粒大小的金属钠从扎有气球的两通管的上方放入,直达扎细线的气球部位,然后用细线在金属钠上部紧紧地用活扣将气球扎紧(如图2所示)。
2)将扎有气球的两通管注满无水乙醇。
3)打开胶塞上两通旋塞管的阀门,将此胶塞紧紧塞在盛有无水乙醇的两通管上管口,此时无水乙醇充满两通旋塞管。
4)关闭两通旋塞管的阀门。
5)将金属钠上方细线活扣解开,此时金属钠与无水乙醇接触并发生反应,立即产生气体。又因金属钠的密度小,在无水乙醇中金属钠迅速上升至两通管的上管口处。产生的气体因被密封在两通管内使其内部压强增大,气球体积膨胀。
6)慢慢打开两通旋塞管上的阀门,使其内部的无水乙醇全部被两通管内的气体顶出后,用点燃的火柴靠近玻璃尖嘴,可以观察到气体在安静地燃烧,产生蓝色火焰。迅速将内壁干燥的烧杯罩在火焰的上方,片刻可以观察到内壁产生水滴。接着在烧杯中加入澄清石灰水,石灰水不变浑,说明实验产生的是氢气而不是二氧化碳。
5 实验优点
构思巧妙,取材容易,实验简单,便于操作,安全可靠,效果明显,有利于培养学生的创新意识。
10.3969/j.issn.1671-489X.2011.03.093

