纤维素高粱红原液着色技术研究
王光银,金 东,黎 谦(, )
1 前言
纤维素是自然界中广泛存在的可再生资源,是由β-D-葡萄糖通过1,4苷键结合而成的高聚物[1]。苷键的存在、纤维分子间和分子内大量存在的氢键间相互作用、纤维局部规整的结晶序列等因素使得纤维素不易水解,普通溶剂难以将其溶解[2-4]。近年来开发有多种纤维素溶剂体系,如N-甲基吗啉-氧化物(NMMO)、LiCl/二甲基乙酰胺、离子液体、氨基甲酸酯以及NaOH/尿素或NaOH/硫脲溶剂体系等[5-6],其中NaOH/尿素/水溶剂体系能快速溶解纤维素且绿色环保,是一种极具发展前途的纤维素溶剂,该溶剂与纤维素的作用对于开发新型再生纤维具有重要意义[7-10]。
目前再生纤维素染色主要采用合成染料,而部分合成染料对人体健康存在潜在危险[11]。合成染料的制备及应用过程中对环境产生的污染问题正日益受到关注,多种危害人类健康的染料已被禁用[12]。天然染料具有无毒、无污染的特点,对人体无毒、无害、无副作用而重新得到人们的重视[13-14]。高粱红是从高粱壳中提取的一种天然色素,性质稳定,为获得较高的得色效果我们可通过原液着色技术实现高粱红对再生纤维素的着色[15-16]。
纤维素纤维原液着色有很多优点,但到目前为止再生纤维的染色还是以后染为主[17]。纤维素原液着色技术预计可实现纤维素制品纺丝和染色的一体化生产,解决染料染色中存在日晒牢度差、色泽不匀等弊病,省略了下游产品的染色环节,减少水和能源消耗,有效解决染厂的污水问题[18-19]。
2 实验部分
2.1 试剂与仪器
主要试剂:棉短绒(DP=100,000);高粱红染料;氢氧化钠;无水硫酸钠;浓硫酸;尿素。
主要仪器:SF-600型电脑测配色仪(DATACOLOR);TU1901紫外可见分光光度计;AS-24振荡染色机。
2.2 透明再生纤维素膜的制备
棉短绒于80℃真空干燥24 h备用。将7wt%NaOH/12wt%尿素水溶液冷却至-12℃加入棉短绒,于室温下快速搅拌制成4wt%的纤维素溶液,离心过滤去除凝胶,超声脱气,得清澈透明纤维素溶液。再将纤维素溶液采用流延法制膜,依次浸入第一凝固浴(5wt%H2SO4/Na2SO4水溶液)及第二凝固浴(5wt%的H2SO4溶液)凝固得透明再生纤维素膜(RC0)。
2.3 高粱红原液着色实验
2.4 再生纤维膜染色实验
将实验制得透明再生纤维素膜(RC0)用高粱红染色,实验处方为:
高粱红:(0.5%,o.w.f )
温度:80℃
时间:30 min
浴比:1∶30
染色工艺曲线(见图1):
图1 染色工艺曲线
将染色纤维素膜水洗后取出于空气中自然风干,制得再生纤维素膜(RC2)。
②目前国内发表的相关成果主要是王立新《美国国家认同的形成及其对美国外交的影响》(《历史研究》2003年第4期)、《美国的国家认同及面临的挑战》(《中国社会科学报》2010年8月24日)等,其中有一定篇幅论及自由主义与美国国家认同的关系。
2.5 UV-Vis紫外光谱分析
将原液着色和染色再生纤维素膜分别用TU1901紫外可见分光光度计测定其吸收光谱曲线。
2.6 K/S值 Lab值 三刺激值的测定
K/S值、Lab值、三刺激值采用Datacolor SF600电脑测配色仪测试,测试条件为膜4层,D65光源和A光源,10°标准视场,扫描范围400~700 nm,读取最大吸收波长处数据。
2.7 水洗牢度的测定
将原液着色和染色的再生纤维素膜分别于振荡机中80℃水洗30 min,再用722型分光光度计测定水洗前后再生纤维素膜在最大吸收波长下的吸光度(A0)及(A1)并计算脱色率。
3 实验结果与讨论
3.1 再生纤维素膜的制备
棉短绒纤维素可在-12℃的7wt%NaOH/12wt%尿素水溶液形成均相透明的溶液,并且当温度升高至室温时也不会析出。-12℃7wt%NaOH/12wt%尿素水溶液有很强的极性,可以将纤维素的分子内氢键打断,同时形成纤维素与溶剂间的氢键,促进纤维素的溶解。
当体系中的成分发生变化时,溶剂的极性降低,分子间氢键减弱,纤维素趋向于形成分子内氢键,从而析出。
3.2 UV-Vis紫外可见光谱分析
对高粱红原液和再生纤维素膜进行紫外光谱分析,得高粱红的吸收光谱曲线图,见图2。
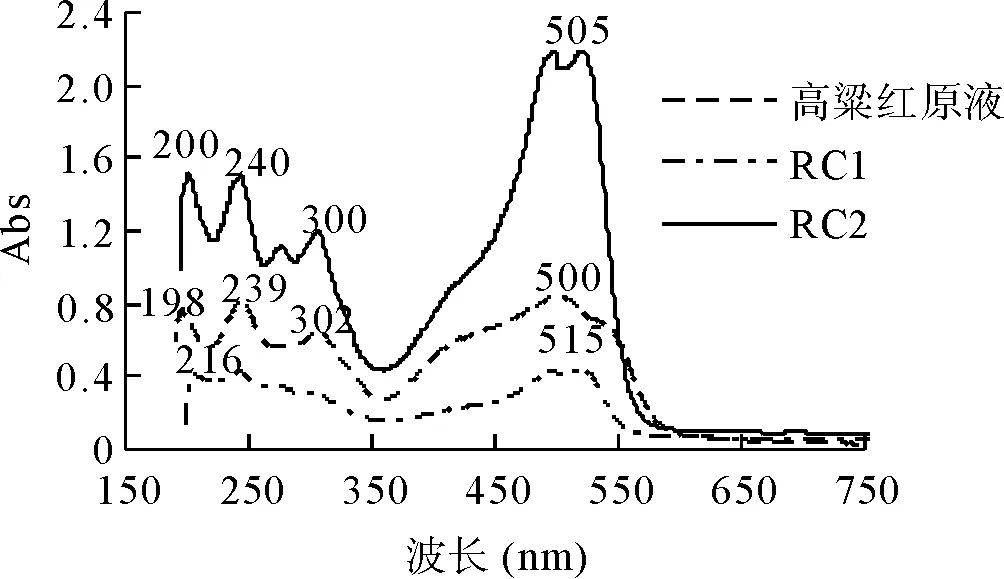
图2 高粱红的吸收光谱图
由图2可知,在可见光波长范围内,高粱红原液的最大吸收波长λmax为500 nm,在紫外光区有3个吸收峰,在λ=275 nm左右出现一较弱的吸收带且呈现出一个很平缓的宽峰形状,其结构中含有苯环。第3个吸收峰出现在λ03=300 nm处,说明结构中含有羰基。RC1吸收光谱曲线,在可见光波长范围内,最大吸收波长为515 nm,在紫外区也有3个吸收峰,但是吸收峰向长波移动发生红移,说明共轭体系增大,共轭双键发生π→π*跃迁。RC2的吸收曲线与高粱红原液的吸收曲线几乎一致,没有发生红移。
3.3 再生纤维素膜K/S值与波长关系
测试再生纤维素膜RC1及RC2的K/S值,制得曲线图(见图3)。
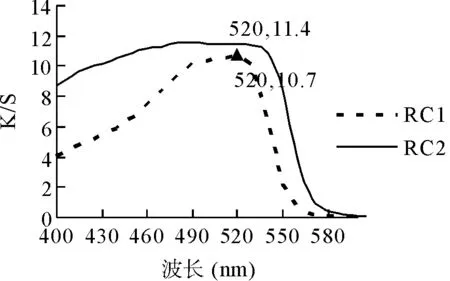
图3 再生纤维素膜RC1及RC2的K/S值
由图3可知,当波长小于520 nm时,K/S值随波长的增加而增大,当波长大于520 nm时,K/S值又随波长的增加而减小;且RC2的K/S值始终大于RC1的K/S值,说明再生纤维素染色膜比原液着色再生纤维素膜表观色深。
3.4 K/S值 Lab值 三刺激值
测试最大吸收波长下RC0,RC1,RC2纤维素膜的K/S值、Lab值及三刺激值如表1所示:
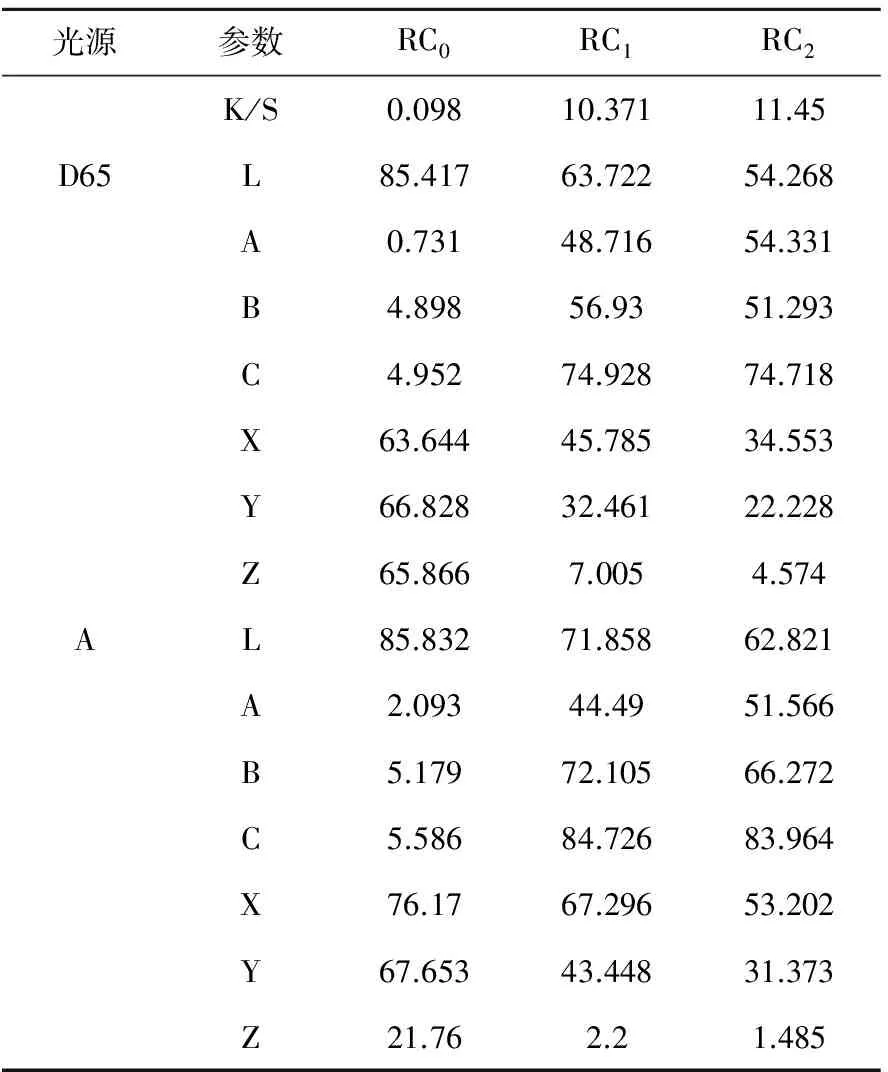
表1 再生纤维素膜的K/S值 Lab值 三刺激值
由表1分析可知,高粱红天然色素对再生纤维素膜着色的直接性较好,两种再生纤维素膜均可获得较深的颜色,RC2的K/S值虽然大于RC1,但由于只是初步染色,尚未寻找最佳染色工艺,可能是由于天然色素的表面吸附而导致的表观色深,产生RC2K/S值更高的结果。而RC1K/S值为10.37,已达到理想效果。
L代表亮度值的大小,由于RC2的K/S值较大,因此其L值亮度小于RC1。红-绿值A显示,RC1和RC2均偏红,且RC2的A值大于RC1的,RC2偏红程度较大;黄-蓝值B显示:RC1和RC2均偏黄,且RC1的B值大于RC2,RC1偏黄程度较大。两种纤维素膜的C值大小相近,因此两种再生纤维素膜的鲜艳度相近。
三刺激值显示RC1中的三原色光红、绿、蓝含量均大于RC2,是因为原液着色时高粱红天然色素已均匀渗透入纤维素内,亮度较大;而再生纤维素膜染色时染料吸附在纤维膜表面,颜色较深,亮度较暗。RC2的三原色光含量较少,所得颜色效果较暗。
3.5 水洗牢度及脱色率的计算(见表2)
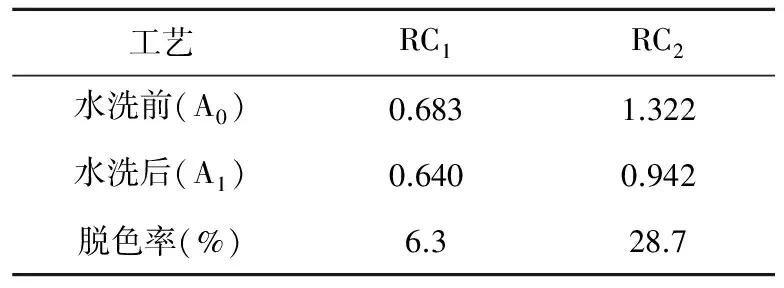
表2 水洗前后RC1 及RC2的吸光度
由表2数据分析可知:RC1水洗前后吸光度差值较小,水洗牢度较好,RC2水洗前后吸光度差值差较大,水洗牢度较差。由脱色率可知:RC2脱色率远远大于RC1脱色率,说明原液着色的再生纤维素膜的水洗牢度好,染色再生纤维素膜由于染料吸附在纤维膜表面易于洗除而水洗牢度较差。
4 结论
-12℃的7wt%NaOH/12wt%尿素水溶液可将棉短绒纤维素溶解形成均相透明溶液,采用该溶剂体系溶解纤维素并采用原液着色法对再生纤维素膜着色,成膜后其K/S值较大为10.37,水洗后彩色再生纤维素膜脱色率较低为6.3%,表明原液着色所得再生纤维素膜的颜色较深,色光度好,水洗牢度好。染色再生纤维素膜染料吸附在纤维膜表面,其K/S值为11.45颜色较深,但是脱色率为28.7%,水洗牢度差。原液着色法对再生纤维素进行着色,染料可以全部利用,不仅减少了染料的浪费还可减少水和能源的消耗,有效解决了印染厂的污水问题。
[1] Hermanutz F,Ga hr F,Uerdingen E,et al.New developments in dissolving and processing of cellulose in ionic liquids[J].macromol symp,2008,262(1):23—27.
[2] 殷延开,陈玉放,戴现波,等. 纤维素的溶解及活化过程[J].纤维素科学与技术,2004,12( 2):54—63.
[3] Zhang W, Okubayashi S, Bechtold T.Modification of fibrillation by textile chemical processing[D].Lenzinger Berichte 2003.
[4] 徐田军,冯玉红,庞素娟.纤维素的溶解研究进展[J].热带生物学报,2010,(2):187—192.
[5] CHANZY H,PEGUY A. Oriented cellulose films and a mesophase system[J]. J Polym Sci: Polylm Phys Ed,1980,(18): 1137—1144.
[6] Zhang S,Yuan B L,Li Fx,et al.Structure and properties of novel cellulose fibers[J].Chem Fibers Int,2008,58(3):171—173.
[7] YANG Zhili,WU Guoning, MEIQianfang.Study on themanufacture of rayon fiber from a PF /DMSO solvent system[J].Cellulose Chem Technol, 1987, (21):443—505.
[8] 吴翠玲,李新平,秦胜利.纤维素溶剂研究现状及应用前景[J].中国造纸学报,2004,19(2):171—175.
[9] 张俐娜,吕昂.纤维素溶剂研究进展[J].高分子学报,2007,(10):937—944.
[10] 茅源.NaOH/尿素溶液中纤维素膜和纤维的凝固条件研究[D].武汉:武汉大学,2005.
[11] Yamashiki T, et al.New class of cellulose fiber spun from the novelsolution of cellulose by wet spinning method[J].Journal of Applied Polymer Science, 1992, 44 (40):691.
[12] 胡昌玉.苯胺类化合物结构-毒性定量构效关系研究[J].中国科学( B 辑),2000,30(1):1—7.
[13] 李景林,李淑芬.高粱红色素的主要成分及结构分析[J].辽宁农业大学,1993,(5):47—49.
[14] Bombalski L,Min K,Dong H.Preparation of Well-defined Hybrid Materials by ATRP in Miniemulsion [J].Macromolecules,2007,(40):7429—7432.
[15] 付少海,张凯,孙贵生,杜长森.纤维素纤维原液着色技术的研究进展[J].纺织导报,2010,(5):73—75.
[16] 解芳,邵自强.天然纤维素纤维的溶解机理及纺丝技术发展[J].华北工学院学报,2002,23(2):119.
[17] Porter L J J,Hrstich J N,Chan B G.Theconversion of proantho cyanidinsand prodelphen idins to cyanidins and delphenidim.PHytochemistry,1986,25(6):223—230
[18] I.G.Farbenindustrie A.-G.Process for the manufacture of dyed filaments and films.GB 448447; June 8, 1936.
[19] 贺连萍,胡开堂.天然纤维素的溶解技术及其进展[J].天津化工,2006,20(1):7.

