城市内河强还原性沉积物耗氧及相关因素研究
马晓磊,徐继荣,张德民,高华生,陈和平
1.宁波大学建筑工程与环境学院,浙江 宁波 315211
2.宁波大学生命科学与生物工程学院,浙江 宁波 315211
3.中国科学院南海海洋研究所,广东 广州 510301
城市内河强还原性沉积物耗氧及相关因素研究
马晓磊1,2,徐继荣1,3*,张德民2,高华生1,陈和平1
1.宁波大学建筑工程与环境学院,浙江 宁波 315211
2.宁波大学生命科学与生物工程学院,浙江 宁波 315211
3.中国科学院南海海洋研究所,广东 广州 510301
2009年7—8月间选择浙江省宁波市4条污染程度不同的内河,采集沉积物和水质样品.采用自制的多管、多电极沉积物耗氧研究装置测得沉积物耗氧(SOD)值高达13.8~9.4×104mg/(m2·h),其中张桂河路林市场段(ST2站)SOD为87.0 mg/(kg·h);同时测定了各站水质、沉积物理化指标.结果表明:水体水温和沉积物w(氨氮)与 SOD有较高的相关性,而有机质、底层ρ(DO)和ρ(CODCr)与SOD的相关性较差.表观污染严重的站位其沉积物表现出强烈的“瞬时耗氧”现象,这很可能是造成水体缺氧的主要原因之一.
城市内河;强还原性沉积物;SOD;瞬时耗氧
随着城市化进程的加快,污水排放总量不断增加,城市内河的污染负荷越来越大.在过去的几十年里,我国多数城市内河水质都经历了从可饮用到鱼虾绝迹、黑臭难耐的恶化过程,内河水环境治理已成为当务之急.目前对于城市内河水环境的研究多集中于水体有机物污染和富营养化[1-7],对沉积物的研究主要集中在重金属元素[8-13]的存在形态方面.而城市内河沉积物中有机质累积造成的内源性污染,尤其是沉积物的耗氧引发的水体缺氧症往往是水环境改善的瓶颈.
沉积物耗氧(SOD)指水体底部沉积物消耗上覆水中溶解氧(DO)的速率[14].研究[15]指出,沉积物耗氧约占整个水体耗氧的90%,对其上覆水DO含量影响很大[16-19].影响 SOD的根本因素是沉积物生物学成分,如沉积物有机质含量和宏观生物或微生物密度.其他比较重要的影响因素有沉积物-水界面的温度、河流深度[20-21]和上覆水流速[22-23]等.TODD等[24]测得佐治亚洲黑水河 SOD值为20.5~591.2 mg/(m2·h),高于文献报道[25]的 18 倍以上,并且指出,固体有机碳和总有机碳可以作为SOD的预测指标.UTLEY等[26]指出,不同河流的低溶解氧含量和SOD值较高问题可能受不同因素的影响.国内对苏州河的研究[27]发现,SOD季节变化明显.水体长期缺氧使得水体和沉积物环境发生一系列变化,如沉积物-水界面宏观底栖生物消失,微生物代谢对有机质的作用从好氧降解变为厌氧降解,CO2,H2O,NO3-和SO42-作为氧的电子供体转变为CH4,NH3,H2S和有机酸等还原性物质[28]. 研究城市内河强还原性沉积物耗氧量及其环境因子的相关性,是该研究的主要目的.
1 材料与方法
1.1 样品采集
1.1.1 采样站位
在宁波市城区选择了污染程度不同的4条河流设4个站位,分别位于宁波市区的江北大河中段、张桂河路林市场段、中塘河东段和西塘河东段,并分别编 号 为 ST1(29°54′24.6″N,121°35′24.3″E),ST2(29°54′16.2″N,121°35′36.5″E),ST3(29°51′10.3″N,121°35′30.4″E),ST4(29°52′46.3″N,121°31′23.4″E).中塘河与西塘河是宁波市的主要景观河道,江北大河是连接城郊的河道,张桂河是污染较为严重的城中村河道,水体颜色为浑浊的黑色.

图1 采样站位Fig.1 Positon of the sample sites
1.1.2 采样装置和方法
使用容积为2.5 L的有机玻璃采样器采集水样,用聚乙烯塑料瓶(500 mL)贮存,采样后立即送至实验室分析.为了使沉积物物样品的层次不被破坏,保证试验的准确性,使用USSC-Ⅱ单管无扰动沉积物采样器[29]采集沉积物样品.采样管也是培养管(透明PC材制,内径50 mm,管长350 mm).采样时可以清楚地观察到沉积物是否受到了明显扰动,如果样品受到扰动,将舍弃重新采集.
每个站位设6个采样点(4个站位共24个),采集6个用于SOD研究的沉积物样品,以培养管贮存;同时采集用于理化分析的沉积物样品,以聚乙烯塑料袋贮存.样品立即送往实验室并在4 h之内测定SOD及相关因子.
1.2 分析方法
1.2.1 理化参数分析
使用在线水质监测仪(Multi 340i,德国WTW公司)现场检测各站位水体温度,p H,电导率和ρ(DO).水样和沉积物样品的实验室检测分析方法均参照国家标准[30].采用自行设计的多管、多电极装置测定SOD.
1.2.2 SOD测量装置与方法
通常不同采样点沉积物中有机质和耗氧物质含量差异较大,常用的单管SOD测定装置存在沉积物样品代表性差和测定效率较低等缺点.笔者设计了多管、多电极SOD研究装置(见图2),主要由恒温水箱、柱状沉积物采样管(用于直接采样和培养)、循环泵组成.采样管的数量可根据需要选用1~6根,相邻采样管间用塑料管串联.根据研究需要可在培养管中置入DO,氧化还原电位(ORP)和S2-选择电极等,同时测定上覆水中ρ(DO),ORP值和 S2-电极电位等参数随时间的变化,其测定结果是各培养管的平均值.

图2 多管、多电极SOD测量装置Fig.2 SOD measuring device equipped with multi-electrodes&tubes
试验过程中控制采样管中泥柱高度为10 cm或称取一定质量沉积物置于底端密封的采样管中,采用DO饱和的纯水替代河水作为沉积物上覆水,用微型蠕动泵(德国GroTech,流量为0~120 mL/min)内部循环6个培养管中上覆水,同时记录各参数变化,当DO电极电位值稳定时(3 h或不再变化)结束测量.SOD计算公式为:
SOD= Δρ(DO)·V/M·t
式中,Δρ(DO)为上覆水 ρ(DO)变化值,即 DO消耗量,mg/L;V为上覆水体积,m3;t为ρ(DO)变化达到稳定的时长,h;M为沉积物质量,g.
2 结果
2.1 SOD测定结果
由表1可知,ST2站 SOD值最大,是 ST4站的7 000多倍,ST1和 ST3站的SOD值属同一数量级.而在测定ST2站SOD时,发现ρ(DO)在2 min降至0 mg/L,考虑到电极的响应时差,实际时间可能更短.鉴于该站沉积物瞬时耗氧十分强烈,SOD值过高,上覆水中DO在极短的时间内耗尽,不能完成后续“非瞬时耗氧”量测定.为此,取10 g ST2站沉积物置于培养管中,以DO饱和的纯水作为上覆水,测其耗氧量为 3.2 mg/L,SOD 为 87.0 mg/(kg·h)〔见图 3(a)〕.
为了研究瞬时耗氧在沉积物总耗氧中所占比例,取10 g ST2站沉积物进行了14 d的SOD研究〔见图3(b)〕.ST2站“瞬时耗氧”量(DO消耗量)为1.5 mg/L(前7.5 h),占总耗氧量的26%,“瞬时耗氧”段〔如图 3(b)〕的 SOD平均值为 11.6 mg/(kg·h),而剩余时间的 SOD平均值为 0.9 mg/(kg·h).为了研究温度对 SOD的影响,取10 g ST2站沉积物.在10,20和30℃下测DO消耗量分别为 1.3,3.3和 4.4 mg/L,SOD 分别为 3.5,9.1 和12.1 mg/(kg·h)(见图4).3个温度下均存在“瞬时耗氧”现象,其耗氧量分别占测量时段内总耗氧量的86%,61%和77%.

表1 各站SOD测定结果Table 1 SOD of the sites

图3 ST2站位沉积物(10 g)的DO消耗量变化Fig.3 DO consumption curve of sediment(10 g)from ST2

图4 ST2站位不同温度下沉积物(10 g)DO消耗量变化Fig.4 DO consumption curves of sediment(10 g)from ST2 under different temperature

图5 ST1站DO消耗量曲线Fig.5 DO consumption curve of sediment from ST1
由图5可知,498 min时,由于上覆水中 DO被耗尽,ST1站 DO消耗量不再增加,此时 SOD值为263.2 mg/(m2·h),更换上覆水后发现DO消耗量下降趋势明显,与之前不同的是,ρ(DO)降低至 4.0 mg/L后,下降趋势变缓,最终趋于稳定,此时SOD值为431.3 mg/(m2·h).因此,ST1站的实际 SOD值应为 694.5 mg/(m2·h).
2.2 各站水质因子测定结果
由表2可知,现场水质指标中各站的水温最大相差4℃,pH最大差值为0.3,ST1和 ST4站表层ρ(DO)明显高于其他两站,ST2站的表层ρ(DO)最低,各站底层ρ(DO)均在0.3 mg/L左右.说明各站沉积物均处于缺氧状态.
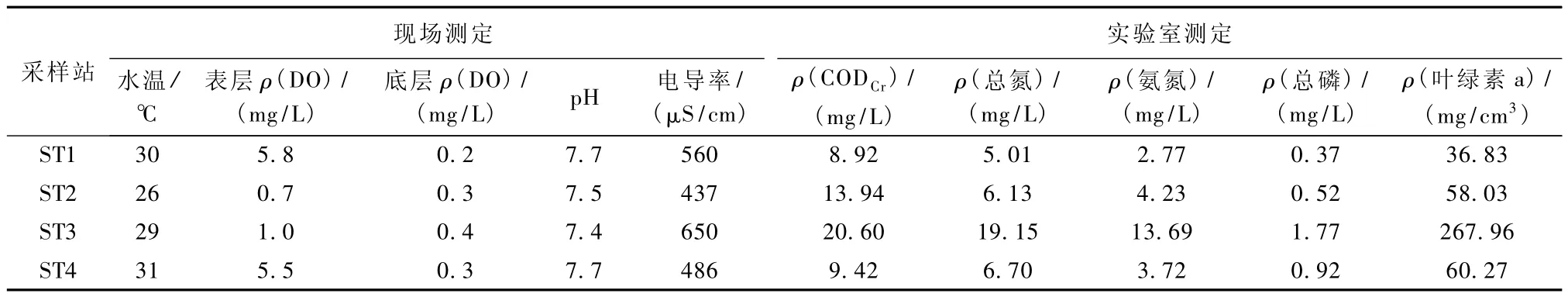
表2 各站水质因子测定结果Table 2 Results of the water quality factors measurement
2.3 沉积物理化因子实验室测定结果
ST2站SOD最高,ST1站和ST3站的 SOD属于同一数量级,只有w(氨氮)符合该规律(见表 3).SOD最低的 ST3站的w(有机质)和w(总氮)最高,SOD最高的 ST2站的w(有机质)居中,其w(总氮)与ST1站相同.3个站沉积物pH均比上覆水低.总体上,各站沉积物的w(总氮),w(氨氮)和w(总磷)均明显高于水体.

表3 ST1,ST2和ST3站底质测定结果Table 3 Results of ST1,ST2,ST3 sediments measurement
2.4 沉积物上覆水ORP电极和S2-选择电极电位的变化
自制 SOD研究装置在测定ST4站 SOD的同时,用ORP电极和S2-选择电极检测上覆水中ORP和S2-电极电位的变化(见图6).

图6 ST4站的DO消耗量,ORP电极和S2-选择电极示数变化曲线Fig.6 Profile of DO,ORP and S2- curve of ST4
从图6可知,水体ORP不断升高,S2-选择电极电位逐渐下降.说明随着ρ(DO)的消耗,水体中的ORP和S2-含量变化存在特定的趋势关系.
3 讨论
3.1 沉积物的瞬时耗氧现象与耗氧特性曲线
用纯水替代上覆水测ST2站SOD时发现耗氧量极高的瞬时耗氧现象.电极测量结果表明,在2 min内电极ρ(DO)示数从最初的7.0 mg/L迅速降为0 mg/L,考虑到DO电极测量的响应时间,DO被耗竭的时间可能比2 min更短,该现象说明沉积物-水体界面发生了瞬时的氧化还原反应.因为速率极高,所以瞬时耗氧过程不可能是生化耗氧过程,而可能是沉积物向水体中扩散的能够发生快速耗氧的强还原性物质,即“瞬时耗氧”物质的耗氧过程.“瞬时耗氧”物质可能是 H2S,FeS,羟胺(NH2OH),硫醇,有机酸及一些强还原性硫化物或某种反应中间体,具体成分有待进一步研究确认.因为遇氧即被氧化,故瞬时耗氧物质的快速耗氧特性用传统的检测方法难以进行准确测量,并且通常用作沉积物耗氧指标的CODCr和有机质含量值中并不包括该类物质的耗氧.
按照单位质量耗氧量87.0 mg/(h·kg)计算,则1 kg沉积物至少可完全消耗10.7~11.7 L水中的DO.该现象说明严重污染的沉积物耗氧作用非常强烈,是导致水体黑臭的重要原因.
研究[30]认为,一般情况下严重污染至黑臭的河流水体中 DO被消耗的过程分4个阶段[31]:还原性耗氧阶段,生物化学碳耗氧第Ⅰ阶段(CBODⅠ),生物化学氮耗氧(NBOD)阶段和生物化学碳耗氧第Ⅱ阶段(CBODⅡ).试验中的瞬时耗氧速率非常快,占水环境整体耗氧的比重很大,不能简单地划分为4阶段耗氧曲线中的第Ⅰ阶段.笔者假设在长期厌氧的条件下生物对底泥作用产生了一些强还原性的“瞬时耗氧物质”.该类耗氧物质可能是河流水环境耗氧的主要因素之一,也是能够最先、最快地消耗水体DO的物质.因此,笔者认为,污染严重的城市内河水体中DO被消耗的过程很可能存在5个阶段:瞬时耗氧阶段,一般氧化还原耗氧阶段,CBODⅠ,NBOD阶段和CBODⅡ(见图7).
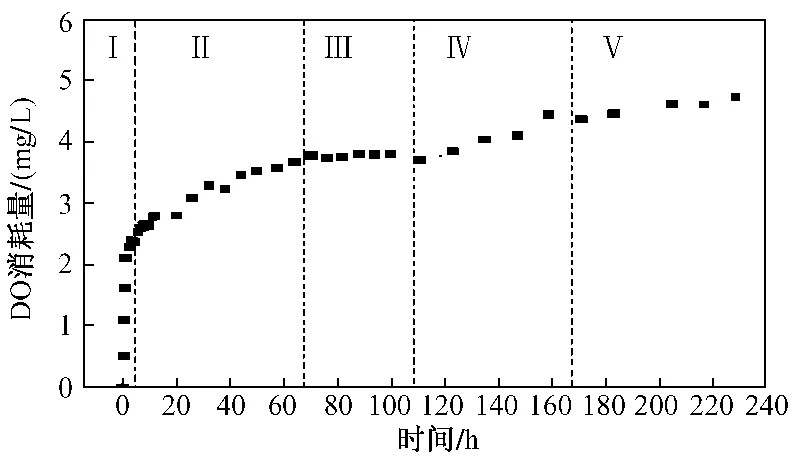
图7 DO消耗量变化5个阶段曲线Fig.7 Curve of five DO comsumption stages
3.2 SOD与相关水质指标的关系
水温与藻类等植物光合作用共同影响水体DO,水温升高 DO饱和度下降,藻类繁盛则表层ρ(DO)增高,在水体温度与沉积物-水界面温度基本同步的情况下,水体温度对沉积物微生物活性的影响较大.总体上水体温度对DO的来源和去向都有较大影响.图4中不同温度下ST2站单位质量沉积物耗氧曲线表明,随着水温升高耗氧量增加,该结果与林卫青等[27]对苏州河不同季节耗氧量的研究结果一致.水质营养盐指标偏高的ST3站水质处于明显的富营养化状态,大量浮游藻类光合作用产生O2在一定程度上可以改善水体-沉积物界面的厌氧条件,但是大量藻类死亡后将会产生新的有机耗氧物质,加重水体厌氧,促进生物对有机质的厌氧降解,进而产生大量还原性产物或瞬时耗氧物质,导致产生高SOD现象.ST2与ST4站除表层ρ(DO)相差4.8 mg/L,其他水质指标基本相近,但二者的 SOD相差很大.这说明瞬时耗氧物质的产生可能主要取决于沉积物的种类和特性.徐祖信等[32]研究了苏州河沉积物对上覆水水质影响时发现,沉积物SOD与水体 ρ(DO)(1~6 mg/L)成反比(R2=0.637 3),而该研究4个站的表层ρ(DO)(0.7~5.8 mg/L)和底层ρ(DO)(≤0.4 mg/L)均不符合该规律,这可能是由于沉积物SOD与水体ρ(DO)的相关性与水质污染程度存在一定关系,当河流污染导致水体底层ρ(DO)均处于较低水平时,ρ(DO)很可能不再是影响 SOD的主要因素.有报道[33-34]指出,ρ(CODCr)与沉积物SOD具有正相关性,即证明水体中有机物的浓度受底泥中有机污染的影响.也有报道[35-36]指出,SOD 与水体ρ(CODCr)不具有绝对的正相关性,因为除沉积物中还原性有机污染物质向水体扩散引起ρ(CODCr)增高外,水体中腐烂的浮游生物也可能对其有较大贡献,故不同水体环境条件下影响水体ρ(CODCr)的主要因素不同.这可能也是各站水体ρ(CODCr)与SOD不具相关性的主要原因,ρ(CODCr)最高的 ST3站其ρ(叶绿素a)远高于其他站.
3.3 沉积物有机质含量与沉积物耗氧的关系
沉积物中一部分还原性的有机质可以直接消耗水体DO,此外,一部分有机质通过微生物降解间接消耗水体DO.微生物在不同条件下对不同特性的有机质进行降解产生多种类型的产物.天然有机质是稳定性极好的天然腐殖质类物质,在实际自然条件下其氧化过程极为缓慢和有限,不会对水体产生污染危害[37].城市污水中的有机质不同于天然有机质,前者更易悬浮和降解,长期厌氧条件下微生物对其进行厌氧降解产生的还原性产物很可能是SOD大幅增高的主要原因.SOD最高的ST2站有机质含量并不是最高的.这说明尽管有机质含量是造成沉积物耗氧的主要原因,但微生物对有机质作用产物对河流水体ρ(DO)的影响不容忽视.如果单纯以有机质来估量河流沉积物耗氧情况很可能产生较大的偏差.另一方面,沉积物产生瞬时耗氧现象很可能需要包括较低或很低的ρ(DO)值在内的其他某些特定环境条件.BORSUK等[38]提出了利用有机物含量预测底部SOD的贝叶斯递阶模型,但其研究对象为河口与海岸区域,无论是水体的物化特性还是水环境生态系统都与该试验所选研究对象差别较大.也有文献[39-40]指出,不同水体环境的SOD受不同的主要因素影响.该研究中除有机质外引起高SOD现象的具体原因仍需要进一步探寻.
4 结论
a.宁波市内河SOD最高值达9.4×104mg/(m2·h),比美国佐治亚洲黑水河的 SOD值〔591.2 mg/(m2·h)〕还要高出159倍.强还原性沉积物耗氧是水质改善的瓶颈,在治理具明显“瞬时耗氧”现象的内河时,采取清淤措施非常必要,否则水体缺氧状况难以改善.
b.宁波市内河沉积物SOD与水温和w(氨氮)有良好的相关性.
c.宁波内河中的城中村黑水河(ST2站)的沉积物内含有大量“瞬时耗氧”物质,是造成水体严重缺氧的主要原因之一.
d.改进的SOD研究装置具有多管、多电极的特点,可以更好研究内河沉积物的耗氧量,包括瞬时耗氧量,并能同步测定沉积物耗氧过程中上覆水ORP,pH和S2-等理化因子的变化.
e.试验过程中发现的沉积物瞬时耗氧物质,遇氧时会立即被氧化,推断可能是一些N,S的还原性物质及还原性有机物质,其主要成分有待进一步研究.
[1] 王焕松,雷坤,李子成,等.辽东湾海域水体富营养化的模糊综合评价[J].环境科学研究,2010,23(4):413-419.
[2] LIU W,QIU R L.Water eutrophication in China and the combating strategies[J].Journal of Chemical Technology &Biotechnology,2007,82(9):781-786.
[3] 濮培民,王国祥,胡春华,等.底泥疏浚能控制湖泊富营养化吗? [J].湖泊科学,2000,12(3):269-279.
[4] HU W F,LO W,CHUA H,et al.Nutrient release and sediment oxygen demand in a eutrophic land-locked embayment in Hong Kong[J].Environment International,2001,26(5):369-375.
[5] 袁文权,张锡辉,张丽萍.不同供氧方式对水库底泥氮磷释放的影响[J].JournaL of Lake Sciences,2004,16(1):28-34.
[6] 叶恒朋,陈繁忠,盛彦清,等.覆盖法控制城市河涌底泥磷释放研究[J].环境科学学报,2006,26(2):262-268.
[7] 张毓祥,刘登国.底泥营养物通量研究进展[J].上海环境科学,2009,28(3):125-129.
[8] 胡忻,曹密.南京市内河道沉积物中重金属元素形态及Pb稳定同位素组成[J].环境科学研究,2009,22(4):398-403.
[9] 张凤荣,储昭升,金相灿,等.洞庭湖平原中小型湖群沉积物铬污染特征与评价[J].环境科学研究,2009,22(12):1420-1425.
[10] 杨丽原,沈吉,张祖陆,等.南四湖表层底泥重金属污染及其风险性评价[J].湖泊科学,2003,15(3):180-214.
[11] 张立,袁旭音,邓旭.南京玄武湖底泥重金属形态与环境意义[J].湖泊科学,2007,19(1):63-69.
[12] 龚霞,刘淑娟,曹维鹏,等.鄱阳湖及支流底泥中重金属形态研究[J].江西农业大学学报,2006,26(4):620-624.
[13] 吕文英,周树杰,黄强南.珠江长州断面底泥重金属污染潜在生态危害评价[J].水资源保护,2009,25(3):22-28.
[14] HATCHER K.Introduction to part 3:sediment oxygendemand measurement[C ]//Sediment oxygen demand: processes,modeling,and measurement.Athens,Georgia:Institute of Natural Resources,University of Georgia,1986:301-305.
[15] BOWMAN G,DELFINO J.Sediment oxygen demand techniques:a review and comparison of laboratory and in situ systems[J].Water Res,1980,14(5):491-499.
[16] PARR L,MASON C.Causes of low oxygen in a lowland,regulated eutrophic river in Eastern England [J].Sci Total Environ,2004,321(1/2/3):273-286.
[17] WALKER R,SNODGRASS W.Model for sediment oxygen demand in lakes[J].Environ Engineering,1986,12(1):25-43.
[18] 李文红,陈英旭,孙建平.不同溶解氧水平对控制底泥向上覆水体释放污染物的影响研究[J].农业环境科学学报,2003,22(2):170-173.
[19] 乔士斌,林钦.大鹏澳网箱养殖区沉积物耗氧的初步研究[J].南方水产,2006,2(3):32-39.
[20] ZIADAT A H,BERDANIER B W.Stream depth significance during in-situ sediment oxygen demand measurements in shallow streams[J].Journal of the American Water Resources Association,2004,40(3):631-638.
[21] MAKENTHUN A,STEFAN H G.Effect of flow velocity on sediment oxygen demand experiments[J].Environ Engineering,1998,124(3):222-230.
[22] TRUAXETA,TRUAX D D,SHINDALA A,et al.Comparison of two sediment oxygen demand measurement techniques[J].Environ Engineering,1995,121(9):619-624.
[23] 王敏,张明旭.苏州河武宁路断面底泥需氧量的测定[J].上海环境科学,2003,22(6):418-422.
[24] TODD J,VELLIDIS G,LOWRANCE R R,et al.High sediment oxygen demand within an in-stream swamp in Southern Georgia:implications for low dissolved oxygen levels in coastal blackwater streams[J].Journal of the American Water Resources Association,2009,45(6):1493-1507.
[25] TRUAX,D D,SHINDALA A,SARTAIN H.Comparison of 2 sediment oxygen-demand measurement techniques[J].Journal of Environmental Engineering,1995,121(9):619-624.
[26] UTLEY C B,LOWRANCE R,SMITH MC.Factors affecting sediment oxygen demand dynamicsin blackwater in streams of Georgias's Coastal Plain[J].American Water Resource Association,2008,4(3):742-754.
[27] 林卫青,顾友直.苏州河底泥的耗氧量[J].上海环境科学,2001,20(5):212-216.
[28] ROGER N R.Introduction to environmental analysis[M].北京:化学工业出版社,2009:22-23.
[29] 王绍友,徐继荣.一种无边界扰动的单管无扰动采样器:中国,ZL200410026847.3[P].2004-04-13.
[30] 国家环境保护总局《水和废水监测分析方法》编委会.水和废水监测分析方法[M].4版.北京:中国环境科学出版社,2002.
[31] 徐祖信.河流污染治理技术与实践[M].北京:中国水利水电出版社,2003:364-365.
[32] 徐祖信,张锦平,廖振良,等.苏州河底泥对上复水水质污染影响[J].城市环境与城市生态,2005,18(6):1-3.
[33] 朱广伟,陈英旭,周根娣,等.运河(杭州段)沉积物耗氧物质释放的模拟试验研究[J].环境污染与防治,2002,24(4):232-235.
[34] MIKE B,CHANG H J.Multi-scale analysis of oxygen demand trends in an urbanizing Oregon watershed,USA[J].Environ Manage,2008,87:567-581.
[35] GIORDANI P,HELDER W,KONING E,et al.Gradients of benthic-pelagic coupling and carbon budgets in the Adriatic and Northern Ionian Sea[J].Journal of Marine Systems,2002:33/34:365-387.
[36] MIDDELBURG J J,DUARTE C M,GATTUSO J P.Respirationin coastal benthic communities[M].New York:Oxford University Press,2005:206-224.
[37] 张宇,陈静生,于涛,等.对黄河泥沙有机质的溶解特性和降解特性的研究[J].环境科学学报,2004,24(1):1-5.
[38] BORSUK M E,HIGDON D,STOW C,et al.A Bayesian hierarchical model to predict benthic oxygen demand from organic matter loading in estuaries and coastal zones[J].Ecological Modelling,2001,143(3):165-181.
[39] MAKOTO H,HEINZ G S.Sedimentary microbial oxygen demand for laminar flow over a sediment bed of finite length[J].Water Res,2005,39(14):3153-3166.
[40] MOHAMED MH.Modeling nitrogen-carbon cycling and oxygen consumption in bottom sediments[J].Advances in Water Resources,2007,30(1):59-79.
Research on Sediment Oxygen Demand and Related Factors for Strong Reductive Sediments in Urban Rivers
MA Xiao-lei1,2,XU Ji-rong1,3,ZHANG De-min2,GAO Hua-sheng1,CHEN He-ping1
1.Faculty of Architectural Civil Engineering and Environment,Ningbo University,Ningbo 315211,China
2.College of Life Science and Biotechnology,Ningbo University,Ningbo 315211,China
3.South China Sea Institute of Oceanography,Chinese Academy of Sciences,Guangzhou 510301,China
Water and sediment samples were collected from urban rivers of four different pollution levels in the city of Ningbo during July to August,2009.SOD(sediment oxygen demand)for each sample was tested using a homemade SOD device equipped with multielectrodes and tubes.Water quality and physical-chemical index of the sediments from all stations were also analyzed.The SOD per area unit were between 13.8 mg/(m2·h)and 9.4 × 104mg/(m2·h) ,and SOD per mass unit was 87.0 mg/(kg·h)in Station 2(ST2).It was clearly shown that there was a significant correlation between water temperature and the concentration of ammonia nitrogen in the sediment with SOD.However,there was no significant correlation between organic matter,DO(dissolved oxygen)and CODinin bottom-layer water with SOD.It was found that sediments from apparently heavily polluted stations appeared to have a strong“instantaneous oxygen consumption”phenomenon,which might be one of the main factors causing anoxia in the waters.
urban river;strong reductive sediments;SOD;instantaneous oxygen consumption
X522
A
1001-6929(2010)12-1499-07
2010-04-19
2010-08-20
国家自然科学基金项目(40676073)
马 晓 磊 (1986 - ), 女, 山 西 大 同 人,maxiaolei5212000@yahoo.com.cn.
*责任作者,徐继荣(1955-),男,安徽宣城人,研究员,主要从事环
境监测,xujirong@nbu.edu.cn

