聚芴类半导体光谱稳定性
梁 婧 钱 妍 解令海,* 石乃恩
陈淑芬1,2 邓先宇1,2 黄 维1,2,*
(1江苏省有机电子与信息显示——省部共建国家重点实验室培育基地,南京 210046; 2南京邮电大学信息材料与纳米技术研究院,南京 210046)
聚芴类半导体光谱稳定性
梁 婧1,2钱 妍1,2解令海1,2,*石乃恩1,2
陈淑芬1,2邓先宇1,2黄 维1,2,*
(1江苏省有机电子与信息显示——省部共建国家重点实验室培育基地,南京 210046;2南京邮电大学信息材料与纳米技术研究院,南京 210046)
有机半导体的物理和化学性质直接影响其光电器件的性能,这为物理化学提出了新的研究内容与挑战.其中,聚芴类蓝光二极管的光谱稳定性及低能发射带(LEEB)的起源问题是国际上近十年的热点问题之一.本文系统概述了低能发射带的现象、表征方法以及可能的形成机理,包括链间作用导致的激基缔合物发射、器件制备或降解过程形成的芴酮缺陷发射、芴酮聚集态发射以及聚芴端羟基界面氧化导致的绿光发射.本文综述各种物理掺杂和界面调控改善聚芴类二极管蓝光稳定性的策略,着重论述非平面基团的空间位阻、分子构象与链的拓扑结构以及引入抗氧化受阻胺光稳定剂来提高其光谱稳定性策略.
电致发光;共轭聚合物;聚芴;低能发射带;光谱稳定性;蓝光半导体
塑料电子的新热潮始于1990年,英国剑桥大学Cavendish实验室Friend等[1]首次报道基于聚(苯乙烯撑)(PPV)半导体的高分子发光二极管(PLEDs). 1991年,Ohmori等[2]首次报道了聚芴应用于PLEDs.自此,聚芴作为宽带隙半导体(Eg≈3.2 eV)因其高的固态量子效率、良好的载流子传输能力和较好的热稳定性等优点,已经成为最具有商业潜力的聚合物蓝光半导体材料之一,并受到塑料电子学领域广泛关注.最近,大量综述总结了其合成方法、结构-性能关系以及器件应用等方面[3-11],如Springer出版了《Polyfluorene》[12].然而,全面深入理解聚芴光谱稳定性综述报道仍很少,特别是低能发射带(LEEB)现象(部分文献称为long-wavelength emission),它直接影响器件的寿命及伏安特性(I-V)、发光效率、色纯度等性能,涉及器件结构中的缺陷与界面等物理与化学过程,对聚芴类半导体的PLED显示与照明器件中的应用与其商业化进程至关重要,成为继聚合物半导体分子能带工程的又一重要研究课题.然而,聚芴类半导体的光谱稳定性涉及电化学、热化学、表面形态以及环境影响等方面.在本文中,我们组将对聚芴光谱稳定性LEEB现象进行文献综述,并阐述各种表征方法在论证LEEB现象的起源方面的研究进展;讨论由于化学结构光或热降解、氧协同的氧化作用、器件结构界面的降解、分子间作用导致形态演化等多种LEEB形成机制,系统全面概述其稳定化策略,最后,对该领域进行总结并展望.

1996年Pei等[13]制备了基于聚芴衍生物(BDOHPF)1的高效蓝光薄膜(量子效率达73%),应用于PLEDs和发光电化学电池(LECs),并观察到薄膜的LEEB现象.图1是其薄膜态的光致发光(PL)λ=367 nm,主发射峰为430和450 nm,同时伴随两个肩峰480和520 nm.1998年Miller等[14]报道了(DHF-15-DPF)2电致光谱中的520 nm的LEEB现象(图2),并将其归因于成膜状态下聚芴链间聚集作用的结果.在其随后的研究中,关于聚芴类半导体的LEEB现象的机理以及起源成为该领域争论的热点问题[5],同时,多元化分子工程光谱稳定化策略相继被报道.

图1 BDOH-PF在溶液和薄膜态的发射光谱[13]Fig.1 PL spectra of BDOH-PF in solution and film[13]
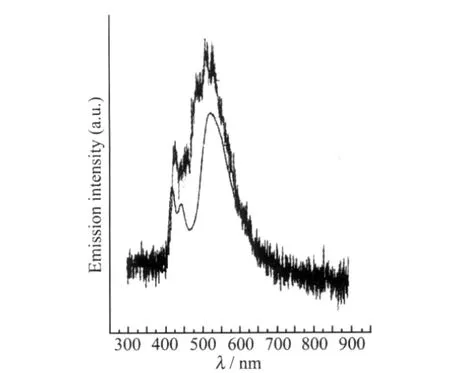
图2 DHF-DPF的电致光谱与200℃热退火1 h的荧光光谱[14]Fig.2 EL spectra and PL spectra of DHF-DPF after annealing at 200℃for 1 h[14]
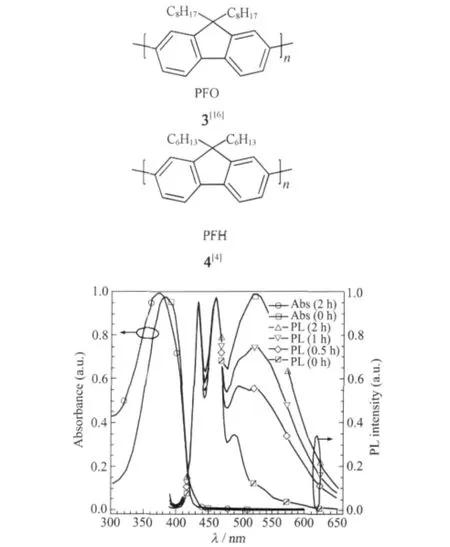
图3 空气中PFO不同紫外光照时间前后的紫外、荧光光谱[16]Fig.3 Time-dependent UV and PL spectra of PFO in air before and after UV irradiation[16]
聚芴类半导体的LEEB现象主要体现于溶液态或者薄膜态的PL光谱行为和EL光谱行为,通常对芴类材料蓝光稳定性研究的监测方式包括在100℃以上高温退火[15],常温紫外光照[16]以及电致发光(EL)器件运行过程的测试[17].下文中将聚(9,9-二辛基芴)简称(PFO)3[16],聚(9,9-二己基芴)简称(PFH)4.图3是PFO薄膜在空气中不同光照时间的紫外吸收(UV)和荧光(PL)光谱图[16],随辐射时间增加,绿光的LEEB强度明显增加,导致色坐标漂移和色纯度下降.据目前研究来看在多数情况下,LEEB现象在多数情况下是指在520-530 nm出现的绿光带(又称gband)[17].然而,据文献报道,LEEB现象还有其他多种表现:(1)2000年Weinfurtner等[18]研究了PFO分子量和聚集行为及PLED光谱稳定性的关系,报道了510 nm为中心的LEEB现象(器件结构为ITO/PEDOT/ PDOFO/Ca,图4).(2)Chen等[19-20]观察到通过XRD表征证实了结晶聚芴的端基相互作用,并指认了507 nm的LEEB来源于未封端聚芴链的端基聚集(图5);(3)电场导致的交联结构可以加强聚集从而产生LEEB现象[21],其LEEB主峰位于485 nm,有明显的精细结构,位置和形状都不同于没有精细结构的520-530 nm的绿光峰.

图4 PFO的荧光光谱及随时间变化的电致光谱[18]Fig4 PL and time dependent EL spectra of PFO[18]

图5 未封端的PFO在不同聚集态的荧光光谱[20]Fig.5 PL spectra of uncapped PFO under different aggregation conditions[20]
具有特殊聚集态结构的PFO薄膜表现出不同光致发光行为.Su等[22]系统制备了各种PFO的相结构,包括N相、β相、α相、α′相,通过X射线衍射和电子显微镜进行表征[23],同时研究了在380 nm激发光下薄膜光谱行为(图6).其四种相的光谱都表现为三组发射带,其中PFO β相的0-0跃迁带在438 nm处,相对N相有11 nm红移.据研究表明,这归因于β相中PFO特殊的构象与聚集行为,β相中链内芴-芴扭曲角接近平面的180°会导致其共轭链长延长.
定量研究LEEB现象为对比与筛选材料提供了重要依据,White[24]和 Huang[25]等利用绿光指数(green index)定量描述了LEEB现象,其定义是聚芴的发射光谱500 nm以上绿光峰与500 nm以下蓝光峰的强度之比,图7为修饰有POSS位阻基团的PFO膜(PFO-POSS)5[24]在空气中200℃退火的LEEB光谱,其绿光指数由退火前的0.05提高至3.70.
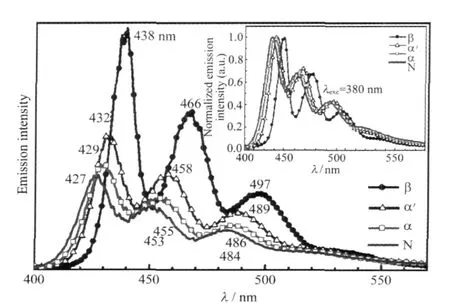
图6 不同相结构的PFO发射光谱[22]Fig.6 PL spectra of PFO with different phases[22] The normalized spectra were given as inset.

图7 PFO-POSS膜LEEB光谱[24]Fig.7 LEEB spectra of PFO-POSS film[24]
目前文献报道了大量的LEEB现象,通过各种仪器表征手段试图证明其机理.迄今,LEEB可能的形成机制主要包括:分子聚集及其激基缔合物(excimer)发射、光氧化、热氧化、电氧化(器件运行过程)以及材料合成中导致的芴酮结构的缺陷等.但是由于聚芴及其衍生物材料的种类不同以及实验条件的差异,这些对深入研究LEEB现象的起源与衡量材料稳定性带来很大困难.迄今,LEEB的起源仍困扰着材料学家:早期的研究者支持聚集或excimer机理,只是通过对比稀溶液和浓溶液,溶液态与薄膜态来定性研究聚集体,没有定量的证据[26];然后,基于芴酮缺陷观点基本确立并占据主流,Scherf等[27]坚持LEEB(530 nm)主要来源于链上芴酮缺陷;相当多的文献中刻意将芴酮单体通过共聚引入聚芴,得到了与正常降解过程极为类似的绿光发射带,进一步确认单链芴酮是LEEB的可能发色团[17].最近,聚集机理的研究又有了新的报道,高纯的三联寡聚芴在不良溶剂中聚集产生LEEB的实验有力支持该观点[28].另外,聚集机理也可以从早期研究中通过共聚扭曲基团、9-位取代树枝化等化学改性途径可以减少LEEB的事实中找到依据.尽管材料改性方面较多可以通过抑制链间聚集来进行分子设计[17,29],但是支持聚集机理的研究者为数不多.
1 LEEB形成机理
Bliznyuk研究组[30]最早对LEEB的起因做了系统的研究和阐述,他们在聚芴蓝光材料及器件的光降解和电降解过程中观察到LEEB,将LEEB来源归属于两个过程:光化学氧化过程以及物理聚集态变化过程,前者通过氧化产生了芳基酮,猝灭发光;后者在形态衍化中发生π发色团堆积形成了激子缺陷,减弱发光强度并使发光带红移.
1.1 聚集或激基缔合物机理
Bradley研究组[31]的早期研究表明在非理想溶剂或器件降解中,聚合物易发生聚集,可以通过紫外光谱观察到433 nm的聚集特征吸收峰.Miller等[14,32-33]系统研究了PFO的薄膜态和溶液态的吸收和发射光谱差异,发现二者吸收光谱近似一致,在热处理实验中,仅观察到分子链排列较为紧密的薄膜聚集态的长波发射光谱,据此推断出LEEB来自链间相互作用导致的激基缔合物(excimer)发射.对聚集机理的研究进行总结,影响聚芴荧光光谱的聚集体主要包括:聚芴主链聚集体、聚芴链的端基聚集体和聚芴链间交联结构三种类型,以下将从热处理和光处理两方面讨论聚集对LEEB的贡献.
我们组[34]对聚芴及其衍生物热稳定性的早期研究支持和证明了聚芴聚集体在产生绿光发射过程中的主要作用,实验对比150℃下空气和氮气退火后聚芴薄膜的发射光谱,都观察到相近的520 nm发射峰,排除了氧气氧化产生芴酮结构对LEEB的主要贡献;将空气中200℃退火后的薄膜,用干冰-甲醇浴淬火,并分散聚合物分子链,此时出现在发射光谱中的LEEB消失,证明聚集产生的分子间激基缔合物是LEEB发射的主要原因.
为研究端基聚集与LEEB之间的关系,Chen等[20]研究分别有封端与无封端的聚芴在100℃退火24 h前后的光谱变化,以苯封端的聚芴只有蓝光发射,而端基为溴的未封端样品观测到明显的聚集体的特征吸收带(431 nm)及相应的绿光发射峰(507 nm),且傅里叶红外光谱(FTIR)检测无1721 cm-1的酮式特征吸收,因此推测其来自端基的聚集.另外, Chen等[35]还设计了有链间相互作用的聚芴分子(POBOHF)6,测试其在不同电压产生绿光带的情况(器件结构为ITO/PEDOT/POBOHF/Ca/Al),并与PL峰对比,发现其电致发光光谱在5 V电压下,第一次扫描即出现424、452和485 nm的宽发射带,并且有520和570 nm的肩峰(图8).随扫描次数增加和扫描电压的增大,蓝光峰下降和绿光峰上升的程度均增加,且在扫描电压重复第6次时,420-460 nm蓝光峰几乎消失,由485-550 nm绿光峰代替,说明绿光带来自电场导致的链间聚集相互作用.最近,对POSS大基团封端的聚芴的研究表明热处理后伴随的交联反应对产生LEEB有重要作用,他们认为可能是由于其阻止了链扭曲,增大了能量跃迁到缺陷上的几率从而导致明显的绿光发射[24].

图8 POBOHF电致与光致发光光谱[35]Fig.8 EL and PL spectra of POBOHF-based device[35]
为了说明聚芴链间堆积得到绿光发射的原理, Chen等[36]设计了侧链修饰带有咔唑基团烷基链的(Cz100PF)7,测试PFO和Cz100PF的紫外吸收、光致、电致发光光谱(图9),并借助时间分辨的电致发光光谱仪(time-resolved(TR)EL)以及分子模拟软件,将Cz100PF的蓝光发射归属于聚芴的主链发射, 530 nm的绿光发射带归属于咔唑侧链之间堆积形成的双分子聚集体导致的电致复合物(electroplex).

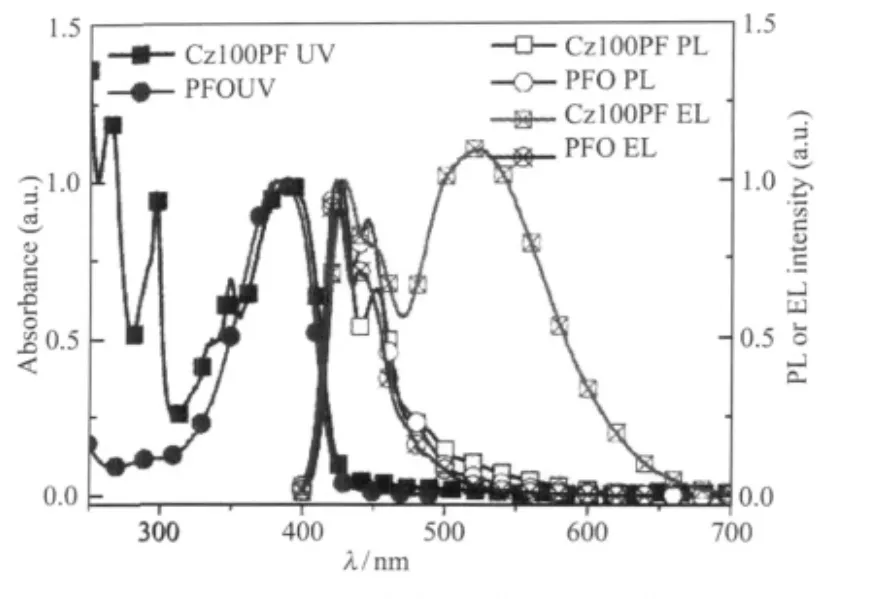
图9 PFO和Cz100PF的紫外吸收、光致、电致发光光谱[36]Fig.9 UV,PL and EL spectra of PFO and Cz100PF[36]
溶液聚集态研究为聚集导致的绿光带提供更有力的证据,早期研究分子间氢键作用的聚芴衍生物Polymer 1(简称P1)8[37]溶液的稳态和瞬态荧光光谱(图10),当减弱P1分子间的氢键聚集作用时,其光谱形态由非指数衰减变为单指数衰减,预示聚集作用的减弱,且LEEB减弱并消失,表明观察到P1在聚集态形成的激基缔合物发射与LEEB的对应关系,而不存在分子间氢键作用的Polymer 2分子无此现象;在稳态荧光光谱表征中,具有分子间氢键作用的聚芴薄膜态表现出明显的聚集绿光发射带,而无分子间作用的聚芴则没有此发射峰.最近, Koizumi等[28]设计比较了亲油性(DHF3)和两亲性(Am-F3)9三联寡聚芴在THF溶剂或THF/H2O混合溶剂中的光物理行为(图11),发现Am-F3在THF/H2O混合溶剂中发生明显的分子凝聚现象,在540 nm处出现了尖锐的绿光带发射,由于合成的寡聚芴的纯度相当高,通过结构表征排除了芴酮的存在,而后将聚集体继续溶解在THF溶剂中,绿光带消失而蓝光发射重新出现,这说明寡聚芴单元的聚集对绿光发射带的产生起了关键的作用.
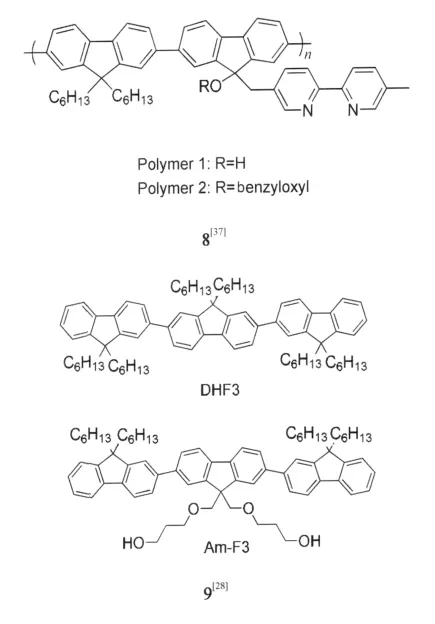

图10 (a)紫外吸收光谱与光致发光光谱,(b)四氢呋喃溶剂和四氢呋喃-甲醇溶剂中的时间分辨荧光光谱[37]Fig.10 (a)Abs spectra,PL spectra,(b)time-resolved photoluminescence decays for polymer in THF solution and THF/methanol solution[37]
最近,rod-coil分子也被用来研究聚芴光稳定性机理[38-40].为了辨别究竟是聚集发射还是芴酮发射在聚芴光降解现象中起主导作用,Chochos等[40]设计了含有不同位阻长度的寡聚芴单元的刚柔嵌段(rodcoil)结构的模型分子,研究其光处理后的发射光谱,得到了只要合理控制链间距离,即使有芴酮结构,也没有观察到绿光带的结果,有力地证明了聚集作用而非芴酮因素是绿光发射的主导因素.
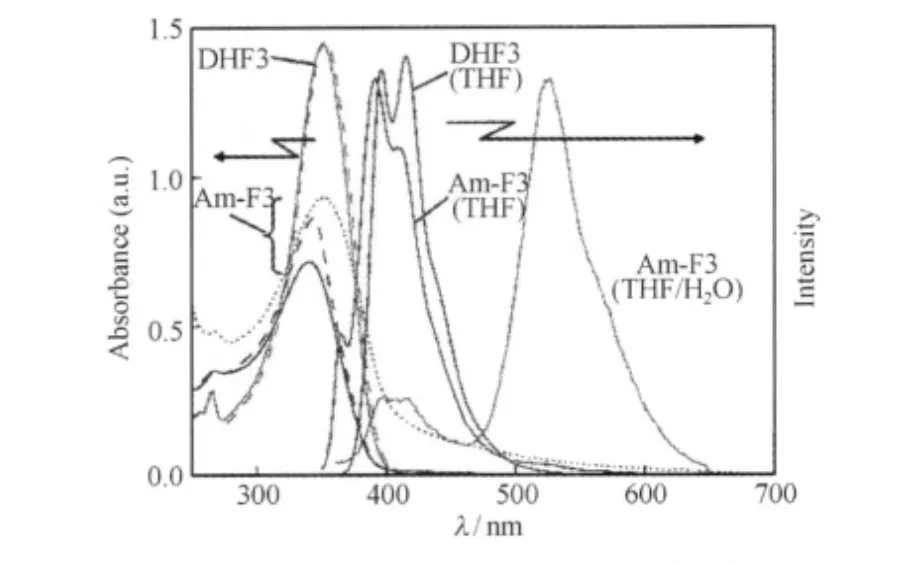
图11 Am-F3和DHF3在四氢呋喃-水溶液中的吸收和发射光谱[28]Fig.11 Abs and PL spectra of Am-F3 and DHF3 in mixtures of THF/H2O[28]

图12 PFO的稳定双链堆积模型[41]Fig.12 Stable packing modes of two chains of PFO[41]
分子模拟研究是研究共轭聚合物链相互作用的理论方法之一.针对PFO体系的薄膜聚集态的分子动力学模拟[41]也有力地支持了上述结论(图12),且指出有效堆积的必要条件为具有合适长度和取代基的基团堆叠[42],且发生链间π轨道的有效堆积可以产生激基缔合物长波发射.
1.2 芴酮缺陷机理
List等[43]提出LEEB起源于链上的酮式缺陷.通过广泛研究聚芴的降解机理和535 nm LEEB的来源,他们认为芴酮结构相当于聚芴链上低能量的发光客体或者激子陷阱,发生由聚芴向芴酮的Förster能量转移,使激子传递中被捕获陷落,产生猝灭蓝光和LEEB现象.表征中,通过傅里叶红外光谱(FTIR)检测到空气中光降解后,聚芴出现在1721 cm-1的羰基特征吸收峰(图13)[43];且该吸收峰强弱(即芴酮浓度)与绿光发射强度有关[44-45],另外,ESCA谱中观测到O的信号也佐证了芴酮的存在[30].
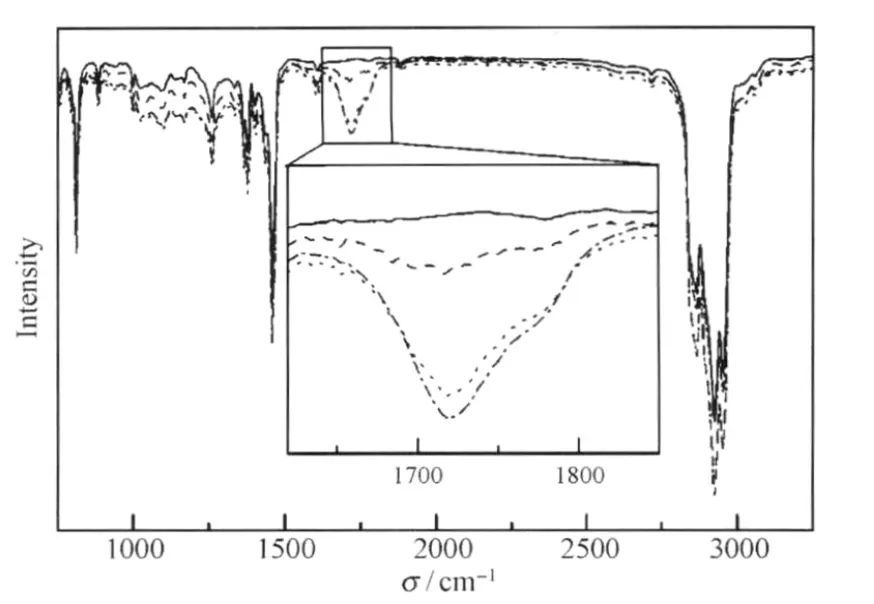
图13 PFO中芴酮结构的FTIR谱[43]Fig.13 FTIR spectra of fluorenone defect in PFO[43]

图14 PFN分别在417与535 nm检测波长下的瞬态荧光光谱[48]Fig.14 Fluorescence decay emission of PFN detected respectively at 417 and 535 nm[48]
在阐述芴酮导致LEEB的过程中,材料学家通过不同的方法,从理论计算、合成特定的模型分子,到研究含芴酮的聚芴或无缺陷的聚芴的不同的荧光寿命,都说明了LEEB来源于不同途径产生的芴酮缺陷.Zojer[46]和Franco[47]等引入量子化学计算的方法,前者证实强的能量转移和芴酮激子的强定域作用使聚芴上含有0.1%-2.0%的芴酮单元就足以产生非常明显的LEEB;后者认为芴酮不是激子猝灭基团,而是作为纯的聚芴材料的黄色发光客体,由于掺杂产生LEEB发射.Jenekhe等[48]以含有不同比例芴酮基团的共聚芴(简称PFN)为模型分子,研究其光谱行为,发现含3%芴酮的共聚芴的溶液在10-7mol·L-1的浓度下就有明显的535 nm绿光带,图14为瞬态荧光光谱,PFN在10-6mol·L-1甲苯溶液, 381 nm紫外光激发下,其535 nm的荧光寿命在5-6 ns,呈现单指数衰减,大大超出420 nm蓝光发射带的寿命(约240-400 ps),暗示芴酮结构是绿光发射的唯一发色基团,且作者将聚集导致的绿光强度的增加解释为链间相互作用增加了从芴到芴酮基团的能量转移加强.
为了分辨LEEB究竟是来自芴的还是芴酮羰基的n-π*跃迁,Wegner等[49]通过瞬态荧光光谱得到了共聚芴酮的寡聚芴(OF5K)10分别在365 nm(对应π-π*跃迁)和453 nm(对应n-π*跃迁)的光激发下的荧光寿命(图15),两种激发波长下,长波发射荧光寿命都在8 ns左右,表明LEEB更可能来自芴酮的发射.


图15 OF5K的荧光强度对时间依赖关系[49]Fig.15 The time dependence of PL intensity for OF5K[49]
Ma等[50-51]最新提出的支链芴酮机理是对经典芴酮机理体系的补充,研究表明芴9-位取代烷基链上的酮结构也对LEEB发射和蓝光猝灭有重要贡献,提出PFO可能的降解产物11.实验中,他们合成了聚芴、烷基酮、芴酮结构单体,进行不同浓度的共混,研究其对绿光带的非辐射猝灭作用,发现绿光带强度与烷基酮浓度有依赖关系:在烷基酮存在的条件下,极低浓度的芴酮即能引起低能绿光发射.

对于芴酮缺陷的来源争论中,金属催化剂的有意或偶然引入对芴酮的形成有重要的作用.List等[43]研究包括在Yamamoto聚合反应中Ni(0)诱导的单烷基链氧化而原位生成的芴酮缺陷和由于光和热氧化导致双烷基链降解而形成的芴酮缺陷,认为Ni(0)在芴酮缺陷形成中起到触发剂的作用.而有人[16,35]认为器件中界面效应导致Ag阳极中含有的Ca离子可能对形成芴酮结构有贡献.Ma等[52]认为偶联聚合的催化剂Pd(0)对生成芴酮有促进作用. Holmes等[53]的研究表明,单体合成中的单烷基缺陷在芴酮的形成过程中扮演重要角色,只要能将其避免,无论用Ni(0)催化的Yamamoto聚合或是Pd(0)催化的Suzuki聚合得到的聚芴均不产生LEEB.然而,Suranna等[54]研究四联寡聚芴的光谱稳定性后提出了不论是单烷基芴还是二烷基芴都可能经历自由基降解过程而形成了芴酮,其可能的降解过程如图16所示.他们发现单烷基芴并非芴酮的唯一来源,这可能只是自由基降解的开端,而添加了Ni(0)金属催化剂杂质后却明显观察到了绿光带的发射,Ni的触发氧化功能再次被证实.

图16 氧化生成芴酮缺陷的自由基氧化途径[54]Fig.16 Pathways of fluorenone defect formation with radical oxidation[54]
最近,Meijer等[55]提出,芴酮的产生与聚芴9-位的取代侧链有重要的联系,他们通过循环凝胶渗透色谱法(rec-GPC),以及基质辅助的激光解吸电离飞行时间质谱法(MALDI-TOF MS)对聚芴的降解过程进行表征(图17),在GPC谱上观察到因为氧化产生的相对分子质量高于原始峰的两个新峰,MS表征得到增加了一个或两个氧原子的质谱峰数据,据此推断,聚芴的降解过程可能包含羧基化或者酮式中间体,其可能的降解过程如图18所示.

图17 五联寡聚芴在空气中降解后的凝胶渗透色谱和质谱[55]Fig.17 GPC and MALDI-TOF MS spectra of pentafluorene after degradation in air atmosphere[55]

图18 寡聚芴的光降解和热降解机理[54]Fig.18 Proposed mechanism for pentafluorene residue by irradiation in air and thermal treatment[54]
Lu等[56]获得了环丙基螺芴(BFSCF)12的单晶堆积结构(图19),螺芴分子成十字型排列,分子间距离为0.27-0.33 nm.晶体结构中没有出现通常意义上聚芴链间π-π面面堆积作用,主要表现为CH…π相互作用.当在空气中150℃热退火时,模型化合物产生了明显的520 nm绿光带,因此可以排除芴链聚集机理,说明LEEB主要来自材料或器件制备过程中残余氧影响下产生的芴酮发射.
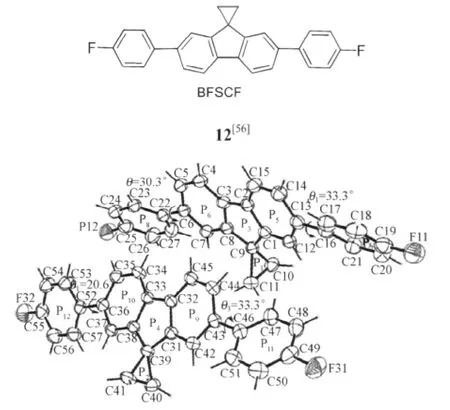
图19 BFSCF的双分子堆积的单晶结构[56]Fig.19 Single crystals of double molecular stacking for BFSCF[56]
最近,Ma等[57]对三聚芴13的研究表明,其分子间面面堆积作用的距离为0.395 nm(图20),在此距离下难以发生π发色团的相互作用.为证明LEEB来自芴酮单体发射,而非聚集体发射,Ma等[58]采用9-位单芳基取代或芳基和甲基取代的梯形聚芴14[58],对比研究纯净的和降解后(200℃下空气中退火2 h)MeLPF的甲苯溶液(50 μg·mL-1),于室温和77 K时400 nm激发下的PL光谱变化,证明有氧气参与的热降解可以产生芴酮结构.通过惰性分散介质将降解的HLPF链间距分散至12 nm,已经超过了链间堆积相互作用的距离(0.4 nm以下),依然有较强的LEEB发射,阐明LEEB仅来自降解产生的酮式发色团.
1.3 芴酮激基缔合物机理
与聚芴链间聚集以及芴酮单分子发射机理不同,芴酮聚集体机理主要指出链间或者链内的芴酮单元之间相互作用形成的激基缔合物或者激基复合物导致的LEEB现象.
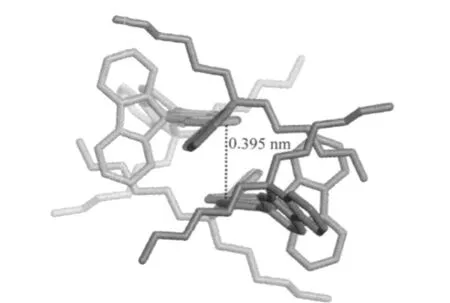
图20 三聚芴单晶的π堆积结构[57]Fig.20 Molecular π-stacking diagram of fluorene trimer[57]
Bradley等[17]率先提出链间芴酮聚集体产生的非定域的激基缔合物(fluorone-based excimer)导致了LEEB的形成,其实验设计将PFO分散到聚苯乙烯聚合物阵列中,在光氧化后检测到芴酮缺陷,却没有观察到明显的绿光发射现象,对比实验中,没有分散的PFO在同样条件处理后却产生了明显的LEEB发射,他们归因为聚苯乙烯分散了PFO由于降解产生的芴酮缺陷而无法形成链间的芴酮聚集体或激基缔合物,因而提出LEEB来自非定域的芴酮激基缔合物发射.随后,Chochos等[40]对在聚苯乙烯中分散的rod-coil嵌段三聚芴进行光降解处理,也观察到类似的实验现象,并且观察到420 nm左右蓝光发射的猝灭和LEEB现象并不是同时出现,说明前者可能由于链上由芴到芴酮的能量转移导致,后者由于链间芴酮结构的聚集导致.
Bo等[59]研究表明链间的芴酮相互作用产生并增强了LEEB发射,采用时间分辨荧光光谱研究了PFN与不同迭代长度的树枝状位阻的共聚芴的共混薄膜,表明树枝状基团可以显著分散PFN链,并减少链间芴酮的聚集体导致的LEEB现象.
最近,Bradley等[60]的研究进一步表明:LEEB来自链间芴酮结构的面面堆积形成的激基缔合物态.他们观察到聚苯乙烯分散的PFO在高于玻璃化转变温度的热退火实验中也产生了LEEB现象,说明热降解改变了聚合物的链间规则度,增强了链间相互作用.另外,当将绿光发射聚合物重新溶解或者重新涂膜,LEEB现象消失(图21),证明链间聚集体为LEEB的必要条件.

图21 降解产生绿光带的PFO薄膜光谱及其溶解后重新成膜的光谱[60]Fig.21 Photoluminescence spectra of degraded PFO film with LEEB and it re-casting film[60]
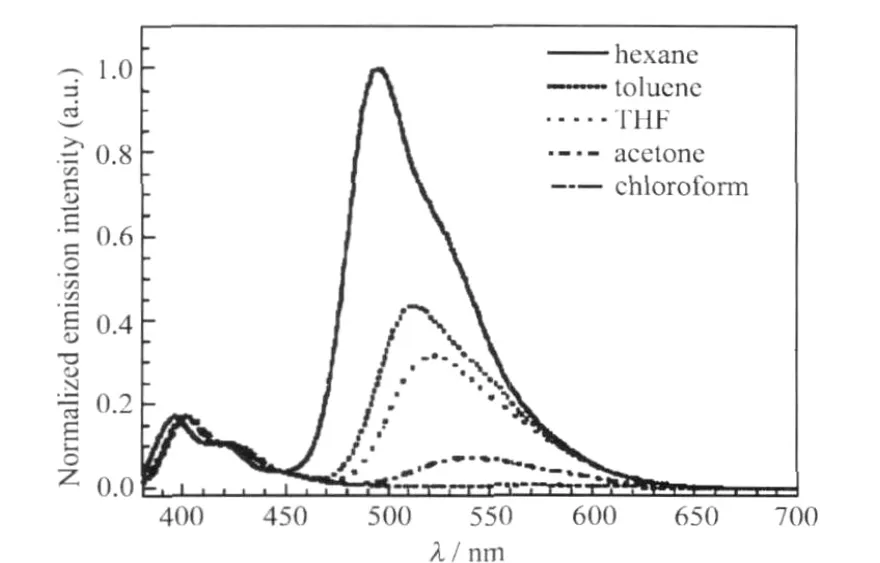
图22 不同极性PFN(10-5mol·L-1)的LEEB光谱[61]Fig.22 LEEB spectra of PFN solution (10-5mol·L-1)of different polarity[61]
Pei等[61]研究比较了共聚不同比例芴酮单体的PFN的稳态荧光光谱和时间分辨荧光光谱,指出LEEB来自链内的芴酮单元间的相互作用.图22为芴酮浓度为12.5%的PFN分别在不同极性溶液中的稳态荧光光谱,当在良溶剂氯仿中,PFN呈单分散态,LEEB几乎观察不到,随着溶液极性的变化, PFN的链扭曲作用增强,产生了明显的LEEB发射.另外,对时间分辨光谱的研究表明,溶液态的单分散PFN产生的LEEB荧光寿命最长,在固态薄膜中,当PFN中芴酮单体浓度从0.1%至25%变化时,其LEEB荧光寿命从8.15 ns减小至4.21 ns,均小于链上芴酮单体的荧光寿命8.39 ns,说明了链内的芴酮基团的相互作用起主要作用.
在绿光究竟来自芴酮单链还是芴酮链间或者链内聚集体的争论中,值得一提的是,Lupton等[62-63]坚持LEEB来自单链芴酮结构的发射,研究含有两个面面堆积芴酮结构的模型分子15,没有发现分子内的缔合物发射信号,但是芴酮之间有较强的发光猝灭作用,用单分子发射光谱检测法研究PFO的光谱性质,发现绿光发射的强度与芴酮的含量有较强的依赖关系.同时,Wegner等[49]通过单晶堆积结构(图23)证明含有芴酮的聚芴链的链间堆积作用不可能形成芴酮的激基缔合物,因此聚芴绿光带只能来源于9-位芴酮的单分子发射,而非芴酮聚集体激基缔合物的发射.

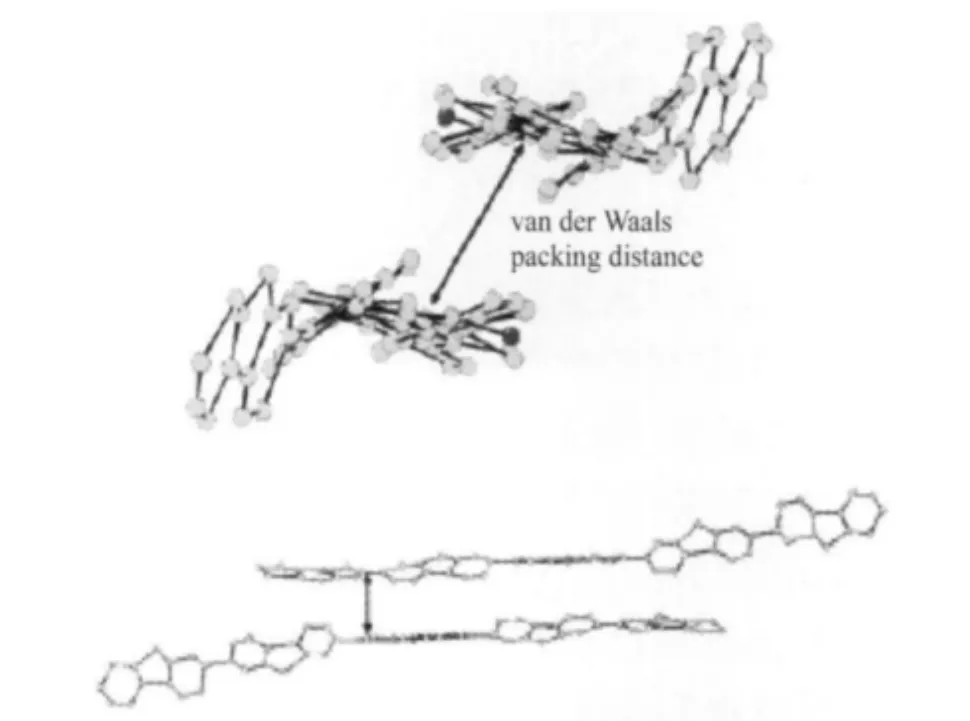
图23 OF5K的分子堆积示意图[49]Fig.23 Molecular packing modes of OF5K[49]
1.4 聚芴端基界面氧化机理
作为对经典聚集以及芴酮机理的补充,Kappaun等[64]的最新研究表明,在解释界面缺陷对LEEB形成的贡献上,LEEB的产生可能源于端羟基在Ca2+离子催化下氧化去质子过程生成氧负离子基(图24).与传统的绿光带位置不同,此低能发射带主要位于500 nm.此前,Moses[16]和Chen[35]等认为电致发光器件中,Ag阳极中含有的Ca2+离子可能催化PFO发光层氧化产生了酮式结构,导致发光的猝灭和LEEB现象的产生;然而聚芴端基的界面氧化机理很好阐释在PLED器件中,金属Ca或Ag电极与聚芴发光层之间相互作用的实质.
总结上述四种机理,我们认为形成绿光带的原因复杂,芴酮和聚集可能都是绿光发射带的主要产生原因,二者在不同的条件下各占主导作用.首先,绿光发射与聚集态关系密切,聚芴薄膜态与溶液态相比更易观察到绿光发射,而溶液态中即使有少量由于降解产生的芴酮单元,也因为分散链减弱能量转移而使绿光发射并不显著;其次,无论是芴酮的激基缔合物还是芴酮单链而导致LEEB,都说明芴酮是一个不可忽视的要素,其中两点已得到公认,一是存在由聚芴主链上的单重激发态到芴酮单元之间存在能量转移;二是芴酮缺陷可以捕获载流子,猝灭发光.
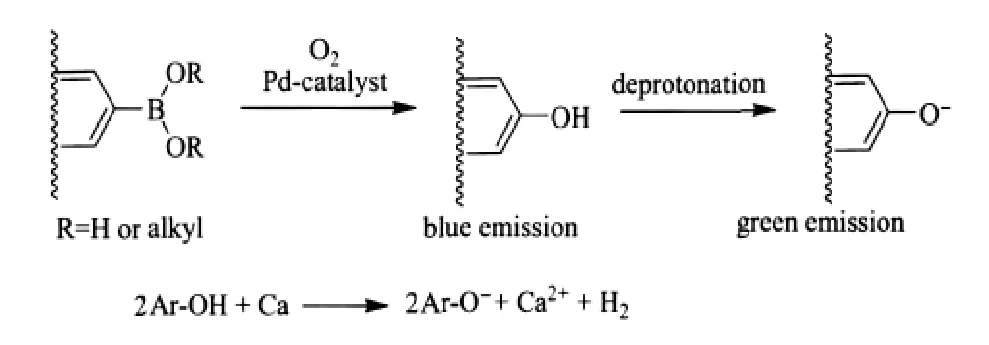
图24 含硼酸端基的聚芴的降解机理示意图[64]Fig.24 Degradation mechanism of polyfluorene with boric end groups[64]
然而,前期对聚集作用的研究几乎都只是定性表征,缺乏对聚集产生绿光发射的临界链间距离的确切证据.Ma等[58]最近实验可以更好阐明聚集态和芴酮发射的相关性:当在聚碳酸酯中分散不同浓度的降解(d-HLPF),在其浓度为0.1%-5%时,都没有明显的LEEB,浓度增加为10%,LEEB显著,此状态下链间距约1.2 nm,远大于链间发色团堆积形成excimer的距离,但是能够发生有效的Förster链间能量转移,说明由聚集导致的聚芴链到芴酮链上的能量转移是LEEB的必要条件.
设计材料的策略中,我们发现控制聚芴主链的排列,保持适当的链间距至关重要,即使有芴酮产生,也能通过避免聚集导致的链间能量转移来消除绿光发射;然而,链间距离不能无限增大,π共轭聚合物分子间是通过共轭链间的堆积作用传递载流子,超过临界距离会由于影响载流子传递而降低器件效率.再者,总结芴酮的形成原因,从聚合过程中金属催化单烷基芴的氧化,到ITO释放的氧和金属电极催化氧化,再到热光电诱导的氧化过程等,都可以看出这是一个多元化的过程.因此,纯化材料和选择合理有效的器件结构也是提高材料寿命的一条重要途径.
2 聚芴光谱稳定化策略
近年来,在研究LEEB起源问题的同时,科学家提出了多种稳定化策略,包括从共混掺杂到器件界面工程再到分子修饰.例如,Neher[65]和Jenekhe[66]等提出通过共混小分子的空穴传输材料或高玻璃化转化温度的聚合物的策略,虽然可以提高发光效率,但只能在一定程度上抑制LEEB的产生.下面将从抑制链间相互作用或芴酮缺陷的角度评述文献报道的各类策略.
2.1 位阻与构象抑制链间相互作用
2.1.1 具有位阻效应的9-位碳3D树枝或螺环化

Müllen等较早地将具有刚性的芳基位阻基团引入到芴9-位材料16[67],主要是利用屏蔽效应来阻隔刚性的聚芴分子链.Shu[68]和Carter[69]等通过不同的合成方法将三维的树枝化结构引入芴的9-位,同时,为保持聚芴材料良好的溶解性和较大的聚合度,通常材料制备中使用的是与9-位烷基取代芴共聚的方法.树枝化基团分为9-位直接与烷基相连或与芳基相连,二者相较:9-位直接连接烷基的聚芴较易于发生光氧化,而9-位直接与芳基相连,可以有效增大位阻和链间距,减少聚集.另外,有报道将具有空穴和电子传输性能的功能位阻结构[70-71]引入到芴的9-位,不仅提高了材料的热稳定性,而且增加了材料与电极的匹配,能够有效地提高发光效率.
芴9-位螺环化也是引入位阻基团的重要形式之一,主要包括引入环烷基、芳香基和杂芳基等结构.由于中心碳原子sp3杂化,使得螺结构的两端构成非平面的空间结构,避免分子间聚集,从而达到稳定的蓝光发射.
我们组最先将螺二芴引入聚芴体系17[72],发现螺芴结构使材料具有良好的热稳定性和较高的玻璃化转变温度.同时由于螺芴大的空间位阻破坏了材料的结晶,降低了激子在链间的传递失活,抑制了激基复合物的形成,从而提高了材料的发光效率,得到较纯净的蓝光发射;又通过增长螺位的长度,进一步改善了该类材料的载流子传输性能[73].Shu等[74]引入环烷基类18可以有效地提高溶解性,并能使材料具有良好的热稳定性;以及通过螺环化将二苯乙烯结构引入聚芴主链上19[75],结果表明:在芴主链上光激发形成的激子能够迁移到螺位,从而调制其发射波长.在最近的一些报道中,开始更多地重视通过在空气环境中来检测热氧化以及光氧化对材料的降解情况的影响.其中,全螺结构的均聚芴20表现出良好的热氧和光氧化稳定性[76-77].

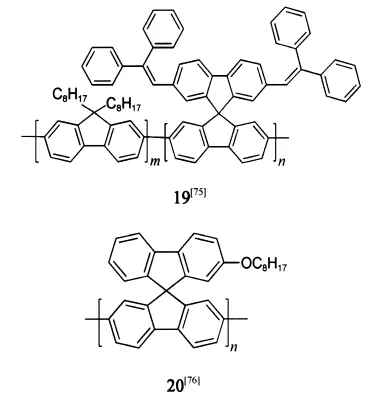
最近,Ma等[78]合成了含咔唑基团的寡聚芴,外量子效率达3.72%,色坐标为(0.16,0.05),接近饱和的深蓝光.另外,多螺环螺芴的合成研究发展迅速[79-83],器件数据表明其在电致蓝光领域有很好的应用潜力.
2.1.2 共聚策略设计扭曲链构象抑制链间聚集
共聚引入功能基团,通常可以将9-位引入立体位阻基团、扭曲基团的芴单元与电荷传输基团或DA给受体基团等功能片段共聚,通过这种共聚方式优化共聚芴的功能性.Miller等[32]早期报道将蒽、联苯基、半共轭的螺芴单元及苯基硅烷咔唑基团等作为扭曲结构团通过无规共聚引入聚芴体系21,有效地控制了共轭链长和抑制聚集,结果明显地抑制了绿光发射.随后,我们课题组[84-85]首次将可溶的烷氧基苯结构与芴单体共聚22,获得了荧光效率为40%,最低启动电压为4 V的深蓝光PLED器件.另外,将螺二芴作为扭曲基团引入聚芴也能得到高效的蓝光材料23[86].
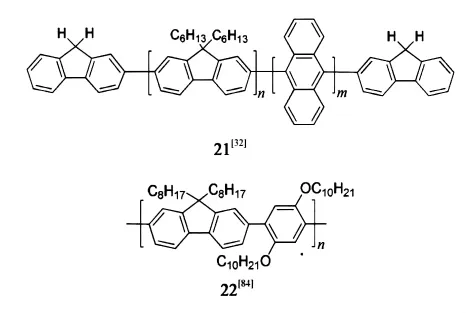
Wong[87]和Jenekhe[88]等设计的含有弯曲形骨架的共聚芴,前者含3,6-位咔唑等稳定结构24,后者引入2,3-二对亚苯基喹喔啉,通过提高其HOMO轨道能,明显增强材料的热稳定性和非平面性,减少聚集的产生.而Scherf等[89]将咔唑的9-位通过柔性的烷基连接后与芴共聚25,得到416 nm的深蓝光,且经过200℃空气退火后没有出现任何长波发射,表明柔性链的引入成功地阻碍了芳环间的相互作用,其器件启动电压4 V,亮度400 cd·m-2.
共聚策略还可以通过引入相应的功能基团,增加材料与电极的匹配性.我们组[90]将芴单体与噁二唑取代苯共聚构建了主链为空穴传输通道,侧链为电子传输通道的十字交叉型聚芴26,同时达到提高载流子传输性能和减弱链间相互作用的目的.另外, Liu[91]和Jen[92]等将四苯基硅烷引入共聚芴体系,通过共聚3,6-咔唑、二烷基芴或螺二芴得到了热稳定性良好的宽带隙蓝光材料,如27[92],其电致发光波长位于409 nm处,器件结构ITO/PEDOT/polymer/ TPBI/CsF/Al,外量子效率2.4%,亮度850 cd·m-2,启动电压5 V.硅烷的引入降低了空穴的注入势垒,有利于平衡载流子传输.

2.1.3 封端、超支化、交联等策略抑制链间相互作用
Chen等[19]提出的聚芴端基聚集机理为聚芴封端以提高光谱稳定性提供了理论依据,封端的分子包括空穴传输基团三苯胺[93]以及缺电子的三唑(TAZ)结构28[94];我们组将咔唑作为侧基引入刚柔(rodcoil)嵌段共聚芴29[95],促进了其固态时链间能量转移,在空气中150℃退火2 h,没有出现长波发射. Gregoriou等[38,96]利用rod-coil嵌段封端方法也得到了稳定的蓝光发射,最近,Kwon等[97]研究表明,将聚[五(乙二醇)甲基甲醚]作为位阻封端基团引入(PFO) 30,可以减少基团堆积形成的激基缔合物,显著提高其热稳定性.

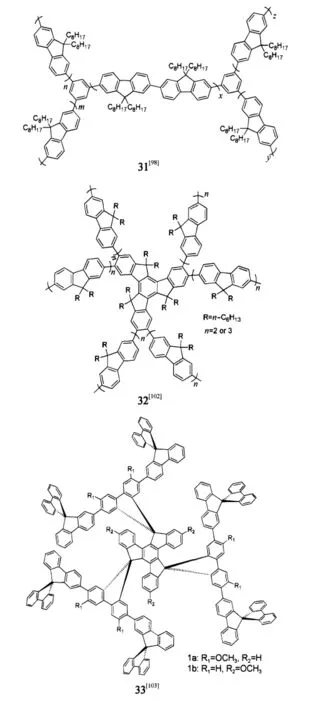
Bo等[98]提出超支化的概念,通过有效的合成手段构建具有独特分子构型的超支化寡聚芴分子31,可以有效地减弱了聚芴分子间的强的相互作用和分子链聚集,引起学术界的关注.我们组[99-102]将超支化应用于提高光谱稳定性,最先设计出具有单分散性的多臂星状纳米尺度聚芴分子32[102],研究表明当支链芴的重复单元为2或3时可获得最稳定的深蓝激光器件,发射峰在437 nm,色坐标为(0.15,0.06),固态量子效率达90%.Pei等[103]设计出基于螺芴框架的发散状三维螺旋立体分子33,其器件发光在7.4 V时亮度为1717 cd·m-2,发射峰在424 nm,色坐标为(0.17,0.08),且具有较高的稳定性.
最早,Miller等[33]在175-200℃下有效引发了苯乙烯基的聚合实现了自交联34,并指出交联能够有效地调控聚芴的超分子堆积结构,从而抑制了链间聚集体或激基复合物的形成.我们组[104]设计可光交联的线性聚芴分子,实现了高量子产率与高光谱稳定性;Ding等[105]合成了主链长度为2-4个芴单元、端基含硼酸基团的寡聚芴35,通过在加热条件下的脱水交联作用,形成了热稳定性良好的蓝光材料.

随后,利用多种方式联合来提高材料稳定性也取得了较好的效果:我们组通过超支化和光交联结合,得到环氧侧链修饰的聚芴36[106],有报道采用引入螺环同时交联的方法来构筑三维立体网络结构37[107],另外,利用稳定的无机POSS核进行支化结构构筑38[108]也是有效的策略之一.

2.1.4 纳米杂化抑制链间聚集行为
随着量子点材料的深入研究和广泛应用,Wei等[109-110]将CdS、Au量子点引入聚芴,通过设计量子点与树枝状聚芴链间有效配位作用(图25),利用量子点三维空间位阻增大链间距离,避免聚集,得到高效稳定的薄膜态蓝光发射.
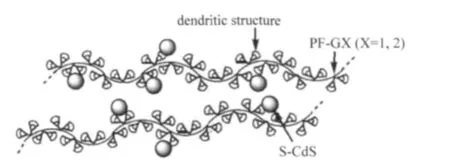
图25 CdS纳米晶修饰的树枝取代聚芴[109]Fig.25 Dendron-substituted polyfluorene modified with CdS nanoparticles[109]
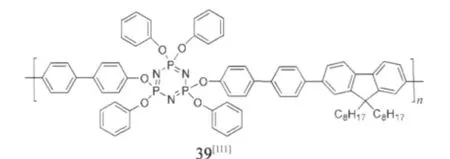
Xu等[111]报道向聚芴体系引入特殊的无机结构基团,如环状叠氮膦(cyclotriphosphazene)基团,得到相应的有机无机杂化材料39.环状叠氮膦基团显著提高聚芴类材料的热稳定性,并通过立体位阻减少聚集,在200℃热退火条件下,仍可获得稳定的蓝光发射.
通过巧妙的合成将β-环糊精等大环分子引入聚芴构筑了聚轮烷(polyrotaxanes)(图26)[112],通过β-环糊精环对聚芴分子线的位阻屏蔽作用,增大链间距离,阻隔发色团堆积,也得到了类似的结论.
2.2 避免化学氧化和芴酮缺陷策略
除了上述的从聚集机理出发设计链结构抑制聚集等物理缺陷的同时,有些一些文献针对化学芴酮结构或界面缺陷进行设计,主要包括从材料的合成纯化、9-位碳原子替代、位阻胺抗光氧化、构建宽带隙D-A能量转移系统以及器件界面优化等方面.

图26 聚芴链与环糊精组成的聚轮烷[112]Fig.26 Polyrotaxanes based on PFO threaded with cyclodextrin[112]
2.2.1 新结构的合成与材料的纯化
Holmes等[113]通过合成共聚9-位Si原子取代的芴单体,有效阻止了芴酮结构的生成,得到聚合物40,其发光器件最大发射波长在425 nm,量子效率为62%的稳定深蓝光;另外,Holmes等[53]从纯化单体,避免单烷基芴缺陷入手,合成无单烷基取代缺陷的聚芴材料,其光致和电致发光光谱均表现出较好的稳定.最近,Lee等[114-115]对芴酮发射的研究表明, LEEB还可能源自芴的9-位碳原子的氧化后,其杂化轨道由sp3转变为sp2杂化,而导致的芴结构中相连苯环的平面形变.因此以双键将芴的4,5-位固定合成高效稳定的蓝光材料PCPP,并合成了相应的材料(BEHP-PCPP)41,得到其热稳定的发射光谱.
与此同时,我们组[116]采用直接碘化的方法得到了通用的中间体42,然后可以方便的得到含硅、锗、锡、硼、磷等杂原子的杂芴单体,以此单体为基础,得到了一系列的杂芴的聚合物;另外,我们组[25,117]还尝试将传统抗氧化基——受阻胺五甲基哌啶醇作为侧链或封端基团引入聚芴体系,如材料43,其荧光发射光谱的稳定性显著提高,绿光区发射现象明显减弱.
2.2.2 共聚体系的D-A能量转移的实现
最近,有人提出设计共聚单元间的能量转移结构获得稳定蓝光分子.聚芴作为蓝光主体发光材料,往往可以通过掺杂,实现处于高能激发态的聚芴发光材料向低能态的客体发光材料的能量转移,从而阻断激子被芴酮缺陷捕获的途径,以实现理想发光色度与OLED器件的发光效率的提高.能量转移的实现,要求引入的大基团或阻断结构同时担当能量转移中心,激发态的纯聚芴给体分子的发射光谱重叠于功能基团受体分子的吸收光谱,达到有效的Förster共振能量转移.Mo等[118]合成了聚3,6-芴的共聚物44,并通过能量转移策略得到最大发射波长位于420 nm稳定的电致蓝光发射光谱.纯3,6-聚芴具有3.6 eV的宽带隙和347 nm的发射波长,其HOMO能级比聚2,7-芴低,为-6.05 eV,表明该材料具有更好的抗氧化能力.
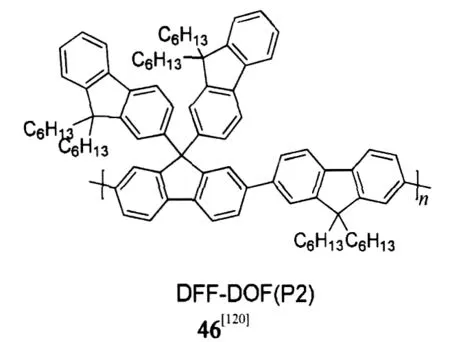
共聚其他类似芴酮的结构如PSO,模拟能量陷落结构是避免LEEB的新策略.Cao等[119]设计共聚2,8-取代或者3,7-取代的稳定高效FSO-PFO蓝光材料45,其器件色坐标(0.16,0.07),外量子效率3.6%. PSO有平衡载流子传输的作用,并调制能带2.8至2.9 eV,为深蓝光发射.另外,最近Kwon等[120]将烷基芴引入PF的9-位制备材料46,即使发生侧链氧化生成芴酮结构,也不会影响主链发射,减少LEEB.

2.2.3 器件结构优化
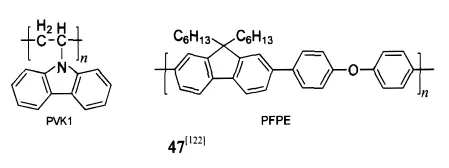
为避免阳极中的Ca离子诱导聚芴氧化为酮式结构而出现明显的绿光发射,Moses等[16]在阳极和发光层之间加入抗氧化缓冲层——电子传输材料CF3OXD,可以使材料的热稳定性和光稳定性都有较大改善,绿光发射现象明显得以抑制.另外,Neher等[4,121]系统研究和论证了向聚芴发光层掺杂小分子空穴传输材料或向器件中加入空穴传输层,都可以提高电致发光效率和蓝光稳定性.因此,通过掺杂旋涂制备PLED器件是提高聚芴器件性能,避免长波发射的另一种途径.Jen等[122]制备掺杂宽带半导体(4.2 eV)的(PVK、PFPE)47材料比例95∶5的旋涂薄膜器件,利用PVK到PFPE的能量转移,得到外量子效率1.81%,6 V电压下发射波长397 nm,半峰宽40 nm的稳定蓝光材料.
3 聚芴蓝光材料稳定性的总结及展望
经过近十年的努力,聚芴材料从器件性能到稳定性方面都得到了大幅度的提高.目前,英国剑桥显示公司(简称CDT)的蓝光材料获得了色坐标(0.15, 0.09)和外量子效率10.4%的掺杂器件.在本文中,我们阐明了LEEB现象产生的两个重要因素——聚集态和芴酮缺陷,以及二者之间的关系;随后,就如何从提高材料形态稳定性和环境稳定性策略展开讨论.(1)在形态稳定性方面,研究表明聚芴的链间ππ堆积对LEEB有较大贡献,由于π-π堆积要求的作用距离约0.3 nm[41-42,49,58,66],且需要良好的结构匹配,保持合适的链间距即可能避免聚集产生的激基缔合物发射,并且保持薄膜态载流子的传输效率.该过程经历了从早期研究的基于P-N嵌段的电子结构调制,到通过位阻和构象修饰实现单链分子发射.最近与形态稳定性调控相关联的β相以及微纳结构调制成为该领域新的研究热点.对于掺杂器件的寿命,其相分离形态稳定性问题仍然亟待解决.(2)环境稳定性主要指聚芴对水氧的稳定性,其中,单线态氧可以将芴9-位氧化,因此合成中材料的纯化和避免缺陷成为重要课题之一;而氧分子也有猝灭发光的作用.无论是合成无单烷基芴缺陷的单体分子[53],还是在用抗氧化受阻胺消除芴酮[25,117],都没有完全去除绿光发射,因此环境稳定方面还有很多工作有待材料学家们继续研究.对于机理研究的模型分子,寡聚物具有高分子的溶液成膜性与小分子的易于纯化的特征,成为目前澄清和解决该问题的重要途径.聚芴类半导体材料的光谱稳定性研究模式为揭示其它共轭聚合物及其退激过程提供了重要参考.
1 Burroughes,J.;Bradley,D.;Brown,A.;Marks,R.;Mackay,K.; Friend,R.;Burns,P.;Holmes,A.Nature,1990,347:539
2 Ohmori,Y.;Uchida,A.;Muro,K.;Yoshino,K.Jpn.J.Appl. Phys.,1991,30:L1941
3 Leclerc,M.J.Polym.Sci.Pol.Chem.,2001,39:2867
4 Neher,D.Macromol.Rapid Commun.,2001,22:1365
5 Lee,J.I.;Klaerner,G.;Miller,R.D.Chem.Mater.,1999,11: 1083
6 Zhu,R.;Feng,J.C.;Huang,W.Chemistry,2005,68:241 [朱 瑞,冯嘉春,黄 维.化学通报,2005,68:241]
7 Tang,C.;Liu,F.;Xu,H.;Huang,W.Prog.Chem.,2007,19:1553 [唐 超,刘 烽,徐 慧,黄 维.化学进展,2007,19:1553]
8 Lai,W.Y.;Mei,Q.B.;Song,J.;Huang,W.J.Nanjing Univ. Posts and Telecom.:Nat.Sci.,2008,28:88 [赖文勇,梅群波,宋 娟,黄 维.南京邮电大学学报:自然科学版,2008,28:88]
9 Chen,Z.Y.;Bai,W.B.;Zhan,C.M.Chin.Polym.Bull.,2007,8: 11 [陈知远,白卫斌,詹才茂.高分子通报,2007,8:11]
10 Jiang,H.J.;Wan,J.H.;Huang,W.Sci.China,Ser.B:Chem., 2008,51:497 [姜鸿基,万俊华,黄 维.中国科学B辑:化学,2008,51:497]
11 Zhao,Q.J.;Wu,W.H.Imaging Sci.Photochem.,2008,26:305 [赵前进,吴文辉.影像科学与光化学,2008,26:305]
12 Scherf,U.;Neher,D.Polyfluorene.Berlin:Springer Press,2008: 1-322
13 Pei,Q.B.;Yang,Y.J.Am.Chem.Soc.,1996,118:7416
14 Klaerner,K.;Furhrer,T.;Karg,J.;Chen,W.;Lee,V.;Scott,J.; Miller,R.Macromolecules,1998,31:1099
15 Xie,L.H.;Liu,F.;Tang,C.;Hou,X.Y.;Hua,Y.R.;Fan,Q.L.; Huang,W.Org.Lett.,2006,8:2787
16 Gong,X.O.;Iyer,P.K.;Moses,D.;Bazan,G.C.;Heeger,A.J.; Xiao,S.S.Adv.Funct.Mater.,2003,13:325
17 Sims,M.;Bradley,D.D.C.;Ariu,M.;Koeberg,M.;Asimakis, A.;Grell,M.;Lidzey,D.G.Adv.Funct.Mater.,2004,14:765
18 Weinfurtner,K.H.;Fujikawa,H.;Tokito,S.;Taga,Y.Appl.Phys. Lett.,2000,76:2502
19 Chen,S.H.;Chou,H.L.;Su,A.C.;Chen,S.A.Macromolecules, 2004,37:6833
20 Chen,X.W.;Tseng,H.E.;Liao,J.L.;Chen,S.A.J.Phys.Chem. B,2005,109:17496
21 Montilla,F.;Mallavia,R.Adv.Funct.Mater.,2007,17:71
22 Chen,S.H.;Su,A.C.;Su,C.H.;Chen,S.A.Macromolecules, 2005,38:379
23 Chen,S.H.;Su,A.C.;Chen,S.A.J.Phys.Chem.B,2005,109: 10067
24 Zhao,W.;Cao,T.;White,J.M.Adv.Funct.Mater.,2004,14: 783
25 Hou,X.Y.;Li,T.C.;Liang,J.;Chen,D.Y.;Xie,L.H.;Huang, W.Acta Chim.Sin.,2008,66:2575 [侯晓雅,李廷成,梁 婧,陈道勇,解令海,黄 维.化学学报,2008,66:2575]
26 Klarner,G.;Lee,J.I.;Davey,M.H.;Miller,R.D.Adv.Mater., 1999,11:115
27 Scherf,U.;List,E.J.W.Adv.Mater.,2002,14:477
28 Koizumi,Y.;Seki,S.;Tsukuda,S.;Sakamoto,S.;Tagawa,S. J.Am.Chem.Soc.,2006,128:9036
29 Burnell,T.;Cella,J.A.;Donahue,P.;Duggal,A.;Early,T.; Heller,C.M.;Liu,J.;Shiang,J.;Simon,D.;Slowinska,K.;Sze, M.;Williams,E.Macromolecules,2005,38:10667
30 Bliznyuk,V.;Carter,S.;Scott,J.;Klarner,G.;Miller,R.D. Macromolecules,1999,32:361
31 Bradley,D.D.C.;Grell,M.;Long,X.;Mellor,H.;Grice,A.Proc. SPIE,1998,3145:254
32 Klarner,G.;Davey,M.H.;Chen,W.D.;Scott,J.C.;Miller,R.D. Adv.Mater.,1998,10:993
33 Klarner,G.;Lee,J.I.;Lee,V.Y.;Chan,E.;Chen,J.P.;Nelson, A.;Markiewicz,D.;Siemens,R.;Scott,J.C.;Miller,R.D.Chem. Mater.,1999,11:1800
34 Zeng,G.;Yu,W.L.;Chua,S.J.;Huang,W.Macromolecules, 2002,35:6907
35 Lu,H.H.;Liu,C.Y.;Jen,T.H.;Liao,J.L.;Tseng,H.E.;Huang, C.W.;Hung,M.C.;Chen,S.A.Macromolecules,2005,38: 10829
36 Liao,J.L.;Chen,X.;Liu,C.Y.;Chen,S.A.;Su,C.H.;Su,A.C. J.Phys.Chem.B,2007,111:10379
37 Pei,J.;Liu,X.;Chen,Z.;Zhang,X.;Lai,Y.;Huang,W. Macromolecules,2003,36:323
38 Chochos,C.L.;Kallitsis,J.K.;Keivanidis,P.E.;Baluschev,S.; Gregoriou,V.G.J.Phys.Chem.B,2006,110:4657
39 Qiang,L.L.;Ma,Z.;Zheng,Z.;Yin,R.;Huang,W.Macromol. Rapid Commun.,2006,27:1779
40 Chochos,C.L.;Kallitsis,J.K.;Gregoriou,V.G.J.Phys.Chem. B,2005,109:8755
41 Surin,M.;Hennebicq,E.;Ego,C.;Marsitzky,D.;Grimsdale,A. C.;Mullen,K.;Bredas,J.L.;Lazzaroni,R.;Leclere,P.Chem. Mater.,2004,16:994
42 Surin,M.;Sonar,P.;Grimsdale,A.C.;Mullen,K.;Lazzaroni,R.; Leclere,P.Adv.Funct.Mater.,2005,15:1426
43 List,E.J.W.;Guentner,R.;de Freitas,P.S.;Scherf,U.Adv. Mater.,2002,14:374
44 Gaal,M.;List,E.J.W.;Scherf,U.Macromolecules,2003,36:4236
45 Gamerith,S.;Gaal,M.;Romaner,L.;Nothofer,H.G.;Guntner, R.;de Freitas,P.S.;Scherf,U.;List,E.J.W.Synth.Met.,2003, 139:855
46 Zojer,E.;Pogantsch,A.;Hennebicq,E.;Beljonne,D.;Bredas,J. L.;de Freitas,P.S.;Scherf,U.;List,E.J.W.J.Chem.Phys., 2002,117:6794
47 Franco,I.;Tretiak,S.Chem.Phys.Lett.,2003,372:403
48 Kulkarni,A.P.;Kong,X.X.;Jenekhe,S.A.J.Phys.Chem.B, 2004,108:8689
49 Chi,C.Y.;Im,C.;Enkelmann,V.;Ziegler,A.;Lieser,G.; Wegner,G.Chem.Eur.J.,2005,11:6833
50 Liu,L.L.;Tang,S.;Liu,M.R.;Xie,Z.Q.;Zhang,W.;Lu,P.; Hanif,M.;Ma,Y.G.J.Phys.Chem.B,2006,110:13734
51 Liu,L.L.;Lu,P.;Xie,Z.Q.;Wang,H.P.;Tang,S.;Wang,Z.M.; Zhang,W.;Ma,Y.G.J.Phys.Chem.B,2007,111:10639
52 Liu,L.L.;Yang,B.;Zhang,H.Y.;Tang,S.;Xie,Z.Q.;Wang,H. P.;Wang,Z.M.;Lu,P.;Ma,Y.G.J.Phys.Chem.C,2008,112: 10273
53 Cho,S.Y.;Grimsdale,A.C.;Jones,D.J.;Watkins,S.E.;Holmes, A.B.J.Am.Chem.Soc.,2007,129:11910
54 Grisorio,R.;Suranna,G.P.;Mastrorilli,P.;Nobile,C.F.Adv. Funct.Mater.,2007,17:538
55 Abbel,R.;Wolffs,M.;Bovee,R.;van Dongen,J.;Lou,X.; Henze,O.;Feast,W.;Meijer,E.;Schenning,A.Adv.Mater., 2009,21:597
56 Wang,Z.X.;Shao,H.X.;Ye,J.C.;Zhang,L.;Lu,P.Adv.Funct. Mater.,2007,17:253
57 Tang,S.;Liu,M.R.;Lu,P.;Cheng,G.;Zeng,M.;Xie,Z.Q.;Xu, H.;Wang,H.P.;Yang,B.;Ma,Y.G.;Yan,D.H.Org.Electron., 2008,9:241
58 Liu,L.L.;Qiu,S.;Wang,B.L.;Wang,H.;Xie,Z.Q.;Ma,Y.G. J.Phys.Chem.C,2009,113:5799
59 Wu,Y.S.;Li,J.;Ai,X.C.;Fu,L.M.;Zhang,J.P.;Fu,Y.Q.; Zhou,J.J.;Li,L.;Bo,Z.S.J.Phys.Chem.A,2007,111:11473
60 Ferenczi,T.A.M.;Sims,M.;Bradley,D.D.C.J.Phys.-Condes. Matter,2008,20:045220
61 Zhou,X.H.;Zhang,Y.;Xie,Y.Q.;Cao,Y.;Pei,J. Macromolecules,2006,39:3830
62 Becker,K.;Lupton,J.M.;Feldmann,J.;Nehls,B.S.;Galbrecht, F.;Gao,D.Q.;Scherf,U.Adv.Funct.Mater.,2006,16:364
63 Da Como,E.;Scheler,E.;Strohriegl,P.;Lupton,J.M.;Feldmann, J.Appl.Phys.-Mater.Sci.Proc.,2009,95:61
64 Kappaun,S.;Scheiber,H.;Trattnig,R.;Zojer,E.;List,E.J.W.; Slugovc,C.Chem.Commun.,2008:5170
65 Sainova,D.;Miteva,T.;Nothofer,H.;Scherf,U.;Glowacki,I.; Ulanski,J.;Fujikawa,H.;Neher,D.Appl.Phys.Lett.,2000,76: 1810
66 Kulkarni,A.P.;Jenekhe,S.A.Macromolecules,2003,36:5285
67 Setayesh,S.;Grimsdale,A.C.;Weil,T.;Enkelmann,V.;Müllen, K.;Meghdadi,F.;List,E.J.W.;Leising,G.J.Am.Chem.Soc., 2001,123:946
68 Chou,C.H.;Shu,C.F.Macromolecules,2002,35:9673
69 Marsitzky,D.;Vestberg,R.;Blainey,P.;Tang,B.T.;Hawker,C. J.;Carter,K.R.J.Am.Chem.Soc.,2001,123:6965
70 Wu,C.W.;Tsai,C.M.;Lin,H.C.Macromolecules,2006,39: 4298
71 Fu,Y.Q.;Li,Y.;Li,J.;Yan,S.;Bo,Z.S.Macromolecules,2004, 37:6395
72 Yu,W.L.;Pei,J.;Huang,W.;Heeger,A.J.Adv.Mater.,2000, 12:828
73 Zhu,R.;Wen,G.A.;Feng,J.C.;Chen,R.F.;Zhao,L.;Yao,H. P.;Fan,Q.L.;Wei,W.;Peng,B.;Huang,W.Macromol.Rapid Commun.,2005,26:1729
74 Wu,F.I.;Dodda,R.;Jakka,K.;Huang,J.H.;Hsu,C.S.;Shu,C. F.Polymer,2004,45:4257
75 Su,H.J.;Wu,F.I.;Shu,C.F.Macromolecules,2004,37:7197
76 Wu,Y.G.;Li,J.;Fu,Y.Q.;Bo,Z.S.Org.Lett.,2004,6:3485
77 Tseng,Y.H.;Shih,P.I.;Chien,C.H.;Dixit,A.K.;Shu,C.F.; Liu,Y.H.;Lee,G.H.Macromolecules,2005,38:10055
78 Tang,S.;Liu,M.;Lu,P.;Xia,H.;Li,M.;Xie,Z.Q.;Shen,T.Z.; Gu,C.;Wang,H.P.;Yang,B.;Ma,Y.G.Adv.Funct.Mater., 2007,17:2869
79 Wu,Y.G.;Zhang,J.Y.;Bo,Z.S.Org.Lett.,2007,9:4435
80 Horhant,D.;Liang,J.J.;Virboul,M.;Poriel,C.;Alcaraz,G.; Rault-Berthelot,J.Org.Lett.,2006,8:257
81 Poriel,C.;Liang,J.J.;Rault-Berthelot,J.;Barriere,F.;Cocherel, N.;Slawin,A.M.Z.;Horhant,D.;Virboul,M.;Alcaraz,G.; Audebrand,N.;Vignau,L.;Huby,N.;Wantz,G.;Hirsch,L. Chem.Eur.J.,2007,13:10055
82 Poriel,C.;Rault-Berthelot,J.;Barriere,F.;Slawins,A.Org.Lett., 2008,10:373
83 Cocherel,N.;Poriel,C.;Rault-Berthelot,J.;Barriere,F.; Audebrand,N.;Slawin,A.M.Z.;Vignau,L.Chem.Eur.J.,2008, 14:11328
84 Yu,W.L.;Pei,J.;Cao,Y.;Huang,W.;Heeger,A.J.Chem. Commun.,1999:1837
85 Yu,W.L.;Cao,Y.;Pei,J.;Huang,W.;Heeger,A.J.Appl.Phys. Lett.,1999,75:3270
86 Wu,F.I.;Dodda,R.;Reddy,D.S.;Shu,C.F.J.Mater.Chem., 2002,12:2893
87 Wong,W.Y.;Liu,L.;Cui,D.M.;Leung,L.M.;Kwong,C.F.; Lee,T.H.;Ng,H.F.Macromolecules,2005,38:4970
88 Kulkarni,A.P.;Zhu,Y.;Jenekhe,S.A.Macromolecules,2005, 38:1553
89 Grigalevicius,S.;Ma,L.;Xie,Z.Y.;Scherf,U.J.Polym.Sci.Pol. Chem.,2006,44:5987
90 Wang,H.Y.;Feng,J.C.;Wen,G.A.;Jiang,H.J.;Wan,J.H.; Zhu,R.;Wang,C.M.;Wei,W.;Huang,W.New J.Chem.,2006, 30:667
91 Liu,X.M.;Xu,J.W.;Lu,X.H.;He,C.B.Macromolecules, 2006,39:1397
92 Zhou,X.H.;Niu,Y.H.;Huang,F.;Liu,M.S.;Jen,A.K.Y. Macromolecules,2007,40:3015
93 Miteva,T.;Meisel,A.;Knoll,W.;Nothofer,H.G.;Scherf,U.; Muller,D.C.;Meerholz,K.;Yasuda,A.;Neher,D.Adv.Mater., 2001,13:565
94 Hung,M.C.;Liao,J.L.;Chen,S.A.;Chen,S.H.;Su,A.C. J.Am.Chem.Soc.,2005,127:14576
95 Lu,S.;Liu,T.X.;Ke,L.;Ma,D.G.;Chua,S.J.;Huang,W. Macromolecules,2005,38:8494
96 Chochos,C.L.;Tsolakis,P.K.;Gregoriou,V.G.;Kallitsis,J.K. Macromolecules,2004,37:2502
97 Kwon,Y.K.;Kim,H.S.;Kim,H.J.;Oh,J.H.;Park,H.S.;Ko,Y. S.;Kim,K.B.;Kim,M.S.Macromolecules,2009,42:887
98 Li,J.;Bo,Z.S.Macromolecules,2004,37:2013
99 Xin,Y.;Wen,G.A.;Zeng,W.J.;Zhao,L.;Zhu,X.R.;Fan,Q. L.;Feng,J.C.;Wang,L.H.;Wei,W.;Peng,B.;Cao,Y.;Huang, W.Macromolecules,2005,38:6755
100 Lai,W.Y.;He,Q.Y.;Zhu,R.;Chen,Q.Q.;Huang,W.Adv. Funct.Mater.,2008,18:265
101 Wen,G.;Xin,Y.;Zhu,X.;Zeng,W.;Zhu,R.;Feng,J.;Cao,Y.; Zhao,L.;Wang,L.;Wei,W.;Peng,B.;Huang,W.Polymer, 2007,48:1824
102 Lai,W.Y.;Xia,R.D.;He,Q.Y.;Levermore,P.A.;Huang,W.; Bradley,D.D.C.Adv.Mater.,2009,21:355
103 Luo,J.;Zhou,Y.;Niu,Z.;Zhou,Q.;Ma,Y.;Pei,J.J.Am.Chem. Soc.,2007,129:11314
104 Yuan,X.D.;Wen,G.A.;Qi,X.Y.;Tang,D.F.;Peng,B.;Wang, L.H.;Wei,W.;Huang,W.Acta Polym.Sin.,2006:1029 [袁翔东,温贵安,戚筱英,汤多峰,彭 波,汪联辉,韦 玮,黄 维.高分子学报,2006:1029]
105 Li,Y.N.;Ding,J.F.;Day,M.;Tao,Y.;Lu,J.P.;D′Iorio,M. Chem.Mater.,2003,15:4936
106 Tang,D.;Wen,G.;Qi,X.;Wang,H.;Peng,B.;Wei,W.;Huang, W.Polymer,2007,48:4412
107 Marsitzky,D.;Murray,J.;Scott,C.;Carter,K.R.Chem.Mater., 2001,13:4285
108 Lin,W.;Chen,W.;Wu,W.;Niu,Y.;Alex,K.Macromolecules, 2004,37:2335
109 Chou,C.;Wang,H.;Wei,K.;Huang,J.Adv.Funct.Mater., 2006,16:909
110 Hsu,S.L.;Chou,C.H.;Chen,C.P.;Wei,K.H.Adv.Funct. Mater.,2007,17:2534
111 Xu,J.W.;Toh,C.L.;Ke,K.L.;Li,J.J.;Cho,C.M.;Lu,X.H.; Tan,E.W.;He,C.B.Macromolecules,2008,41:9624
112 Cacialli,F.;Wilson,J.;Michels,J.;Daniel,C.;Silva,C.;Friend, R.;Severin,N.;Samorì,P.;Rabe,J.;O′Connell,M.Nat.Mater., 2002,1:160
113 Chan,K.L.;McKiernan,M.J.;Towns,C.R.;Holmes,A.B. J.Am.Chem.Soc.,2005,127:7662
114 Park,S.H.;Jin,Y.;Kim,J.Y.;Kim,S.H.;Kim,J.;Suh,H.;Lee, K.Adv.Funct.Mater.,2007,17:3063
115 Kim,J.;Jin,Y.;Song,S.;Kim,S.H.;Park,S.H.;Lee,K.;Suh,H. Macromolecules,2008,41:8324
116 Chen,R.;Fan,Q.;Zheng,C.;Huang,W.Org.Lett.,2006,8:203 117 Si,S.M.;Xie,L.H.;Wei,W.;Peng,B.;Huang,W.Acta Polym. Sin.,2007:148 [司三民,解令海,韦 玮,彭 波,黄 维.高分子学报,2007:148]
118 Mo,Y.Q.;Jiang,X.;Cao,D.R.Org.Lett.,2007,9:4371
119 Li,Y.Y.;Wu,H.B.;Zou,J.H.;Ying,L.;Yang,W.;Cao,Y.Org. Electron.,2009,10:901
120 Jin,J.K.;Kwon,S.K.;Kim,Y.H.;Shin,D.C.;You,H.;Jung,H. T.Macromolecules,2009,42:6339
121 Yang,X.H.;Jaiser,F.;Neher,D.;Lawson,P.V.;Brdéas,J.L.; Zojer,E.;Güntner,R.;deFreitas,P.S.;Forster,M.;Scherf,U. Adv.Func.Mater.,2004,14:1097
122 Huang,F.;Niu,Y.H.;Liu,M.S.;Zhou,X.H.;Tian,Y.Q.;Jen, A.K.Y.Appl.Phys.Lett.,2006,89:081104
June 1,2009;Revised:November 13,2009;Published on Web:February 23,2010.
Spectral Stability of Polyfluorene-Based Semiconductors
LIANG Jing1,2QIAN Yan1,2XIE Ling-Hai1,2,*SHI Nai-En1,2CHEN Shu-Fen1,2DENG Xian-Yu1,2HUANG Wei1,2,*
(1Key Laboratory for Organic Electronics&Information Displays,Nanjing 210046;2Institute of Advanced Materials,Nanjing University of Posts and Telecommunication,Nanjing 210046,P.R.China)
The physical and chemical properties of organic semiconductors play key roles in the performance of optoelectronic devices.The manipulation of these properties offers research opportunities and challenges in physical chemistry.The spectral stability and the origin of the low-energy emission band(LEEB)in polyfluorenes-based blue light-emitting diodes have
much attention over the past few decades.In this review,we categorized various LEEB phenomena according to characterization and related mechanisms,including inter-chain aggregates and/or excimers,on-chain ketone defect emissions,interchain ketone-based excimers,and hydroxy-terminated oxidation on the interface of devices.Recent advances in highly stable blue light-emitting polyfluorenes are categorically summarized.This review highlighted the contributions of the steric hindrance effects of various nonplanar bulky groups,molecular conformations and topologies of chains and antioxidant hindered amine light stabilizers(HALS), together with physical blending as well as interface engineering.
Electroluminescent;Conjugated polymer;Polyfluorene;Low-energy emission band;Spectrum stability; Blue light-emitting semiconductor
O649
*Corresponding authors.Email:iamlhxie@njupt.edu.cn,iamwhuang@njupt.edu.cn;Tel:+86-25-85866008.
The project was supported by the National Key Basic Research Program of China(973)(2009CB930600),National Natural Science Foundation of China(20774043,20704023,60876010,60706017,60907047),Key Project of Chinese Ministry of Education(707032,104246,208050),Natural Science Foundation of Jiangsu Province,China(BK2008053,BK2009423,08KJD150016,08KJB510013,09KJB150009,SJ209003,TJ207035),
and NJUPT(NY207042,NY207041,NY207038).
国家重点基础研究发展规划(973)项目(2009CB930600),国家自然科学基金(20774043,20704023,60876010,60706017,60907047),教育部重大培育基金项目(707032),教育部重点项目(104246,208050),江苏省基础研究计划(自然科学基金)(BK2008053,BK2009423),江苏省高校自然科学基础研究(08KJD150016,08KJB510013,09KJB150009,SJ209003),江苏省高等学校优秀科技创新团队(TJ207035),南京邮电大学引进人才启动基金(NY207042,NY207041,NY207038)资助
黄维,于1979年进入北京大学化学系学习并先后获得理学学士、硕士和博士学位.

