新型3-氯-1-(3-氯-2-吡啶)-1H-吡唑甲酰胺类化合物的合成*
郑 毅, 王俊芳, 张应鹏, 窦花妮, 杨云裳
(1. 兰州理工大学 石油化工学院,甘肃 兰州 730050; 2. 浙江省化工研究院,浙江 杭州 310023)
农药开发工作中最有成效的是众多杂环化合物被开发为超高效农药[1]。含氮杂环化合物是当今农药发展的主体,尤其是吡啶和吡唑这两类化合物最为突出。近年来杜邦公司将邻苯二甲酸酰亚胺变化为邻氨基苯甲酰胺而获得较高的活性,也使此类化合物为近年来农药开发的研究热点。而在此类化合物中羧酸部分为吡啶基吡唑类羧酸时杀虫活性明显优于其它羧酸类[2,3]。
本文在吡啶基吡唑类羧酸化合物中引入活性较高的环氨,以期取得有较高活性的新一类化合物。2,3-二氯吡啶肼解制得中间体(2); 2与马来酸二乙酯环化制得中间体(3);3经氯代、氧化、水解制得3-氯-1-(3-氯-2-吡啶)-1H-吡唑甲-1-甲酸(6);6经二氯亚砜酰氯化、环胺酰胺化合成了13个新型3-氯-1-(3-氯-2-吡啶)-1H-吡唑甲酰胺类化合物(1a~1m, Scheme 1),其结构经1H NMR和MS表征。
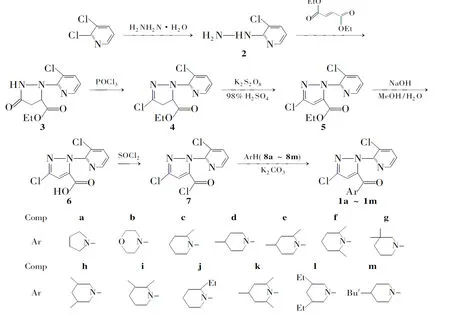
Scheme 1
1 实验部分
1.1 仪器与试剂
Varian INVOA 400型核磁共振仪(DMSO-d6为溶剂,TMS为内标);Finnigan Trace 2000 MS型质谱仪。
所用试剂为分析纯或化学纯。
1.2 合成
(1) 2的合成[4,5]
在三口烧瓶中加入2,3-二氯吡啶148 g(1.0 mol)和85%水合肼500 mL(7.0 mol),搅拌下回流反应3.5 h(反应体系先变澄清,后析出固体,TLC跟踪)。倒入冷水(500 mL)中,析出更多的白色针状晶体,抽滤,滤饼用水洗涤,红外灯干燥得白色针状晶体2 137.3 g,收率95.7%;1H NMRδ: 4.21(s, 2H), 6.62(dd, 1H), 7.53(s,1H), 7.57(d, 1H), 8.05(d, 1H); EI-MSm/z: 144(M+, 100%)。
(2)3的合成[6~8]
在三口烧瓶中加入绝对乙醇250 mL和21%乙醇钠溶液190 mL(504 mmol),回流(83 ℃)状态下加入268 g(474 mmol),搅拌下回流反应约5 min;滴加马来酸二乙酯88 mL(544 mmol)(多于5 min), 回流反应1 h。冷却到约65 ℃,加入冰乙酸50 mL(有固体析出),加水650 mL溶解沉淀,置入冰箱中冷却析晶(约5 h),抽滤,滤饼用40%乙醇(3×50ml)洗涤后再用乙醚淋洗,红外灯干燥得微黄绿色粉末360 g,收率47.0%;1H NMRδ: 1.22(t, 3H), 2.60(m, 1H), 2.91(m, 1H), 3.26(m, 1H), 4.20(d, 2H), 4.84(m,1H), 7.19(m, 1H), 7.91(m,1H), 8.27(m, 1H); EI-MSm/z: 270(M++1, 100%)。
(3)4的合成[9~11]
在三口烧瓶中加入324 g(89 mmol)和适量乙腈,搅拌下缓慢滴加三氯氧磷10mL(107 mmol),滴毕,再滴加DMF 2滴,回流反应约30 min时沉淀完全溶解,再继续反应约1 h(体系变为黑绿色)。减压蒸除溶剂,残余物倒入25%碳酸氢钠溶液(150 mL)中,剧烈搅拌至无气体产生,再用二氯甲烷(3×150 mL)萃取,合并萃取液,加助滤剂(硅藻土)5 g,搅拌30 min,用砂芯漏斗过滤(除去黑色焦油状物);滤液用适量二氯甲烷和水稀释,加硅藻土约5 g,过滤,滤液分层,在有机相中加入无水硫酸镁(10 g)和硅胶(4 g),搅拌30 min,过滤,滤饼用二氯甲烷淋洗,合并滤液,减压浓缩得深琥珀色油状液体424.9 g,收率97.1%;1H NMR(CDCl3)δ: 1.20(t, 3H), 3.18(m, 1H), 3.38(m, 1H), 4.18(d, 2H), 5.30(m, 1H), 6.86(m, 1H), 7.66(m, 1H), 8.08(m, 1H); EI-MSm/z: 288 (M+, 100%)。
(4)5的合成[9~11]
在三口烧瓶中加入424.9 g(87 mmol)和乙腈250 mL,搅拌下滴加98%硫酸9 mL(169 mmol),自然升温至22 ℃~35 ℃,加过硫酸钾35 g(129 mmol),回流反应约4.5 h。冷却至60 ℃左右,过滤,滤饼用乙腈(30 mL)淋洗,合并滤液,浓缩至约100 mL,加水250 mL,搅拌5 min,过滤,滤饼经红外灯干燥得桔黄色固体517.7 g,收率71.6%;1H NMRδ: 1.08(t, 3H), 4.16(d, 2H), 7.29(m, 1H), 7.71(m, 1H), 8.27(m, 1H), 8.57(m, 1H); EI-MSm/z: 286(M+, 100%)。
(5)6的合成[9~11]
在单口烧瓶中加入517.7 g(62 mmol),无水甲醇58 mL,水32 mL和氢氧化钠3 g(75 mol),搅拌下升温至22 ℃~35 ℃反应约1 h。减压浓缩至约50 mL,加水100 mL,用乙醚萃取,水相转移至单口烧瓶中。搅拌下缓慢滴加浓盐酸至体系为酸性(有桔黄色固体析出),抽滤,滤饼用水(100 mL)淋洗后经红外灯干燥得桔黄色固体612.7 g,收率79.5%;1H NMRδ: 7.178(s, 1H), 7.68(m, 1H), 8.24(m, 1H), 8.56(m, 1H); EI-MSm/z: 258(M+, 100%)。
(6)7的合成[7,12]
在单口烧瓶中加入68 g(31 mmol)和二氯亚砜30 mL,搅拌下回流反应约3 h。蒸除过量二氯亚砜得红黑色液体75.1g,收率59.5%。
(7)1的合成(以1a为例)[9~11]
在单口烧瓶中加入7385.0 mg(1.4 mmol),二氯甲烷10 mL,四氢吡咯(8a) 99.4 mg(1.4 mmol)和碳酸钾193 mg(1.4 mmol),搅拌下于室温反应2 h。搅拌下加水15 mL,分液,水相用二氯甲烷萃取,合并有机相,用无水硫酸镁干燥,经柱层析[洗脱剂:V(乙酸乙酯) ∶V(石油醚)=1 ∶3]分离得1a0.23 g。
用类似方法合成1b~1m。
1a: 微黄棕色固体,收率52.8%(以7计算,下同);1H NMRδ: 1.86(m, 4H), 3.33(m, 2H), 3.65(m, 2H), 7.10(s, 1H), 7.59(m, 1H), 8.18(m, 1H), 8.49(m, 1H); MSm/z: 311(M+)。
1b: 微黄白色固体,收率51.8%;1H NMRδ: 3.49~3.58(m, 8H), 6.97(s, 1H), 7.61(m, 1H), 8.23(m, 1H), 8.52(m, 1H); MSm/z: 327(M+)。
1c: 微黄白色固体,收率48.3%;1H NMRδ: 1.07~1.41(m, 4H), 1.41~1.71(m, 5H), 3.66(m, 1H), 4.36(m, 2H), 6.88(s, 1H), 7.60(m, 1H), 8.23(m, 1H), 8.48(m, 1H); MSm/z: 339(M+)。
1d: 微黄棕色固体,收率50.0%;1H NMRδ: 0.90~0.92(m, 4H), 1.07(m, 1H), 1.64(d, 3H), 2.68(m, 1H), 3.31(m, 1H), 3.87(m, 1H), 4.19(m, 1H), 6.89 (s, 1H), 7.60(m, 1H), 8.22(m, 1H), 8.48(m, 1H); MSm/z: 339(M+)。
1e: 微黄白色固体,收率40.4%;1H NMRδ: 0.83~1.31(m, 7H), 1.52(m, 2H), 1.85(m, 2H), 3.23(m, 2H), 3.67(m, 1H), 6.88(s, 1H), 7.59(m, 1H), 8.22(m, 1H), 8.46(m, 1H); MSm/z: 353(M+)。
1f: 白色固体,收率37.3%;1H NMRδ: 1.17(d, 6H), 1.41~1.53(m, 6H), 4.33(m, 2H), 6.91(s, 1H), 7.60(m, 1H), 8.23(m, 1H), 8.47(m, 1H); MSm/z: 353(M+)。
1g: 微黄白色固体,收率50.6%;1H NMRδ: 0.83(s, 6H), 1.39(m, 2H), 1.57(m, 2H), 3.18(s, 2H), 3.42(m, 2H), 6.93(s, 1H), 7.60(m, 1H), 8.23(m, 1H), 8.46(m, 1H); MSm/z: 353(M+)。
1h: 白色固体,收率52.2%;1H NMRδ: 0.78(d, 6H), 1.42(m, 2H), 1.82(m, 2H), 3.26(m, 2H), 3.79(m, 1H), 4.21(m, 1H), 6.89(s,1H), 7.60(m, 1H), 8.22(m, 1H), 8.47(m, 1H); MSm/z: 353(M+)。
1i: 微黄白色固体,收率48.7%;1H NMRδ: 0.82(d, 3H), 0.94(m, 2H), 1.11(m, 1H), 1.41(d, 3H), 1.59(m, 2H), 3.12~3.35(m, 3H), 6.88(s, 1H), 7.60(m, 1H), 8.23(m, 1H), 8.48(m, 1H); MSm/z: 353(M+)。
1j: 白色固体,收率45.9%;1H NMRδ: 0.76(t, 3H), 1.49~1.89(m, 8H), 3.14~3.29(m, 3H), 6.88(s, 1H), 7.60(m, 1H), 8.25(m, 1H), 8.47(m, 1H); MSm/z: 353(M+)。
1k: 微黄棕色固体,收率35.2%;1H NMRδ: 0.92(d, 3H), 1.13~1.39(m, 11H), 4.17(m, 2H), 6.90(s, 1H), 7.60(m, 1H), 8.24(m, 1H), 8.39(m, 1H); MSm/z: 367(M+)。
1l: 微黄白色固体,收率35.8%;1H NMRδ: 0.79(d, 6H), 1.07~1.21(m, 8H), 3.62~3.83(m, 2H), 4.15~4.31(m, 2H), 6.90(s, 1H), 7.60(m, 1H), 8.24(m, 1H), 8.48(m, 1H); MSm/z: 381(M+)。
1m: 微黄白色固体,收率42.1%;1H NMRδ: 0.83(s, 9H), 0.99(m, 2H), 1.26(m, 1H), 1.65(m, 2H), 3.96(m, 2H), 4.31(m, 2H), 6.92(s, 1H), 7.60(m, 1H), 8.23(m, 1H), 8.44(m, 1H); MSm/z: 381(M+)。
2 结果与讨论
合成2时,水合肼分批加入比较好,因为在回流状态下水合肼易挥发从而影响其反应浓度;反应时间越长越好,但是过长没有实际意义。合成3时,反应时间稍长有利于提高产率,若析不出产物可延长冷却时间,必要时可以将体系结冻再融化。合成1的常用方法[13]是以乙腈、丙酮、二氯甲烷或THF等为溶剂,以三乙胺、N-取代吗啉、氢氧化钠、碳酸钠、吡啶等位缚酸剂,在低温下滴加酰氯到胺溶液制备酰胺。我们通过实验比较后选择以二氯甲烷为溶剂,碳酸钾为缚酸剂,虽然产率不能达到最高但是得到的产物颜色较浅,纯度较高。
1对黄瓜霜霉病菌、黄瓜白粉病菌和黄瓜灰霉病菌的防效几乎为零,杀虫和除草活性也几乎为零,其它生物活性有待进一步研究确定。
[1] 慕长炜,覃兆海.吡啶类农药的研究进展[J].现代农药,2003,2(2):1-6.
[2] 柴宝山,林丹,刘远雄,等. 新型邻甲酰氨基苯甲酰胺类杀虫剂的研究进展[J].农药,2007,46(3):148-153.
[3] 欧晓明,唐德秀. 新型邻甲酰氨基苯甲酰胺类农药氯虫酰胺的研究概述[J].世界农药,2007,29(5):6-9.
[4] 李叶青,陆明. 2-氨基-6-氯吡啶的制备[J].中国医药工业杂志,2006,37(5):305-306.
[5] 范铮,单尚. 2,4,6-三硝基苯肼的合成[J].应用化工,2006,35(2):104-105.
[6] 张自义,张艳. 肼类衍生物在五元唑环杂环合成中的应用进展[J].有机化学,2004,24(11):1348-1365.
[7] 郭丽琴,徐尚成,马海军,等. 1-芳基-5-吡唑酰胺类化合物的合成与生物活性研究[J].农药研究与应用,2008,12(2):15-18.
[8] Donald J P Pinto, Michael J Orwat. Discovery of 1-[3-aminomethyl)phenyl]-N-3-fluro-2′-(methylsulfonyl)-[1,1′-biphenyl]-4-yl]-3-(trifluoromethyl)-1-H-pyrazole-5-carboxamide(DPC423),a highly potent,selective,and orally vioavailable inhibitor of blood coagulation factor xa′[J].Journal of Medicinal Chemistry,2001,44(4):566-578.
[9] Lahm, George Philip, Selby,etal. Arthropodicidal anthranilamides[P].WO 2 003 015 519,2003.
[10] Hughes Kenneth Andrew, Lahm George Philip, Selby Thomas Paul. Novel anthranilamide insecticides[P].WO 2 004 046 129,2004.
[11] 李斌,相东,柴宝山,等. 苯甲酰胺类化合物及其应用[P].WO 2 008 134 969,2008.
[12] Jeffrey G Varnes, Dean A Wacker. Design,structure-activity relationship,and pharmacokinetic profile of pyrazole-based indoline factor Xa inhibitors[J].Bioorganic & Medicinal Chemistry Letters,2007,(17):6481-6488.
[13] 吕献海,张袖丽,江万权. 新型含氟吡唑酰胺衍生物的合成[J].合成化学,2009,17(3):342-344.

