以二苯甲酮为端基的第一代树状取代酞菁锌的合成*
刘建生, 彭亦如, 黄丽珊, 陈莉莉, 阙寿林
(福建师范大学 化学与材料学院,福建 福州 350007)
光动力疗法(PDT)是一种治疗肿瘤的新方法,而光敏剂则是PDT治疗中的关键因素。由于酞菁配合物的光热稳定性好,在600 nm~850 nm具有较强的摩尔吸光系数,单线态氧产率高,被认为是很有潜力的第二代光敏剂[1]。但是,由于酞菁分子之间强的π-π作用导致荧光量子产率下降,三线态寿命缩短,降低了光敏效果[2,3]。树枝状大分子是近几年来出现的一类具有高度支化结构的大分子[4]。树枝状聚合物由核心、支化单元和外围官能团三部分构成,随着代数的增加,官能团数目呈指数增长。研究结果表明,树枝状大分子引入到酞菁周边,可以增加酞菁核周围的空间位阻,实现对酞菁核的位点分离,将有效的降低酞菁配合物的聚集效应。
鉴于上述考虑,本文设计并合成了以二苯甲酮基为外围基团的第一代树枝状分子取代的酞菁锌配合物————四[3,5-二(二苯甲酮-4-甲氧基)苯甲氧基]锌酞菁[ZnPc(C35H27O5)4](4, Chart 1)。4-甲基二苯甲酮经N-溴代丁二酰亚胺(NBS)溴代制得4-溴甲基二苯甲酮(1);1与3,5-二羟基苯甲醇反应合成了外围带有二苯甲酮取代基的第一代树枝状分子3,5-二(二苯甲酮-4-甲氧基)苯甲醇(2); 2与4-硝基邻苯二甲腈缩合制得外围带有二苯甲酮取代基的第一代树枝状分子4-[3,5-二(二苯甲酮-4-甲氧基)苯甲氧基]邻苯二甲腈(3); 3经“液相法”环合制得4(Scheme 1),其结构经1H NMR, IR和MS表征。
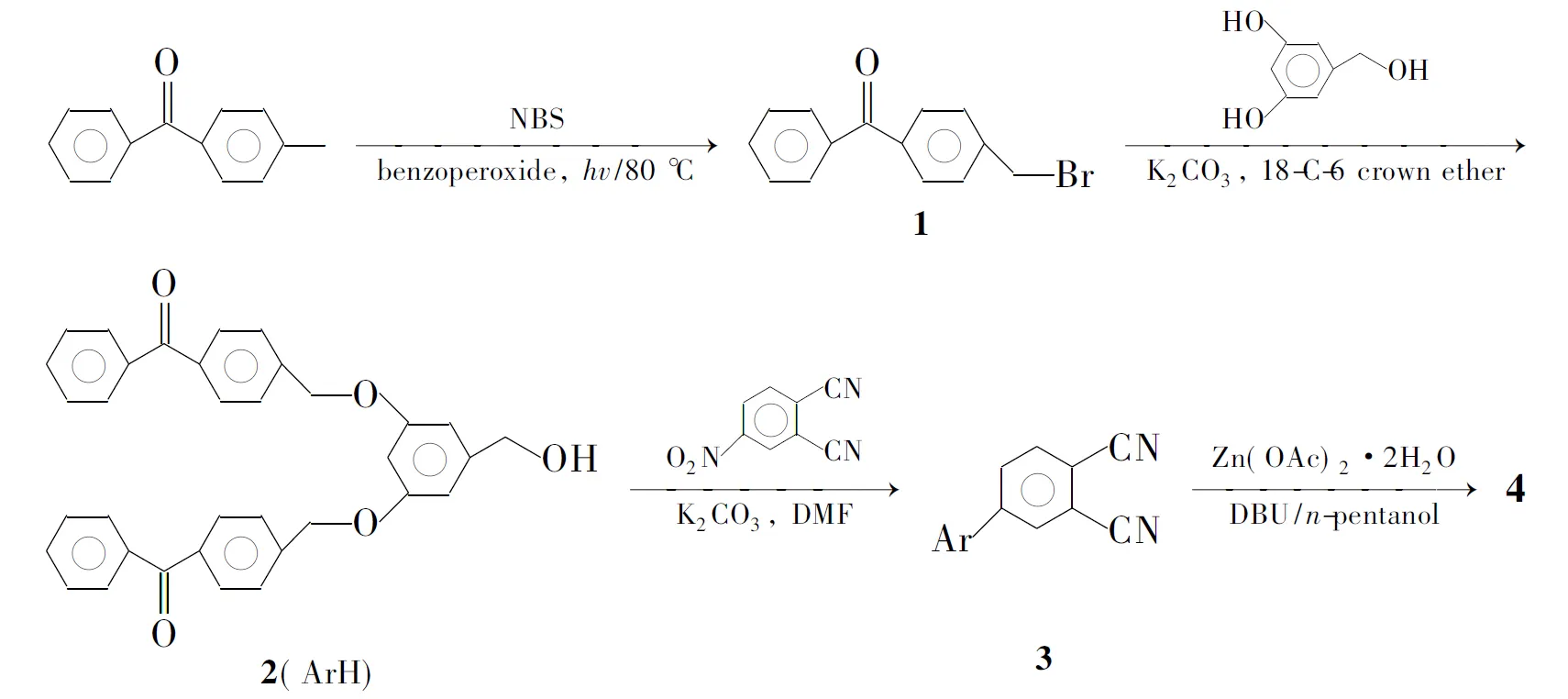
Scheme 1
1 实验部分
1.1 仪器与试剂
Cary 50型紫外可见吸收光谱仪;FL900/FS920型稳态和瞬态荧光光谱仪;UNITY 500型核磁共振仪(CDCl3为溶剂,TMS为内标);PE-983G型红外光谱仪(KBr压片);MALDI-TOF-MS Reflex Ⅲ型和LCQ Deca XP MAX型质谱仪。
所用试剂均为分析纯。
1.2 合成
(1)1的合成[5]
在三口瓶中加入4-甲基二苯甲酮3.92 g(20 mmol), NBS 3.6 g(20 mmol),过氧化苯甲酰0.4 g,四氯化碳25 mL,强光照射,搅拌下于78 ℃反应7 h。趁热过滤,滤液置冰水浴中冷却析晶,过滤,滤饼用无水乙醇重结晶得白色固体12.7 g,产率49%, m.p.108 ℃~110 ℃;1H NMRδ: 7.80(t, 4H), 7.60(t, 1H), 7.51~7.46(m, 4H), 4.53(s, 2H); IRν: 1 646, 1 600, 1 448, 1 278, 1 154, 1 046, 598 cm-1; MSm/z: 273(M+)。
(2)2的合成[6]
在三口瓶中加入120 g(72 mmol), 3,5-二羟基苯甲醇4.9 g(35 mmol), 18-C-6冠醚1.85 g(7 mmol),无水碳酸钾12.1 g(87 mmol),丙酮180 mL,氮气保护,剧烈搅拌下于55 ℃反应48 h。过滤,滤液减压蒸干,剩余物用三氯甲烷和水萃取洗涤,水层用三氯甲烷萃取三次,合并有机相,用无水硫酸镁干燥,浓缩至干,用混合溶剂[V(正己烷) ∶V(二氯甲烷)=2 ∶3]重结晶得白色粉末215 g,产率81%, m.p.135 ℃~136 ℃;1H NMRδ: 7.83(t, 8H), 7.46~7.59(m, 10H), 6.56(s, 1H), 6.66(s, 2H), 5.14(s, 4H), 4.66(s, 2H); IRν: 1 654, 1 602, 1 445, 1 314, 1 280, 1 154, 1 060 cm-1; MSm/z: 529(M+)。
(3)3的合成
在三口烧瓶中加入2 1.06 g(2 mmol), 4-硝基邻苯二甲腈350 mg(2 mmol),无水碳酸钾420 mg(3 mmol)的DMSO(30 mL)溶液,搅拌下于室温反应24 h。抽滤,滤液倒入冰水中析晶,过滤,滤饼用甲醇重结晶2次~3次,真空干燥得浅绿色固体30.92 g,产率70%;1H NMRδ: 7.84~7.86(d,J=8 Hz, 1H), 7.81~7.83(t,J=8 Hz, 8H), 7.72(s, 1H), 7.46~7.60(m, 10H), 7.33~7.34(d, 1H), 6.67(s, 2H), 6.65(s, 1H), 5.17(s, 4H), 5.13(s, 2H); IRν: 2 230, 1 652, 1 597, 1 449, 1 318, 1 281, 1 165, 1 069 cm-1; MSm/z: 655(M+)。
(4)4的合成
在三口烧瓶中加入3260 mg(4 mmol), Zn(OAc)2·2H2O 20 mg(1 mmol)和正戊醇10 mL,氮气保护,搅拌下于130 ℃反应30 min;待其完全溶解后滴加DBU(二氮杂二环)1 mL,于140 ℃反应24 h。冷却至室温,过滤,滤饼经柱层析[洗脱剂:V(MeOH) ∶V(CHCl3)=1 ∶9]分离纯化两次得深绿色固体40.17g,产率63%;1H NMRδ: 7.82~7.84(d,J=8 Hz, 4H), 7.80~7.82(t,J=8 Hz, 32H), 7.65(s, 4H), 7.47~7.62(m, 40H), 7.11~7.13(d,J=8 Hz, 4H), 6.80(s, 8H), 6.68(s, 4H), 5.15(s, 24H); IRν: 1 650, 1 606, 1 486, 1 448, 1 278, 1 154, 1 046 cm-1; MSm/z: 2 680(M)。
2 结果与讨论
IR分析表明:3在1 652 cm-1处出现C=O的伸缩振动吸收峰,1 597 cm-1为苯环的特征骨架振动,1 050 cm-1~1 150 cm-1的吸收峰可以指认为树状芳醚分子中C-O-C的伸缩振动,在2 230 cm-1处为氰基的特征振动吸收峰,说明合成的3与Scheme 1期待吻合。4在2 230 cm-1处氰基的特征吸收峰消失,1 606 cm-1为苯环的特征骨架振动,在1 400 cm-1~1 500 cm-1的吸收峰可指认为酞菁环上C=C和C=N的伸缩振动,说明合成了酞菁。
1H NMR分析表明,3在位于7.86~7.84, 7.33~7.34和7.72的三组信号分别对应邻苯二甲腈上的三个质子,位于4.66处的亚甲基质子峰消失,并在5.13处出现了一个苯甲醚质子峰,进一步说明成功合成了3。4在7.84~7.82, 7.65和7.11~7.13的吸收峰分别被指认为酞菁环的三个质子;7.82, 7.47~7.62, 6.80和6.68分别对应于树状外围的苯环质子;5.15对应芳醚链中亚甲基质子。芳香区与烷烃的质子的实测信号比(3.07 ∶0.73)与理论值(4 ∶1)基本一致。
质谱分析(蒽酚为基质)表明,4的最大丰度分子离子峰m/z: 2 680与其分子量[ZnPc(C172H120N8O20Zn, 2 680]吻合。

λ/nm图 1 4在DMSO中的UV谱图*Figure 1 UV spectra of 4 in DMSO
*c(4)=n×10-5mol·L-1(n=1, 2, 3, 4, 5)

λ/nm图 2 4在DMSO中的荧光光谱图*Figure 2 Fluorescence spectrum of 4 in DMSO
*c(4)=2×10-5mol·L-1
测定了4在DMSO中的UV谱图(图1)和荧光光谱图(图2)。由图1可见,4在DMSO中主要以单体形式存在,其摩尔吸光系数为8.692 5×105mol-1·cm-1·L;从图2可以看出,4的发射光波长位于696 nm。
通过Frechet合成法合成了外围带有二苯甲酮树枝状分子四取代的酞菁锌(4),引入二苯甲酮树枝状分子取代基后,4在DMSO中主要以单体形式存在。
[1] Barbara C, Gabrio R, Donata D,etal. Synthesis and antimycotic activity of new unsymmetrical substituted zinc phthalocyanines[J].Tetrahedron,2003,59:10025-10030.
[2] Vacus J, Simon J. Luminescence andanti-aggregative properties of polyxyethylene-substituted phthalocyanine complexes[J].Adv Mater,1995,7:797-800.
[3] Dhami S, Phillips D. Comparison of the photophysics of an aggregating and non-aggregating aluminum phthalocyanine system incorporated into unilamellar vesicles[J].J Photochem Photobiol,A:Chem,1996,100:77-84.
[4] 徐敏,谭克. 树状高分子的功能化进展[J].功能高分子学报,2001,4:482-487.
[5] 方培基,王尔鉴. 光敏功能表面活性剂及稳态光谱性质[J].感光科学与光化学,1988,8(3):12-16.
[6] 陈金平,韩永滨,张鲁,等. 芳醚树枝形聚合物的合成及分子内光敏异构化反应研究[J].有机化学,25(9):1077-1083.

