NHPI/Co(Salen) 催化氧化取代甲苯*
沈晓冬, 卓广澜
(浙江理工大学 化学系,浙江 杭州 310018)
取代苯甲酸是一类重要的有机中间体。取代甲苯的直接氧化为合成取代苯甲酸提供一条简捷的合成路线,其合成方法主要分为化学试剂氧化法[1~3]、电化学氧化[4,5]和金属催化剂氧化[6~8]等。目前工业上普遍使用过渡金属离子和溴化盐作催化剂[9~11],并使用氧气氧化的催化体系具有反应快,产率高等优点。但是该方法反应条件要求高温高压,对设备具有较强的腐蚀性,同时产生大量污染物。
N-羟基邻苯二甲酰亚胺(NHPI)与过渡金属离子催化氧化取代甲苯是最近研究的一个热门方向[12~15]。Yasutaka[16]报道了以NHPI/Co(OAc)2催化氧化甲苯制备苯甲酸的方法。该方法反应条件温和,以空气或氧气作为氧化剂,是一条低毒低腐蚀性的环境友好型合成路线。
双水杨醛缩乙二胺合钴配合物[Co(Salen)]具有类卟啉结构,是典型的具有载氧功能的仿酶模型化合物,能有效地活化分子氧,在合成上经常用于烯烃的分子氧环氧化,醇的选择性催化氧化以及催化氧化Baeyer-Villiger 反应等,由于其优良的吸氧功能,可以加快氧化反应的速率。而且Co(Salen)原料易得、合成方法简单。
在Yasutaka等[16]报道的NHPI/Co(OAc)2催化氧化体系中,通常用乙酸钴或乙酰丙酮钴作为主催化剂,尚没有用Co(Salen)作催化剂的报道。本文以NHPI/Co(Salen)为催化体系,偶氮二异丁腈(AIBN)为助引发剂,AcOH为溶剂,分子氧氧化取代甲苯(1a~1j)制备取代苯甲酸(2a~2j, Scheme 1),尝试寻找一种低温低压且具有较高活性的催化体系。
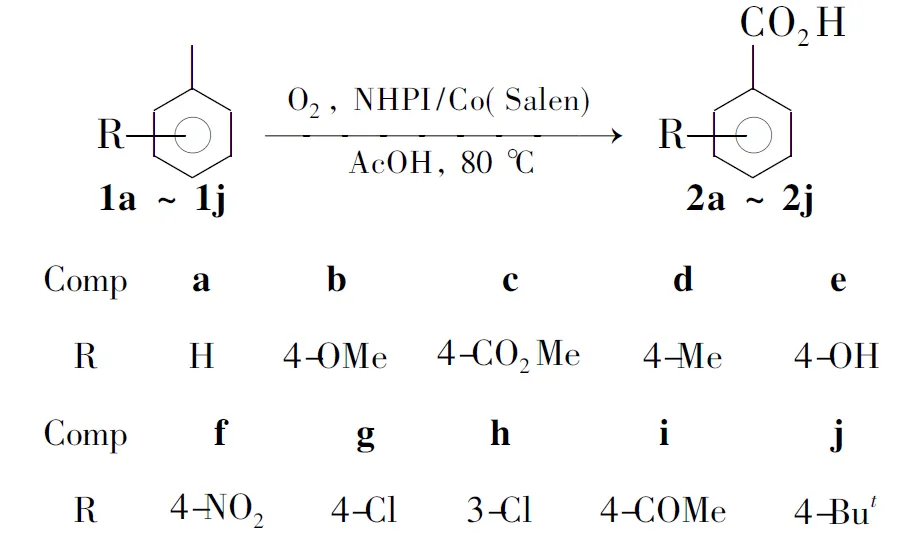
Scheme 1
1 实验部分
1.1 仪器与试剂
Bruker Avanceav 400 MHz型核磁共振仪(DMSO-d6为溶剂,TMS为内标);Nicolet Avatar 37型红外光谱仪(KBr压片);GC-7900(FID)型气相色谱仪;Agilent 1100型高效液相色谱仪。
所用试剂均为分析纯。
1.2 实验步骤
(1) M(Salen)的制备
在三颈瓶中加入乙二胺0.64 g(10.6 mmol)的乙醇(70 mL)溶液,搅拌下于50 ℃缓慢滴加水杨醛2.63 g(21.5 mmol)的乙醇(80 mL)溶液,滴毕,回流反应约5 h。浓缩至干,用乙醇重结晶得亮黄色片状固体双水杨醛缩乙二胺(Salen) 2.60 g,产率91.0%, m.p.126 ℃~128 ℃;1H NMRδ: 3.92(s, 4H), 6.84~6.90(m, 4H), 7.29~7.34(m, 2H), 7.40~7.43(dd,J=1.6 Hz, 7.6 Hz, 2H), 8.59(s, 2H);13C NMR(CDCl3)δ: 59.77, 116.96, 118.64, 118.69, 131.49, 132.40, 161.0, 166.51; IRν: 3 438, 1 635, 1 577, 1 372, 1 283 cm-1。
按文献[17]方法制得M(Salen)(M=Co, Mn, Cu)。
Co(Salen): 红棕色粉末,m.p.>300 ℃; UVλ: 400.5, 390.5 nm; IRν: 3 420, 1 606, 1 449, 1 349, 1 290, 589, 473 cm-1。
Mn(Salen): 灰褐色粉末,m.p.>300 ℃; UVλ: 773, 397 nm; IRν: 3 438, 1 623, 1 598, 1 542, 1 443, 1 291, 802, 643, 467 cm-1。
Cu(Salen): 深绿色粉末,m.p.>300 ℃; UVλ: 360, 259 nm; IRν: 1 649, 1 629, 1 528, 1 450, 726, 614, 579 cm-1。
(2)2a的制备
在三颈瓶中依次加入甲苯(1a)6 mmol, NHPI, M(Salen), AIBN,醋酸10 mL,用O2置换三次,保持压力0.1 MPa,搅拌下于预定温度反应(GC跟踪)。
2 结果与讨论
2.1 氧化反应的条件选择
以合成2a为模型反应,系统考察了催化体系,催化剂与引发剂摩尔比{r[M(Salen)] =n[M(Salen)] ∶n(引发剂)},引发剂用量{q(引发剂)=n(引发剂)/n(1a)×100%},催化剂用量{q[M(Salen)]=n[M(Salen)]/n(1a)×100%=r[M(Salen)] ×q(引发剂)},AIBN用量{q(AIBN)=n(AIBN)/n(1a)×100%},反应温度和反应时间对氧化反应的影响。
(1) 催化体系
1a6 mmol,r[M(Salen)] =5%,q(引发剂)=10%, HOAc 10 mL,于80 ℃反应20 h,其余反应条件同1.2(2),考察不同催化体系对氧化反应的影响,结果见表1。从表1可以看出,当以NHPI为引发剂时,具有相对较高的转化率和选择性。TEMPO和AIBN作引发剂对应的转化率和选择性都较低,反应伴有大量副产物。以NHPI为引发剂,Co(Salen)为催化剂的组合具有较高的活性,转化率90.1%,选择性84.6%(Entry 1);同样条件下,以Mn(Salen)或Cu(Salen)作催化剂时,转化率和选择性稍低(Entry 2和Entry 3)。说明Co(Salen)具有最好的催化活性。以Entry 1为基本反应条件,加入AIBN[q(AIBN)=1%],转化率(92.7%)和选择性(88.9%)都显著提高(Entry 10)。由此可见,最佳催化体系为NHPI/Co(Salen)。
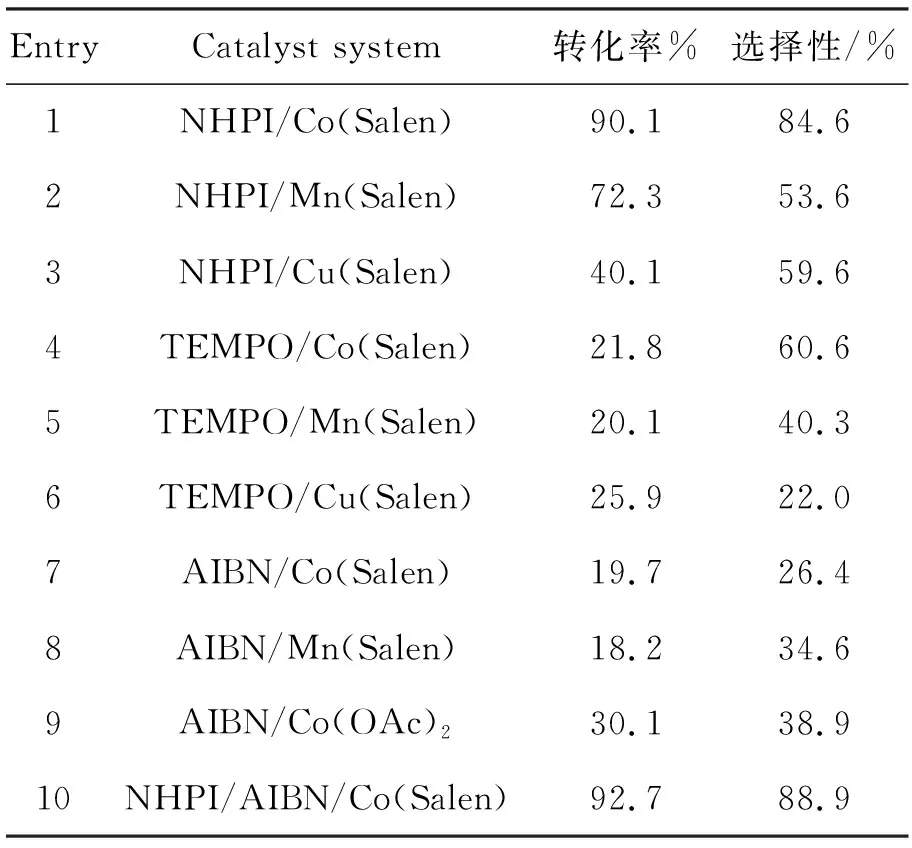
表 1 催化体系对1a氧化反应的影响*Table 1 Effect of catalyst system on oxidation of 1a
*1a6 mmol,q[M(Salen)]=n[M(Salen)] /n(1a)×100%=0.5%,q(引发剂)=n(引发剂)/n(1a)×100%=10%, HOAc 10 mL,于80 ℃反应20 h,其余反应条件同1.2(2)

表 2 r[Co(Salen)] 对1a氧化反应的影响*Table 2 Effect of r[Co(Salen)]on oxidation of 1a
*q(NHPI)=10%,其余反应条件同表1;r[Co(Salen)]=n[Co(Salen)] ∶n(NHPI)
(2)r[Co(Salen)]
1a6 mmol,q(NHPI)=10%,其余反应条件同2.1(1),考察r[Co(Salen)]对氧化反应的影响,结果见表2。由表2可见,当r[Co(Salen)] 为0.5%时,转化率28.7%;转化率和选择性均随r[Co(Salen)] 的增加有明显提高。r[Co(Salen)] =5%时,转化率和选择性达到最高。再增加r[Co(Salen)] ,转化率开始下降。文献[18]方法在单独使用NHPI时,转化率也能达到15.8%;r[Co(Salen)] 增加至5[19]时,1a基本无反应。因此,r[Co(Salen)]应选择5%,q[Co(Salen)]=r[Co(Salen)]×q(NHPI)=5%×10%=0.5%。
(3)q(NHPI)
1a6 mmol,q[Co(Salen)]=0.5%,其余反应条件同2.1(1),考察q(NHPI)对氧化反应的影响,结果见图1。由图1可见,当q(NHPI)=3.15%时,转化率和选择性分别为39.1%和51.3%;逐渐增加q(NHPI),转化率和选择性也随之上升,当q(NHPI)=10%时,转化率和选择性达到最高;再增大q(NHPI),转化率和选择性均缓慢下降。宜选择q(NHPI)=10%。

q(NHPI)/%图 1 q(NHPI)对1a氧化反应的影响*Figure 1 Effect of q(NHPI) on oxidation of 1a
*1a6 mmol,q[Co(Salen)]=0.5%, 其余反应条件同2.1(1);q(NHPI)=n(NHPI) ∶n(toluene)

表 3 q(AIBN)对1a氧化反应的影响* Table 3 Effect of q(AIBN) on oxidation of 1a
*q[Co(Salen)]=0.5%,q(NHPI)=10%,其余反应条件同2.1(3);q(AIBN)=n(AIBN)/n(1a)×100%
(4)q(AIBN)
1a6 mmol,q[Co(Salen)]=0.5%,q(NHPI)=10%,其余反应条件同2.1(3),考察q(AIBN)对氧化反应的影响,结果见表3。由表3可见,当q(AIBN)=1.0%时,转化率和产率分别为92.7%和82.4%。继续增加q(AIBN)时,反应趋于平衡。AIBN[20]作为助引发剂时可以促进反应的进行。q(AIBN)=1.0%对反应较为有利。
(5) 反应温度与时间
1a6 mmol,q[Co(Salen)]=0.5%,q(NHPI)=10%,q(AIBN)=1.0%, O2(0.1 MPa), AcOH 10 mL,考察反应温度和时间对氧化反应的影响,结果分别见图2和图3。从图2可以看出,在35 ℃反应时,转化率41.9%,选择性75.1%;当反应温度为80 ℃时,转化率和选择性分别为92.7%和88.9%。当温度继续升高时,转化率继续上升,但选择性却明显下降,反应伴有大量副产物。当温度接近沸点时,溶液沸腾可能会破坏钴与氧气配合,降低氧气在溶剂中溶解度,从而使选择性降低。因此80 ℃是最为合适的反应温度。

Temperature/℃图 2 反应温度对1a氧化反应的影响*Figure 2 Effect of reaction temperature on oxidation of 1a
*1a6 mmol,q[Co(Salen)]=0.5%,q(NHPI)=10%,q(AIBN)=1.0%, O2(0.1 MPa), AcOH 10 mL,反应时间20 h
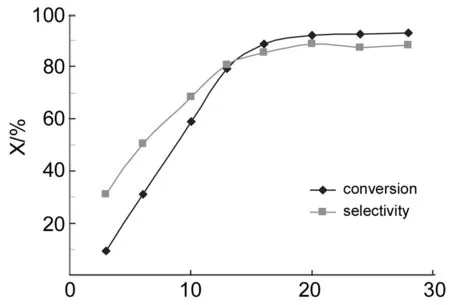
Time/h图 3 反应时间对1a氧化反应的影响*Figure 3 Effect of reaction time on oxidation of 1a*1a 6 mmol, q[Co(Salen)]=0.5%, q(NHPI)=10%, q(AIBN)=1.0%, O2(0.1 MPa), AcOH 10 mL,反应温度80 ℃
由图3可见,于80 ℃反应20 h,转化率和选择性都趋于平衡。
综上所述,氧化1a制备2a的最佳反应条件为:1a6 mmol,q(NHPI)=10%,q(AIBN)=1.0%,q[Co(Salen)]=0.5%, O2(0.1 MPa), AcOH 10 mL,于80 ℃反应20 h。
2.2 底物扩展
在最佳反应条件下,以取代甲苯作为底物,研究该催化体系对不同取代甲苯的催化活性,结果见表4。从表4可以看出,1d和1j的转化率达到90%以上。1b的转化率为50%,选择性较差。1e和1f的转化率和产率均较低,原因尚不清楚。

表 4 底物扩展实验结果*Table 4 Experamental results of substrate survey
*16 mmol,q[Co(Salen)]=0.5%,q(NHPI)=10%,q(AIBN)=1%, O2(0.1 MPa), AcOH 10 mL,于80 ℃反应20 h
3 结论
本文研究了NHPI/Co(Salen)催化体系对甲苯及取代甲苯的催化活性并优化了反应条件。研究表明,NHPI/Co(Salen)催化体系对甲苯具有较好的催化性能,转化率92.7%,选择性88.9%。
[1] 高山,尹永波. 催化氧化合成4-氯-2-硝基苯甲酸[J].染料与染色,2006,43(3),41.
[2] 聂西度,李晓如. 相转移催化氧化合成氯代苯甲酸[J].合成化学,2004,12:405-407.
[3] 韩雪峰,孔洁. KMnO4-Al2O3氧化法制备苯甲酸[J].廊坊师范学院学报,2005,21:106-107.
[4] Dorin B, Jean L. Electrochemical assitance of catalytic oxidation in liquid phase using molecular oxygen:Oxidation of toluenes[J].Catalysis Today,1999,48:363-369.
[5] A B Isaev; Z M Aliew. Influence of the dissolved oxygen under pressure to electrochemical oxidation toluene and acetone aqueous mixtures[J].Electrochemistry Communication,2007,9:1400-1403.
[6] Gary M Dugmore, Gregory J Powels. Mechanistic aspects of benzylic bromide formation and oxidation during the cobalt acetate bromide catalyzed oxidation of alkylbenzenes in carboxylic acids[J].J Mol Catal A:Chemical,1995,99:1-12.
[7] Praveen K Tandon, Manish S. Iridium(Ⅲ) catalyzed oxidation of toluene and ethyl benzene by cerium(Ⅳ) in acidic aqueous medium[J].J Mol Catal A:Chemical,2009,304:101-106.
[8] Bottino A,Capannelli G. Vapor phase oxidation of toluene in V/Al2O3-TiO2catalytic reactors[J].Catalysis Today:2005,99:171-177.
[9] AnJun H, ChenXu L. Selective oxidation ofp-chlorotoluene catalyzed by Co/Mn/Br in acetic acid medium[J].Ind Eng Chem Res,2006,45:5688-5692.
[10] Kamiya. The autoxidation of tetralin catalysed by cobalt salt and sodium bromide in acetic acid[J].Tetrahedron,1966,22:2029-2038.
[11] SH W T, Bin L. Scale formation and its mechanism in the liquid phase oxidation of toluene by air[J].Ind Eng Chem Res,2007,46:7826-7829.
[12] Naruhisa H, Naoko S, Norihiro N. Oxidation of substituted toluenes with molecular oxygen in the presence ofN,N′,N″-trihydroxyisocyanuric acid as a key catalyst[J].J Org Chem,2003,68:6587-6590.
[13] Akihiro S, Satoshi S. Aerobic oxidation of methylpyridines to pyridinecarboxylic acids catalyzed byN-hydroxyphthalimide[J].Org Pro Res & Dev,2000,4:505-508.
[14] Yasutaka T, Takahiro I. A new strategy for the preparation of terephthalic acid by the aerobic oxidation ofp-xylene usingN-hydroxyphthalimide as a catalyst[J].Adv Synth Catal,2001,343:220-225.
[15] Basudeb S, Nobuyoshi K.N-hydroxyphthalimides and metal cocatalysts for the autoxidation ofp-xylene to terephthalic acid[J].J Phys Chem A,2004,108:425-431.
[16] Yasushi Y, Yoshiaki H, Takahiro I. Catalytic oxidation of alkylbenzenes with molecular oxygen under normal pressure and temperature byN-hydroxyphthalimide combined with Co(OAc)2[J].J Org Chem,1997,62:6810-6813.
[17] X H L. Synthesis,characterization and catalytic property of tetradentate Schiff-base complexes for the expoxidation of styrene[J].J Mol Catal A:Chemical,2006,250:62-69.
[18] 卓广澜,赵卫娟. 甲苯氧化制苯甲酸的新催化体系[J].有机化学,2004,24:962-965.
[19] 方亚辉,卢安军. NHPI/过渡金属催化甲苯氧化制苯甲酸[J].化工进展,2006,25:1358-1361.
[20] Naoko S, Satoshi S. Oxidation of nitrotoluenes with air usingN-hydroxyphthalimide analogues as key catalysts[J].Tetrahedron Lett,2003,44:2053-2056.

