一株银杏内生真菌菌株的抑菌活性成分研究
周松林,陈双林,谭光宏,王 华,黄用豪,陈 凡
1海南医学院热带病重点实验室,海口 571101;2南京师范大学生命科学学院,南京 210046
一株银杏内生真菌菌株的抑菌活性成分研究
周松林1*,陈双林2,谭光宏1,王 华1,黄用豪1,陈 凡1
1海南医学院热带病重点实验室,海口 571101;2南京师范大学生命科学学院,南京 210046
从银杏叶柄分离筛选到具抗菌活性的内生真菌 Colletotrichum.SP NTB-2菌株,利用硅胶柱色谱、制备高效液相色谱等方法在其发酵产物中分离到抗枯草芽孢杆菌、鼠伤寒沙门氏菌等具有广谱抑菌活性的化合物,经MS、NMR等波谱数据确认该活性成分为芹菜素-8-C-葡萄糖苷(apigenin-8-C-β-D-glucopyranoside),该化合物首次从真菌中分离得到。
内生真菌;银杏;芹菜素-8-C-葡萄糖苷
1 材料与方法
1.1 材料
1.1.1 仪器与试剂
1100系列高压液相色谱仪 (美国 Agilent公司);制备色谱柱:Hichrom C18(10×250 mm,10 μm);Vario ELⅢ元素分析仪 (德国元素分析系统公司)分析;Burker AM 400核磁共振仪 (瑞士 Bruker公司);Autospec VG-3000质谱仪 (美国 Autospec公司);XT-4双目显微熔点测定仪(北京泰克仪器有限公司)。
柱色谱用 200~300目硅胶 (Silica G),薄层层析用硅胶 G(均为青岛海洋硅胶厂生产),其余试剂均为国产分析纯。
1.1.2 菌种
内生真菌NTB-2为本实验室从江苏省南通市的银杏树叶柄上通过组织分离法获得的,通过显微形态观察,按 Sutton[5]的腔孢纲分类系统鉴定为刺盘孢 Colletotrichumsp.。
大肠埃希氏菌 (Escherichia coliATCC 25922),金黄色葡萄球菌 (StaphylococcusaureusATCC 6538),枯草芽孢杆菌 (Bacillus subtilisATCC 9372),铜绿假单胞菌 (Pseudom onas aeruginosaATCC 27853 ),鼠伤寒沙门氏菌 (Sa lm onella typh im uriumCCG MC 11190),以上均购自江苏省疾病预防控制中心;不动杆菌 (Acinetobacterspp.B667),洋葱假单孢菌(Pseodom onas cepacia438),肺炎克雷伯氏菌 B673 (Klebsiella pneum oniae B667),柠 檬 酸 杆 菌(Citrobacter spp.38)、阴沟肠杆菌 (Enterobacter cloacae98-23),以上菌株由江苏省省人民医院惠赠。
1.1.3 培养基
快落山的太阳光洒进房间里,有点暗淡,又有点温暖。齐海峰看着窗外想,周末要不要约她再去一次电影院呢?却听她在外面扯着嗓子喊:“老齐,今晚包水饺好不好?”
马铃薯葡萄糖(PDA)液体(固体)培养基:马铃薯 200 g,葡萄糖 20 g,(琼脂 18 g),水 1000 mL,自然 pH。LB(Luria Bertani)液体 (固体)培养基:蛋白胨 10g,NaCl 5 g,酵母粉 5 g,(琼脂 16 g),用 1 mol/ L NaOH调 pH 7.0,重蒸馏水定容至 1000 mL。
1.2 方法
1.2.1 菌株NTB-2发酵
制备马铃薯葡萄糖培养液,于500 mL三角瓶中装液 250 mL。按 1/20接种量将 NTB-2孢子悬液(浓度为 107个/mL)接种到 PDA液体培养基中,26℃、150 r/min下培养 3~5 d后,再接种到 7 L的种子发酵罐 (装液为5 L)中,26℃、150 r/min下培养5 d后,再放罐到 70 L的中式发酵罐 (装液为 50 L)中,26℃、150 r/min下培养 7 d。期间不断补充马铃薯葡萄糖液体培养基,使发酵罐内的总体积保持不变。
1.2.2 提取与分离
发酵结束后,用四层纱布滤过,使菌体与发酵液分开,菌体用 70%的乙醇浸泡,浸泡 24 h后用滤纸滤过,滤液减压浓缩,再用 70%的乙醇浸泡菌体,重复 3次。发酵液用乙酸乙酯萃取 3次,减压浓缩萃取液,分别得浓缩物 8.3和 4.0 g。
合并菌体和发酵液的提取物共 12.3 g,上硅胶柱,用氯仿:甲醇 (100:0)和氯仿:甲醇 (90:10)梯度洗脱,100 mL收集组分,对各组分进行薄层色谱分离,合并主产物相同的组分,得到粗产品化合物 1为148 mg。粗产品中的2 mg用去做抑菌的实验,追踪其活性成分的去向,剩余的然后在通过制备型HPLC进行精制,得到化合物 1为 37.4 mg。
1.2.3 抑菌实验
本药敏实验采用纸片琼脂扩散法 (K-B法)。将 10种供试菌株标化后 15 min之内接种于药敏培养基,以无菌棉团蘸取已制备好的细菌菌液,并在管壁上挤压除去多余的菌液后,向一个方向均匀涂布接种于LB琼脂平板表面,然后将平板每转动 60度涂布一次,共涂 3次,最后沿平板边缘涂布一圈。盖上平皿盖,置室温干燥 3~5 min,待平皿面稍干后用无菌镊子将含药纸片平放于含菌琼脂平板表面,并轻压使其紧贴在上面。平板经室温放置 15 min再倒置于 37℃培养箱中,培养 16~18 h后阅读结果,以上实验每处理重复 3次。
2 结果与讨论
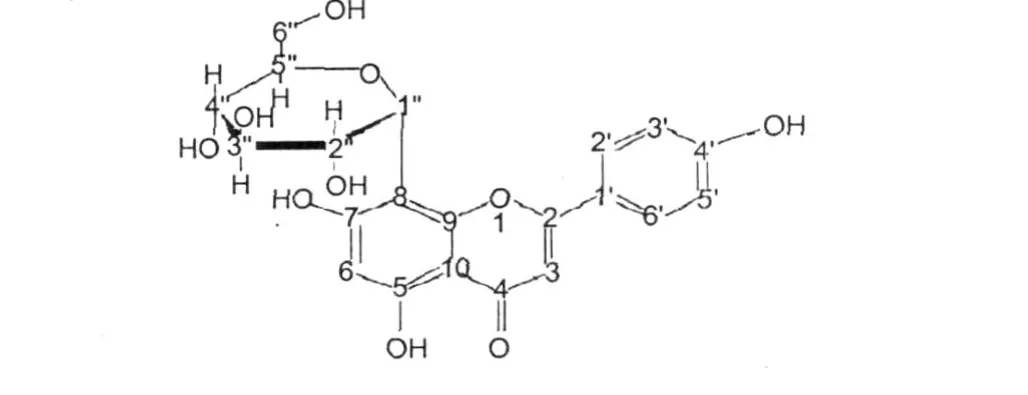
图 1 化合物 1芹菜素-8-C-葡萄糖苷的化学结构Fig.1 Apigenin-8-C-β-D-glucopyranoside isolated from Colletotrichumsp.NTB-2
2.1 化合物 1的结构鉴定
芹菜素-8-C-葡萄糖苷 黄色粉末,mp.253~260℃。[α18°(c 2,吡啶)。EI-MSm/z(%): 433.4([M]+H),结合1H、13C NMR数据推测其分子式为 C21H20O10。UVnm:272,335,(MeOH +NaOAc)280,375,(MeOH +A ICI3)277,304, 346;1H NMR(DMSO-d6,400 MHz)δ:6.26(1H,s, 3-H),6.64(1H,s,6-H),7.98(1H,d,J=8.4 Hz,2′-H),6.83(1H,d,J=8.8 Hz,3′-H),6.83(1H,d,J= 8.4 Hz,5′-H),7.98(1H,d,J=8.8 Hz,6′-H),13.16 (1H,s,5-OH),10.79(1H,s,7-OH),10.38(1H,s, 4′-OH),3.77(1H,d,J=7.8 Hz,1′′-H),3.61(1H, m,2′′-H),3.36(1H,m,3′′-H),3.61(1H,m,4′′-H),4.67(1H,m,5′′-H),3.24(2H,m,6′′-H);13C NMR(DMSO-d6,100 MHz)δ:163.9(C-2),98.2(C-3),182.1(C-4),160.5(C-5),104.6(C-6),162.6 (C-7),102.4(C-8),156.0(C-9),104.3(C-10), 121.6(C-1′),128.9(C-2′),115.8(C-3′),163.9(C-4′),115.8(C-5′),128.9(C-6′),73.4(C-1′′),70.8 (C-2′′),78.0(C-3′′),70.6(C-4′′),81.9(C-5′′), 61.3(C-6′′)。其理化性质、波谱数据与芹菜素-8-C-葡萄糖苷 (apigenin-8-C-β-D-glucopyranoside)[6-8]的数据一致。
2.2 抑菌结果
化合物 1对各种细菌的抑菌试验结果见表 1和图 2~5,化合物 1对所有供试细菌都有明显的抑菌作用,尤其是对枯草芽孢杆菌、鼠伤寒沙门氏菌、洋葱假单胞菌作用明显,其抑菌圈的大小都超过18mm,属于高度敏感类型;而对大肠杆菌、不动杆菌、柠檬酸杆菌都有明显的抑菌作用,属于比较敏感类型;属于对所测菌高度敏感。
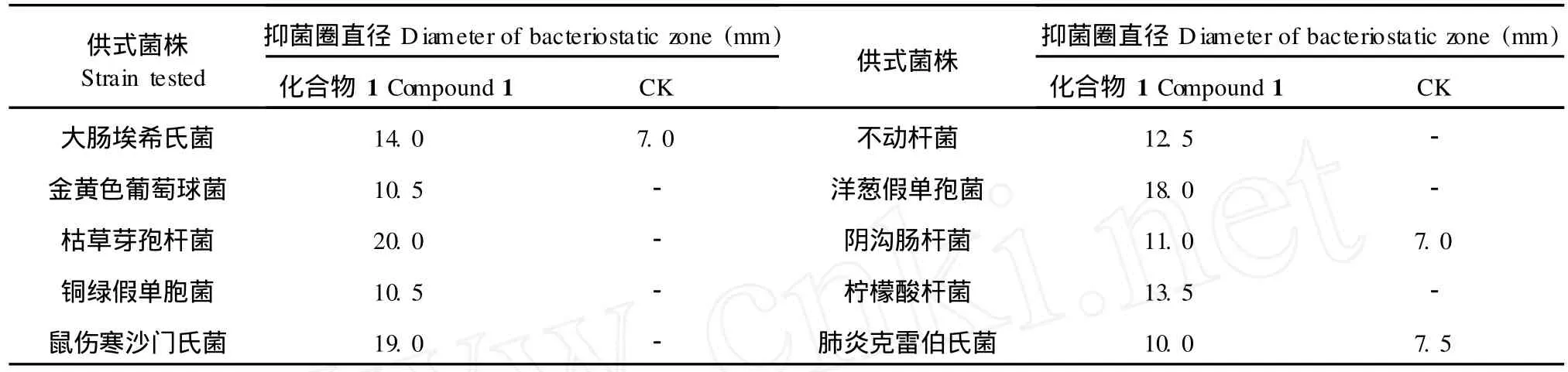
表 1 刺盘孢 Colletotrichumsp.NTB-2的产物对不同细菌的抑菌作用Table 1 Inhibitory effect ofColletotrichumsp.against different bacteria
图 5 化合物 1对不动杆菌的抑制作用Fig.5 Inhibitory effect of compound 1 againstCitrobacterspp
2.3 讨论
银杏所含的化学成分相当复杂,其中黄酮类和萜内酯是银杏叶发挥独特药理活性的有效成分。其黄酮类苷元主要是:山奈酚、槲皮素、异鼠李素、杨梅醇及木樨素,另外还有少量芹菜素等,它们通常以糖苷形式存在[2,9]。芹菜素-8-C-葡萄糖苷,其天然的产物来源并不是很广泛,曾在掌叶槭,黄瓜叶、夏至草等少数植物中分离得到,它主要作为一种抗氧化剂,可以清除体内的自由基、超氧化基及抗衰老等作用[6-8,10]。从该菌株的液体培养基中分离到芹菜素-8-C-葡萄糖苷,这也为产芹菜素-8-C-葡萄糖苷提供一种新的来源。但我们看到产量还是不够,需要进一步的优化其培养条件。虽然目前的文献还没有报道从银杏叶或果实中分离得到芹菜素-8-C-葡萄糖苷。这也可能是因为内生真菌在长期的进化过程中与宿主植物建立了互惠共生关系,不仅参与了植物次生代谢产物的合成,而且有可能独立承担一些活性物质的代谢合成,与宿主达到共赢互利的效果。植物内生真菌及其代谢产物的多样性为我们发现一些结构新颖、活性专一的物质提供了可能,值得我们进一步的深人研究。
1 Strobel G,Daisy B.Bioprospecting for microbial endophytes and their natural products.J M icrobiology And M olecularB iology,2003,67:491-502.
2 Li HY(李海燕),Liu L(刘丽).Recent advances on bioactive compounds producing endophytes.Nat Prod ResDev(天然产物研究与开发),2004,16:482-485.
3 Luo XD(罗顺德),Zhou BH(周本宏),Wu KY(吴克媛). Advances in the studies of the pharmacology from the leaves ofGinkgo bilobaL..Acta Chin M ed and Phar m(中医药学报),1995,6:48-49.
4 Wang MX(王梅霞),Chen SL(陈双林),Yan SZ(闫淑珍),et al.A preliminary study on the isolation identification and media of an endophytic fungus producing flavones.J Nanjing Nor m alUniv,Nat Sci(南京师范大学报,自科版), 2003,26(1):106-110.
5 Sutton BC.The Coelomycetes.Kew,CM I.1980.
6 Harborne JB,Mabry TJ.The Flavonoids:Advances in Research.New York:Chapman and Hall,1982.
7 NawwarMAM,El-Mousallamy AMD,Barakat HH,et al.Flavonoid lactates from leaves of Marrubium.Phytochem istry, 1989,28,3201-3206.
8 McnallyDavid J,Wurms kirstin V,Caroline L,et al.Complex C-glycosyl flavonoid phytoalexins from cucumis sativus.Journal of Nat Prod,2003,66,1280-1283.
9 Gao JM(髙锦名),Wang L(王蓝),Zhang AL(张鞍灵),et al.Advances in the studiesof the constituents from the leaves ofGinkgo bilobaL..J Northwest Forestry Coll(西北林学院学报),1995,10(4):94-100.
10 Jin HK,Bum CL,Jin HK,et al.The Isolation and Antioxidative Effects of vitexin from Acer palmatum.A rch Phar m Res, 2005,28(2):195-202.
Antibacterial Substances of Endophytic Fungus Isolated fromGinkgo biloba
ZHOU Song-lin1*,CHEN Shuang-lin2,TAN Guang-hong1,WANG Hua1,HUANG Yong-hao1,CHEN Fan11Hainan Provincial Key Laboratory of TropicalM edicine,Hainan M edical Collge,Haikou 571101,China;2Life Science College of Nanjing Nor m alUniversity,Nanjing 210046,China
To study the antibacterial components from endophytic fungus strain,Colletotrichum.SP NTB-2 fromGinkgo biloba,silica gel column chromatography and pre-HPLC were used for the isolation and purification.A active compound was isolated from the fermentation broth of stains NTB-2 and identified as apigenin-8-C-beta-D-glucopyranoside on the basis of spectral data analysis.
endophytic fungus;Ginkgo biloba;apigenin-8-C-β-D-glucopyranoside
1001-6880(2010)02-0193-04
2009-02-03 接受日期:2009-04-08
国家自然科学基金 (30560160);海南省自然科学基金(808157)
*通讯作者 Tel:86-898-66893322;E-mail:zhousonglin106@163.com
R965;Q58
A

